固体氧化物燃料电池(solid oxide fuel cells,SOFCs)作为一种清洁、高效的电化学发电装置,有助于解决环境污染和能源紧张问题[1-2]。SOFCs分为氧离子导体基固体氧化物燃料电池(oxide-ion conductor based SOFCs,O-SOFCs)和质子导体基固体氧化物燃料电池(the proton conducting SOFCs,H-SOFCs)。虽然H-SOFCs研究起步较晚,但是由于具有较低的离子传导活化能和较高的燃料利用效率等优点,得到国际上广泛重视[3-4]。此外,H-SOFCs的反应产物水是在阴极处产生,并且电池内部的极化电阻主要是由阴极/电解质界面极化所引起,因此研究阴极材料具有重要意义[5]。
不同稀土和金属元素掺杂BaFeO3的离子、电子混合导体作为SOFCs阴极材料得到了广泛研究。相对于含Co阴极材料而言,BaFeO3基阴极材料具有较高浓度氧空位和低成本等优点[6]。通常认为,在H-SOFCs阴极材料中加入质子导体,如电解质材料,可增大三相反应界面从而提高单电池的输出性能[7-9],但Sun等发现,以NiO-BZCY为阳极、BZCY为电解质、立方钙钛矿材料Ba0.5Sr0.5FeO3-δ(BSF)与氧离子导体SDC的混合材料为质子阻塞复合阴极构成的单电池,在750 ℃时的最大功率密度为792 mW/cm2,这是当时文献报道的BZCY基单电池的最大功率密度[10]。进一步工作表明,相对于质子导体复合阴极而言,质子阻塞复合阴极具有更好的电化学性能[11]。Zhao等在以质子阻塞Sm0.5Sr0.5CoO3-δ(SSC)-SDC为阴极的H-SOFC中也观察到了类似现象,并对其进行了深入分析,认为当氧空位扩散和氧离子运输为阴极反应的主要控制因素时,质子阻塞复合阴极比质子导体复合阴极更有利于提高单电池性能[12]。
尽管Co基钙钛矿氧化物中Pr掺杂研究有很多[13-14],但Fe基阴极材料中Pr掺杂研究还较少。此外,考虑到Pr掺杂可提高离子电子混合导体的导电性,且质子阻塞复合阴极具有更好的性能,本文通过Pr部分替代Ba0.5Sr0.5FeO3-δ钙钛矿氧化物中的Ba和Sr,获得新型钙钛矿氧化物Pr0.5Ba0.25Sr0.25FeO3-δ(PBSF),与Ce0.8Sm0.2O1.9(SDC)混合制成质子阻塞型复合阴极材料PBSF-SDC。在相结构分析、化学相容性和热膨胀系数测量基础上,研究了NiO-BaZr0.1Ce0.7Y0.2O3-δ(BZCY)|BZCY|PBSF-SDC单电池的电化学性能。
1 试验方案 1.1 粉体制备PBSF、SDC、BZCY和NiO-BZCY粉体均采用EDTA-柠檬酸络合法制备[15]。以PBSF的合成为例,步骤如下:
① 按照化学计量比称量Pr(NO3)3·6H2O、Ba(NO3)2、Sr(NO3)2、Fe(NO3)3·9H2O,溶于去离子水形成溶液;
② 以EDTA(质量浓度99.5%)和柠檬酸(质量浓度99.8%)为络合剂和助燃剂加入溶液中,EDTA和柠檬酸与溶液中金属离子物质的量为1:1:1;
③ 在溶液中加入适量的氨水将pH值调至7,利用恒温加热磁力搅拌器80 ℃水浴加热6 h得到湿凝胶,移至电炉上继续加热到自燃,得到初级粉体;
④ 将得到的初级粉体在高温箱式炉中1 000 ℃下煅烧6 h得到PBSF粉体。
合成BZCY粉体所用的原料为Ba(NO3)2、Zr(NO3)4·5H2O、Ce(NO3)4·6H2O和Y(NO3)3·6H2O; 合成SDC粉体所用的原料为Sm2O3和Ce(NO3)4·6H2O,其中Sm2O3先溶于浓硝酸中制备成硝酸盐溶液; 合成NiO-BZCY粉体所用的原料为Ba(NO3)2、Zr(NO3)4·5H2O、Ce(NO3)4·6H2O、Y(NO3)3·6H2O和Ni(NO3)2·6H2O,其中NiO和BZCY的质量比是6:4。BZCY和NiO-BZCY初级粉体分别在高温箱式炉中于1 000 ℃煅烧5 h,SDC初级粉体在高温箱式炉中于700 ℃煅烧5 h,得到最终粉体。
1.2 单电池制备采用共压法制备阳极支撑半电池[16-17],首先将阳极粉体在单轴200 MPa下压制,然后将电解质BZCY粉体与阳极片在300 MPa共压制备,在高温箱式炉中1 350 ℃煅烧5 h,得到阳极支撑具有致密电解质膜的半电池。质子阻塞复合阴极PBSF-SDC的质量比为7:3,与文献[10]相同。将PBSF、SDC、乙基纤维素和松油醇按质量比7:3:1:10混合,研磨2 h使其充分混合均匀制备成阴极浆料。将阴极浆料涂到半电池BZCY电解质膜上,烘干后在高温箱式炉中于950 ℃烧结3 h得到单电池,阴极面积为0.237 cm2。
1.3 性能表征用X射线衍射(X-ray diffraction,XRD; Rigaku D/max-2500/PC,CuKα辐射)对合成的粉体进行物相分析。同时,用XRD分析研究PBSF与SDC和电解质BZCY的化学相容性,将3种粉体按照质量比1:1:1混合,在室温下研磨1 h,然后在1 000 ℃下共烧6 h,对混合共烧后的粉体做XRD物相结构分析。扫描2θ范围为20°~90°,扫描速度为10°/min,步长为0.01°。
采用国产直流电子负载电池测试系统(ITech electronics,型号IT 8511)测试单电池的功率密度,将单电池固定在氧化铝管的一端,用导电胶进行封装,银浆涂覆在阴极表面进行电流收集,银丝作导线。测试温度范围为600~750 ℃,每隔50 ℃测一次。测试条件为:阳极端通入湿润的氢气(湿度:3%H2O; 速率:30 mL/min)作为燃料,阴极端暴露于静态空气中,以空气中的氧气作为阴极氧化剂。用阻抗分析仪(上海辰华,CHI650E)测量单电池在开路条件下的电化学阻抗谱(AC信号:5 mV; 频率范围:0.1~100 kHz)。采用国产STR-B型多功能直流电阻测试仪,通过van der Pauw四电极法[18]来测量PBSF的电导率,样品在1 200 ℃烧结6 h形成圆片状,所测样品厚度为1 mm。
用扫描电子显微镜(scanning electron microscope, SEM, JSM-6700F)观察经过电化学测试后的单电池微观结构。利用高温线性膨胀仪(LINSEIS DIL-L76)测试BZCY、PBSF和PBSF-SDC(PBSF:SDC质量比7:3)的热膨胀系数,样品在1 250 ℃烧结6 h成致密材料后进行打磨,所测样品直径为10 mm,高为3.5 mm。采用升温测量,升温速率为5 ℃/min,范围为20~750 ℃。
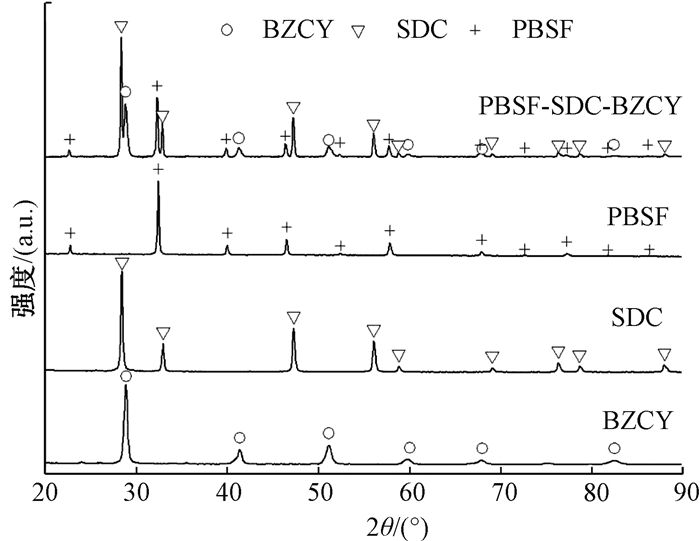
2 结果与讨论 2.1 晶体结构与化学相容性分析图 1为烧结态PBSF、BZCY和SDC 3种粉体,及其混合物经1 000 ℃、6 h共烧后的XRD图谱,并对图中衍射峰进行了标定。由图可知,PBSF、BZCY和SDC粉体均呈单一相,无明显杂峰。利用PowderX软件对3种粉体衍射峰进行分析。表 1是对应的标准卡片、晶系、空间群、拟合的晶格常数和晶胞体积。其衍射峰位与Ba0.5Sr0.5FeO3-δ[10]和Ba1-xLaxFeO3-δ(x=0.1~0.6)[19]等类似,PBSF也为立方钙钛矿结构。BZCY为立方钙钛矿结构,SDC为立方萤石结构,其衍射峰位与文献结果一致[10, 20]。此外,3种粉体混合共烧后的XRD谱仍呈现出PBSF、SDC、BZCY的独立相结构,且相应峰位也未发生明显偏移,这表明3种粉体在高温条件下具有良好化学相容性。
|
图 1 PBSF、SDC、BZCY 3种单独粉体及其混合共烧后的XRD Fig. 1 Powder XRD patterns of PBSF, SDC, BZCY and co-fired PBSF-SDC-BZCY |
|
|
表 1 粉体晶格常数拟合结果 Tab. 1 Fitted lattice constant of powders |
早在1926年,Goldschmidt容忍因子t就被提出用来判断ABO3型氧化物是否为钙钛矿结构,其公式为
| $ t=\frac{r_{A}+r_{0}}{\sqrt{2}\left(r_{B}+r_{0}\right)}, $ | (1) |
式中:rA、rB和rO分别代表A3+、B3+和O2-的离子半径[21]。t在0.77~1.1之间时,ABO3化合物为钙钛矿结构; t < 0.77时,以铁钛矿形式存在; t>1.1时,以方解石或文石型存在。在PBSF中,Pr3+、Ba2+、Sr2+、Fe3+和O2-离子半径分别为0.130 nm、0.161 nm、0.144 nm、0.064 5 nm和0.140 nm[22],代入式(1)得t=0.972,这也证实了PBSF晶体结构为钙钛矿型结构。
2.2 微结构观察图 2(a)是单电池PBSF-SDC|BZCY|NiO-BZCY经过电化学性能测试后的截面SEM图像,电解质厚度在12 μm左右。单电池在经升降温测试后,阴极层与电解质膜仍紧密结合,形成良好的阴极/电解质界面,无开裂和分层的迹象,表明单电池可以持久工作。图 2(b)是阴极层的高倍照片,阴极层颗粒大小分布均匀,无明显的团聚现象,有利于提高燃料电池的电化学性能; 同时孔洞整体分布均匀有序,有利于增加三相界面的催化活性位点,对燃料电池的输出性能有积极影响。
|
图 2 单电池经电化学测试后的SEM照片 Fig. 2 SEM photos of single cell after electrochemical test |
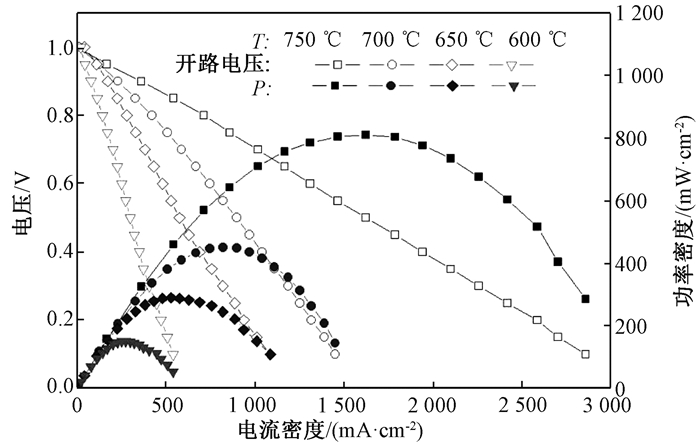
图 3是单电池PBSF-SDC|BZCY|NiO-BZCY的I-V和I-P曲线。在600 ℃、650 ℃、700 ℃和750 ℃时,开路电压分别为1.003 V、1.001 V、0.988 V和0.970 V; 最大功率密度分别为(153±11、303±17、486±20、865±38) mW/cm2。在750 ℃时,以PBSF-SDC为阴极制作的单电池功率密度(865±38) mW/cm明显高于以BSF-SDC为阴极的单电池功率密度(792 mW/cm)[10]。由于PBSF相对于BSF是Pr3+对Ba2+、Sr2+进行了部分置换,电子浓度得到了增加,从而提高了电化学性能。

|
图 3 单电池在600 ℃、650 ℃、700 ℃和750 ℃时I-V和I-P曲线 Fig. 3 The I-V and I-P curve of the single cell at 600 ℃, 650 ℃, 700 ℃ and 750 ℃ |
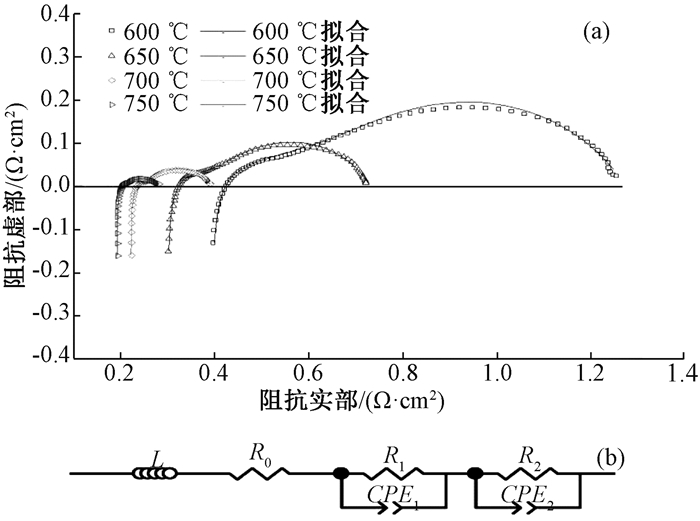
图 4(a)是单电池PBSF-SDC|BZCY|NiO-BZCY的电化学阻抗谱(electrochemical impedance spectroscopy,EIS)。由图 4(a)可观察到阻抗谱曲线由两段弧组成,因此选取图 4(b)作为拟合EIS所用的等效电路图。在等效电路中,L是由连接线或设备的高频相移引起的电感; 电阻R0对应于单电池的欧姆电阻; R1和R2分别代表高频部分和低频部分的极化电阻; CPE1和CPE2是恒定的相位元件[23]。电池的总极化电阻Rp为R1和R2之和,电池的总电阻Rt为R0和Rp之和。通过软件Zview对EIS进行拟合,结果如表 2所示。在750 ℃时,PBSF-SDC|BZCY|NiO-BZCY单电池总电阻为(0.284±0.005) Ω·cm2,明显低于BSF-SDC|BZCY|NiO-BZCY单电池的总电阻(0.314 Ω·cm2)[10],这也表明本文制备的单电池具有更高的性能(图 3)。同时,本实验电解质厚度(12 μm)比文献[10]中的电解质厚度(20 μm)薄,也有利于降低单电池总电阻。
|
图 4 单电池PBSF-SDC|BZCY|NiO-BZCY的电化学性能 Fig. 4 Electrochemical performance of single cell PBSF-SDC/BZCY/NiO-BZCY (a)单电池在600 ℃、650 ℃、700 ℃和750 ℃时EIS; (b)拟合EIS所用等效电路图 |
|
|
表 2 阻抗谱拟合结果 Tab. 2 Fitting results of EIS spectra |
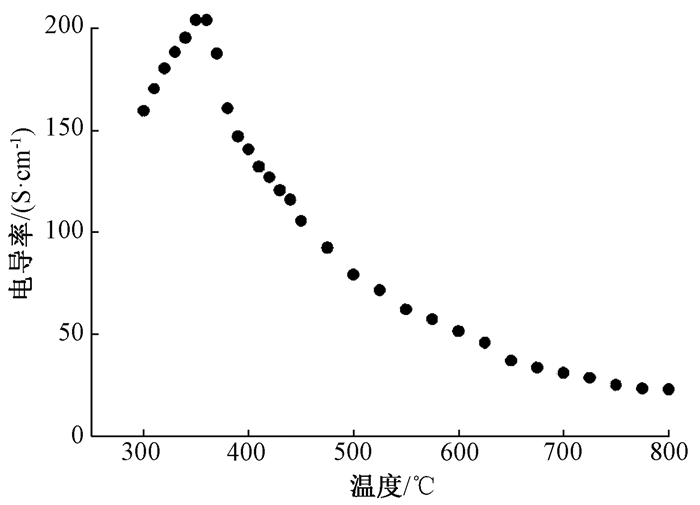
图 5是致密PBSF电导率温度关系。由图可知,在350 ℃以下,PBSF电导率随温度升高而增大,表现出类半导体导电行为; 而在350 ℃以上,电导率随温度升高快速下降,则表现出明显的类金属行为; 即PBSF在350 ℃附近存在类半导体向类金属转变[24]。此外,在600~800 ℃时,PBSF的电导率为51.4~22.9 S/cm,略高于BSF(40~15 S/cm)[25],这也间接说明了PBSF单电池具有更高的最高功率密度(max power density, MPD)(图 3)。这是因为Pr3+部分置换Ba2+和Sr2+可提高混合离子-电子导体(mided ionic-electronic conductor, MIEC)的电子浓度,从而提高导电性。
|
图 5 致密PBSF电导率温度关系 Fig. 5 Dependence of electrical conductivity of dense PBSF on temperature |
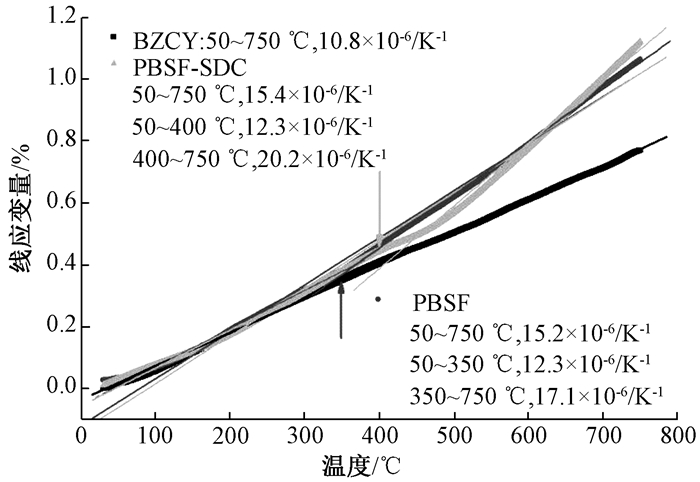
图 6是致密BZCY、PBSF和PBSF-SDC在静态空气中的热膨胀曲线。BZCY的热膨胀系数(thermal expansion coefficient,TEC)与文献所报道的10.1×10-6 K-1基本一致[26]。在低温段,致密PBSF和PBSF-SDC的TEC一致,均为12.3×10-6 K-1,与BZCY的TEC(10.8×10-6 K-1)值相近。但当温度升高时,PBSF和PBSF-SDC的TEC明显增大,分别在350 ℃和400 ℃附近发生明显变化,这与晶格氧的丢失(氧空位的形成),以及可能存在的铁离子由高价态还原到低价态有关[27-28]。PBSF和PBSF-SDC的TEC转变温度和高温区TEC差异可能与SDC和PBSF氧空位形成能力差异有关。整体而言,PBSF的TEC远远低于Co基钙钛矿材料,如PrBa1-xCo2O5+δ(x=0~0.08)的TEC范围为(22.8~23.4)×10-6/K-1[29],PrBa0.5Sr0.5Co2-xFexO5+δ(x=0.5, 1.0, 1.5)的TEC范围为(19.2~21.3)×10-6/K-1[30]。
|
图 6 BZCY、PBSF和PBSF-SDC圆柱状样品在静态空气中30~750 ℃热膨胀曲线 Fig. 6 Thermal expansion curves of BZCY, PBSF and PBSF-SDC cylindrical samples in the temperature range of 30~750 ℃ with static air |
1) 制备的Pr0.5Ba0.25Sr0.25FeO3-δ(PBSF)具有单一立方钙钛矿结构,其容忍因子t=0.972,且PBSF与Ce0.8Sm0.2O1.9(SDC)和BaZr0.1Ce0.7Y0.2O3-δ(BZCY)在1 000 ℃时具有良好的化学相容性。
2) NiO-BZCY |BZCY|PBSF-SDC单电池在600 ℃、650 ℃、700 ℃和750 ℃时,开路电压分别为1.003 V、1.001 V、0.988 V和0.970 V; 最大功率密度为(153±11) mW·cm-2、(303±17) mW·cm-2、(486±20) mW·cm-2和(865±38) mW·cm-2; 极化电阻为0.912 Ω·cm2、0.448 Ω·cm2、0.173 Ω·cm2和0.092 Ω·cm2。经升降温测试后,单电池三层材料依然能保持良好接触。
3) 在350 ℃附近,PBSF电导率存在类半导体向类金属转变,TEC也发生转折。低温区TEC为12.4×10-6 K-1,高温区TEC为17.1×10-6 K-1,高温膨胀系数增大主要与晶格氧丢失(氧空位形成),以及可能存在的铁离子由高价态还原到低价态有关。
总之,复合材料PBSF-SDC在H-SOFCs阴极材料中具有潜在的应用前景。
| [1] |
SINGHAL S C. Advances in solid oxide fuel cell technology[J]. Solid state ionics, 2000, 135(1/2/3/4): 305-313. (  0) 0) |
| [2] |
SONG C S. Fuel processing for low-temperature and high-temperature fuel cells challenges, and opportunities for sustainable development in the 21st century[J]. Catalysis today, 2002, 77(1/2): 17-49. (  0) 0) |
| [3] |
毛宗强. 燃料电池[M]. 北京: 化学工业出版社, 2005. MAO Z Q. Fuel cell[M]. Beijing: Chemical Industry Press, 2005. (  0) 0) |
| [4] |
衣宝廉. 燃料电池现状与未来[J]. 电源技术, 1998, 22(5): 216-221. YI B L. Status and future of fuel cell[J]. Chinese journal of power sources, 1998, 22(5): 216-221. (  0) 0) |
| [5] |
PENG R R, WU T Z, LIU W, et al. Cathode processes and materials for solid oxide fuel cells with proton conductors as electrolytes[J]. Journal of materials chemistry, 2010, 20(30): 6218. DOI:10.1039/c0jm00350f (  0) 0) |
| [6] |
SUGA Y, HIBINO M, KUDO T, et al. Electrochemical oxidation of BaFeO2.5 to BaFeO3[J]. Electrochimica acta, 2014, 137: 359-362. DOI:10.1016/j.electacta.2014.05.162 (  0) 0) |
| [7] |
YANG L, ZUO C, WANG S Z, et al. A novel composite cathode for low-temperature SOFCs based on oxide proton conductors[J]. Advanced materials, 2008, 20(17): 3280-3283. DOI:10.1002/adma.200702762 (  0) 0) |
| [8] |
LIN B, DING H P, DONG Y C, et al. Intermediate-to-low temperature protonic ceramic membrane fuel cells with Ba0.5Sr0.5Co0.8Fe0.2O3-δ-BaZr0.1Ce0.7Y0.2O3-δ composite cathode[J]. Journal of power sources, 2009, 186(1): 58-61. DOI:10.1016/j.jpowsour.2008.09.041 (  0) 0) |
| [9] |
LI M L, NI M, SU F, et al. Proton conducting intermediate-temperature solid oxide fuel cells using new perovskite type cathodes[J]. Journal of power sources, 2014, 260: 197-204. DOI:10.1016/j.jpowsour.2014.03.013 (  0) 0) |
| [10] |
SUN W P, SHI Z, FANG S M, et al. A high performance BaZr0.1Ce0.7Y0.2O3-δ-based solid oxide fuel cell with a cobalt-free Ba0.5Sr0.5FeO3-δ-Ce0.8Sm0.2O3-δ composite cathode[J]. International journal of hydrogen energy, 2010, 35(15): 7925-7929. DOI:10.1016/j.ijhydene.2010.05.084 (  0) 0) |
| [11] |
SUN W P, FANG S M, YAN L T, et al. Proton-blocking composite cathode for proton-conducting solid oxide fuel cell[J]. Journal of the electrochemical society, 2011, 158(11): B1432-1438. DOI:10.1149/2.076111jes (  0) 0) |
| [12] |
ZHAO L, HE B B, GU J Q, et al. Reaction model for cathodes cooperated with oxygen-ion conductors for solid oxide fuel cells using proton-conducting electrolytes[J]. International journal of hydrogen energy, 2012, 37(1): 548-554. DOI:10.1016/j.ijhydene.2011.09.084 (  0) 0) |
| [13] |
JIN F J, XU H W, LONG W, et al. Characterization and evaluation of double perovskites LnBaCoFeO5+δ (Ln=Pr and Nd) as intermediate-temperature solid oxide fuel cell cathodes[J]. Journal of power sources, 2013, 243: 10-18. DOI:10.1016/j.jpowsour.2013.05.187 (  0) 0) |
| [14] |
LIN Y, RAN R, ZHANG C M, et al. Performance of PrBaCo2O5+δ as a proton-conducting solid-oxide fuel cell cathode[J]. The journal of physical chemistry A, 2010, 114(11): 3764-3772. DOI:10.1021/jp9042599 (  0) 0) |
| [15] |
LEI L B, TAO Z T, HONG T, et al. A highly active hybrid catalyst modified (La0.60Sr0.40)0.95Co0.20Fe0.80O3-δ, cathode for proton conducting solid oxide fuel cells[J]. Journal of power sources, 2018, 389: 1-7. DOI:10.1016/j.jpowsour.2018.03.058 (  0) 0) |
| [16] |
SUN W P, YAN L T, SHI Z, et al. Fabrication and performance of a proton-conducting solid oxide fuel cell based on a thin BaZr0.8Y0.2O3-δ electrolyte membrane[J]. Journal of power sources, 2010, 195(15): 4727-4730. DOI:10.1016/j.jpowsour.2010.02.012 (  0) 0) |
| [17] |
LING Y H, YU J, LIN B, et al. A cobalt-free Sm0.5Sr0.5Fe0.8Cu0.2O3-δ-Ce0.8Sm0.2O2-δ composite cathode for proton-conducting solid oxide fuel cells[J]. Journal of power sources, 2011, 196(5): 2631-2634. DOI:10.1016/j.jpowsour.2010.11.017 (  0) 0) |
| [18] |
FUTAMATA M. A computer-controlled measurement system for electrical conductivity using the van der Pauw method at various temperatures[J]. Measurement science and technology, 1992, 3(9): 919-921. DOI:10.1088/0957-0233/3/9/019 (  0) 0) |
| [19] |
OKIBA T, SATO T, FUJISHIRO F, et al. Preparation of Ba1-xLaxFeO3-δ (x=0.1~0.6) with cubic perovskite phase and random distribution of oxide ion vacancy and their electrical conduction property and thermal expansion behavior[J]. Solid state ionics, 2018, 320: 76-83. DOI:10.1016/j.ssi.2018.02.036 (  0) 0) |
| [20] |
SAWANT P, VARMA S, WANI B N, et al. Synthesis, stability and conductivity of BaCe0.8-xZrxY0.2O3-δ as electrolyte for proton conducting SOFC[J]. International journal of hydrogen energy, 2012, 37(4): 3848-3856. DOI:10.1016/j.ijhydene.2011.04.106 (  0) 0) |
| [21] |
RICHTER J, HOLTAPPELS P, GRAULE T, et al. Materials design for perovskite SOFC cathodes[J]. Monatsh chem, 2009, 140(9): 985-999. DOI:10.1007/s00706-009-0153-3 (  0) 0) |
| [22] |
SHANNON R D. Revised effective ionic radii and systematic studies of interatomic distances in halides and chalcogenides[J]. Acta cryst, 1976, A32: 751-767. (  0) 0) |
| [23] |
CHEN X H, TAO Z T, HOU G H, et al. La0.7Sr0.3FeO3-δ composite cathode enhanced by Sm0.5Sr0.5CoO3-δ impregnation for proton conducting SOFCs[J]. Electrochimica acta, 2015, 165: 142-148. DOI:10.1016/j.electacta.2015.02.237 (  0) 0) |
| [24] |
WANG B, LONG G H, JI Y, et al. Layered perovskite PrBa0.5Sr0.5CoCuO5+δ as a cathode for intermediate-temperature solid oxide fuel cells[J]. Materials research innovations, 2014, 18(S4): 128-131. (  0) 0) |
| [25] |
SUN W P, YAN L T, ZHANG S Q, et al. Crystal structure, electrical conductivity and sintering of Ba0.5Sr0.5ZnxFe1-xO3-δ[J]. Journal of alloys and compounds, 2009, 485(1/2): 872-875. (  0) 0) |
| [26] |
ZHU Z W, QIAN J, WANG Z T, et al. High-performance anode-supported solid oxide fuel cells based on nickel-based cathode and Ba(Zr0.1Ce0.7Y0.2)O3-δ electrolyte[J]. Journal of alloys and compounds, 2013, 581: 832-835. DOI:10.1016/j.jallcom.2013.07.210 (  0) 0) |
| [27] |
KHARTON V V, YAREMCHENKO A A, PATRAKEE M V, et al. Thermal and chemical induced expansion of La0.3Sr0.7(Fe, Ga)O3-δ ceramics[J]. Journal of the European ceramic society, 2003, 23(9): 1417-1426. DOI:10.1016/S0955-2219(02)00308-4 (  0) 0) |
| [28] |
LI N, LV Z, WEI B, et al. Characterization of GdBaCo2O5-δ cathode for IT-SOFCs[J]. Journal of alloys and compounds, 2008, 454(1/2): 274-279. (  0) 0) |
| [29] |
PANG S L, JIANG X N, LI X N, et al. Characterization of Ba-deficient PrBa1-xCo2O5+δ as cathode material for intermediate temperature solid oxide fuel cells[J]. Journal of power sources, 2012, 204: 53-59. DOI:10.1016/j.jpowsour.2012.01.034 (  0) 0) |
| [30] |
JIANG L, WEI T, ZENG R, et al. Thermal and electrochemical properties of PrBa0.5Sr0.5Co2-xFexO5+δ (x=0.5, 1.0, 1.5) cathode materials for solid-oxide fuel cells[J]. Journal of power sources, 2013, 232: 279-285. DOI:10.1016/j.jpowsour.2013.01.064 (  0) 0) |
 2020, Vol. 52
2020, Vol. 52


