2. 郑州大学 公共卫生学院 河南 郑州 450001;
3. 河南省功能分子绿色构建与生物分析国际联合实验室 河南 郑州 450001
2. College of Public Health, Zhengzhou University, Zhengzhou 450001, China;
3. Henan Joint International Research Laboratory of Green Construction of Functional Molecules and Their Bioanalytical Applications, Zhengzhou 450001, China
脱氧雪腐镰刀菌烯醇(deoxynivalenol,DON)又称呕吐毒素,是由禾谷镰刀菌和粉红镰刀菌等真菌产生的次级代谢物,广泛存在于谷类作物中.其性质比较稳定,经过一般的食品加工后仍保留毒性,且毒性会随着人们对谷物的食用进入人体内部,从而对健康造成严重损害.2017年10月27日,在世界卫生组织国际癌症研究机构公布的致癌物清单里,DON位列其中.因此,DON的检测对于人类健康具有重要意义[1-3].传统DON检测方法为酶联免疫吸附分析(ELISA),该方法利用抗原、抗体的特异性结合,再通过酶标反应,被催化成有色产物,根据吸光度的大小进行定量分析.传统的ELISA方法中,通过物理吸附包被在96孔板上的抗原(或抗体)分布不均匀、易脱落,且固相和液相的接触面积相对较小,反应速率慢.近年来分离技术得到迅速发展,尤其是磁分离技术[4-5].以磁性纳米颗粒作为固相载体,一方面,利用磁颗粒实现了固液两相快速分离; 另一方面,由于磁颗粒具有较大的比表面积,增大了反应物的接触面积,从而加快了反应速率.这种新颖的磁性载体为ELISA方法提出了一种新的思路.
Fe3O4纳米颗粒是常用的磁性材料,但其生物相容性较差且容易聚沉,严重影响偶联效率,为此开发新型的磁性材料显得尤为重要.铁蛋白是一种由24个亚基组成的具有铁核的球状天然高分子生物材料,经脱铁处理可得到脱铁铁蛋白(apoferritin,AF).因AF具有特殊的内部空腔结构以及生物矿化过程而成为理想的纳米材料反应器,以其为模板合成纳米材料的技术逐渐成为研究热点[6-8].文献[9]通过调节硫代乙酸的浓度,控制AF空腔内所合成硫化铜尺寸的大小,成功制备出硫化铜半导体纳米颗粒; 文献[10]通过控制金离子复合物缓慢的矿化过程,在AF空腔内合成了金纳米阵列.另外,AF的外表面具有氨基、羧基、巯基等可供修饰且具有特殊功能的基团,易标记一些配体作为识别目标物的探针.因此,该研究拟利用AF为生物反应器,通过矿化过程在AF空腔内合成具有磁性的Fe3O4,得到AF@Fe3O4.然后,利用AF表面的活性基团与抗原DON结合,制备人工抗原DON免疫磁性铁蛋白复合物(DON@AF@Fe3O4).该复合物生物相容性好、尺寸单一,磁响应性较好且易于分离纯化,其表面通过化学反应结合的抗原不易脱落,具有良好的免疫原性,可用于磁酶联免疫吸附分析中,既解决了传统ELISA中抗原易脱落的问题,又克服了磁性Fe3O4纳米颗粒易聚沉且生物相容性差的缺点,为磁酶联免疫吸附分析法检测DON奠定了基础.
1 实验部分 1.1 主要试剂与仪器AF(37 g/L,Sigma),硫酸亚铁铵、3-[(1,1-二甲基-2-羟乙基)氨基]-2-羟基-丙磺酸(AMPSO)、三甲基氮氧化物(Me3NO)、羧基二咪唑(CDI)(国药集团化学试剂有限公司); 所用试剂均为分析纯,实验用水均为MilliQ水.
场发射扫描电子显微镜(JSM-6700F),紫外可见分光光谱仪(UV-2450),酶标仪(TECAN),电感耦合等离子体质谱仪(NexION 300X),电子自旋共振波谱仪(A300),电热恒温鼓风干燥箱(DHG-9146A),透析袋(Sigma).
1.2 实验方法 1.2.1 磁性铁蛋白颗粒的制备根据文献[11-12], 利用AF生物模板法合成Fe3O4或者Fe2O3磁性颗粒,其反应过程为:3Fe2++2Me3NO+4H2O→Fe3O4+2Me3N+6H++H2O2.通过控制总铁量和Me3NO配比、反应pH、反应物浓度、反应温度以及加料、搅拌方式等,在AF空腔内部生成Fe3O4或者Fe2O3磁性颗粒,用磁性分离器进行分离, 然后用MilliQ水洗涤至中性备用.合成步骤如下:取配制好的AMPSO溶液100 mL,用N2除氧1 h并持续搅拌.然后加入20 mg AF,加热至65 ℃.保持整个反应发生在N2条件下且持续搅拌. AF均匀分散后,使用密封微量注射器逐滴滴加Fe2+和Me3NO溶液,使其比值为3:2.第1次时,只滴加Fe2+,不滴加Me3NO.从第2次开始,先滴加Fe2+,然后再滴加Me3NO,每次滴加完毕后反应20 min,共循环9次.反应完成后,使用磁性分离器分离所合成的磁性铁蛋白并浓缩至5 mL,在4 ℃下用双蒸水进行透析,每天更换蒸馏水两次,透析3 d,透析结束后保存于4 ℃冰箱中备用.
1.2.2 DON@AF@Fe3O4复合颗粒的制备采用羧基二咪唑法合成DON免疫磁性复合颗粒,以合成的磁性铁蛋白作为化学发光免疫分析中的固相载体,并将所制备的DON@AF@Fe3O4复合颗粒作为化学发光酶免疫分析方法中的人工抗原.具体制备过程如下:将1 mg DON(296.3 g/mol)溶于500 μL丙酮中,再加入10 mg CDI, 室温振荡反应1 h.反应完成后,在反应瓶中滴加20 μL去离子水,迅速向反应瓶中通入N2,挥干其中的丙酮,然后加入16 mg AF@Fe3O4(溶于500 μL,0.1 mol/L,pH 9.6的碳酸盐缓冲溶液),4 ℃下搅拌反应过夜.反应完成后,在PBS缓冲液(0.01 mol/L,pH 7.4)中透析72 h,每天更换溶液2次,透析结束后保存于4 ℃冰箱中备用.
2 结果与讨论 2.1 磁性铁蛋白AF@Fe3O4的表征 2.1.1 磁性分析磁性分离前后的AF@Fe3O4如图 1所示.左瓶是磁性分离前的溶液,右瓶是磁性分离后的溶液,将磁铁置于瓶的底部,磁性铁蛋白纳米颗粒因磁铁的引力作用而迅速沉降至瓶的底部,瓶内上清液澄清透明,分离效果良好,这表明合成的磁性铁蛋白具有良好的磁性.

|
图 1 磁性分离前后的AF@Fe3O4 Fig. 1 AF@Fe3O4 before and after magnetic separation |
在电子顺磁共振器中,若在垂直于恒磁场的方向上附加一个适当频率的交变磁场,当产生的能量等于某两个能级的能量差时,电子将会吸收该交变磁场的能量从而发生跃迁, 交变磁场的能量将会减少,这种现象称为共振吸收.产生共振吸收时必须满足以下关系式:
| $ h{\rm{ }}\upsilon = g\beta B $ |
式中:g为朗德因子; β为玻尔磁子; υ为频率; B为共振磁场.
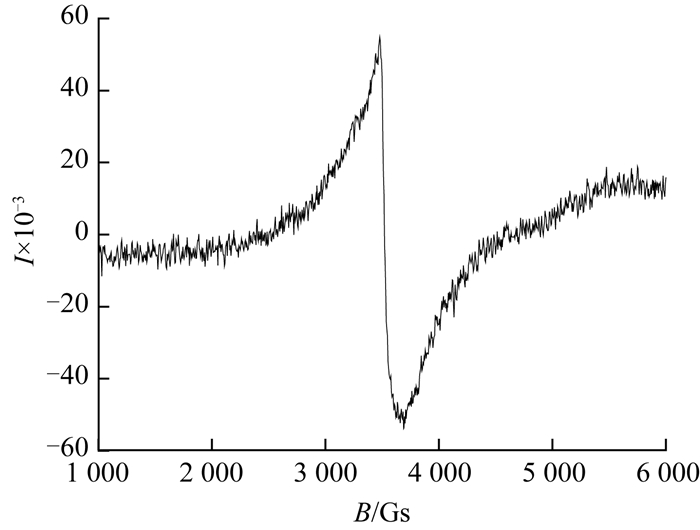
在该共振表达式中,朗德因子g是一个无量纲数,它是由轨道量子数、自旋量子数和总量子数决定的.不同的物质由于轨道角动量与自旋角动量的耦合作用不同,朗德因子g也会各不相同,它反映了不同物质的结构特征,在实验中需要测得样品朗德因子g的具体数值来确定其结构特征.本实验中磁性铁蛋白的电子自旋共振波谱图如图 2所示.
|
图 2 AF@Fe3O4的电子自旋共振波谱 Fig. 2 Electron spins resonance spectra of AF@Fe3O4 |
由原子物理可知,当朗德因子g=2时,原子磁矩完全由电子轨道磁矩贡献.本实验中,通过测量AF@Fe3O4的电子自旋共振波谱可以得到频率υ=9.847 7 GHz,从而计算出朗德因子g=1.998 3,非常接近于2.因此,可知所合成的磁性铁蛋白具有顺磁性.
2.1.3 扫描电镜图 3为AF和AF@Fe3O4的扫描电镜图.从图中可以看出,与AF相比,AF@Fe3O4的尺寸明显变大,粒径大小约为20 nm. AF@Fe3O4内部具有较高的电子密度,其轮廓比AF更加清晰.由于AF@Fe3O4具有磁性引力,所以从扫描电镜图中可以看到AF@Fe3O4颗粒之间有一定程度的聚集.因此,可以推测成功合成了磁性铁蛋白.

|
图 3 AF和AF@Fe3O4的扫描电镜图 Fig. 3 SEM image of AF and AF@Fe3O4 |
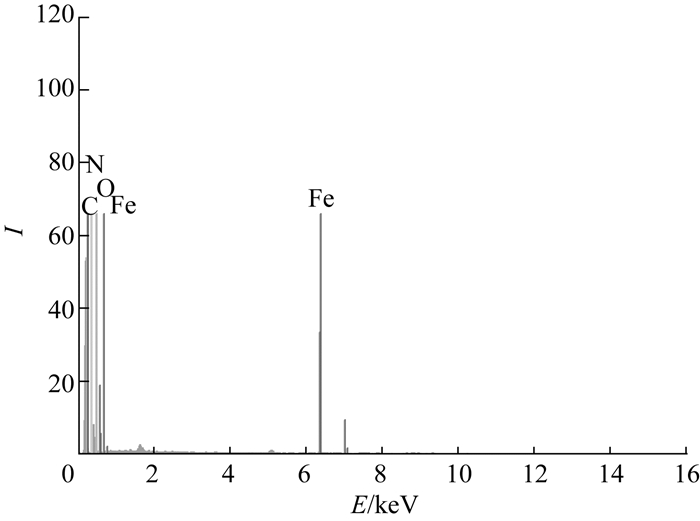
该实验通过矿化过程将Fe2+包载于AF的空腔内部.为了证实蛋白腔内部的元素组成,对所合成的AF@Fe3O4进行了EDX元素分析,结果如图 4所示.可以看出,蛋白腔内部含有铁、氧元素.结合磁性分析,推测铁、氧元素在AF的空腔内部以Fe2O3或Fe3O4的形式存在.
|
图 4 AF@Fe3O4的EDX谱 Fig. 4 EDX image of AF@Fe3O4 |
称取已干燥至恒重的AF@Fe3O4(准确至0.001 g)于瓷坩埚中,置电炉上低温碳化变黑后,加入0.9 mL浓H2SO4,重置电炉上碳化,待浓烟挥尽后,放入马弗炉(500 ℃)中使灰化完全,取出,冷却后加体积比1:1盐酸溶液2 mL,置水浴上加热至干,将生成的氯化盐加水溶解,用玻璃棒将溶液转移备用.通过电感耦合等离子体质谱仪(ICP-MS)检测出溶液中铁的质量浓度为46 mg/L,经过计算可以得到AF中铁原子载入量为791.
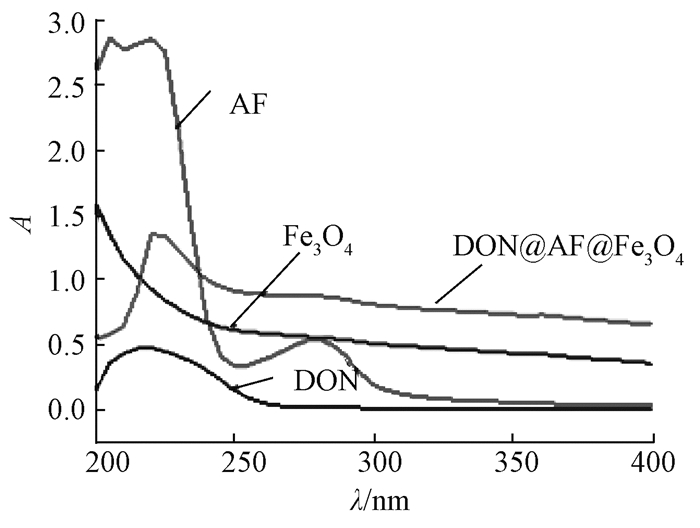
2.2 DON免疫磁性铁蛋白的表征 2.2.1 紫外吸收光谱分别对AF、DON、Fe3O4、DON@AF@Fe3O4进行紫外吸收光谱扫描,扫描波长范围为200~400 nm,结果如图 5所示.可以看出,AF在280 nm处有强的特征吸收峰,因为蛋白中有肽键的存在,所以在200~250 nm内有杂峰; DON在200~250 nm处有宽的吸收峰; 裸露的Fe3O4颗粒没有吸收峰; 制备的DON@AF@Fe3O4在280 nm附近有不明显的吸收峰.这与文献[13]中报道的AF包载物质以后特征吸收峰由强峰变为肩峰的结果一致,可能是由于Fe3O4的影响,280 nm处的吸收峰变平; DON@AF@Fe3O4在225 nm处有强的吸收峰,这可能是由于DON@AF@Fe3O4中DON或AF或DON和AF的吸收,表明人工抗原偶联成功.
|
图 5 DON@AF@Fe3O4的紫外吸收光谱 Fig. 5 UV spectra of DON@AF@Fe3O4 |
ELISA方法是以抗原(或抗体)的固相化和抗体(或抗原)的酶标记为基础.包被在固相载体上的人工抗原通常具有免疫活性,酶标抗体(或抗原)兼具有免疫活性和酶活性.当检测目标物为抗原时,加入的待测抗原与固相载体上的抗原竞争结合单抗,随后加入酶标二抗与单抗结合,通过洗涤除去未作用的酶标二抗,最后加入酶反应底物,底物将被酶催化成有色产物,而有色产物的量与待测抗原的量直接相关.因此,可以根据吸光度的大小对待测抗原进行定量分析.
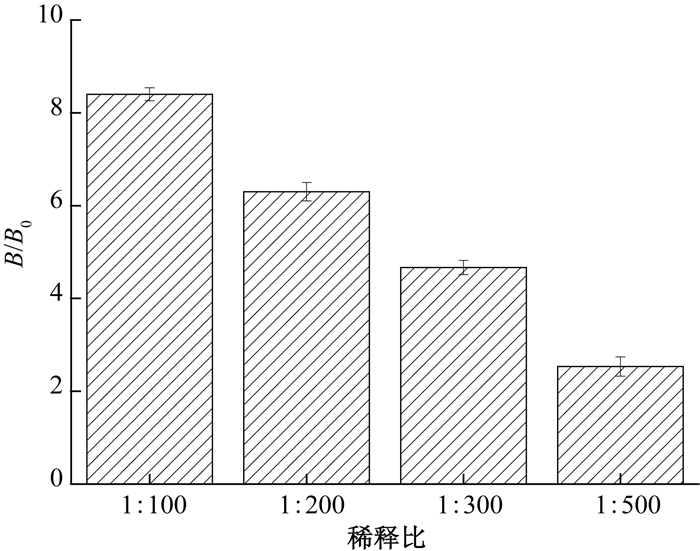
鉴于此,本实验采用不同稀释比进行ELISA方法表征人工抗原DON@AF@Fe3O4.首先采用单抗识别人工抗原DON@AF@Fe3O4,通过洗涤除去未作用的单抗后,进一步在体系中加入酶标二抗,洗涤后加入底物进行显色反应,ELISA表征结果如图 6所示.可以看出,随着稀释比的增大,吸光度阳性/空白值(B/B0)降低,表明人工抗原DON@AF@Fe3O4具备免疫活性.结合扫描电镜、紫外吸收光谱、EDX元素分析的结果,进一步证明人工抗原DON@AF@Fe3O4制备成功.
|
图 6 DON@AF@Fe3O4的ELISA表征 Fig. 6 ELISA characteritation of DON@AF@Fe3O4 |
通过蛋白分子模板法合成了易标记、生物相容性好的磁性铁蛋白AF@Fe3O4,采用磁性分析、扫描电镜、EDX元素分析、电子自旋共振波谱进行表征,结果表明,所合成的磁性铁蛋白具有良好的磁性,蛋白腔体内部含有铁元素和氧元素,AF@Fe3O4的粒径大小约为20 nm,ICP-MS检测出AF的铁原子载入量为791.选择羧基二咪唑法制备人工抗原DON@AF@Fe3O4,通过紫外吸收光谱和ELISA方法对合成的人工抗原进行表征,证明DON@AF@Fe3O4复合物偶联成功,且具有免疫原性.制备的DON@AF@Fe3O4将生物相容性与磁性有机结合,可实现固液快速分离且保持良好的免疫原性,为后续磁酶联免疫吸附分析提出了一种新的思路.
| [1] |
吴振兴, 鲍蕾, 静平, 等. 小麦和玉米中脱氧雪腐镰刀菌烯醇与雪腐镰刀菌烯醇的免疫亲和净化-高效液相色谱检测方法研究[J]. 食品安全质量检测学报, 2014, 5(12): 3848-3852. (  0) 0) |
| [2] |
王伟, 刘安法, 李明奇, 等. 免疫亲和柱净化-高效液相色谱法检测小麦中的脱氧雪腐镰刀菌烯醇[J]. 粮食与饲料工业, 2013, 12(1): 60-61. (  0) 0) |
| [3] |
SHAR Z H, SUMBAL G A, SHERAZI S T H, et al. Determination of deoxynivalenol in poultry feed by three gas chromatographic detection techniques[J]. Chromatographia, 2014, 77(3/4): 337-346. (  0) 0) |
| [4] |
ZHANG H S, QI S W. A rapid and sensitive chemiluminescence immunoassay based on magnetic particles for squamous cell carcinoma antigen in human serum[J]. Clinica chimica acta, 2011, 412(17/18): 1572-1577. (  0) 0) |
| [5] |
XIAO Q, LI H F, LIN J M. Development of a highly sensitive magnetic particle-based chemiluminescence enzyme immunoassay for thyroid stimulating hormone and comparison with two other immunoassays[J]. Clinica chimica acta, 2010, 411(15/16): 1151-1153. (  0) 0) |
| [6] |
SUN C J, YANG H, YUAN Y, et al. Controlling assembly of paired gold clusters within apoferritin nanoreactor for in vivo kidney targeting and biomedical imaging[J]. Journal of the American chemical society, 2011, 133(22): 8617-8624. DOI:10.1021/ja200746p (  0) 0) |
| [7] |
XING R M, WANG X Y, YAN L L, et al. Fabrication of water soluble and biocompatible CdSe nanoparticles in apoferritin with the aid of EDTA[J]. Dalton transactions, 2009, 10(10): 1710-1713. (  0) 0) |
| [8] |
NAITO M, IWAHORI K, MIURA A, et al. Circularly polarized luminescent CdS quantum dots prepared in a protein nanocage[J]. Angewandte chemie, 2010, 49(39): 7006-7009. DOI:10.1002/anie.201002552 (  0) 0) |
| [9] |
NOBUSAWA K, OKAMOTO N, LIN X, et al. Dispersed gold nanoparticle array produced by apoferritins utilizing biomineralization and chemical conversion[J]. Journal of the American chemical society, 2017, 2(4): 1424-1430. (  0) 0) |
| [10] |
IWAHORI K, TAKAGI R, KISHIMOTO N, et al. A size controlled synthesis of CuS nano-particles in the protein cage, apoferritin[J]. Materials letters, 2011, 65(21/22): 3245-3247. (  0) 0) |
| [11] |
MARTINEZ-PÉREZ M J, MIGUEL R, CARBONERA C, et al. Size-dependent properties of magnetoferritin[J]. Nanotechnology, 2010, 21(46): 465707. DOI:10.1088/0957-4484/21/46/465707 (  0) 0) |
| [12] |
MITROOVA Z, BALEJCIKOVA L, KOVAC J, et al. Synthesis and characterization of magnetoferritin[J]. Acta physica polonica, 2012, 121(5): 1318-1320. (  0) 0) |
| [13] |
RUOZI B, VERATTI P, VANDELLI M A, et al. Apoferritin nanocage as streptomycin drug reservoir: technological optimization of a new drug delivery system[J]. International journal of pharmaceutics, 2017, 518(1/2): 281-288. (  0) 0) |
 2019, Vol. 51
2019, Vol. 51


