| 急性或亚急性骨质疏松性椎体压缩骨折后骨髓水肿MRI信号变化分析 |
2. 山东中医药大学第二附属医院骨科,山东 济南 250012;
3a. 山东省威海卫人民医院脊柱外科,山东 威海 261002;
3b. 山东省威海卫人民医院重症医学科,山东 威海 261002
随着社会人口老龄化,骨质疏松导致的椎体压缩骨折呈增多趋势。据报道[1],全世界每年有890多万患者发生骨质疏松性骨折,其中40%为骨质疏松性椎体压缩骨折(osteoporotic vertebral compression fractures,OVCFs)。骨髓水肿是诊断急性或亚急性OVCFs的金标准[2]。MRI T1WI和T2WI在骨髓水肿的检出中发挥了重要作用[3]。目前,仅少数研究[4-5]对骨髓水肿在急性或亚急性OVCFs中的价值进行评价。因此,本研究目的是分析骨髓水肿MRI信号变化特征,探讨其对OVCFs患者椎体骨折愈合的判断价值及其在临床康复治疗中的意义。
1 资料与方法 1.1 一般资料选取山东中医药大学第二附属医院2013年6月至2018年10月收治的125例(168节椎体)OVCFs患者,其中男35例,女90例。所有患者均行脊柱MRI检查,并证实存在骨髓水肿。入选标准:①年龄>50岁;②轻微外伤后背痛≤3个月;③骨密度T值≤-2.5;④具有完整的临床资料。排除标准:既往行椎体成形术或患脊柱感染、妊娠、肥胖、脊柱畸形、椎体肿瘤者或MRI禁忌证者。
根据骨折时间,分为4期:Ⅰ期(0~15 d);Ⅱ期(16~30 d);Ⅲ期(31~60 d);Ⅳ期(61~90 d)。各期OVCFs临床资料见表 1。本研究得到医院伦理委员会的批准,患者均签订知情同意书。
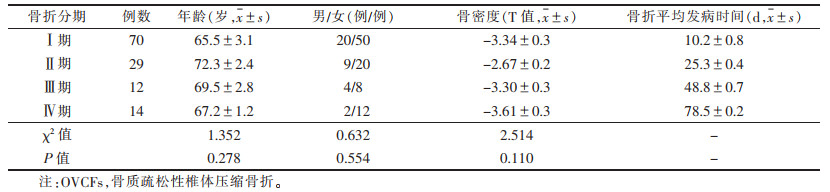
| 表 1 各期OVCFs临床资料比较 |
 |
1.2 仪器与方法
采用GE Signa 1.5 T MRI扫描仪。矢状位T1WI、T2WI和STIR序列均采用快速自旋回波技术获得。由2名放射科医师(分别有8年和6年的脊柱影像阅片经验)对脊柱MRI图像进行独立的回顾性检查,结果不一致时经协商解决。
1.3 骨髓水肿评估椎体骨髓水肿定义为骨折椎体T1WI低信号,T2WI和STIR高信号[6]。选取椎体中心矢状位图像进行分析,记录骨髓水肿的位置、形态和强度。根据T1WI上骨髓水肿在椎体中所占比例,参考VOORMOLEN等[7]的研究将其分为3类:轻度(1% ~24%)、中度(25% ~74%)和重度(75%~100%)。
1.4 椎体形态测定根据矢状位图像上骨折椎体压缩最明显处前、中、后缘的高度[8],将椎体畸形分为4种类型:无变化型、楔型、双凹型和粉碎型骨折。
1.5 统计学分析采用SPSS 20.0统计软件行数据分析。定量资料以x±s表示,定性资料以百分比(%)表示。多组间比较采用单因素方差分析,定性资料比较采用χ2检验。所有因素均纳入Logistic回归分析。以P<0.05为差异有统计学意义。
2 结果 2.1 一般资料125例中,Ⅰ期70例(83节),Ⅱ期29例(41节),Ⅲ期12例(20节),Ⅳ期14例(24节)。各期年龄、性别比例、骨密度比较,差异均无统计学意义(均P>0.05)(表 1)。
168节伤椎中,胸椎77节(T7 7节,T8 7节,T10 8节,T11 16节,T12 39节),腰椎91节(L1 34节,L2 21节,L3 15节,L4 10节,L5 11节),胸腰段(T10~L2)发生率高达70.2%(118/168)。
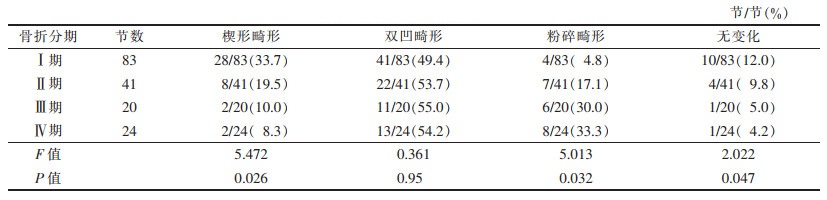
2.2 骨折椎体形态改变168节伤椎中,楔形畸形40节(23.8%),双凹畸形87节(51.8%),粉碎畸形25节(14.9%),16节(9.5%)椎体无明显改变。随着病程延长,楔形畸形由33.7%降至8.3%,椎体形态无变化由12.0%降至4.2%,椎体粉碎畸形由4.8%升至33.3%,差异均有统计学意义(均P<0.050.05)(表 2)。
| 表 2 骨折椎体形态分析 |
 |
2.3 骨髓水肿特征
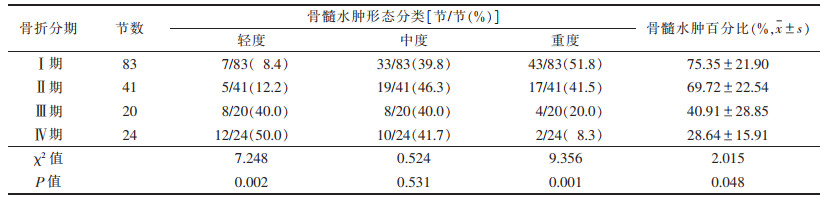
168节椎体中,轻度骨髓水肿32节,中度70节,重度66节。随时间推移,骨髓水肿信号强度逐渐由均匀向非均匀转变,信号范围逐渐减小,边界逐渐清晰;轻度骨髓水肿发生率由8.4%升至50.0%,重度由51.8%降至8.3%,差异均有统计学意义(均P<0.050.05)(表 3)。①Ⅰ期:骨髓水肿比例迅速上升,达到峰值。T1WI、T2WI信号均匀分布,T1WI呈低信号,T2WI和STIR呈高信号,扩散至正常骨髓,呈弥漫性、均匀性、边界不清的形态分布(图 1)。②Ⅱ期:信号分布变得不均匀,水肿范围逐渐受限,并出现点、片状T1WI低信号,T2WI和STIR高信号(图 2)。③Ⅲ期:骨髓水肿较前一期下降,水肿范围局限于骨折区,信号混杂;部分椎体T1WI呈等、低信号,T2WI及STIR呈低、等、高信号(图 3)。④Ⅳ期:骨髓水肿百分比降至最低。T1WI骨折区可见低信号区,边界清晰。T2WI和STIR信号与相邻正常椎体相同(图 4)。
| 表 3 T1WI上的椎体骨髓水肿形态分类 |
 |
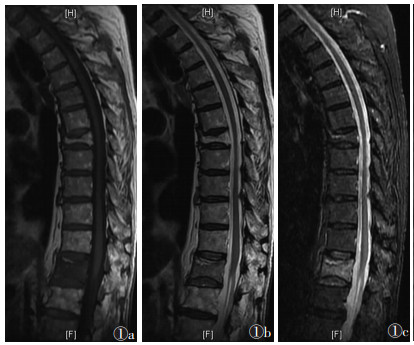 |
| 图 1 男,85岁,Ⅰ期骨质疏松性椎体压缩骨折(OVCFs)。MRI示骨折位于T12,T1WI(图 1a)呈均匀低信号,T2WI(图 1b)和STIR(图 1c)呈均匀高信号。上终板下方线性透亮影表示断裂线,T12呈双凹畸形 |
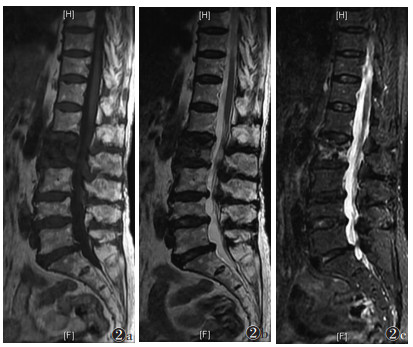 |
| 图 2 女,75岁,Ⅱ期OVCFs,L2骨折。MRI示明显混合信号,T1WI(图 2a)呈不均匀低信号,T2WI(图 2b)及STIR(图 2c)呈不均匀高信号 |
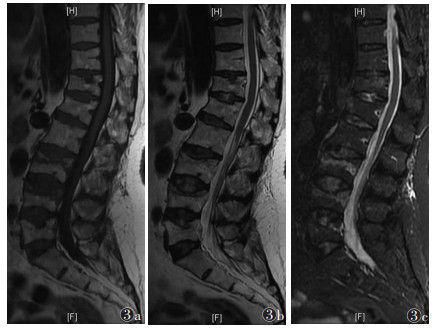 |
| 图 3 女,69岁,Ⅲ期OVCFs。MRI示骨折位于L3和L4,双凹畸形,MRI示T1WI(图 3a)呈稍低信号,T2WI(图 3b)及STIR(图 3c)均呈稍高信号,矢状位示水肿信号范围缩小至骨折线附近 |
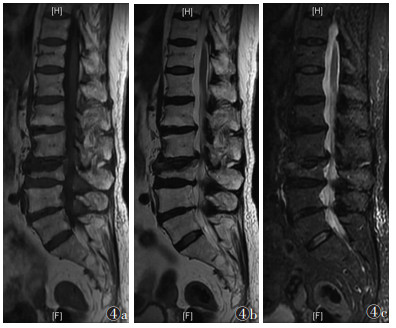 |
| 图 4 女,77岁,Ⅳ期OVCFs。MRI示骨折位于L3,T1WI(图 4a)呈低信号,T2WI(图 4b)及STIR(图 4c)呈等或稍高信号,边界清晰 |
3 讨论
松质骨骨折愈合方式与皮质骨不同,其愈合过程中无明显的类似皮质骨的骨痂形成[9]。传统的X线平片或CT检查不易判断骨折处于哪个阶段,而MRI对松质骨骨折后骨髓内创伤修复的病理改变,以及骨折椎体中骨髓水肿的存在、位置和程度非常敏感[10],明显优于其他检查。张淑娴等[11]利用兔的椎体骨折愈合模型观察其病理变化特点,并与MRI进行对比分析,认为MRI在一定程度上可反映骨折愈合过程。
骨折椎体中的骨髓水肿不仅被认为是急性或亚急性OVCFs的特征,且是经皮椎体成形术/经皮后凸成形术术后疼痛缓解良好反应的一个强有力的预测因子[12-16]。矢状位T1WI示早期骨髓水肿程度与后期随访椎体畸形类型显著相关[17]。
创伤后不久,骨髓中产生血肿,骨髓含水量增加,导致T1和T2弛豫时间延长,T1WI呈低信号,T2WI和STIR均呈高信号。这种急性期的病理改变常范围很广,并不局限于骨折线。因此,MRI上的骨髓水肿信号呈弥漫性、均匀性和边界不清的形态学分布。本研究创伤后2周内水肿期信号最高,随时间推移,水肿和出血逐渐被吸收。骨折后2~4周内,水肿逐渐吸收,成纤维细胞增殖,新生毛细血管增生,血肿开始机化,纤维蛋白增生,形成肉芽组织和局灶性软骨组织[18]。肉芽组织的MRI信号与水肿不同,其T1WI呈低或等信号,T2WI和STIR呈略高信号。另外,肉芽组织和纤维软骨分散分布和成熟度的差异使信号不均匀,表现为斑片状、点状或条状形态分布,边界逐渐清晰。这一阶段MRI信号的变化主要反映骨折早期病理改变。骨折后4~8周内,骨小梁增多,大量类骨样组织形成,钙盐沉积,进一步降低了局部信号,使得MRI高信号面积大幅度缩小,集中于骨折线附近。然而,由于部分椎体内坏死液化组织的出现,引起相应区域异常高信号,因此MRI呈混杂信号,表明松质骨骨折尚未完全愈合。骨折后8~12周内骨小梁趋于成熟,水肿吸收,血肿清除,T1WI上可见边界清晰的低信号影,考虑是骨折修复后的痕迹,T2WI和STIR上高信号大部分消失,与相邻正常椎体信号相同。
近年来,虽然保守治疗对大多数OVCFs患者效果良好[19-20],但椎体成形术等微创脊柱手术已在临床得到广泛应用,并已被证明对OVCFs有效[21]。Ⅰ期处于急性水肿期,应及时给予保守治疗(包括止痛药物、卧床休息、外固定支架)或手术治疗(椎体成形术);Ⅱ期、Ⅲ期均为骨折修复期,不宜早期负重,可继续保守治疗或尽早手术;Ⅳ期骨折大部分基本愈合,症状消失,功能锻炼可逐步开始。若部分骨折椎体后期存在后凸畸形或空隙征,导致持续慢性症状,可酌情行经椎弓根截骨术或椎体成形术等。
总之,骨髓水肿的MRI信号变化在一定程度上可反映病理变化,对于评估OVCFs患者椎体骨折的愈合情况及继发性病理改变有很大帮助。
| [1] |
JOHNELLl O, KANIS J A. An estimate of the worldwide prevalence and disability associated with osteoporotic fractures[J]. Osteoporos Int, 2006, 17(12): 1726-1733. DOI:10.1007/s00198-006-0172-4 |
| [2] |
JUNG H S, JEE W H, MCCAULEY T R, et al. Discrimination of metastatic from acute osteoporotic compression spinal fractures with MR imaging[J]. Radiographics, 2003, 23(1): 179-187. DOI:10.1148/rg.231025043 |
| [3] |
BROWN D B, GLAIBERMAN C B, GILULA L A, et al. Correlation between preprocedural MRI findings and clinical outcomes in the treatment of chronic symptomatic vertebral compression fractures with percutaneous vertebroplasty[J]. AJR Am J Roentgenol, 2005, 184(6): 1951-1955. DOI:10.2214/ajr.184.6.01841951 |
| [4] |
TANIGAWA N, KOMEMUSHI A, KARYA S, et al. Percutaneous vertebroplasty:relationship between vertebral body bone marrow edema pattern on MR images and initial clinical response[J]. Radiology, 2006, 239(1): 195-200. |
| [5] |
YANG H L, WANG G L, NIU G Q, et al. Using MRI to determine painful vertebrae to be treated by kyphoplasty in multiplelevel vertebral compression fractures:a prospective study[J]. J Int Med Res, 2008, 36(5): 1056-1063. DOI:10.1177/147323000803600524 |
| [6] |
PIAZZOLLA A, SOLARINO G, LAMARTINA C, et al. Vertebral bone marrow edema (VBME) in conservatively treated acute vertebral compression fractures (VCFs):evolution and clinical correlations[J]. Spine, 2015, 40(14): E842-E848. DOI:10.1097/BRS.0000000000000973 |
| [7] |
VOORMOLEN M H J, ROOIJ W J, GRAAF Y V, et al. Bone marrow edema in osteoporotic vertebral compression fractures after percutaneous vertebroplasty and relation with clinical outcome[J]. Am J Neuroradiol, 2006, 27(5): 983-988. |
| [8] |
LENCHIK L, ROGERS L F, DELMAS P D, et al. Diagnosis of osteoporotic vertebral fractures :importance of recognition and description by radiologists[J]. AJR Am J Roentgenol, 2004, 183(4): 949-958. DOI:10.2214/ajr.183.4.1830949 |
| [9] |
李勇刚, 王仁法, 黄晓琳, 等. 磁共振成像在椎体骨折与康复评估中的临床应用[J]. 中华物理医学与康复杂志, 2004, 26(3): 176179. |
| [10] |
郭献日, 李又成, 李建策, 等. MRI对椎体骨折的诊断价值[J]. 放射学实践, 2006, 21(9): 945-947. |
| [11] |
张淑娴, 王雪芹, 王超, 等. 磁共振成像在兔椎体骨折及愈合评估中的应用[J]. 实用放射学杂志, 2014, 30(2): 313-315. |
| [12] |
DO H M. Magnetic resonance imaging in the evaluation of patients for percutaneous vertebroplasty[J]. Top Magn Reson Imaging, 2000, 11(4): 235-244. |
| [13] |
MODIC M T, STEINBERG P M, ROSS J S, et al. Degenerative disk disease:assessment of changes in vertebral body marrow with MR imaging[J]. Radiology, 1988, 166: 193-199. DOI:10.1148/radiology.166.1.3336678 |
| [14] |
BAKER L L, GOODMAN S B, PERKASH I, et al. Benign versus pathologic compression fractures of vertebral bodies:assessment with conventional spin-echo, chemical-shift, and STIR MR imaging[J]. Radiology, 1990, 174(2): 495-502. |
| [15] |
YAMATO M, NISHIMURA G, KURAMOCHI E, et al. MR appearance at different ages of osteoporotic compression fractures of the vertebrae[J]. Radiat Med, 1998, 16(5): 329-334. |
| [16] |
VOORMOLEN M H J, ROOIJ W J V, SLUZEWSHI M, et al. Pain response in the first trimester after percutaneous vertebroplasty in patients with osteoporotic vertebral compression fractures with or without bone marrow edema[J]. Am J Neuroradiol, 2006, 27(7): 1579-1585. |
| [17] |
EUN A S, NAM R K, SEON P J, et al. Early bone marrow edema pattern of the osteoporotic vertebral compression fracture: can be predictor of vertebral deformity types and prognosis?[J]. J Korean Neurosurg Soc, 2016, 59(2): 137-142. DOI:10.3340/jkns.2016.59.2.137 |
| [18] |
GREENBAUM M A, KANAT I O. Current concepts in bone healing. Review of the literature[J]. J Am Podiatr Med Assoc, 1993, 83(3): 123-129. DOI:10.7547/87507315-83-3-123 |
| [19] |
KIM D H, VACCARO A R. Osteoporotic compression fractures of the spine; current options and considerations for treatment[J]. Spine J, 2006, 6(5): 479-487. |
| [20] |
VENMANS A, KLAZEN C A, LOHLE P N, et al. Natural history of pain in patients with conservatively treated osteoporotic vertebral compression fractures:results from VERTOS Ⅱ[J]. Am J Neuroradiol, 2012, 33(3): 519-521. DOI:10.3174/ajnr.A2817 |
| [21] |
KASPERK C, HILLMEIER J, NOLDGE G, et al. Treatment of painful vertebral fractures by kyphoplasty in patients with primary osteoporosis:a prospective nonrandomized controlled study[J]. J Bone Miner Res, 2005, 20(4): 604-612. |
 2020, Vol. 18
2020, Vol. 18


