| 磨玻璃密度肺结节的CT诊断 |
2. 复旦大学附属中山医院放射诊断科,上海 200032
随着医学影像学诊断及技术的发展,胸部CT在临床检查中的应用越来越广泛,肺内细微结构显示愈加清晰,肺结节检出率越来越高。其中,磨玻璃密度肺结节(ground-glass nodule,GGN)占19%~38%[1],准确诊断和风险分析是制订个体化临床处理策略的基础。笔者从分类、CT技术、CT征象及病理基础、新技术应用等方面对GGN进行总结,以期为其CT诊断提供思路。
1 GGN概述 1.1 定义GGN又称亚实性结节,影像学上定义为CT肺窗上观察到的肺内局部CT值轻度增加区域,边界清或不清,类似絮状或云雾状,不掩盖其下的正常肺实质、支气管、血管等结构[2]。
1.2 分类 1.2.1 影像学分类影像学上以病灶在CT纵隔窗能否显示实性成分将GGN分为[3]:①纯GGN,不包含实性成分(图 1);②部分实性GGN,既有磨玻璃密度成分,也有实性成分(图 2)。
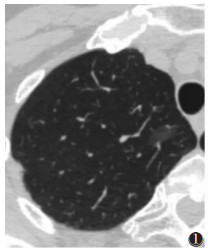 |
| 图 1 女,60岁,右肺上叶微浸润腺癌,右肺上叶纯磨玻璃密度结节,边界清楚,密度均匀 |
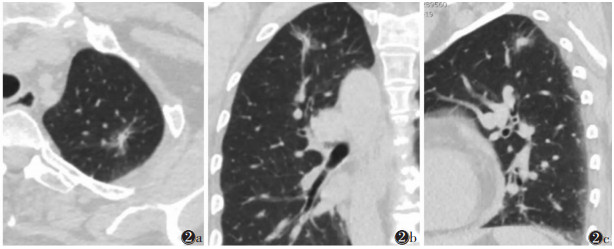 |
| 图 2 女,66岁,左肺上叶浸润性腺癌 图 2a~2c 左肺上叶尖后端部分实性磨玻璃密度结节,边界清,边缘见分叶 |
1.2.2 病理学分类
GGN的病理基础为肺泡腔的不完全填充、肺泡间隔增厚、肺泡部分塌陷及毛细血管血容量增加[4]。良性GGN主要包括肺出血、局部纤维化、炎症等,经短期随访或早期治疗后,复查可观察到病灶吸收或缩小。恶性或潜在恶性倾向的GGN多为腺癌或癌前病变。国际肺癌研究学会、美国胸科学会和欧洲呼吸学会提出病理学、影像学、分子生物学及临床诸学科的腺癌综合诊断标准,并公布了2011年肺腺癌的国际多学科新分类方案,将腺癌分为非黏液型和黏液型,其中,非黏液型腺癌占90%以上。根据病变的侵袭性,恶性或潜在恶性倾向的GGN可分为4类:非典型腺瘤样增生(atypical adenomatous hyperplasia,AAH)、原位腺癌(adenocarcinoma in situ,AIS)、微浸润腺癌(minimally invasive adenocarcinoma,MIA)和浸润腺腺癌(invasive adenocarcinoma,IA)。在最新公布的WHO肺肿瘤组织学分类中(2021年3月),AAH和AIS为腺体前驱病变,存在潜在恶性倾向。影像学诊断的意义在于准确判断GGN的良恶性,并对可疑恶性病灶进行风险分级,为制订治疗或随访方案提供依据。
2 CT技术 2.1 常规扫描MDCT是目前临床上检测GGN最常用的方法,极大地提升了扫描速度及扫描容积,改善了图像z轴方向的分辨力,减少了部分容积效应的影响,可更清晰展现GGN的细节特征,提高结节检测的敏感度及特异度。一般扫描参数为120 kV、250 mAs。对于含实性成分的GGN,增强扫描可观察病灶的动脉血供及血管走行。常规增强扫描是在注入水溶性有机碘对比剂后,按普通扫描方法于25、75 s行动脉期和静脉期扫描,获取病灶的动脉血供和组织灌注的初步信息。
随着肺癌筛查的普及,受检者范围扩大、检查频率升高,对CT辐射剂量的要求更高,低剂量CT可降低管电流,从而降低辐射剂量,扫描参数为120 kV,40~100 mAs(智能D-right)。低剂量CT采用迭代重建算法可有效降低图像噪声,弥补低剂量扫描的噪声,提升图像质量使其满足诊断需求[5]。
2.2 精准扫描 2.2.1 高分辨力CT扫描高分辨力CT扫描可显示结节的细微结构,利用薄层扫描及高分辨算法重建获得容积扫描数据,可行MPR、CPR、MIP、MinIP、表面遮盖(SSD)和VR等后处理[6]。
2.2.2 靶扫描[7]靶扫描可精确显示结节的边界,采用小视野(以病灶为中心,上下各加3 cm),大矩阵(512×512),肺窗,层厚1 mm,层距1 mm。超高分辨力靶扫描即在靶扫描的基础上使用更薄层及更高分辨率算法,一般扫描参数为120 kV、300 mAs,超大矩阵(1 024×1 024),层厚0.8~1 mm,层距0.4~0.5 mm。
2.3 特殊扫描当GGN位于背侧胸膜下或膈肌附近,因重力所致的坠积效应影响观察时,可变换患者体位配合呼吸以显示结节,如让患者侧躺深吸气后屏住呼吸再扫描,称作生理通气G方案[8]。
3 CT征象及病理基础GGN的CT征象有助于判断其良恶性及侵袭性,本文结合Fleischner协会胸部成像术语表[9]及各类文献,对各种CT征象及其病理基础作总结。2017年Fleischner协会肺结节指南中[10],对首次发现的肺结节行3~6个月复查,原因为炎性结节可在3个月内发生显著变化;中华医学会肺癌临床诊疗指南指出对于首次随访无变化的病灶,可逐渐延长随访时间间隔,随访稳定的纯GGN可1~2年体检一次。Fleischner协会和美国胸科医师学会(ACCP)指南对稳定的实性结节也采用18~24个月的随访间隔,但对于永存GGN,即使结节长期稳定,也不可完全放弃体检,以免贻误最佳干预时机。对于随访增大或密度增加,以及病灶出现空泡征、毛刺征、分叶征或支气管血管改变等恶性征象时,应终止随访,行手术治疗。
3.1 空泡征空泡征是指病灶内直径1~2 mm的透亮区,形状可不规则,病理基础为正常的含气肺组织未被有形物质组织所充填。空泡征高度提示结节恶性,有单中心研究报道,空泡征在手术肺结节内检出率8.5%,其中恶性结节占74.7%[11]。
3.2 毛刺征毛刺征在CT图像上表现为自肿瘤边缘向周围肺组织放射状伸出的细密短线影,多见于实性为主的GGN,纯GGN或以磨玻璃密度为主的部分实性GGN罕见此征。毛刺征的病理基础为肿瘤细胞浸润周围基质,并牵拉周围组织,或因肿瘤内不规则纤维组织增生牵拉所致。毛刺征作为肺结节的高度恶性征象,在ACCP指南中其也是肺结节恶性预测模型中的独立预测因素,但毛刺征亦可见于良性结节[12]。
3.3 分叶征分叶征在CT图像上表现为病灶表面呈花瓣状多个弧形,其病理学基础为:①肿瘤组织异质性,不同方向的生长速度及浸润程度不同;②肿瘤内纤维增生组织牵拉收缩;③肺间质结构阻挡肿块的生长。分叶征是肺部结节的高度恶性征象,有研究报道其对周围型小肺癌诊断的特异度97.6%,敏感度60.7%[13]。
3.4 棘突征棘突征是一种特殊类型的分叶,在CT图像上呈基底位于肿瘤表面的尖角状突起,横断面显示凸起一侧可有弧形膨起。其病理基础为肿瘤在分叶的基础上向外先行浸润的肿瘤组织,特异性强,是肺癌的重要征象,也反映了肿瘤的异质性。
3.5 晕征与反晕征 3.5.1 晕征晕征是指结节边缘模糊不清的磨玻璃密度影,以炎性病变多见,提示病变可能通过肺泡孔蔓延。晕征起初报道自侵袭性曲霉病例,后在支气管肺泡癌中也有描述,亦可见于部分肺转移瘤(如血管肉瘤、绒癌及骨肉瘤等恶性肿瘤)[14]。
3.5.2 反晕征反晕征指结节中心区域磨玻璃密度影,外周由环形或新月形实性高密度影包绕,起初报道于隐源性机化性肺炎,其病理机制可能为中心低密度区为肺泡间隔的炎性渗出和肺泡腔内的细胞碎屑,而周围环形或新月形的实变高密度影是远端气腔内的肉芽组织栓[15]。反晕征在其他感染性和/或非感染性疾病中也能观察到,包括少数几例肺腺癌[16]。研究表明,在GGN中表现为外周呈环形磨玻璃密度,而中心低于外周密度的特殊类型的反晕征,大多提示结节为恶性,可能与肿瘤细胞的贴壁式生长模式相关[17]。
3.6 GGN与支气管-血管关系 3.6.1腺体前驱病变(AAH、AIS)的肿瘤细胞内附于肺泡壁,且无侵袭性,无肿瘤细胞的支气管浸润及间质增生牵拉,支气管的走行、管腔及管壁未见明显异常,无扭曲、狭窄、扩张及增厚等异常改变;浸润性病变(MIA、IA)的肿瘤细胞因沿着气道浸润和间质增生牵拉等,支气管走行可出现杯口状截断及牵拉扭曲,管腔内壁不光整、呈鼠尾样狭窄,管壁出现局限不规则增厚。若病灶内支气管壁弥漫均匀增厚,并伴周围渗出,炎性病变可能性大。
3.6.2腺体前驱病变(AAH、AIS)内的血管一般表现正常,无增粗、扭曲及变形等异常改变;而浸润性病变(MIA、IA)内的血管可出现扭曲、增粗及聚集等异常改变,其病理基础为肿瘤组织浸润支气管-血管束或小叶间隔,纤维组织增生牵拉周围结构所致。
3.7 结节邻近结构改变部分实性GGN较易引起邻近结构改变,主要因病灶中实性成分增多进而组织收缩、牵拉形成,以胸膜凹陷征及血管集束征较典型。
3.7.1 胸膜凹陷征胸膜凹陷征是指病灶牵拉脏层胸膜,使其与壁层胸膜之间形成喇叭状凹陷,凹陷间隙内为水样密度,其病理基础为病灶小叶间隔及胸膜下间质内小叶纤维组织增生。当病灶距离太远未达胸膜,而紧贴胸膜多伴胸膜的粘连及增厚,因此胸膜凹陷征多见于距离胸膜约2 cm的恶性结节。
3.7.2 血管集束征血管集束征是指结节周围的小血管因肿瘤细胞产生的促血管生成因子增粗,受牵拉向病灶处聚拢,并在病灶处中断或穿行其中的征象,多见于恶性病变[18]。
4 新技术的应用计算机辅助诊断(computer aided diagnosis,CAD)系统近年来受到广泛关注并迅速发展,基于深度学习的CAD是当前研究的主流。多任务CAD系统在肺GGN定量、定性及随访过程中都发挥重要作用。
4.1 CAD系统定量诊断CAD系统可用于结节的检出、筛查及随访,定量测量亚实性结节大小、体积、密度及亚实性结节内实性成分等。在肺分割算法基础上,基于密度和形状等规则的检测方案仅适用部分结节,漏诊率较高;基于深度学习的方案可根据大量的训练数据不断调整,肺结节检出率随之提高,假阳性率持续降低[19]。有研究表明,当其他扫描参数相同时,使用1 mm层厚检测GGN为最佳[20]。
4.2 CAD系统定性诊断CAD系统可用于判断结节的良恶性、侵袭性及预后。放射组学是一个新兴领域,其利用CAD系统使用大量自动提取的数据表征算法将ROI内影像数据转换为高维可挖掘特征空间数据,可建立与临床决策相关的模型[21]。有研究提取GGN的纹理特征与临床病理等信息构建放射组学模型判断结节的侵袭性[22]。
综上所述,随着CT技术不断的进步、GGN的检出率不断提高,应用合适的CT扫描技术,仔细分析其CT征象,再借助CAD系统的辅助筛检和诊断,GGN的处理策略将更加精准。
| [1] |
HENSCHKE C I, YANKELEVITZ D F, MIRTCHEVA R, et al. CT screening for lung cancer: frequency and significance of part-solid and nonsolid nodules[J]. AJR Am J Roentgenol, 2002, 178(5): 1053-1057. DOI:10.2214/ajr.178.5.1781053 |
| [2] |
REMY-JARDIN M, REMY J, GIRAUD F, et al. Computed tomography assessment of ground-glass opacity: semiology and significance[J]. J Thorac Imaging, 1993, 8(4): 249-264. DOI:10.1097/00005382-199323000-00001 |
| [3] |
NAIDICH D P, BANKIER A A, MACMAHON H, et al. Recommendations for the management of subsolid pulmonary nodules detected at CT: a statement from the Fleischner Society[J]. Radiology, 2013, 266(1): 304-317. DOI:10.1148/radiol.12120628 |
| [4] |
LEE H J, LEE C H, JEONG Y J, et al. IASLC/ATS/ERS International Multidisciplinary Classification of Lung Adenocarcinoma: novel concepts and radiologic implications[J]. J Thorac Imaging, 2012, 27(6): 340-353. DOI:10.1097/RTI.0b013e3182688d62 |
| [5] |
张丽, 于红, 刘士远, 等. 迭代重建技术对低剂量肺部平扫CT图像质量的影响[J]. 中华放射学杂志, 2013, 47(4): 316-320. |
| [6] |
LACOUT A, MARCY P Y, NGO T M, et al. Multidetector row CT scan in hypersensitivity pneumonitis: contribution of minimum intensity projection reformation[J]. J Med Imaging Radiat Oncol, 2011, 55(3): 291-295. DOI:10.1111/j.1754-9485.2011.02267.x |
| [7] |
李惠民, 肖湘生, 刘士远. 螺旋CT靶扫描对肺部小结节的诊断价值[J]. 临床放射学杂志, 2001, 20(6): 424-427. |
| [8] |
李鲁, 李惠民, 舒锦尔, 等. 生理通气辅助超高分辨率CT扫描技术探讨[J]. 中国医学计算机成像杂志, 2015, 21(3): 228-231. |
| [9] |
HANSELL D M, BANKIER A A, MACMAHON H, et al. Fleischner society: glossary of terms for thoracic imaging[J]. Radiology, 2008, 246(3): 697-722. DOI:10.1148/radiol.2462070712 |
| [10] |
MACMAHON H, NAIDICH D P, GOO J M, et al. Guidelines for management of incidental pulmonary nodules detected on CT images: from the Fleischner Society 2017[J]. Radiology, 2017, 284(1): 228-243. DOI:10.1148/radiol.2017161659 |
| [11] |
庄远迪, 傅钢泽, 纪晓微, 等. 含空泡征肺小结节的CT征象与病理对照研究[J]. 医学影像学杂志, 2019, 29(7): 1135-1140. |
| [12] |
张元元. 肺良恶性结节的CT表现分析[J]. 中国中西医结合影像学杂志, 2019, 17(6): 622-624. |
| [13] |
刘大亮, 马大庆, 陈广. CT的分叶征表现在肺内孤立结节影像诊断中的价值[J]. 中华放射学杂志, 2007, 41(5): 487-489. |
| [14] |
PINTO P S. The CT halo sign[J]. Radiology, 2004, 230(1): 109-110. DOI:10.1148/radiol.2301020649 |
| [15] |
KIM S J, LEE K S, RYU Y H, et al. (2003) Reversed halo sign on high-resolution CT of cryptogenic organizing pneumonia: diagnostic implications[J]. AJR Am J Roentgenol, 2003, 180(5): 1251-1254. DOI:10.2214/ajr.180.5.1801251 |
| [16] |
MARCHIORI E, ZANETTI G, HOCHHEGGER B, et al. Reversed halo sign on computed tomography: state-of-the-art review[J]. Lung, 2012, 190(4): 389-394. DOI:10.1007/s00408-012-9392-x |
| [17] |
任华, 李惠民, 虞峻崴, 等. 表现为反晕征的肺磨玻璃结节CT诊断[J]. 中国医学计算机成像杂志, 2018, 24(2): 127-131. |
| [18] |
陈子敏, 向子云, 王毅, 等. 三维重建在孤立性肺结节血管集束征的诊断价值[J]. CT理论与应用研究, 2017, 26(1): 69-76. |
| [19] |
WANG Y, WU B, ZHANG N, et al. Research progress of computer aided diagnosis system for pulmonary nodules in CT images[J]. J Xray Sci Technol, 2020, 28(1): 1-16. |
| [20] |
PARK S, LEE S M, KIM W, et al. Computer-aided detection of subsolid nodules at chest CT: improved performance with deep learning-based CT section thickness reduction[J]. Radiology, 2021, 299(1): 211-219. DOI:10.1148/radiol.2021203387 |
| [21] |
MAYERHOEFER M E, MATERKA A, LANGS G, et al. Introduction to radiomics[J]. J Nucl Med, 2020, 61(4): 488-495. DOI:10.2967/jnumed.118.222893 |
| [22] |
WU G, WOODRUFF H C, SHEN J, et al. Diagnosis of invasive lung adenocarcinoma based on chest CT radiomic features of part-solid pulmonary nodules: a multicenter study[J]. Radiology, 2020, 297(2): 451-458. DOI:10.1148/radiol.2020192431 |
 2021, Vol. 19
2021, Vol. 19


