| 基于ReHo和fALFF的优势半球与非优势半球基底节区脑梗死后运动障碍的静息态脑功能成像研究 |
2. 深圳大学第六附属医院康复医学科, 广东 深圳 518052;
3. 福建省厦门市湖里区江头街道社区卫生服务中心针灸科, 福建 厦门 361009
2. Department of Rehabilitation Medicine, 6th Affiliated Hospital of Shenzhen University, Shenzhen 518052, China;
3. Department of Acupuncture and Moxibustion, Jiangtou Street Community Health Service Center of Huli District in Xiamen City, Xiamen 361009, China
脑梗死又称缺血性脑卒中,是一种由于局部脑组织缺血、缺氧性坏死或软化引起的脑神经功能损伤的常见脑血管疾病[1-2]。基底神经节与新皮质和边缘结构存在广泛的联系,具有调控运动执行速度、方向、强度等作用,因此基底节区脑梗死患者常伴不同程度的肢体运动功能障碍[3-4]。静息态fMRI是一种通过检测脑部血氧水平生理变化来评估局部脑功能的技术[5-6]。局部一致性(regional homogeneity,ReHo)和比率低频振幅(fraction amplitude of low-frequency fluctuation,fALFF)常用于观察脑局部活动。ReHo是一种通过观察持续活动的脑区与邻近脑区神经活动的时间同步性反映局部神经活动一致性的影像学分析方法[7-8]。fALFF通过检测血氧水平依赖波动的局部神经活动强度反映脑部血流自发的神经活动[9-10]。作为2种基于不同神经生理机制的方法,ReHo在观察局部自发神经活动异常方面比fALFF灵敏,fALFF则被证明是ReHo测量全脑局部神经功能变化的有力补充[11]。目前,优势大脑半球与非优势大脑半球在神经影像学上差异尚不明确[12],故本研究以优势大脑半球与非优势大脑半球为切入点,采用ReHo和fALFF方法探讨基底节区脑梗死后运动障碍患者局部脑区特征,以期为脑梗死后运动障碍的临床康复提供更多信息。
1 资料与方法 1.1 一般资料收集2018年5月至2022年12月就诊于深圳大学第六附属医院、福建中医药大学附属康复医院的基底节区脑梗死后运动障碍患者共20例,均处于恢复期;其中优势半球脑梗死(优势半球脑梗死组)11例,男8例,女3例,年龄42~68岁,平均(55.18±7.28)岁,病程15~60 d,平均(26.00±14.70) d;非优势半球脑梗死9例(非优势半球脑梗死组),男8例,女1例,年龄44~70岁,平均(53.61±6.39)岁,病程15~83 d,平均(44.00±24.71)d。同期招募在深圳市的性别、年龄与脑梗死患者基本匹配的18例健康志愿者作为对照组,其中男14例,女4例;年龄42~67岁,平均(55.89±7.37)岁。3组性别、年龄差异均无统计学意义(均P > 0.05),优势半球脑梗死组与非优势半球脑梗死组病程差异无统计学意义(Z=-1.717,P=0.086)。本研究经深圳市南山区人民医院(现深圳大学第六附属医院)及福建中医药大学附属康复医院伦理委员会的批准(2018092501,2020KY-028-01),受试者或其监护人均签署知情同意书。
脑梗死患者纳入标准:①符合脑梗死诊断标准[13],同时经CT或MRI证实为基底节区脑梗死;②生命体征稳定,意识清晰,认知良好;③单侧偏瘫,Brunnstrom分期为Ⅰ~Ⅳ期;④年龄40~70岁;⑤发病2周至6个月;⑥右利手。
对照组纳入标准:①与脑梗死患者年龄、性别相匹配;②无头部外伤史、脑肿瘤史、精神疾病史;③受试前无劳累、情绪激动等影响因素;④右利手。
所有受试者的排除标准:①既往存在脑外伤史、脑肿瘤史、精神疾病史;②有严重认知障碍而无法配合;③有幽闭恐惧症、心脏起搏器、颅骨缺陷或金属植入物;④存在严重颈椎病变,如严重颈椎管狭窄、颈椎失稳;⑤依从性较差;⑥妊娠期妇女。
1.2 仪器与方法采用Siemens Magnetom Skyro 3.0 T MRI扫描仪,8通道头部线圈,采集静息态fMRI图像。嘱受试者在试验过程中尽可能保持头部静止状态,减少吞咽运动,戴耳塞以降低扫描仪噪音,减少试验误差。功能图像数据的采集采用EPI序列,TR 2 000 ms,TE 30 ms,翻转角90°,视野224 mm×224 mm,矩阵64×64,层厚3.5 mm,无间隔。3D-T1WI解剖像采用SE脉冲序列,TR 2 530 ms,TE 2.01 ms,翻转角7°,视野256 mm×256 mm,矩阵256×256,层厚1 mm,无间隔。
1.3 数据处理在Matlab R2013b运行环境下,基于SPM12(https://www.fil.ion.ucl.ac.uk/spm/software/spm12)的DPARSF 6.2工具包行数据预处理与分析。步骤包括[14-15]:①将DICOM格式图像转化为NIFTI格式文件;②剔除数据的前10个时间点;③将每一套数据内所有层面都向扫描中间的时间点对齐;④将功能像与T1像进行配准,分割结构像,分出白质、灰质、头骨等;⑤剔除头动 > 3 mm或旋转 > 3°的数据;⑥将功能像配准至蒙特利尔神经病学研究所(Montreal Neurological Institute,MNI)坐标,每个体素大小为3 mm×3 mm×3 mm;⑦除去感兴趣信号外的白质及脑脊液等协变量的影响;⑧去线性漂移。
ReHo分析:在预处理的基础上,对数据行0.01~0.08 Hz的滤波处理,使用DPARSF软件包分析ReHo,评估所有体素与邻近体素时间序列的一致性。计算每个体素与相邻26个体素的ReHo值,对ReHo值行平滑处理,提高SNR,得到全脑ReHo图[16]。
fALFF分析:在预处理的基础上,设置平滑核半高宽为6 mm×6 mm×6 mm提高SNR,使用DPARSF软件分析fALFF。最后对fALFF值行0.01~0.08 Hz的滤波处理,得到全脑fALFF图[17]。
1.4 统计学分析利用DPARSF软件对3组的ReHo值、fALFF值行两两组间双样本t检验。将受试者性别、年龄、头动参数为协变量,行GRF多重校正,体素水平P < 0.01,团块水平P < 0.05,体素个数 > 50则认为该体素在组间对比中差异有统计学意义。应用MNI坐标和解剖学自动标记模板(anatomical automatic labeling,AAL)对差异脑区行标准坐标定位和识别。
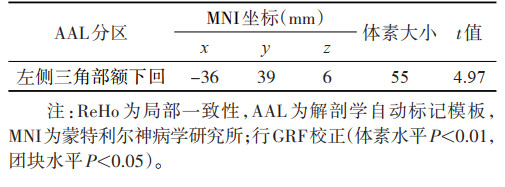
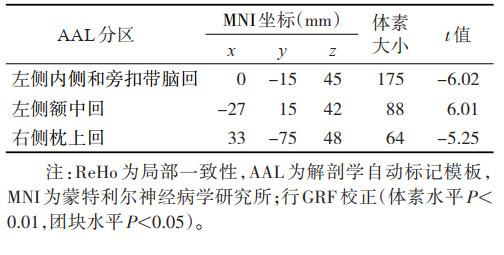
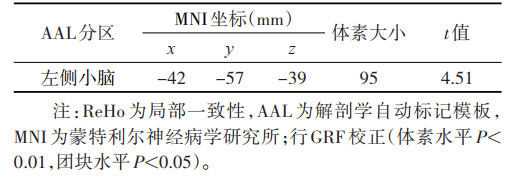
2 结果 2.1 3组ReHo值比较与对照组相比,优势半球脑梗死组左侧三角部额下回的ReHo值显著增高(t=4.97,P < 0.05);非优势半球脑梗死组左侧额中回的ReHo值显著升高(t=6.01,P < 0.05),左侧内侧和旁扣带脑回、右侧枕上回的ReHo值显著降低(t=-6.02,-5.25;均P < 0.05)。与非优势半球脑梗死组相比,优势半球脑梗死组左侧小脑的ReHo值显著升高(t=4.51,P < 0.05)(表 1~3,图 1)。
| 表 1 与对照组比较,优势半球脑梗死组ReHo值变化的脑区 |
 |
| 表 2 与对照组比较,非优势半球脑梗死组ReHo值变化的脑区 |
 |
| 表 3 与非优势半球脑梗死组比较,优势半球脑梗死组ReHo值变化的脑区 |
 |
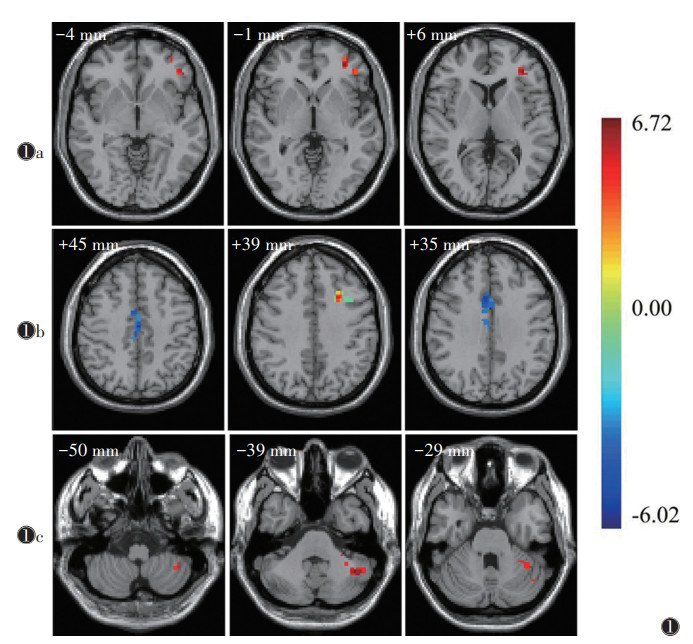 |
| 注:图 1a~1c分别为优势半球脑梗死组与对照组、非优势半球脑梗死组与对照组、优势半球脑梗死组与非优势半球脑梗死组的ReHo值比较(体素水平P < 0.01,团块水平P < 0.05,GRF校正)。右边为t值颜色条,冷色代表ReHo值降低,暖色代表ReHo值升高,颜色越红表示ReHo值越高,颜色越蓝表示ReHo值越低,靠近字母侧为大脑右侧,靠近颜色条为大脑左侧 图 1 局部一致性(ReHo)值差异脑区图 |
2.2 3组fALFF结果
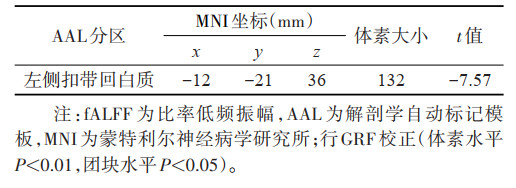
与对照组相比,优势半球脑梗死组左侧扣带回白质的fALFF值显著降低(t=-7.57,P < 0.05);非优势半球脑梗死组右侧眶部额下回、左侧枕中回的fALFF值显著升高(t=5.01,4.74;均P < 0.05),右侧内侧和旁扣带脑回fALFF值显著降低(t=-5.58,P < 0.05)。与非优势半球脑梗死组相比,优势半球脑梗死组左侧三角部额下回、左侧舌回、左侧额中回的fALFF值显著升高(t=5.29,5.63,6.72;均P < 0.05)(表 4~6,图 2)。
| 表 4 与对照组比较,优势半球脑梗死组fALFF值变化的脑区 |
 |
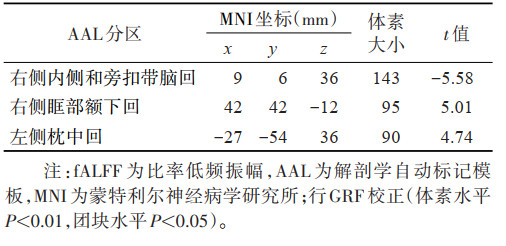
| 表 5 与对照组比较,非优势半球脑梗死组fALFF值变化的脑区 |
 |
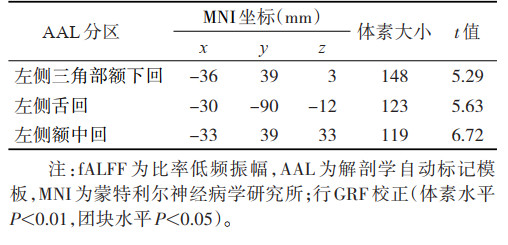
| 表 6 与非优势半球脑梗死组比较,优势半球脑梗死组fALFF值变化的脑区 |
 |
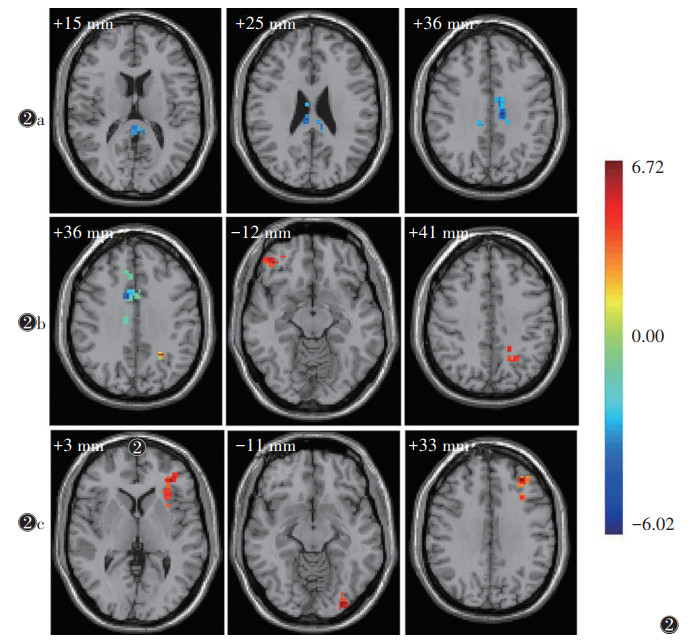 |
| 注:图 2a~2c分别为优势半球脑梗死组与对照组、非优势半球脑梗死组与对照组、优势半球脑梗死组与非优势半球脑梗死组fALFF值比较(体素水平P < 0.01,团块水平P < 0.05,GRF校正)。右边为t值颜色条,冷色代表fALFF值降低,暖色代表fALFF值升高,颜色越红表示fALFF值越高,颜色越蓝表示fALFF值越低,靠近字母侧为大脑右侧,靠近颜色条为大脑左侧 图 2 比率低频振幅(fALFF)值差异脑区图 |
3 讨论
本研究采用ReHo和fALFF观察基底节区脑梗死后运动障碍患者的脑局部异常神经活动。ReHo可在全脑范围内对局部功能活动差异性脑区进行准确定位,其增高或降低提示该脑区局部神经元功能活动异常[18]。fALFF通过低频功率谱除以全频段的功率谱来降低脑脊液等非特异性信号的影响并减少SNR,避免了低频振幅的弊端,有利于提高自发神经活动信号检测的特异度和敏感度[19]。
本研究发现,优势半球基底节区脑梗死患者相对于健康人左侧三角部额下回局部神经元活动明显变化。额下回在注意力控制方面发挥重要作用,同时控制运动的发生和发展[20]。Wu等[21]发现,亚急性期缺血性卒中患者ReHo值在左侧楔前叶、小脑、左侧额下回三角部和左侧颞下回的区域同质性升高,在左侧前扣带回和左侧眶内额上回、双侧脑岛的区域同质性降低,涉及运动、感觉和情绪处理等多个方面,提示脑梗死后功能损伤不仅发生在运动区域,还涉及其他区域的损伤。本研究中优势半球损伤后局部神经元活动变化可能与基底节区损伤会导致周围脑区功能损害有关,在不同程度上产生运动功能受损,具体表现为运动执行速度减慢、方向变化。
本研究发现,非优势半球基底节区脑梗死患者左侧额中回、双侧内侧和旁扣带脑回、右侧枕上回、右侧眶部额下回及左侧枕中回局部神经元活动异常。前额叶皮质是额顶网络的核心脑区,优势半球脑梗死后额顶叶网络明显激活,表明在优势半球的运动回路受损时会出现功能恢复的代偿性神经通路[22-23]。扣带皮质与基底神经节及躯体运动区存在广泛连接,被认为是运动的连接中枢,在运动控制中起重要作用[24-25]。后扣带皮质对来自顶叶皮质的空间和动作相关信息进行加工、学习,中扣带回皮质将加工过的信息向前运动皮质传递,影响运动执行过程[26-27]。王想敏等[28]将16例左侧皮质下病变脑梗死后运动功能障碍患者与16例年龄性别相匹配的健康志愿者比较,结果发现fALFF值降低区域位于丘脑、基底节区神经核团和枕叶,基底神经节和丘脑属于皮质下灰质核团,参与构成脑结构网络。本研究发现,非优势半球丘脑ReHo值及fALFF值均变化,可能与基底节-丘脑-皮质回路的逆行性神经退变导致病灶远端脑区的功能和结构损伤有关。
本研究表明,优势半球基底节脑梗死患者相对于非优势半球基底节脑梗死患者左侧小脑、左侧三角部额下回、左侧舌回、左侧额中回局部神经元活动发生明显变化。小脑作为重要的躯体运动调节中枢之一,接受脊髓小脑的传入冲动,通过传出冲动调节骨骼肌中抗重力肌群的活动,维持并调节人体肌张力[29-33]。付彩红等[34]研究发现,脑梗死后偏瘫患者ReHo值升高区域多位于病灶对侧,而右侧额中回、右侧中央前回、右侧扣带回ReHo减弱,提示脑梗死恢复期主要以健侧脑区运动皮质的代偿功能为主,皮质功能重组能有效预测运动功能恢复情况。运动控制理论表明感觉、认知和活动在运动控制过程中具有共同作用,本研究发现脑梗死后优势半球比非优势半球能更快建立新的运动控制网络。
本研究不足之处:①入组的脑梗死患者基线资料基本一致,但样本量相对较小,结果可能有一定偏倚,需招募更多患者验证相关发现。②未行独立的运动功能相关量表评估,未来考虑加入相关量表评估并与大脑静息态变化差异行相关性分析。③未观察ReHo值及fALFF值的动态变化,可通过进一步的研究阐明纵向的ReHo及fALFF值改变。
综上所述,采用静息态fMRI技术联合ReHo和fALFF发现,静息状态下,与对照组相比,优势半球与非优势半球基底节区脑梗死后双侧大脑皮质运动、感觉及认知等多个脑区神经元活动发生变化;与非优势半球脑梗死相比,优势半球脑梗死能更快地使相关脑区出现代偿性激活,增强神经元活动,可为进一步理解不同半球间基底节区脑梗死后运动障碍患者大脑局部神经影像学差异及临床康复提供更多影像学数据支持。
致谢: 感谢福建中医药大学附属康复医院神经康复五科、放射科对课题的大力支持!| [1] |
FESKE S K. Ischemic stroke[J]. Am J Med, 2021, 134: 1457-1464. DOI:10.1016/j.amjmed.2021.07.027 |
| [2] |
AKELLA A, BHATTARAI S, DHARAP A. Long noncoding RNAs in the pathophysiology of ischemic stroke[J]. Neuromolecular Med, 2019, 21: 474-483. DOI:10.1007/s12017-019-08542-w |
| [3] |
BEVAN M D. Motor control: a basal ganglia feedback circuit for action suppression[J]. Curr Biol, 2021, 31: 191-193. DOI:10.1016/j.cub.2020.11.067 |
| [4] |
黄浩洁, 李懿婷, 侯莉娟, 等. 基底神经节在运动调控作用中的研究进展[J]. 生命科学, 2019, 31(11): 1099-1105. |
| [5] |
KREMNEVA E I, SINITSYN D O, DOBYNINA L A, et al. Resting state functional MRI in neurology and psychiatry[J]. Zh Nevrol Psikhiatr Im S S Korsakova, 2022, 122: 5-14. |
| [6] |
ZHONG X Z, CHEN J J. Resting-state functional magnetic resonance imaging signal variations in aging: the role of neural activity[J]. Hum Brain Mapp, 2022, 43: 2880-2897. DOI:10.1002/hbm.25823 |
| [7] |
ZANG Y, JIANG T, LU Y, et al. Regional homogeneity approach to fMRI data analysis[J]. Neuroimage, 2004, 22: 394-400. DOI:10.1016/j.neuroimage.2003.12.030 |
| [8] |
LI Q, HU S, MO Y, et al. Regional homogeneity alterations in multifrequency bands in patients with basal ganglia stroke: a resting-state functional magnetic resonance imaging study[J]. Front Aging Neurosci, 2022, 14: 938646. DOI:10.3389/fnagi.2022.938646 |
| [9] |
ZOU Q H, ZHU C Z, YANG Y, et al. An improved approach to detection of amplitude of low-frequency fluctuation(ALFF)for resting-state fMRI: fractional ALFF[J]. J Neurosci Methods, 2008, 172: 137-141. DOI:10.1016/j.jneumeth.2008.04.012 |
| [10] |
ZHAN Y, PEI J, WANG J, et al. Motor function and fALFF modulation in convalescent-period ischemic stroke patients after scalp acupuncture therapy: a multicentre randomized controlled trial[J]. Acupunct Med, 2023, 41(2): 86-95. DOI:10.1177/09645284221086289 |
| [11] |
AN L, CAO Q J, SUI M Q, et al. Local synchronization and amplitude of the fluctuation of spontaneous brain activity in attention-deficit/hyperactivity disorder: a resting-state fMRI study[J]. Neurosci Bull, 2013, 29: 603-613. DOI:10.1007/s12264-013-1353-8 |
| [12] |
GAO J, YANG C, LI Q, et al. Hemispheric difference of regional brain function exists in patients with acute stroke in different cerebral hemispheres: a resting-state fMRI study[J]. Front Aging Neurosci, 2021, 13: 691518. DOI:10.3389/fnagi.2021.691518 |
| [13] |
中华医学会神经病学分会, 中华医学会神经病学分会脑血管病学组. 中国各类主要脑血管病诊断要点2019[J]. 中华神经科杂志, 2019, 52(9): 710-715. |
| [14] |
YAN C G, WANG X D, ZUO X N, et al. DPABI: data processing & analysis for(resting-state)brain imaging[J]. Neuroinformatics, 2016, 14(3): 339-351. DOI:10.1007/s12021-016-9299-4 |
| [15] |
WAHEED S H, MIRBAGHERI S, AGARWAL S, et al. Reporting of resting-state functional magnetic resonance imaging preprocessing methodologies[J]. Brain Connect, 2016, 6(9): 663-668. DOI:10.1089/brain.2016.0446 |
| [16] |
LV Y, LI L, SONG Y, et al. The local brain abnormalities in patients with transient ischemic attack: a restingstate fMRI study[J]. Front Neurosci, 2019, 13: 24. DOI:10.3389/fnins.2019.00024 |
| [17] |
WANG H, HUANG Y, LI M, et al. Regional brain dysfunction in insomnia after ischemic stroke: a restingstate fMRI study[J]. Front Neurol, 2022, 13: 1025174. DOI:10.3389/fneur.2022.1025174 |
| [18] |
周玉梅, 孙佳蕾, 武平. 静息态fMRI技术在临床的应用-局部一致性研究[J]. 中风与神经疾病杂志, 2014, 31(4): 382-384. |
| [19] |
LV H, WANG Z, TONG E, et al. Resting-state functional MRI: everything that nonexperts have always wanted to know[J]. AJNR Am J Neuroradiol, 2018, 39(8): 1390-1399. |
| [20] |
SWANN N C, CAI W, CONNER C R, et al. Roles for the pre-supplementary motor area and the right inferior frontal gyrus in stopping action: electrophysiological responses and functional and structural connectivity[J]. Neuroimage, 2012, 59: 2860-2870. DOI:10.1016/j.neuroimage.2011.09.049 |
| [21] |
WU P, ZENG F, LI Y X, et al. Changes of resting cerebral activities in subacute ischemic stroke patients[J]. Neural Regen Res, 2015, 10(5): 760-765. DOI:10.4103/1673-5374.156977 |
| [22] |
OLAFSON E, RUSSELLO G, JAMISON K W, et al. Frontoparietal network activation is associated with motor recovery in ischemic stroke patients[J]. Commun Biol, 2022, 5(1): 993. DOI:10.1038/s42003-022-03950-4 |
| [23] |
JAPEE S, HOLIDAY K, SATYSHUR M D, et al. A role of right middle frontal gyrus in reorienting of attention: a case study[J]. Front Syst Neurosci, 2015, 9: 23. |
| [24] |
JUMAH F R, DOSSANI R H. Neuroanatomy, cingulate cortex[M]. Treasure Island: StatPearls Publishing, 2022: 23-25.
|
| [25] |
MALDONADO I L, PARENTE DE MATOS V, CASTRO CUESTA T A, et al. The human cingulum: from the limbic tract to the connectionist paradigm[J]. Neuropsychologia, 2020, 144: 107487. DOI:10.1016/j.neuropsychologia.2020.107487 |
| [26] |
ROLLS E T. The cingulate cortex and limbic systems for emotion, action, and memory[J]. Brain Struct Funct, 2019, 224(9): 3001-3018. DOI:10.1007/s00429-019-01945-2 |
| [27] |
TAKENOBU Y, HAYASHI T, MORIWAKI H, et al. Motor recovery and microstructural change in rubrospinal tract in subcortical stroke[J]. Neuroimage Clin, 2013, 4: 201-208. |
| [28] |
王想敏, 赵智勇, 尹大志, 等. 脑卒中静息态下脑活动异常的比率低频振幅fMRI研究[J]. 磁共振成像, 2016, 7(6): 401-406. |
| [29] |
许超群, 朱正华, 章俊, 等. 静息态功能MRI对脑梗死后失语症语言康复效果评价[J]. 医学影像学杂志, 2023, 33(7): 1261-1265. |
| [30] |
JONES T A. Motor compensation and its effects on neural reorganization after stroke[J]. Nat Rev Neurosci, 2017, 18(5): 267-280. |
| [31] |
李敏红, 李志铭, 庄卓霖, 等. 静息态功能磁共振成像技术对rTMS治疗脑卒中患者认知功能障碍效果研究[J]. 医学影像学杂志, 2023, 33(4): 670-673. |
| [32] |
COLLOBY S J, OBRIEN J T, BRIEN J T, et al. Patterns of cerebellar volume loss in dementia with Lewy bodies and Alzheimer's disease: a VBM-DARTEL study[J]. Psychiatry Res, 2014, 223(3): 187-191. |
| [33] |
王苏珊, 陈蓓蕾, 于海龙, 等. 脑小血管病患者认知功能障碍的静息态功能磁共振成像研究[J]. 医学影像学杂志, 2021, 31(2): 183-186, 193. |
| [34] |
付彩红, 宁艳哲, 张勇, 等. 针刺阳陵泉对中风偏瘫病人局部一致性影响的静息态fMRI研究[J]. 中西医结合心脑血管病杂志, 2019, 17(11): 1623-1629. |
 2024, Vol. 22
2024, Vol. 22


