| 亚腹膜间隙及腹腔淋巴结分布的影像学实践(一) |
亚腹膜间隙是包绕脏器的腹膜在移行或反折过程中形成的双层腹膜结构,包括系膜、网膜、韧带及隐窝等,对脏器起着连接和固定的作用,同时也是脏器营养相关的血管、神经及淋巴管出入的通道,是病变在腹腔内播散的解剖学基础[1]。
从临床实践来看,亚腹膜间隙内主要含有脂肪,生理状态下淋巴结显示不典型、腹膜结构复杂且隐匿,给影像学定性及定位诊断造成困难,增加临床工作负担。因此,本篇以横结肠及其系膜为界,将亚腹膜间隙分为结肠上区和结肠下区[2],并以腹腔脏器位置为索引,对亚腹膜间隙结构及淋巴组群进行概述,提高对其影像解剖的认识。
1 结肠上区 1.1 胃周间隙及淋巴引流胃前壁右侧份邻近左半肝,左侧份上部紧邻膈,下部接近腹前壁,胃后壁隔网膜囊与胰、左肾上腺、左肾、脾、横结肠及其系膜毗邻,这些结构共同形成胃床[3](图1)。胃表面几乎完全被腹膜包裹,与邻近器官形成紧密的韧带结构(图2)。胃结肠韧带位于胃下方,为胃大弯下延至横结肠的2层腹膜,是大网膜的一部分,有胃网膜血管穿行。胃膈韧带位于胃上部,是贲门与膈之间的腹膜皱襞。胃脾韧带位于胃大弯左侧,是胃底与脾之间的双层腹膜,有胃短血管穿行。肝胃韧带位于胃右侧,是肝门与胃小弯之间的双层腹膜,是小网膜的一部分,有胃左血管走行。胃胰韧带位于胃后壁,连接胰腺,胃小弯贲门处至胰腺的腹膜皱襞内有胃左静脉[3]。在门静脉高压时,血液可经胃左静脉至食管静脉、奇静脉流入上腔静脉,发生食管胃底静脉曲张。小网膜分为右侧的肝十二指肠韧带和左侧的肝胃韧带两部。全胃切除时,须切断上述韧带[4]。行脾切除术时应避免损伤胃短动脉,以防造成大出血。
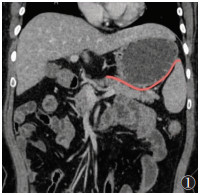 |
| 图 1 胃床CT示意图(红色条带) |
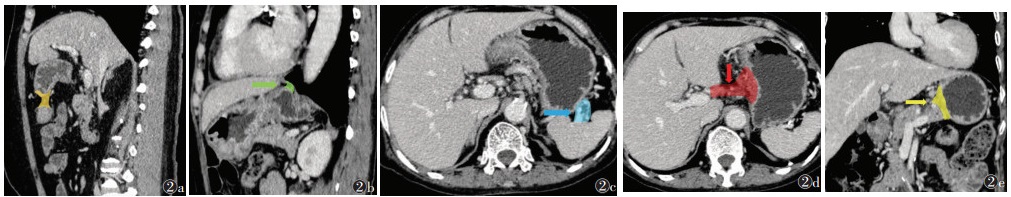 |
| 注:图2a为胃结肠韧带(橙色区域),图2b为胃膈韧带(绿色区域),图2c为胃脾韧带(蓝色区域),图2d为肝胃韧带(红色区域),图2e为胃胰韧带(黄色区域) 图 2 胃周韧带CT示意图 |
近年来,胃裸区的范围和临床意义日益受到重视。胃裸区是指在食管贲门结合部及胃小弯近侧部分的胃后壁后方与胃膈韧带之间存在的无腹膜覆盖区[5]。由于胃裸区的存在,一些学者认为胃应是腹膜间位器官而不是腹膜内位器官[6]。该区域仅有疏松结缔组织与膈相连,正常情况其CT表现为脂肪密度影(图3),大小1.6~16.2 cm[6]。大多数学者认为,左肾旁前间隙及胰腺周围间隙向上与胃裸区相通连[7-8],因此肾旁前间隙内的炎症(如急性胰腺炎)可累及胃裸区,CT表现为混浊、条纹状液体密度。研究显示,肿瘤侵犯胃裸区可能是影响胃癌患者预后的独立危险因素[9]。由于胃裸区无腹膜覆盖且隐匿,故较难诊断的贲门癌易侵犯至腹膜后隙,从而增加手术切除的难度[10]。
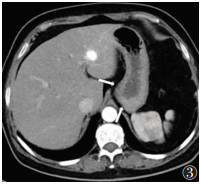 |
| 图 3 胃裸区(白箭)正常CT图像 |
胃的淋巴引流包括内引流与外引流,其中内引流包括黏膜下与浆膜下引流;外引流则是在胃外形成淋巴管。正常情况下,胃上1/3的淋巴管沿胃左动脉、胃后动脉与脾动脉走行,胃下1/3的淋巴管则伴肝总动脉与肠系膜上动脉走行,胃中1/3为混合引流,所有淋巴管最终汇入腹主动脉旁淋巴结[11]。胃癌的淋巴结转移通常是循序渐进的,即先由原发部位经淋巴网向胃周淋巴结转移,继而癌细胞沿血管周围淋巴结向心性转移,并向更远的重要血管周围转移,但有时也可表现为跳跃性转移,因此如何确定淋巴结清扫范围目前尚存在一定争议,需在影像诊断过程中甄别病理性淋巴结。日本胃癌协会(Japanese Gastric Cancer Association,JGCA)将胃淋巴结组群分为23组[12](图4)。
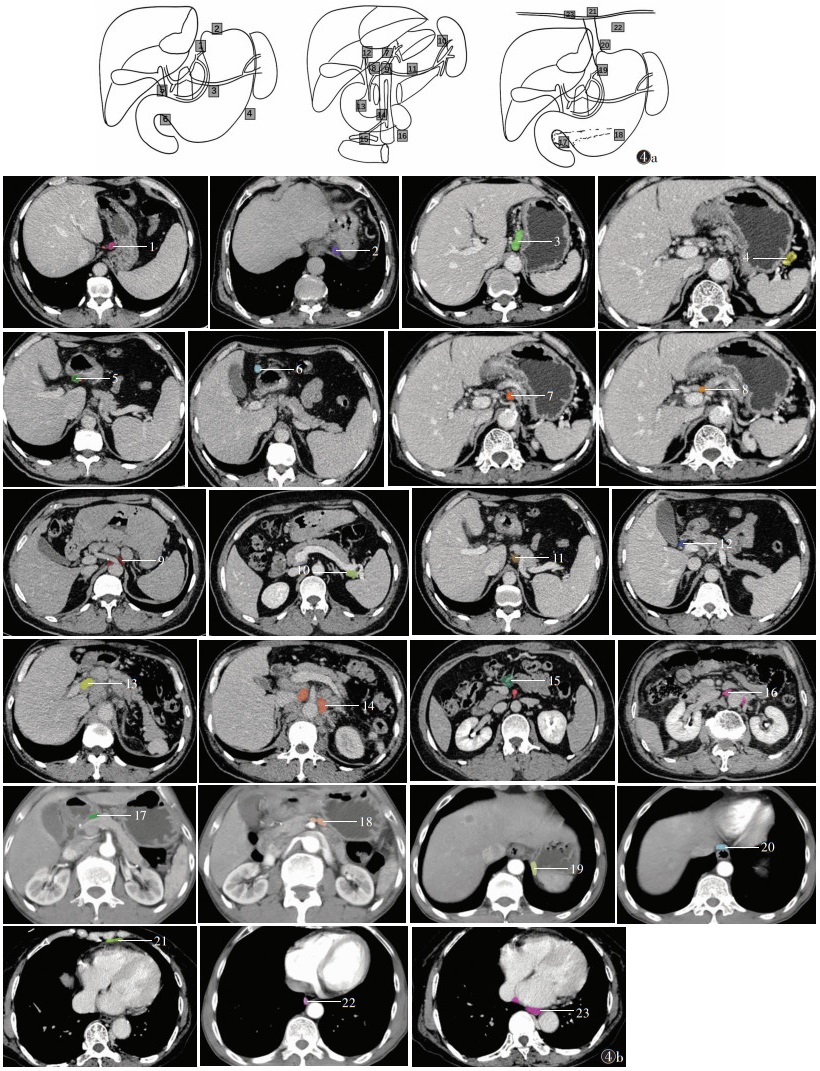 |
| 注:图4a为胃癌淋巴结分组示意图,图4b为胃癌淋巴结分组CT图像。1为贲门右淋巴结,2为贲门左淋巴结,3为胃小弯淋巴结,4为胃大弯淋巴结,5为幽门上淋巴结,6为幽门下淋巴结,7为胃左动脉周围淋巴结,8为肝总动脉周围淋巴结,9为腹腔干周围淋巴结,10为脾门淋巴结,11为脾动脉淋巴结,12为肝十二指肠韧带淋巴结,13为胰头后淋巴结,14为肠系膜根部淋巴结,15为结肠中动脉旁淋巴结,16为腹主动脉旁淋巴结,17为胰头前淋巴结,18为胰体下淋巴结,19为膈下淋巴结,20为食管裂孔部淋巴结,21为膈肌上淋巴结,22为胸下段食管旁淋巴结,23为中纵隔后淋巴结 图 4 胃癌淋巴结分组示意图及CT图像 |
CT图像不仅能显示胃肿瘤位置、大小、侵犯范围和肿瘤周围结构关系,还可量化观察胃引流区各组淋巴结径值、数目及对比剂增强特点等。现有文献对于CT图像判断淋巴结转移尚缺乏统一的标准,Dai等[13]研究表明,当分别以淋巴结短径≥8 mm、短长径之比≥0.7、强化期平均密度≥80 HU为诊断标准判断淋巴结转移时,其与术后病理结果一致性较高(K=0.831、0.873、0.849)。Jiang等[14]研究表明,当以淋巴结短径≥5 mm、短长径之比≥0.7、平扫期密度≥25 HU或静脉期密度≥75 HU为联合诊断标准时,N分期整体准确率为86.3%。因正常淋巴结多为椭圆形,当发生转移时,其形态更趋于类圆形或不规则形,因此普遍认为测量短径能更好诊断转移淋巴结[15-16]。当前,评估胃癌术前N分期仍以CT为首选影像学方法,其准确率可达73.80%~86.30%[14,17];MRI则由于空间分辨率不足与伪影限制,美国癌症联合委员会(American Joint Committee on Cancer,AJCC)胃癌管理指南并不推荐应用[18]。
1.2 肝周间隙及淋巴引流肝周间隙包括肝上间隙与肝下间隙。镰状韧带将肝上间隙分为左肝上间隙与右肝上间隙,其中左肝上间隙借左三角韧带分为左肝上前间隙与左肝上后间隙。左肝上前间隙位于肝与横膈之间、镰状韧带左侧方直到肝左外叶外侧缘、肝左三角韧带前层前方直至肝左外叶前缘;左肝上后间隙位于肝左三角韧带后层后方、向后下在肝左外叶后方直至肝后缘;左肝上前间隙与左肝上后间隙在左三角韧带游离缘相交通。正常情况下在CT和MRI图像上很难识别上述两间隙,在大量积血积液的情况下可在矢状面识别左三角韧带,从而可进一步辨别左肝上前、后间隙。右肝上间隙的左界为镰状韧带,后界为冠状韧带上层,右侧向下与右结肠旁沟交通。
肝圆韧带将肝下间隙分为左、右肝下间隙,左肝下间隙又借小网膜和胃分为左肝下前间隙(肝胃隐窝)和左肝下后间隙(网膜囊)(图5,6)。右肝下间隙的左界为肝圆韧带,上界为肝右叶脏面,下界为横结肠及其系膜。左肝下前间隙上界为肝左叶脏面,下界为横结肠及其系膜,右界为肝圆韧带,后界为胃和小网膜。根据腹膜解剖与压力梯度变化,腹部感染更易延伸至右侧而不是左侧,且经常累及肝周间隙,尤其是肝后间隙[19]。
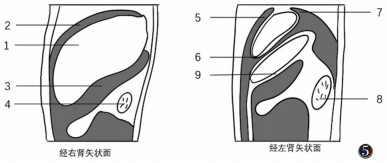 |
| 注:1为肝右叶,2为右肝上间隙,3为右肝下间隙,4为右肾,5为左肝上前间隙,6为左肝下前间隙,7为左肝上后间隙,8为左肾,9为左肝下后间隙(网膜囊) 图 5 肝周间隙矢状面示意图 |
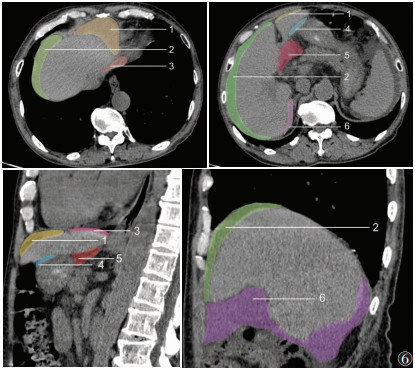 |
| 注:1为左肝上前间隙,2为右肝上间隙,3为左肝上后间隙,4为左肝下前间隙(肝胃隐窝),5为左肝下后间隙(网膜囊),6为右肝下间隙 图 6 肝周间隙CT图像 |
肝十二指肠韧带自肝门延伸至十二指肠球部后方,构成小网膜的游离右缘,其内含有门静脉、胆总管、肝固有动脉和门腔淋巴结等(图7),在左上方与肝胃韧带相延续。淋巴管和胆道的存在使肝十二指肠韧带成为各种感染的传播途径[20]。
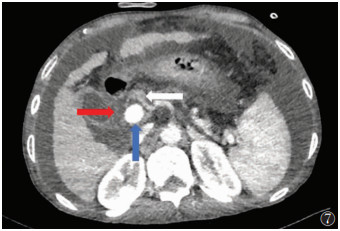 |
| 注:蓝箭所示为门静脉,白箭所示为肝动脉,红箭所示为胆总管 图 7 肝十二指肠韧带内部结构CT图像 |
网膜囊围绕肝尾状叶并分布在胃和胰腺之间,形态不规则,正常情况下仅含少量浆液,为一潜在的腔隙。其前壁由上而下依次为小网膜、胃后壁腹膜和大网膜前2层;下壁为大网膜前后反折处(胃结肠韧带);后壁由下向上依次为大网膜后2层、横结肠及其系膜;左界为胃脾韧带、脾和脾肾韧带;右界为网膜孔。肝脏及网膜囊的病变有时也可作为其他器官疾病的评估标准。网膜孔又称Winslow孔,是网膜囊与大腹膜腔交通的唯一孔道,前界为肝十二指肠韧带,后界为覆盖下腔静脉的腹膜,上界为肝尾状叶,下界为覆盖胰头的腹膜[21]。网膜孔疝约占所有内疝的8%,其内容物多为小肠,典型征象为网膜囊内出现朝向网膜孔的鸟嘴状气液积聚[22]。囊内感染积液往往由胃后壁或十二指肠后壁穿孔直接引起,也可因腹膜腔内大量积液由网膜孔进入引起,如30%~50%的急性胰腺炎患者在最初48 h内会在网膜囊内出现胰周液体积聚[23];随着积液增多,可逐渐进入右侧膈下、肝下间隙、右侧结肠旁沟,或向下破坏横结肠系膜、小肠系膜根部进入结肠下间隙,在右侧结肠下间隙会被下方的系膜阻挡,在左侧结肠下间隙则易进入盆腔[24](图8)。Suidan多因素评估量表多用来评估晚期上皮性卵巢癌肿瘤细胞减灭术结局[25],需结合CT图像准确判断腹腔各区域范围。
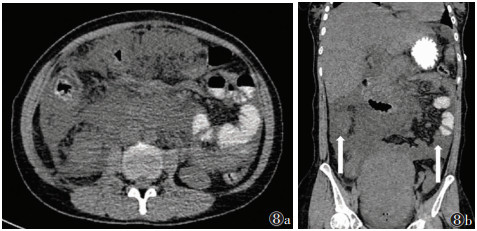 |
| 注:图8a为横断面,图8b为冠状面。胰周液体积聚并进入左、右结肠下间隙(白箭) 图 8 急性胰腺炎患者胰周积液CT图像 |
在门静脉与下腔静脉间存在相对狭窄的间隙,即门腔间隙(图9),其上、下界分别为肝门静脉分叉处与合成处。解剖学上门腔间隙包括三部分:①门静脉后间隙,位于门静脉的后壁与网膜囊前壁腹膜之间。②腹膜内间隙,相当于网膜孔的位置。③腔静脉前间隙,位于网膜囊后壁腹膜与腔静脉前壁之间[22]。门腔间隙内主要结构有肝尾状突、网膜孔、门腔淋巴结、胰钩突,以及走行于其中的血管。其中门腔淋巴结主要有2组,即网膜孔淋巴结组与胰十二指肠淋巴结组,在CT横断面图像上常将其误认为胰钩突,通过连续断面观察其是否与胰腺相延续即可辨别。
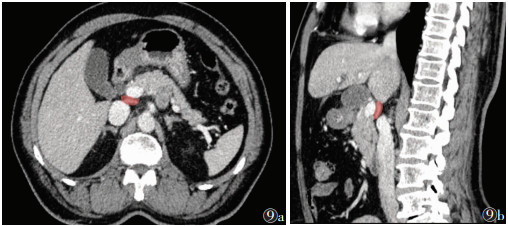 |
| 注:图9a为横断面,图9b为矢状面 图 9 门腔间隙CT图像 |
肝脏的淋巴引流分深、浅2组。浅层系统位于肝实质表面的浆膜下,分膈面与脏面两部分。膈面分为左、中、右3组:左组淋巴管注入贲门旁淋巴结;中组淋巴管经腔静脉孔进入胸腔,注入膈上淋巴结及纵隔后淋巴结;右组注入主动脉前淋巴结。脏面淋巴管大部分注入肝门淋巴结,少部分注入纵隔后淋巴结。深层淋巴引流伴随门静脉与肝静脉的分支,在肝内形成升、降两干。其中升干随肝静脉出第二肝门经膈注入纵隔后淋巴结,降干伴肝门静脉注入肝淋巴结[26](图10)。
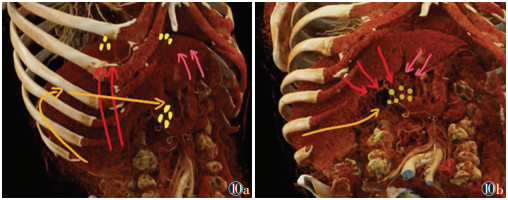 |
| 注:粉箭所示为左组淋巴结,红箭所示为中组淋巴结,橙箭所示为右组淋巴结 图 10 肝脏CT重建图像示淋巴结引流方向 |
胆囊的淋巴经由以下2条通路:右侧通路为先引流至肝十二指肠韧带内沿胆管分布的淋巴结(图11),经胰头后淋巴结汇入腹主动脉旁淋巴结;左侧通路为先引流至肝十二指肠韧带内沿肝固有动脉分布的淋巴结,经肝总动脉周围淋巴结、腹腔干周围淋巴结汇入腹主动脉旁淋巴结。胆囊肝面的淋巴直接引流入肝内淋巴结,肝外胆管的淋巴引流入肝总管与胆总管后方的淋巴结[2]。
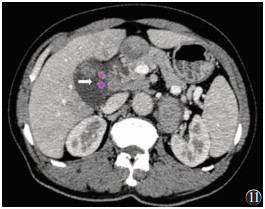 |
| 图 11 胆囊癌淋巴结转移CT图像 |
肝周区域淋巴结主要包括腹膜周围组、门静脉组、腹主动脉旁组、门腔静脉组、胰周组、腹主动脉腔静脉组及腔静脉后组(图12)。不同于胃癌,肝细胞癌淋巴结转移率较低(<30.3%)且差异较大[27],其中腹膜周围组、门静脉组及腹主动脉旁组转移率较高(<17%)[28-29]。由于肝癌患者大多数患有肝炎和肝硬化,伴反应性淋巴结肿大,目前CT与MRI均以最大短径≥10 mm为标准鉴别淋巴结良恶性[30],因此动脉期明显强化、门脉期及延迟期强化程度增强可提高恶性淋巴结的诊断准确性。
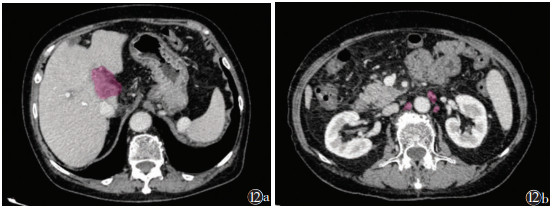 |
| 注:图12a为肝门区淋巴结转移,图12b为腹主动脉旁淋巴结转移 图 12 肝癌肝周区域淋巴结转移CT图像 |
1.3 脾周间隙及淋巴引流
脾周间隙由4个隐窝组成:脾胃面、胃与胃脾韧带上方之间为胃脾隐窝;左肾上极、脾与脾肾韧带后方之间为脾肾隐窝,胃脾隐窝与脾肾隐窝在上方与左肝上后间隙相通;网膜囊脾隐窝分别借胃脾韧带及脾肾韧带与胃脾隐窝和脾肾隐窝相邻;脾结肠隐窝位于脾、脾结肠韧带后层、结肠左曲和降结肠之间,以CT矢状面显示最佳[31](图13)。
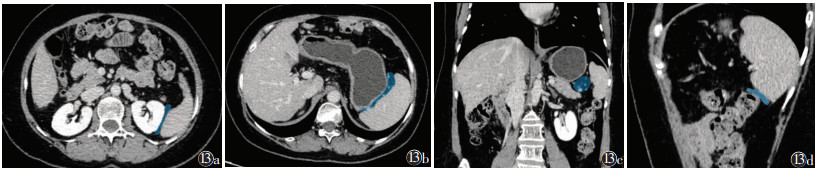 |
| 注:图13a为脾肾隐窝,图13b为胃脾隐窝,图13c为网膜囊脾隐窝,图13d为脾结肠隐窝 图 13 脾周间隙CT图像 |
脾周区域的异常可源自先天变异、炎症、感染或肿瘤等,常见病变有副脾、脾动脉瘤、脾周积气积液等,此处为腹腔转移瘤好发部位[32]。脾的毛细淋巴管起于脾白髓的动脉周围淋巴鞘,这些淋巴管与中央动脉伴行,再经较大的淋巴管引流至脾门和胰尾周围的淋巴结;随后淋巴回流至胰上淋巴结、胰下淋巴结和网膜淋巴结,并从此处回流入腹腔淋巴结和乳糜池(图14,15)。临床上对于脾脏淋巴结的研究绝大多数为胃癌根治术的脾门淋巴结切除。脾脏原发肿瘤临床上较少见,且良性肿瘤发生率约0.14%,恶性肿瘤不超过全部恶性肿瘤的0.64%[33]。
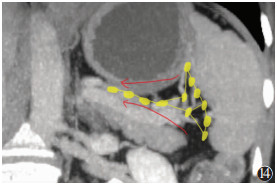 |
| 注:红箭示淋巴引流方向,黄色区域为淋巴结 图 14 脾淋巴引流示意图 |
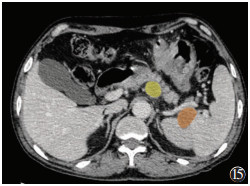 |
| 注:褐色区域为脾门淋巴结转移,黄色区域为胰体下淋巴结转移 图 15 胃癌淋巴结转移 |
| [1] |
PANNU H K, OLIPHANT M. The subperitoneal space and peritoneal cavity: basic concepts[J]. Abdom Imaging, 2015, 40(7): 2710-2722. DOI:10.1007/s00261-015-0429-5 |
| [2] |
STANDRING S. Gray’s anatomy: the anatomical basis of clinical practice[M]. Elsevier Medicine, 2020.
|
| [3] |
SOYBEL D I. Anatomy and physiology of the stomach[J]. Surg Clin North Am, 2005, 85(5): 875-894. DOI:10.1016/j.suc.2005.05.009 |
| [4] |
JAPANESE GASTRIC CANCER ASSOCIATION. Japanese gastric cancer treatment guidelines 2021(6th edition)[J]. Gastric Cancer, 2023, 26(1): 1-25. DOI:10.1007/s10120-022-01331-8 |
| [5] |
廖正银, 闵鹏秋. 胃裸区的放射解剖学研究及其临床意义[J]. 中国医学影像学杂志, 2002, 10(5): 386-387. |
| [6] |
丁国芳, 王海斌, 吴德昌. 胃裸区的形态观察及其临床意义[J]. 中国临床解剖学杂志, 1991, 9(1): 26-27. DOI:10.13418/j.issn.1001-165x.1991.01.015 |
| [7] |
刘树伟, 刘汉明, 栾铭箴, 等. 膈下间隙的横断面解剖研究[J]. 中华外科杂志, 1996, 34(2): 120-122. |
| [8] |
MOLMENTI E P, BALFE D M, KANTERMAN R Y, et al. Anatomy of the retroperitoneum: observations of the distribution of pathologic fluid collections[J]. Radiology, 1996, 200(1): 95-103. DOI:10.1148/radiology.200.1.8657951 |
| [9] |
CHEN Y, XU S, HUANG C, et al. Cancer cells invasion to the gastric bare area adipose tissue: a poor prognostic predictor for gastric cancer[J]. World J Surg Oncol, 2020, 18(1): 300. DOI:10.1186/s12957-020-02066-5 |
| [10] |
SUN R J, TANG L, LI X T, et al. CT findings in diagnosis of gastric bare area invasion: potential prognostic factors for proximal gastric carcinoma[J]. Jpn J Radiol, 2019, 37(7): 518-525. DOI:10.1007/s11604-019-00837-z |
| [11] |
DI LEO A, MARRELLI D, ROVIELLO F, et al. Lymph node involvement in gastric cancer for different tumor sites and T stage: Italian Research Group for Gastric Cancer(IRGGC)experience[J]. J Gastrointest Surg, 2007, 11(9): 1146-1153. DOI:10.1007/s11605-006-0062-2 |
| [12] |
JAPANESE GASTRIC CANCER ASSOCIATION. Japanese classification of gastric carcinoma: 3rd English edition[J]. Gastric Cancer, 2011, 14(2): 101-112. DOI:10.1007/s10120-011-0041-5 |
| [13] |
DAI C L, YANG Z G, XUE L P, et al. Application value of multi-slice spiral computed tomography for imaging determination of metastatic lymph nodes of gastric cancer[J]. World J Gastroenterol, 2013, 19(34): 5732-5737. DOI:10.3748/wjg.v19.i34.5732 |
| [14] |
JIANG M, WANG X, SHAN X, et al. Value of multi-slice spiral computed tomography in the diagnosis of metastatic lymph nodes and N-stage of gastric cancer[J]. J Int Med Res, 2019, 47(1): 281-292. DOI:10.1177/0300060518800611 |
| [15] |
CRIMI F, BAO Q R, MARI V, et al. Predictors of metastatic lymph nodes at preoperative staging CT in gastric adenocarcinoma[J]. Tomography, 2022, 8(3): 1196-1207. DOI:10.3390/tomography8030098 |
| [16] |
黄瑞庭, 徐林. 胃引流区淋巴结短径值与胃癌转移相关性探讨[J]. 中国中西医结合影像学杂志, 2013, 11(1): 22-24. |
| [17] |
YAN C, ZHU Z G, YAN M, et al. Value of multidetectorrow computed tomography in the preoperative T and N staging of gastric carcinoma: a large-scale Chinese study[J]. J Surg Oncol, 2009, 100(3): 205-214. DOI:10.1002/jso.21316 |
| [18] |
RENZULLI M, CLEMENTE A, SPINELLI D, et al. Gastric cancer staging: is it time for magnetic resonance imaging?[J]. Cancers(Basel), 2020, 12(6): 1402. |
| [19] |
BONNIN A, DUROT C, DJELOUAH M, et al. MR imaging of the perihepatic space[J]. Korean J Radiol, 2021, 22(4): 547-558. DOI:10.3348/kjr.2019.0774 |
| [20] |
ALESSANDRINO F, IVANOVIC A M, SOUZA D, et al. The hepatoduodenal ligament revisited: cross-sectional imaging spectrum of non-neoplastic conditions[J]. Abdom Radiol(NY), 2019, 44(4): 1269-1294. DOI:10.1007/s00261-018-1829-0 |
| [21] |
王建良, 朱玉春, 邢伟. 多层螺旋CT对门腔间隙的解剖学观察及其临床意义[J]. 医学综述, 2015, 21(11): 2047-2049. |
| [22] |
MORIS D, TSILIMIGRAS D I, YEROKUN B, et al. Foramen of Winslow hernia: a review of the literature highlighting the role of laparoscopy[J]. J Gastrointest Surg, 2019, 23(10): 2093-2099. DOI:10.1007/s11605-019-04353-3 |
| [23] |
ELMOHR M M, BLAIR K J, MENIAS C O, et al. The lesser sac and foramen of Winslow: anatomy, embryology, and CT appearance of pathologic processes[J]. AJR Am J Roentgenol, 2020, 215(4): 843-851. DOI:10.2214/AJR.19.22749 |
| [24] |
黄子星, 宋彬. 腹膜腔的影像解剖与临床实践[J]. 中国普外基础与临床杂志, 2021, 28(10): 1360-1364. |
| [25] |
LEDERMANN J A, RAJA F A, FOTOPOULOU C, et al. Newly diagnosed and relapsed epithelial ovarian carcinoma: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up[J]. Ann Oncol, 2018, 29(4): 259. |
| [26] |
PUPULIM L F, VILGRAIN V, RONOT M, et al. Hepatic lymphatics: anatomy and related diseases[J]. Abdom Imaging, 2015, 40(6): 1997-2011. DOI:10.1007/s00261-015-0350-y |
| [27] |
CHEN X, LU Y, SHI X, et al. Development and validation of a novel model to predict regional lymph node metastasis in patients with hepatocellular carcinoma[J]. Front Oncol, 2022, 12: 835957. |
| [28] |
黄娟, 周翔平, 姚晋, 等. 原发性肝细胞性肝癌局部淋巴结转移的螺旋CT表现[J]. 放射学实践, 2004, 19(3): 190-193. |
| [29] |
KATYAL S, OLIVER J H, PETERSON M S, et al. Extrahepatic metastases of hepatocellular carcinoma[J]. Radiology, 2000, 216(3): 698-703. |
| [30] |
ZENG Y R, YANG Q H, LIU Q Y, et al. Dual energy computed tomography for detection of metastatic lymph nodes in patients with hepatocellular carcinoma[J]. World J Gastroenterol, 2019, 25(16): 1986-1996. |
| [31] |
刘树伟, 王凡, 王永贵. 肝周间隙的矢状断面解剖及其影象学应用[J]. 中国超声医学杂志, 1991, 7(2): 39-42. |
| [32] |
ETCHISON A, MENIAS C O, GANESHAN D M, et al. A review of anatomy, pathology, and disease spread in the perisplenic region[J]. Abdom Radiol(NY), 2021, 46(2): 805-817. |
| [33] |
黄权钰, 刘天祥. 原发性脾脏肿瘤的诊断与治疗[J]. 甘肃科技, 2022, 38(12): 109-111, 119. |
 2023, Vol. 21
2023, Vol. 21


