| 睾丸恶性生殖细胞来源肿瘤的CT表现 |
睾丸肿瘤约占全身肿瘤的1%,绝大多数为恶性,好发于20~40岁。组织学可分为2大类:一类来源于睾丸生殖细胞,约占95%,包括精原细胞瘤、胚胎性癌、畸胎瘤、卵黄囊瘤等;另一类来源于睾丸间质,如睾丸间质细胞瘤和支持细胞瘤、淋巴瘤等[1]。睾丸生殖细胞来源肿瘤病理类型多样,不同组织类型的恶性程度不同,治疗及预后差异较大,其中畸胎瘤CT特征典型,易诊断,且绝大多数为良性,预后良好。笔者搜集44例经手术病理证实的睾丸恶性生殖细胞来源肿瘤,分析探讨其CT特征,以提高对这类肿瘤的认识。
1 资料与方法 1.1 一般资料回顾性分析我院2017年2月至2022年5月经手术病理证实的44例睾丸恶性生殖细胞来源肿瘤患者,年龄1~70岁,平均(27.6±3.4)岁。其中精原细胞瘤22例,卵黄囊瘤7例,胚胎性癌4例,混合性生殖细胞肿瘤11例。44例均为单发,其中21例位于右侧睾丸,21例位于左侧睾丸,2例位于隐睾。44例均以不明原因睾丸肿大就诊,病程5 d至2年余。6例伴轻度睾丸肿痛;2例就诊时已发生双肺、腹腔及腹腔后淋巴结转移,3例术后发生腹腔及腹膜后淋巴结转移。术前甲胎蛋白(AFP)检查阳性11例,阴性33例;术前血β-HCG检查仅3例轻度升高。
1.2 仪器与方法44例均行CT平扫及增强扫描。采用Siemens Somatom Definition双源CT及Siemens Somatom Force双源CT。扫描参数:120 kV,250 mAs,层厚5 mm。增强扫描使用双筒高压注射器团注对比剂碘海醇(碘浓度300 mg/mL),成人剂量70~100 mL,小儿剂量1.5 mL/kg体质量,流率3.5 mL/s,于注射后30、60 s行动、静脉期扫描。
1.3 图像分析由2位高年资泌尿生殖系统影像诊断医师,在不知病理结果情况下独立阅片,观察CT增强扫描病灶的数目、分布、大小、形态、密度、强化程度及方式等特征,意见分歧时,经上级医师综合分析后,达成统一意见。
2 结果 2.1 精原细胞瘤22例中,20例来源于睾丸,12例右侧、8例左侧;腹内型隐睾精原细胞瘤1例;腹股沟隐睾精原细胞瘤1例。肿块位于睾丸者,病变侧睾丸不同程度增大(图 1);位于腹腔及腹股沟者,肿块体积较大,相应阴囊内睾丸未显示。肿块轮廓较清晰,强化更清晰,密度不均,可见低密度囊变坏死区,未见脂肪及钙化成分;肿块实质部分呈不同程度强化,可见分隔样强化,部分可见粗大的供血动脉(睾丸动脉)。4例伴鞘膜积液,1例伴腹股沟疝。
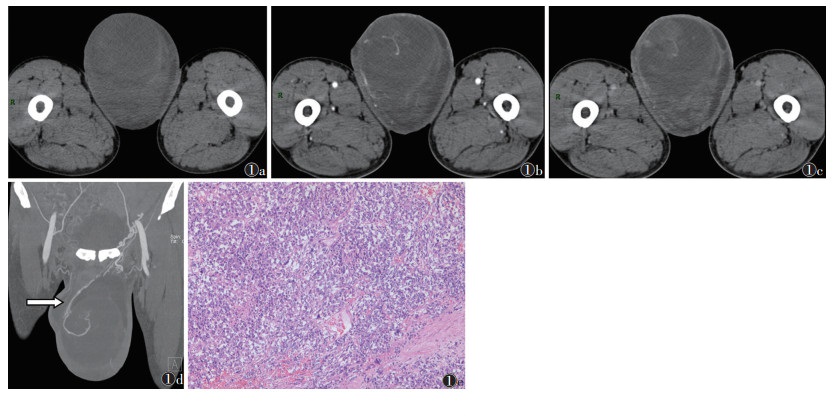 |
| 注:患者,男,49岁。图 1a~1c分别为平扫、动脉期和静脉期图像,左侧睾丸见混杂密度肿块,体积较大,内见多发液化坏死区;动脉期肿瘤实性成分轻中度强化,囊性坏死区无强化,分隔强化,未见脂肪及钙化成分;静脉期肿瘤内供血血管强化程度减退。图 1d为MIP图像,示肿块内见粗大供血动脉(睾丸动脉)(白箭)。图 1e为病理图像,示肿瘤细胞弥漫性增生伴散在淋巴细胞浸润,排列成片状、巢状或条索状,细胞异型性大,具有明显的细胞膜,核分裂象常见(HE染色,高倍放大) 图 1 睾丸精原细胞瘤CT图像及病理图像 |
2.2 卵黄囊瘤
7例中,2例位于右侧睾丸,5例左侧。肿块体积较大,密度不均、形态欠规则,CT值15~45 HU,中心见多发液化坏死区。肿瘤实性成分明显不均匀强化,可见不规则斑片状、结节状、条索状强化影,呈渐进性强化,肿块内坏死区无强化,边界清晰,未见钙化及脂肪成分(图 2)。2例术前已发生远处转移,2例术后1年腹腔多发淋巴结转移。
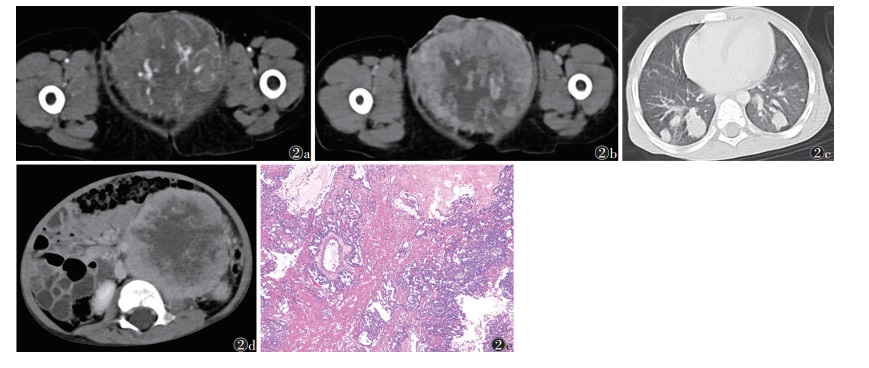 |
| 注:患者,男,2岁。图 2a,2b分别为增强扫描动脉期和静脉期图像,示睾丸体积显著增大,可见类圆形肿块,密度不均,中心见大片液化坏死区,动脉期肿瘤实性成分明显不均匀强化,可见不规则斑片状、条索状强化影;静脉期强化持续增加,呈渐进性强化特征;未见钙化及脂肪成分。图 2c,2d分别为肺窗和腹部CT图像,可见双肺、腹腔及腹膜后多发转移。图 2e为病理图像,示肿瘤细胞胚外(主要为卵黄囊)分化,见网状-微囊、附壁、卵黄囊、管状结构,并见Schiller-Duval小体形成,核深染而不规则,核仁明显,核分裂象可见(HE染色,低倍放大) 图 2 睾丸卵黄囊瘤CT图像及病理图像 |
2.3 胚胎性癌
4例中,1例位于右侧睾丸,3例左侧。睾丸密度不均,CT值20~50 HU,中心见液化坏死区,肿瘤实性成分呈轻中度强化,强化较均匀,囊性坏死区无强化,边界不清,周围脂肪间隙消失,肿块内未见脂肪及钙化成分(图 3)。
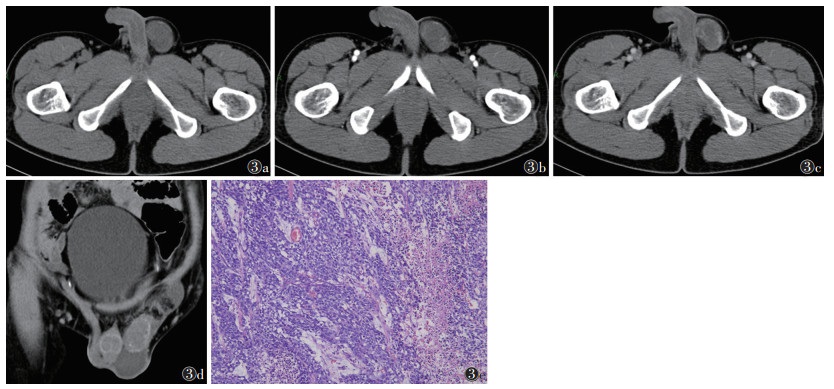 |
| 注:患者,男,33岁。图 3a~3c分别为平扫、动脉期和静脉期图像;平扫图像示睾丸体积轻度增大,见类圆形肿块,密度不均匀,形态较规则,中心见少许液化坏死区;动脉期肿瘤实性成分呈轻中度不均匀强化,未见钙化及脂肪成分;静脉期肿瘤强化程度减退。图 3d为冠状位重建图像,可见明显鞘膜积液。图 3e为病理图像,示肿瘤细胞排列成腺泡状、管状、乳头状或实性结构,伴合体性生长及坏死、出血和纤维化区域,细胞异形性显著,核大而突出,可见瘤巨细胞和奇异性肿瘤细胞,核染色质粗糙,核膜清楚,核仁明显,可见病理性核分裂象(HE染色,高倍放大) 图 3 睾丸胚胎性癌CT图像及病理图像 |
2.4 混合性生殖细胞肿瘤
11例中,6例位于右侧睾丸,5例左侧。密度不均,CT值15~80 HU,肿瘤实性成分呈中度不均匀强化,边界清,囊性坏死区无强化,未见脂肪及钙化成分(图 4)。1例术后1个月复查发生远处转移。
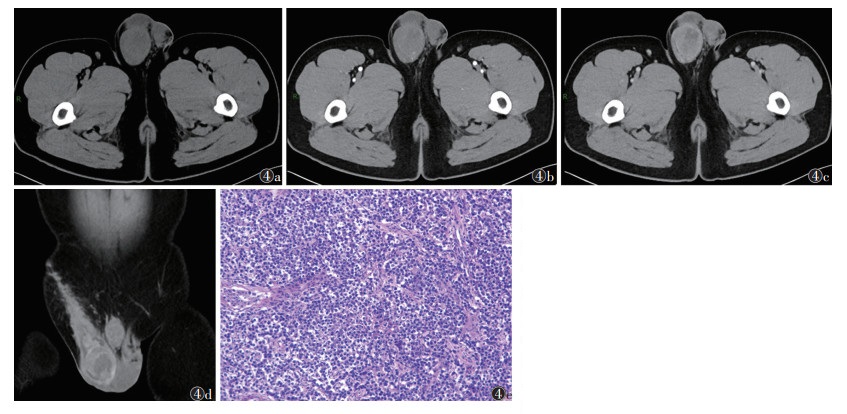 |
| 注:患者,男,27岁。图 4a~4c分别为平扫、动脉期和静脉期图像;平扫图像示右侧睾丸体积轻度增大,见类圆形肿块,形态较规则,密度欠均匀,中心见片状液化坏死区;动脉期肿瘤实性成分呈中度不均匀强化,未见钙化及脂肪成分;静脉期肿瘤内供血血管强化程度减退。图 4d为冠状位重建图像,可见明显鞘膜积液。图 4e为病理图像,示肿瘤包含2种不同的类型的生殖细胞肿瘤成分,绝大多数为胚胎性癌(约占90%),少数为精原细胞瘤(约占10%)(HE染色,高倍放大) 图 4 睾丸混合性生殖细胞肿瘤CT图像和病理图像 |
3 讨论
约95%的睾丸生殖细胞来源肿瘤源于精曲小管的生殖上皮细胞,以精原细胞瘤最常见。本组精原细胞瘤22例,占50.0%,其中2例发生于隐睾。临床上睾丸肿瘤典型表现为无痛性睾丸增大或睾丸肿块,少数患者伴轻微疼痛或坠胀感。睾丸位置表浅,超声是该类疾病的主要检查方法,但分辨力较低,对其鉴别诊断困难。CT有着良好的空间分辨力和软组织密度分辨力,增强扫描还能追踪病变供血动脉和引流静脉,较超声优势明显,可为临床诊断及分期、评估预后提供重要帮助。
精原细胞瘤属低度恶性肿瘤,好发于中青年,多为单侧,右侧略多于左侧,本研究与文献[2]报道一致。睾丸下降不全是该病发生的最重要诱因,隐睾患者发生睾丸肿瘤的概率明显高于正常人[2]。本研究中,20例肿瘤位于睾丸内,1例位于腹腔内,1例位于腹股沟区。CT平扫示:肿块密度大多较正常睾丸组织密度稍高、较均匀,边界清晰,睾丸白膜较韧厚,肿瘤极少突破白膜向外侵犯[3]。睾丸精原细胞瘤主要由睾丸动脉供血,血供较丰富,增强扫描病灶边缘和/或瘤内呈明显分隔样强化,实性部分呈轻中度强化,且强化程度较分隔样强化弱。分隔样强化是精原细胞瘤特征性表现,病理基础为肿瘤内的纤维血管分隔强化[3-4]。本研究中大部分为分隔样强化,与文献[4]报道一致。增强扫描动脉期于肿块边缘见增粗扭曲的睾丸动脉供血,静脉期见增粗扭曲的睾丸静脉引流,具有特征性[5-6],国外学者将其称为睾丸血管蒂征[7]。本组可见增粗的睾丸动脉供血和睾丸静脉引流,未见血管扭曲。
卵黄囊瘤约80%发生于性腺,以卵巢居多;20%发生于性腺以外。其影像学表现主要是边界不清欠规则的囊实性病变,可伴出血;增强扫描实性部分及囊内分隔明显强化,渐进性强化是其重要征象[8]。血清AFP显著升高为其重要诊断依据。本研究7例卵黄囊瘤血清AFP值均显著升高,其中1例高达148 542.00 μg/L,且入院胸部及腹部CT检查示双肺多发转移及腹腔、腹膜后转移。另1例腹部CT示腹腔及腹膜后多发淋巴结转移。另2例随访术后1年腹腔见多发淋巴结转移。睾丸恶性生殖细胞来源肿瘤中,卵黄囊瘤恶性程度较高,易较早发生远处转移,且术后仍易发生远处转移,预后差。血清AFP对其术前正确诊断意义重大,结合影像学特点,术前多可准确诊断。
胚胎性癌为高度恶性肿瘤,多见于20~30岁,其主要特征是肿瘤短期迅速增大,以实性成分为主,常有广泛出血、坏死,可伴少许钙化,易出现淋巴结及血行转移,增强扫描不均匀强化[9-10]。本组4例病变实性成分轻中度均匀强化,腹部未见明显转移,可能处于发病早期阶段。
混合性生殖细胞肿瘤于肿块内见多种肿瘤成分共存,其影像学表现与肿块内所含成分及所占比例有关。本组11例中,6例为精原细胞瘤与胚胎性癌不同比例混合,CT增强扫描肿瘤实性成分中度不均匀强化,囊性坏死区无强化,肿块内未见脂肪及钙化成分,其影像学表现介于精原细胞瘤与胚胎性癌之间。3例以精原细胞瘤为主、与其他生殖细胞肿瘤混合,其影像表现与精原细胞瘤类似。2例多种肿瘤共存的混合性生殖细胞肿瘤影像表现不典型,诊断较困难。
睾丸恶性生殖细胞来源肿瘤除需在生殖细胞瘤之间鉴别外,还需与非精原细胞瘤鉴别:①睾丸淋巴瘤,发病年龄较大,常 > 60岁,可双侧同时发病,其他部位可有淋巴结肿大。影像表现为密度或信号均匀肿块,边界清,增强扫描呈明显均匀强化,可有小血管穿行,体积较大者可有液化坏死;同时伴其他部位淋巴结肿大[11]。②睾丸间质细胞瘤,多发生于隐睾、睾丸萎缩和不育症患者,主要发生于20~60岁,另一高峰年龄为5~10岁。其影像表现为位于睾丸外周肿块,边界清晰,一般体积较小,密度较均匀,部分体积较大者伴液化坏死;增强扫描呈显著持续强化,伴异常激素分泌症状时,应首先考虑睾丸间质细胞瘤[12]。
总之,睾丸恶性生殖细胞来源肿瘤的CT表现具有一定特征性,早期无明显症状,肿块较大时密度不均匀,无脂肪及钙化成分。精原细胞瘤增强扫描肿块实性成分常呈轻中度均匀强化,分隔样强化是其特征性表现;卵黄囊瘤增强扫描肿块实性成分明显不均匀强化,渐进性强化是其重要征象;胚胎性癌增强扫描肿瘤实性成分呈轻中度较均匀强化,早期可有淋巴结及血行转移;混合性生殖细胞肿瘤CT表现与肿块内所含成分及所占比例有关。结合实验室AFP等指标,有助于提高对该类疾病的诊断准确率,最终确诊需依靠组织病理学检查。
| [1] |
DALAL P U, SOHAIB S A, HUDDART R. Imaging of testicular germ cell tumours[J]. Cancer Imaging, 2006, 6(1): 124-134. DOI:10.1102/1470-7330.2006.0020 |
| [2] |
GLIMELIUS B, BEETS-TAN R, BLOMQVIST L, et al. Mesorectal fasciainstead of circumferential resection margin in preoperative staging of rectal cance[J]. J Clin Oncol, 2011, 29(16): 2142-2143. DOI:10.1200/JCO.2010.34.4473 |
| [3] |
王培旭, 陈洁婷, 涂蓉. 睾丸精原与非精原细胞瘤CT与MRI影像学诊断研究[J]. 临床放射学杂志, 2021, 40(5): 965-969. |
| [4] |
贾承晔, 张晓琴, 杨署, 等. 睾丸实性肿块的CT和MRI表现特征[J]. 中国医学影像技术, 2017, 33(6): 929-932. |
| [5] |
李斌, 徐志锋, 朱彬. 腹内型隐睾精原细胞瘤的MSCT特征[J]. 医学影像学杂志, 2016, 26(11): 2065-2068. |
| [6] |
石义志, 吕国士, 赖丙林, 等. 睾丸精原细胞瘤的MSCT及MRI表现[J]. 中国中西医结合影像学杂志, 2016, 14(6): 716-718. DOI:10.3969/j.issn.1672-0512.2016.06.034 |
| [7] |
VALDEVENITO J P, GALLEGOS I, FERNANDEZ C, et al. Correlation between primary tumor pathologic features and presence of clinical metastasis at diagnosis of testicular seminoma[J]. Urology, 2007, 70(4): 777-780. DOI:10.1016/j.urology.2007.05.020 |
| [8] |
赵振, 胡俊, 费维敏. 儿童睾丸卵黄囊瘤的MRI诊断[J]. 临床放射学杂志, 2021, 40(8): 1574-1576. |
| [9] |
冯莉娟, 杨青, 杨菲菲, 等. 睾丸胚胎癌的影像学表现及鉴别诊断[J]. 实用放射学杂志, 2021, 37(3): 424-426. |
| [10] |
王建明, 赵双全, 宋世军, 等. 睾丸良恶性肿块的CT、MRI表现及鉴别诊断[J]. 中国中西医结合影像学杂志, 2019, 17(2): 143-146. DOI:10.3969/j.issn.1672-0512.2019.02.009 |
| [11] |
刘伟. 原发性睾丸淋巴瘤的MRI表现[J]. 中国中西医结合影像学杂志, 2021, 19(1): 69-71, 77. DOI:10.13929/j.issn.1003-3289.2020.09.020 |
| [12] |
龙德云, 谭细凤, 张艳, 等. 睾丸间质细胞瘤的CT/MRI表现及文献复习[J]. 中国临床医学影像杂志, 2014, 25(2): 136-138. |
 2024, Vol. 22
2024, Vol. 22


