| 基于CT影像组学预测胃腺癌淋巴结转移的价值 |
2. 江苏省扬州市第二人民医院影像科,江苏 扬州 225007
近年来,胃癌死亡率和发病率分别居全球恶性肿瘤的第4位和第5位[1]。胃腺癌是胃癌中最常见的一种病理类型,占胃癌患者的90%以上[2],多数患者就诊时已处于进展期[3]。淋巴结转移是胃癌最常见的转移方式[4]。根治性胃切除术是该病最重要的治疗方法,部分晚期患者仍需在此基础上进行辅助或新辅助治疗[5],因此术前评估淋巴结是否发生转移对临床治疗方案选择尤为重要。目前,CT增强扫描是胃癌的首选影像检查方法[6]。影像组学是一种新兴的技术,其基于影像图像,提取影像特征参数建立影像组学模型,用以辅助临床疾病诊疗[7-8]。近年来,影像组学研究已在预测肿瘤的基因表型、病理类型、淋巴结转移及预后等方面显示出重要潜能[9-11]。本研究拟用影像组学方法预测胃腺癌的淋巴结转移。
1 资料与方法 1.1 一般资料回顾性收集2019年1月至2021年12月经术后病理证实为胃腺癌患者的腹部CT增强扫描图像及临床资料。纳入标准:(1)外科手术切除且术后病理确诊为胃腺癌;(2)临床资料及术后病理资料完整;(3)术前行CT增强扫描检查且癌灶显示确切;(4)术前未行放化疗、新辅助治疗等。排除标准:(1)术前曾行放化疗、新辅助治疗等;(2)CT增强扫描图像质量不符合要求(图像质量不佳、无法清晰显示病灶等);(3)未有确切病理结果者。共纳入174例患者,其中男133例,女41例;年龄46~89岁,平均(67.29±8.10)岁。根据有无淋巴结转移,将患者分为阳性组104例和阴性组70例。
1.2 仪器与方法采用GE Optima CT660 MSCT扫描仪。增强扫描前常规禁食8 h,检查前15 min一次性口服2.0%泛影葡胺溶液800~1 000 mL,经肘静脉注射对比剂碘海醇(碘浓度300 mg/mL),剂量80~100 mL,注射流率2.5~3.0 mL/s。层厚、层距均为5 mm。于注射后25~30、60~70 s行动脉期、门静脉期扫描。
1.3 图像分析及处理将所有图像以DICOM格式导入到“uAI Research Portal”平台上,由1名具有多年CT诊断经验的影像科医师于动脉期及门静脉期图像最大横断层面手动勾画ROI。同一患者的增强扫描动脉期及门静脉期图像保持在同一界面,选择病灶最大截面,避开周围气体及液体,在距肿瘤边缘2 mm处绘制肿瘤区域。再由1名诊断经验丰富的高年资影像科医师对ROI勾画分割结果进行校对,意见不统一时,经讨论达成共识(图 1)。并对勾选的ROI进行影像组学特征提取。共提取7类影像组学特征:一阶特征、形态、灰度行程矩阵、灰度共生矩阵、灰度大小区域矩阵、灰度依赖矩阵及邻域灰度差分矩阵。
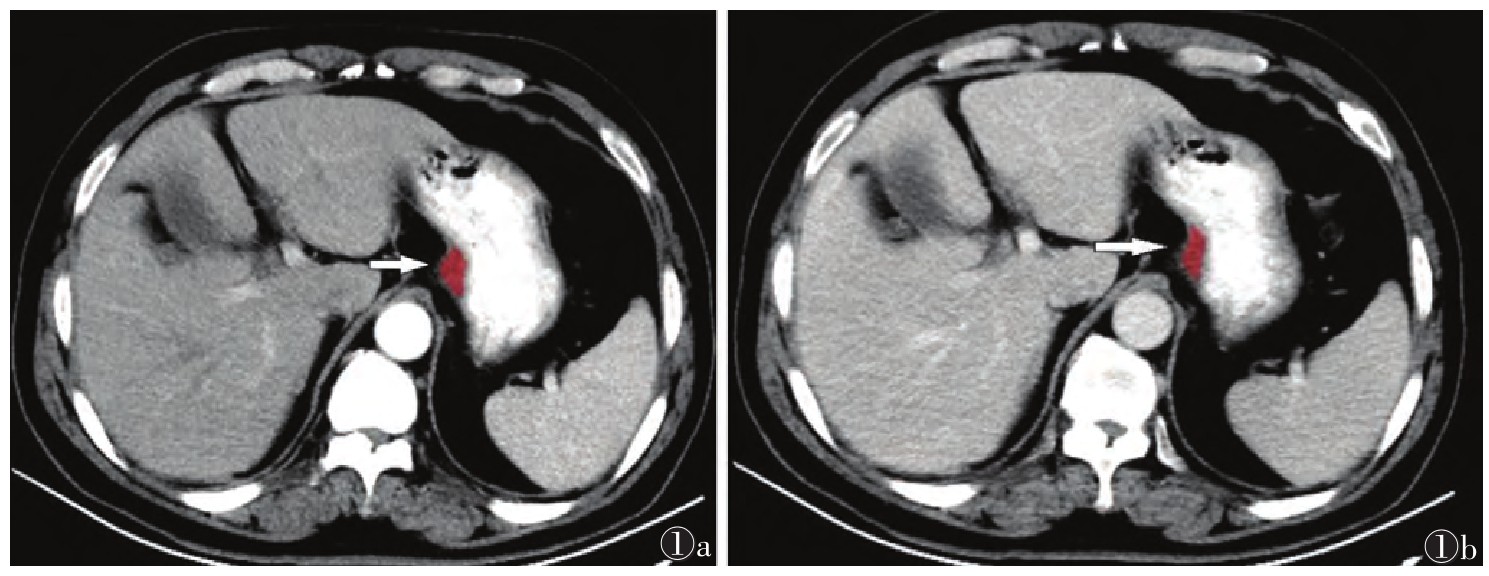 |
| 注:患者,男,67岁。图 1a为CT动脉期最大横断层面勾画ROI(箭头),图1b为CT门静脉期最大横断位层面勾画ROI(箭头) 图 1 胃腺癌的ROI勾画示意图 |
1.4 特征提取和筛选
在“uAI Research Portal”平台从动脉期及门静脉期CT图像中提取影像组学特征各2 600个,数据分组采用5折交叉验证,采用Z分数归一化及最小绝对收缩与选择算子(LASSO)特征选择方法,并设置最优协调参数alpha值分别为0.08、0.05,提取最优特征参数。双期融合模型则在动脉期及门静脉期提取的特征基础上设置α=0.05,进一步筛选最佳特征参数。
1.5 模型建立与评估根据选择的特征对数据分类,3种预测模型均采用Z分数归一化对数据做预处理,使用逻辑回归分类器分类构建动脉期、门静脉期及双期融合模型。所有样本经5折交叉验证后分为训练集139例(淋巴结转移83例,淋巴结未转移56例)和测试集35例(淋巴结转移21例,淋巴结未转移14例)。用ROC曲线及AUC评价训练集模型的预测能力,用测试集数据验证相应模型的预测能力。AUC结果:0.50~0.59为差;0.60~0.69为一般;0.70~0.79为良好;0.80~0.89为非常好;0.90~1.00为优秀。
1.6 统计学分析采用SPSS 25.0软件进行统计分析。计量资料采用Shapiro-Wilk检验,数据符合正态分布,采用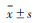
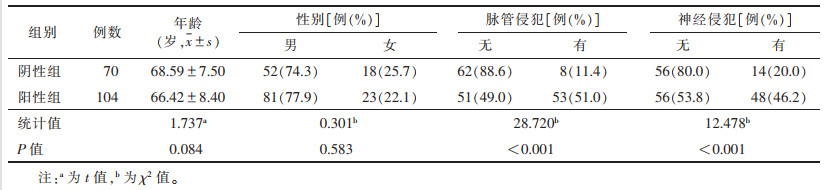
2组年龄、性别差异均无统计学意义(均P > 0.05),脉管侵犯、神经侵犯情况比较差异均有统计学意义(均P < 0.05)(表 1)。
| 表 1 淋巴结转移阴性组、阳性组临床特征比较 |
 |
2.2 影像组学预测模型
对动脉期及门静脉期各原始特征参数(2 600个)过滤筛选后分别得到10、14个特征参数,将其双期融合筛选后共得到15个特征参数(表 2)。
| 表 2 动脉期、门静脉期及双期融合筛选的影像组学特征参数 |
 |
动脉期、门静脉期及双期融合3种模型中的特征参数wavelet_glszm_wavelet-hhh-zoneentropy在淋巴结阴性组及阳性组之间差异均有统计学意义(均P < 0.001)。
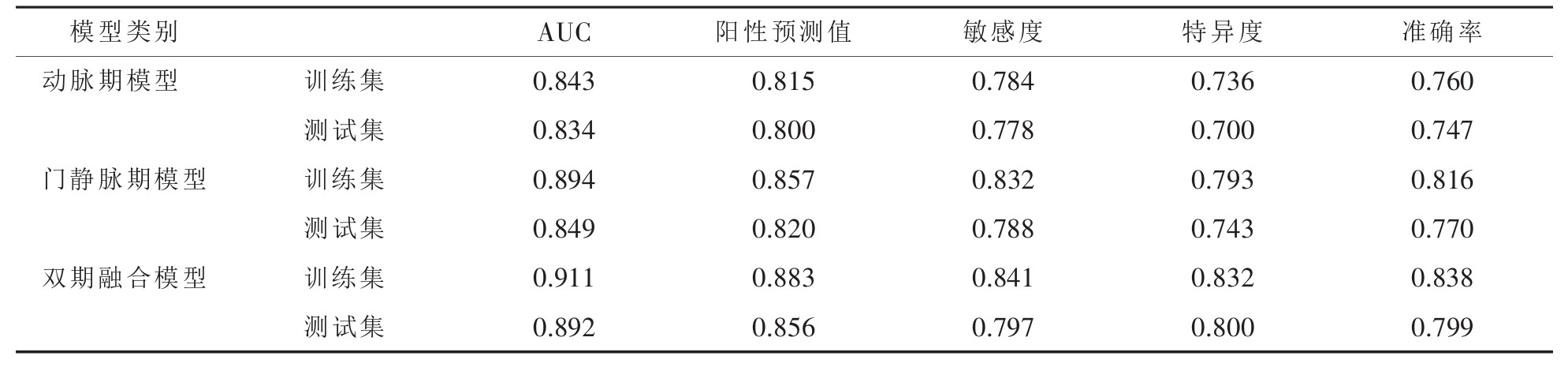
动脉期、门静脉期及双期融合模型训练集AUC分别为0.843、0.894、0.911(图 2),测试集分别为0.834、0.849、0.892(图 3)。3个影像组学模型对淋巴结转移均具有较好的预测效能,其中融合模型较单纯动脉期或门静脉期模型效果更好,精确率、敏感度、特异度及准确率优于前两者(表 3)。
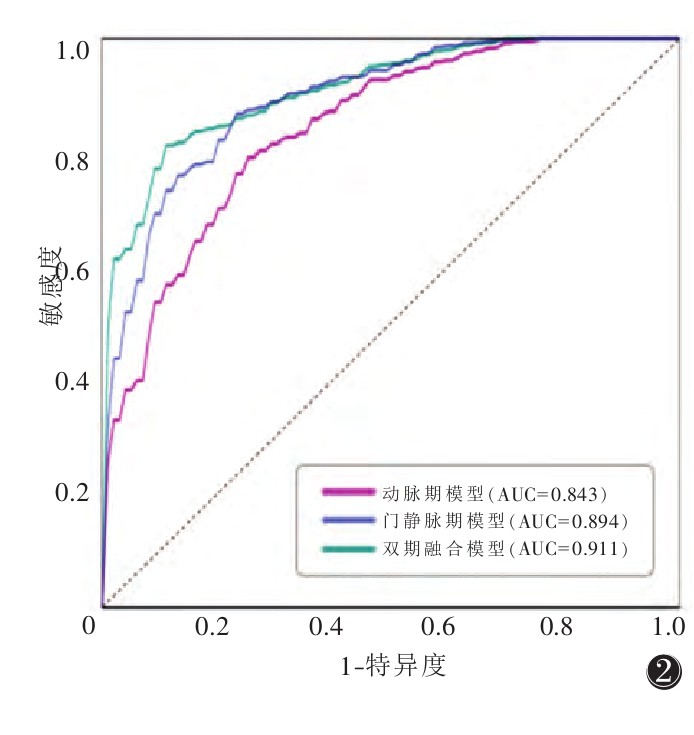 |
| 图 2 训练集不同期相逻辑回归模型ROC曲线 |
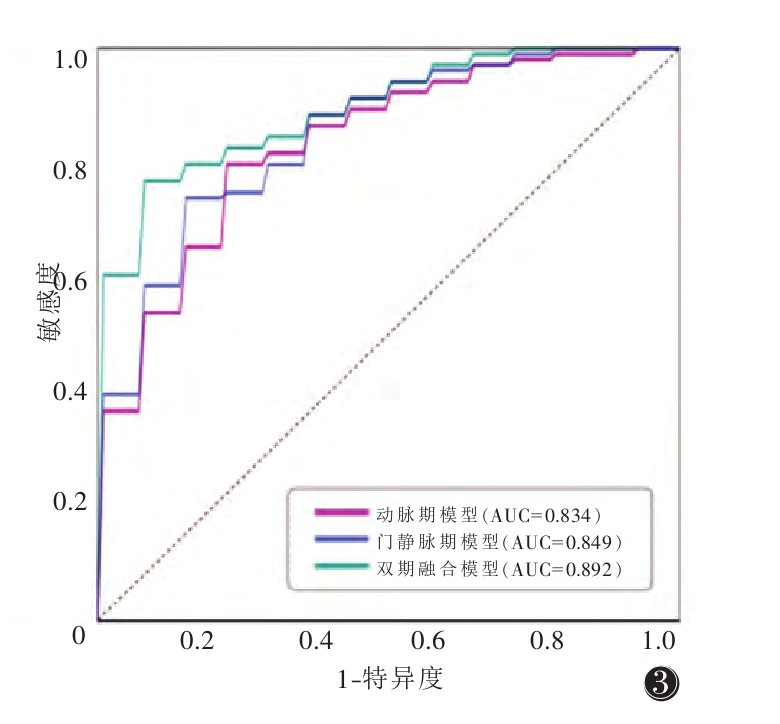 |
| 图 3 测试集不同期相逻辑回归模型ROC曲线 |
| 表 3 影像组学模型预测胃腺癌淋巴结转移的评估效能分析 |
 |
3 讨论
我国是全球胃癌发病率最高的国家,且我国胃癌患者在临床病理学特征、治疗方式及药物选择等方面与全球其他区域有差异[12]。淋巴结转移是胃癌最常见转移方式,亦是影响预后的重要因素之一[13]。术前准确评估胃癌淋巴结转移情况对手术规划至关重要。而CT检查是胃癌术前评估淋巴结转移的主要手段[14]。影像组学可从医学图像中提取大量数据信息,全面、动态评估肿瘤的异质性,定量描述肿瘤表型[15]。
本研究利用影像组学方法深度挖掘肿瘤自身图像的细微差别,提取可评价淋巴结情况的特征信息,并采用逻辑回归分类器建立模型用以预测淋巴结转移情况。胃腺癌深部纤维结缔组织较多,门静脉期的强化程度高于动脉期[16],本研究显示门静脉期AUC大于动脉期,表明肿瘤门静脉期特征对反映肿瘤特征更具优势,与Li等[17]研究一致。Wang等[18]所构建动脉期模型AUC达0.886,较本研究略高,可能与分类器差异有关。Li等[17]建立了动脉期和门静脉期影像组学模型用于预测胃腺癌淋巴结转移的效能,结果显示门静脉期AUC为0.76,高于动脉期(0.71),其研究采用双能CT图像,不同能量图像的组合丰富了输入特征,拓展了传统CT的能力。本研究采用普通CT增强扫描图像,获得的图像信息较其有所不足,不过预测模型具有更广泛的适用性,纳入例数虽较其略少,但增加了双期融合预测模型,且所得动脉期及门静脉期模型AUC均较Li等[17]报道的略高,提示融合模型能更好预测胃腺癌淋巴结转移。
本研究显示,年龄及性别在胃腺癌淋巴结转移组与非转移组之间差异无统计学意义,脉管及神经侵犯情况在2组间差异有统计学意义,与既往研究[19-21]一致。淋巴结转移阳性组发生脉管侵犯及神经侵犯的概率分别为51.0%、46.2%,较阴性组的11.4%、20.0%显著升高,提示脉管侵犯及神经侵犯与淋巴结转移存在一定相关性。肿瘤细胞侵及胃壁黏膜下层时,会在其脉管系统中形成癌栓,且浸润越深越易发生,癌栓是癌细胞发生扩散和转移的关键环节[22-23]。脉管及神经组织侵犯的胃腺癌具有较强的浸润和转移能力[20-21],同时脉管和神经侵犯也是进展期胃癌患者术后肿瘤复发、转移的独立危险因素[24]。脉管及神经侵犯直接影响胃癌治疗方式,部分有神经束或血管、淋巴管浸润胃癌患者需行辅助化疗[25],术中无法扩大切除、存在或疑有脉管、神经侵犯及分化类型差再化疗敏感度较低的胃癌患者可考虑术中放疗[12]。
目前,各种组学软件较多,特征参数亦不尽相同。本研究动脉期、门静脉期及双期融合3种模型中特征参数wavelet_glszm_wavelet-hhh-zoneentropy在淋巴结转移阴性组及阳性组间差异均有统计学意义,提示其可能是预测胃腺癌淋巴结是否转移的关键特征参数,但其是否为确切关键特征参数仍有待进一步研究。
本研究存在的不足:①对肿瘤的勾画仅选取了最大直径层面,未对三维立体的肿瘤进行评价;②样本量较小,缺乏多中心研究;③未与其他临床指标结合建立联合模型。
总之,通过获取胃腺癌不同期相CT增强扫描图像影像组学特征,构建逻辑回归模型能够有效地进行术前胃腺癌淋巴结转移的预测,且具有较好的预测效能。但影像组学所提取的特征受诸多因素影响,未来研究的样本量仍需进一步扩大,为胃腺癌患者术前诊断及治疗方案的选择提供更全面的依据。
| [1] |
SUNG H, FERLAY J, SIEGEL R L, et al. Global cancer statistics 2020: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J]. CA Cancer J Clin, 2021, 71(3): 209-249. DOI:10.3322/caac.21660 |
| [2] |
王思月, 张洪梅, 胡文倩, 等. 胃腺癌相关关键基因的筛选及其调控通路研究[J]. 华北理工大学学报(医学版), 2022, 24(2): 99-106, 112. DOI:10.19539/j.cnki.2095-2694.2022.02.003 |
| [3] |
东强, 曲丽洁, 张宏, 等. 双能量CT碘值及增强值与进展期胃腺癌病理分化程度的相关性[J]. 临床放射学杂志, 2020, 39(5): 931-935. DOI:10.13437/j.cnki.jcr.2020.05.019 |
| [4] |
ZHU Y, FANG X, WANG L, et al. A predictive nomogram for early death of metastatic gastric cancer: a retrospective study in the SEER database and China[J]. J Cancer, 2020, 11(18): 5527-5535. DOI:10.7150/jca.46563 |
| [5] |
VAN CUTSEM E, SAGAERT X, TOPAL B, et al. Gastric cancer[J]. Lancet, 2016, 388(10060): 2654-2664. DOI:10.1016/S0140-6736(16)30354-3 |
| [6] |
寸红丽, 李华秀, 张大福, 等. 双能CT影像组学在诊断不同分化程度胃癌中的应用[J]. 中国医学影像学杂志, 2020, 28(9): 669-672, 687. |
| [7] |
LIU Z, WANG S, DONG D, et al. The applications of radiomics in precision diagnosis and treatment of oncology: opportunities and challenges[J]. Theranostics, 2019, 9(5): 1303-1322. DOI:10.7150/thno.30309 |
| [8] |
LAMBIN P, LEIJENAAR R T H, DEIST T M, et al. Radiomics: the bridge between medical imaging and personalized medicine[J]. Nat Rev Clin Oncol, 2017, 14(12): 749-762. DOI:10.1038/nrclinonc.2017.141 |
| [9] |
SUTTON E J, OH J H, DASHEVSKY B Z, et al. Breast cancer subtype intertumor heterogeneity: MRI-based features predict results of a genomic assay[J]. J Magn Reson Imaging, 2015, 42(5): 1398-1406. DOI:10.1002/jmri.24890 |
| [10] |
李丽, 郑玉荣, 张静, 等. MRI参数与三阴性乳腺癌组织病理学分级及淋巴结转移的相关性研究[J]. 中国中西医结合影像学杂志, 2020, 18(4): 374-378. |
| [11] |
PENG H, DONG D, FANG M J, et al. Prognostic value of deep learning PET/CT-based radiomics: potential role for future individual induction chemotherapy in advanced nasopharyngeal carcinoma[J]. Clin Cancer Res, 2019, 25(14): 4271-4279. DOI:10.1158/1078-0432.CCR-18-3065 |
| [12] |
中国抗癌协会胃癌专业委员会. 胃癌诊治难点中国专家共识(2020版)[J]. 中国实用外科杂志, 2020, 40(8): 869-904. |
| [13] |
KINAMI S, NAKAMURA N, TOMITA Y, et al. Precision surgical approach with lymph-node dissection in early gastric cancer[J]. World J Gastroenterol, 2019, 25(14): 1640-1652. |
| [14] |
唐磊. 胃癌术前影像学精准分期存在的争议与困惑[J]. 中华胃肠外科杂志, 2016, 19(2): 165-169. |
| [15] |
黄庆, 王卫东, 郎锦义. 影像组学技术进展及其在非小细胞肺癌中的应用[J]. 肿瘤预防与治疗, 2018, 31(3): 206-212. |
| [16] |
高歌, 梁盼, 王睿, 等. CT鉴别诊断胃神经内分泌癌与胃腺癌[J]. 中国介入影像与治疗学, 2021, 18(8): 465-469. |
| [17] |
LI J, DONG D, FANG M, et al. Dual-energy CT-based deep learning radiomics can improve lymph node metastasis risk prediction for gastric cancer[J]. Eur Radiol, 2020, 30(4): 2324-2333. |
| [18] |
WANG Y, LIU W, YU Y, et al. CT radiomics nomogram for the preoperative prediction of lymph node metastasis in gastric cancer[J]. Eur Radiol, 2020, 30(2): 976-986. |
| [19] |
王睿, 李靖, 梁盼, 等. 能谱CT术前预测胃腺癌淋巴结转移的价值[J]. 临床放射学杂志, 2019, 38(3): 469-474. |
| [20] |
王文鹏, 黄光磊, 薛英威. 胃腺癌脉管浸润的临床病理特征及预后分析[J]. 肿瘤学杂志, 2015, 21(12): 988-992. |
| [21] |
王林, 李海刚, 曾弘, 等. 胃腺癌神经浸润的临床病理学意义[J]. 中国热带医学, 2006, 6(9): 1612-1613. |
| [22] |
FUJIKAWA H, KOUMORI K, WATANABE H, et al. The clinical significance of lymphovascular invasion in gastric cancer[J]. In Vivo, 2020, 34(3): 1533-1539. |
| [23] |
LI P, HE H Q, ZHU C M, et al. The prognostic significance of lymphovascular invasion in patients with resectable gastric cancer: a large retrospective study from Southern China[J]. BMC Cancer, 2015, 15: 370. |
| [24] |
HWANG J E, HONG J Y, KIM J E, et al. Prognostic significance of the concomitant existence of lymphovascular and perineural invasion in locally advanced gastric cancer patients who underwent curative gastrectomy and adjuvant chemotherapy[J]. Jpn J Clin Oncol, 2015, 45(6): 541-546. |
| [25] |
国家卫生健康委员会. 胃癌诊疗规范(2018年版)[J/CD]. 中华消化病与影像杂志(电子版), 2019, 9(3): 118-144.
|
 2023, Vol. 21
2023, Vol. 21


