| MRI对弥漫性轴索损伤的诊断及预后评估 |
弥漫性轴索损伤(diffuse axonal injury,DAI)是一种弥漫性脑损伤,由于头部受到加速旋转外力重创,在剪切力下导致脑内神经轴索断裂、毛细血管损伤而引起原发性脑损伤,多见于重度创伤性患者[1-2]。DAI的诊断主要依据CT和MRI结果[3-5],病理分级则主要依靠Adams分级方法。本文采用MRI 3种序列量化DAI病灶分布,并尝试建立MRI分级标准评估长期预后。
1 资料与方法 1.1 一般资料前瞻性研究我院自2016年1月至2018年1月收治的30例DAI患者,均经CT和MRI双重确诊。其中男26例,女4例;年龄16~60岁,平均(31.21±4.62)岁。纳入标准:年龄>15岁;格拉斯哥昏迷评分(Glasgow Coma Score,GCS) < 9分或格拉斯哥运动评分(Glasgow Motor Score,GMS) < 6分;软组织肿块 < 25 cm、意识清醒;MRI证实脑动脉相关病灶、无凝血或抗凝治疗史。受伤原因:交通损伤18例,运动伤7例,跌倒4例,攻击1例。
1.2 治疗方法一线治疗,使用间歇性静脉注射吗啡镇痛法和连续静脉注射异丙酚(1~4 mg·kg-1·h-1),进行气管通气。所有患者均行颅内压力及脑灌注压监护,并持续测量。PaCO2 30~35 mmHg(1 mmHg=0.133 kPa);30°抬高床头,中心静脉压力为0~5 mmHg。将颅内压力保持 < 20 mmHg,脑灌注压保持>60 mmHg。二线治疗,持续戊巴比妥钠输注治疗和(或)减压开颅手术。
1.3 仪器与方法入院初步行CT检查,按照Marshall CT进行评分。待病情稳定、创伤1周内立即行MRI检查。MRI使用GE Discovery 750 W 3.0 T MRI扫描仪,扫描序列和参数:T2*GRE序列TR 500 ms,TE 14 ms,翻转角30°,体素0.9 mm×0.9 mm×3.0 mm;DWI序列SE-EPI,b值1 000 s/mm2,TR 4 700 ms,TE 89 ms,体素1.2 mm×1.2 mm×5.0 mm;SWI序列TR 49 ms,TE 40 ms,翻转角15°,体素0.9 mm×0.9 mm×1.5 mm。
1.4 病理分级及一致性评估采用Adams病理分级标准,对每个序列病灶进行分级。Adams组织病理学分级为1~3级,灰白质交界面(Ⅰ级)、胼胝体(Ⅱ级)和背外侧、吻侧脑干(Ⅲ级)。计算每个MRI序列显示的大脑中线两侧的DAI相关病灶,计算与Adams病理分级一致性。
1.5 预后评估指标根据扩展格拉斯哥结局量表(extended glasgow outcome scale,GOSE)[6]评估预后:死亡、植物状态、重度残疾、严重残疾、中度残疾、中等残疾(恢复以前的工作但需要一些调整)、恢复良好(伴有轻微的身体和智力缺陷)、恢复良好,对应分别记为1、2、3、4、5、6、7、8分,并电话随访,评估治疗6个月后的预后情况。
1.6 统计学方法采用SPSS 21.0统计软件进行数据分析。分类变量采用线性加权Cohen K分析[7],连续变量采用组内相关系数(intraclass correlation coefficient,ICC)表示。正态分布使用t检验,Fisher精确检验用于组间比较,Mann-Whitney U检验用于偏态分布。以GOSE为因变量,Logistics回归分析预后因素。以P < 0.05为差异有统计学意义。
2 结果 2.1 临床基本特征及单因素分析(表 1)| 表 1 人口统计学数据和临床因素与长期预后(GOSE)的相关性 |
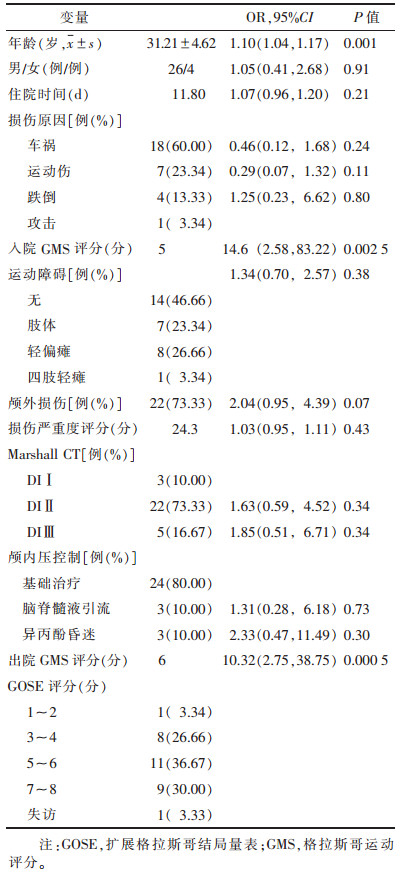 |
单因素分析显示,年龄、入院时和出院时GMS评分与长期不良预后显著相关(均P < 0.05)。
2.2 病灶分布及单因素分析(表 2)| 表 2 Logistic分析DAI病灶与长期预后(GOSE)的关系 |
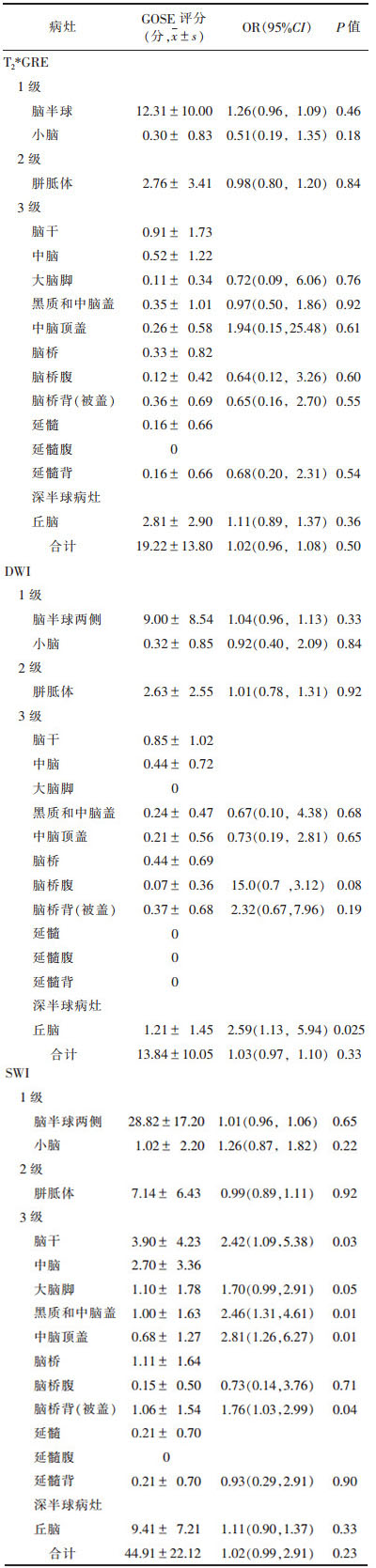 |
SWI序列比T2*GRE序列在脑半球、胼胝体、脑干中发现更多的出血病灶(均P < 0.05)。SWI比DWI发现更多病灶,包括脑半球、胼胝体、脑干、丘脑、基底神经节、内囊(均P < 0.05)。T2*GRE和DWI序列在显示病灶分布方面,无明显差异(P > 0.05)。
SWI序列显示黑质和中脑盖、中脑顶盖和背侧脑桥出血病灶均与长期不良预后显著相关(均P < 0.05)。
DWI显示丘脑病灶与长期不良预后有显著相关性(P < 0.05)。T2*GRE序列示病灶与长期不良预后均无显著相关性(均P > 0.05)。
SWI序列发现10例双侧脑干病灶,DWI序列发现3例,T2*GRE序列发现2例。SWI序列显示双侧脑干出血性病灶与长期不良预后显著相关(P=0.03)。
2.3 DAI的MRI分级(表 3)| 表 3 MRI所示病灶分级 |
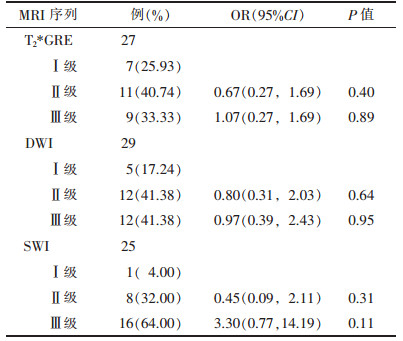 |
30例中21例(70.00%)是Adams 3级患者。SWI序列比T2*GRE序列识别更多DAI 3级患者(P=0.006)。
2.4 评判间一致性DAI分级,黑质和中脑被盖区病灶分级,与Cohen K>0.8大体一致(均值0.90,0.82~0.91)。组内相关系数表明,3种序列量化DAI相关病灶,具有良好的一致性,平均ICC 0.66(0.62,0.68)。
2.5 多变量分析预后因子以GOSE为因变量进行多变量分析,结果显示,DWI序列显示的丘脑病灶及SWI序列显示的黑质和中脑被盖区病灶均与长期不良预后显著相关(均P < 0.05)。≥30岁患者的黑质和中脑被盖出血性病灶与长期不良预后独立相关(P=0.012)。
3 讨论 3.1 MRI序列病灶分布MRI因诊断准确率高,已成为临床检测出血和非出血性DAI病灶的首选方式[8]。DWI可显示非出血病灶,T2*GRE和SWI可显示出血病灶,但SWI序列能更好地显示组织间的敏感性差异,因此对出血病灶的敏感性高于T2*GRE。以往研究[9]证明,SWI比T2*GRE显示更多的微出血病灶,与本研究结果一致。但由于脱氧、缺血可能被误读为出血性病灶,使得SWI序列比T2*GRE和DWI序列更难鉴别[10]。SWI发现的病灶数量多于DWI,但DWI序列中,细胞水肿增加了信号强度,T2信号也增强,两者可见不同的损伤改变,各有优势[11-12]。
本研究中,患者在受伤后的1周内接受MRI检查,DWI序列出血性病灶似乎在急性期后仍然存在,因此采用DWI序列时,更要重视检查时机。本研究发现额叶、颞叶及胼胝体均有病灶。脑干病灶比例最高且主要在中脑和上脑桥。Moen等[13]研究了128例DAI患者,在0~28 d内接受MRI检查,发现DWI序列显示胼胝体病灶是预后最重要的预测因子,与本研究结果不同。然而,其研究包含了不同程度的脑外伤患者,其中31%的患者存在转移性肿块病灶。另有研究[14-15]表明,基底神经节和内囊深部病灶,特别是丘脑病灶可预测DAI的不良预后。丘脑病灶也被认为是植物生存状态的主要特征。此种相关性可在DWI序列深度幕上病灶中发现,但调整了其他预后因素后,此种相关性失去了意义。单因素分析显示,SWI序列中脑顶盖和背侧脑桥与长期不良预后相关。然而,多因素分析发现仅黑质和中脑被盖病灶具有独立的预后价值。多项研究[16-18]发现,DAI相关病灶中,脑干病灶最具争议。浅表脑干病灶可能是受脑干幕缘影响,而深部病灶可能是真正的损伤机制,因此深部病灶与长期不良预后存在较强的相关性。
多因素分析显示,脑室和顶盖病灶位于浅表部位,与长期不良预后无显著联系。与T2*GRE相比,SWI对出血灶的检测检出率更高,因此可对脑干病灶进行更精准的定位。仅使用T2*GRE,可能漏掉中脑中部区域的病灶,因此建议行T2*GRE序列扫描后,再补充SWI序列。
3.2 预后因素分析多项研究[19-20]显示老年DAI患者死亡率更高,长期预后更差。本研究中,患者平均年龄(31.21±4.62)岁,比一般的DAI患者年轻。年龄,无论是作为连续变量还是作为二分类变量,在调整其他预后因素后,仍是长期不良预后的独立预测因素。此外,本研究发现在入院和出院时,GMS检测到长期不良预后与意识水平下降之间存在关联;但调整其他因素之后,未发现GMS的任何独立预后预测价值。
3.3 MRI分级标准分析本组DAI患者中,70%的患者脑干病灶符合Adams 3级。然而,Adams分级与长期预后无显著关系。本研究基于SWI序列,发现黑质和中脑被盖病灶,可作为长期不良预后指标。这些结果可补充Adams分级标准,从而建立MRI分级标准。最近的一项研究[21]成果为MRI分类标准的建立,增加了一种基于病理机制的方法,包括脑干损伤机制。结合本研究结果,笔者提出了一种基于Adams分级标准的DAI的MRI扩展分级标准:Ⅰ级,脑半球病灶;Ⅱ级,胼胝体病灶;Ⅲ级,脑干病灶;Ⅳ级,黑质和中脑被盖病灶。该扩展系统使用简单,具有显著的预后评估价值,但仍需进一步验证。
综上所述,SWI序列较T2*GRE和DWI序列更能识别与DAI相关的早期病灶。SWI序列显示的黑质和中脑被盖病灶与长期不良预后显著相关。笔者新提出的扩展MRI分级标准,可用于DAI患者的长期预后评估。
| [1] |
李欣文, 韩伟, 刘涛, 等. 脑弥漫性轴索损伤诊断中应用CT, MRI的效果观察[J]. 临床医学研究与实践, 2017, 2(25): 135-136. |
| [2] |
江红霞, 李国荣, 汤晨东, 等. 交通事故致弥漫性轴索损伤72例法医精神病伤残鉴定案例分析[J]. 中华全科医学, 2017, 20(11): 1935-1937. |
| [3] |
张雨婷, 李禄生, 何玲, 等. 磁共振弥漫张量成像对儿童弥漫性轴索损伤程度评估的定量研究[J]. 重庆医学, 2017, 46(30): 41964199. |
| [4] |
张丽君, 周昊, 邱妮妮. 早期弥漫性轴索损伤患者CT影像特点与预后危险因素分析[J]. 中国CT和MRI杂志, 2017, 15(9): 2527. |
| [5] |
王丽华, 管霞, 孟磊, 等. 磁共振磁敏感成像(SWI)在弥漫性轴索损伤诊断及预后评估中的应用价值[J]. 现代医用影像学, 2017, 26(6): 1650-1652. |
| [6] |
Temkin N, Satris G, Machamer J, et al. Glasgow outcome scale extended-differences counting disability from only brain injury versus brain and other system injuries[C]//Journal Of Neurotrauma. 140 Huguenot Street, 3rd Fl, New Rochelle, Ny 10801 Usa: Mary Ann Liebert, Inc, 2017, 34: A86.
|
| [7] |
Abu Hamdeh S, Marklund N, Lannsjo M, et al. Extended anatomical grading in diffuse axonal injury using MRI:hemorrhagic lesions in the substantia nigra and mesencephalic tegmentum indicate poor long-term outcome[J]. J Neurotrauma, 2017, 34: 341352. |
| [8] |
李文臣, 刘磊, 陈勃, 等.磁敏感加权成像对重度出血性弥漫性轴索损伤的诊断价值和预后评价[J/CD].中华神经创伤外科电子杂志, 2017, 3(3): 136-141. http://www.cqvip.com/QK/72028X/201703/672309313.html
|
| [9] |
Hodel J, Rodallec M, Gerber S, et al. Susceptibility weighted magnetic resonance sequences "SWAN, SWI and VenoBOLD":technical aspects and clinical applications[J]. J neuroradiol, 2012, 39: 71-86. |
| [10] |
Mittal S, Wu Z, Neelavalli J, et al. Susceptibility-weighted imag ing:technical aspects and clinical applications, part 2[J]. AJNR Am J Neuroradiol, 2009, 30: 232-252. DOI:10.3174/ajnr.A1461 |
| [11] |
You X, Xu Y. Application potential of susceptibility-weighted imaging (SWI), diffusion weighted imaging (DWI) and diffusion tensor imaging (DTI) in the diagnosis of soft tissue tumors[J]. Biomedical Research, 2018, 28: 9674-9678. |
| [12] |
Jovin TG, Saver JL, Ribo M, et al. Diffusion-weighted imaging or computerized tomography perfusion assessment with clinical mismatch in the triage of wake up and late presenting strokes undergoing neurointervention with Trevo (DAWN) trial metho ds[J]. Int J Stroke, 2017, 12: 641-652. DOI:10.1177/1747493017710341 |
| [13] |
Moen K G, Brezova V, Skandsen T, et al. Traumatic axonal in jury:the prognostic value of lesion load in corpus callosum, brain stem, and thalamus in different magnetic resonance ima ging sequences[J]. Journal of neurotrauma, 2014, 17: 14861496. |
| [14] |
Smitherman E, Hernandez A, Stavinoha P L, et al. Predicting outcome after pediatric traumatic brain injury by early magnet ic resonance imaging lesion location and volume[J]. Journal of neurotrauma, 2016, 1: 35-48. |
| [15] |
Adams J H, Graham D I, Jennett B. The neuropathology of the vegetative state after an acute brain insult[J]. Brain, 2000(7): 1327-1338. |
| [16] |
Chew BG, Spearman CM, Quigley MR, et al. The prognostic sig nificance of traumatic brainstem injury detected on T2-weighted MRI[J]. J Neurosurg, 2012, 117: 722-728. DOI:10.3171/2012.6.JNS111736 |
| [17] |
Haghbayan H, Boutin A, Laflamme M, et al. The prognostic va lue of MRI in moderate and severe traumatic brain injury:a systematic review and meta-analysis[J]. Critl Care Med, 2017, 45: e1280-e1288. DOI:10.1097/CCM.0000000000002731 |
| [18] |
张文龙. CT与MRI诊断弥散性颅脑轴索损伤的效果比较[J]. 基层医学论坛, 2018, 22(5): 651-652. |
| [19] |
Roozenbeek B, Maas AI, Menon DK. Changing patterns in the epidemiology of traumatic brain injury[J]. Nat Rev Neurol, 2013, 9: 231-236. DOI:10.1038/nrneurol.2013.22 |
| [20] |
Peeters W, Majdan M, Brazinova A, et al. Changing epidemiolo gical patterns in traumatic brain injury:a longitudinal hospital based study in Belgium[J]. Neuroepidemiology, 2017, 48: 63-70. DOI:10.1159/000471877 |
| [21] |
Andriessen TM, Horn J, Franschman G, et al. Epidemiology, sev erity classification, and outcome of moderate and severe traum atic brain injury:a prospective multicenter study[J]. J Neurot rauma, 2011, 28: 2019-2031. DOI:10.1089/neu.2011.2034 |
 2019, Vol. 17
2019, Vol. 17


