| 基于CT的深度学习模型在甲状腺结节良恶性鉴别中的应用 |
2. 山东省威海市妇幼保健院超声科二科,山东 威海 264200;
3. 山东省威海市妇幼保健院CT室,山东 威海 264200;
4. 山东省威海市妇幼保健院耳鼻喉头颈外科,山东 威海 264200
人工智能是当前信息技术领域最重要的革命性技术之一, 随着软件算法与硬件算力不断进步, 人工智能已在诸多领域中发挥巨大作用, 其在医疗界的发展也已取得长足进步[1-2]。甲状腺肿瘤是临床常见病, 近几年, 我国甲状腺肿瘤发病率呈上升趋势, 且发病年龄逐渐年轻化。CT是甲状腺结节常用的影像学检查方法, 但由于CT层数较多, 人工阅片耗时耗力, 检出率也不稳定。笔者提出一个基于CT深度学习模型的甲状腺结节良恶性诊断的方法, 利用深度学习的优势, 通过逐层特征提取, 将样本在原空间的特征表示变换到一个新特征空间, 自动客观判读甲状腺结节, 并结合相应的诊断标准给出诊断意见, 可有效减少诊断医师之间的差异, 从而使分类或诊断更准确清晰[3-4]。本研究探讨CT人工智能辅助诊断系统在鉴别甲状腺结节良恶性中的诊断价值。
1 资料与方法 1.1 一般资料选取2012年11月至2018年12月我院经活检或手术病理确诊的672例甲状腺结节患者, 其中男158例, 女514例; 年龄22~76岁, 平均(50.2±10.7)岁; 恶性结节542例(包括乳头状癌、微小乳头状癌), 良性结节130例(包括甲状腺肿、腺瘤、亚急性甲状腺炎)。330例用于深度学习模型训练, 342例用于模型验证。所有结节最大径均>0.5 cm。排除甲状腺癌弥漫性钙化型及弥漫性病变, 以及甲状腺部分切除术后的结节。
1.2 模型构建和验证 1.2.1 图像标注先对甲状腺结节CT图像行预处理, 后通过模版匹配或基于规则等方法找出结节, 对其分割与特征提取, 量化并比较结节与已知结节图像的相似度, 检出甲状腺结节[5]。CT医师以病理为标准将图像分成良性与恶性2类, 并精准标注图像中的病灶范围。
1.2.2 图像预处理将标注好的CT图像进行裁剪、颜色空间变换、去噪、图像形态学操作及归一化等系列处理, 消除人为和环境干扰, 更好地展示图像特征[6]。将所有图像分成6个子样本, 4个用于训练, 2个保留用于验证模型。
1.2.3 构建和训练模型采用卷积神经网络(convolutional neural networks, CNN)构建多个深度学习模型, 分别将训练集投入模型进行训练; 甲状腺结节诊断的CNN结构由标准的堆叠卷积层、池化层、1个或多个完全连接层组成, 能够通过多个中间层捕获输入和输出之间的高度非线性映射, 可训练的卷积滤波器、局部邻域池操作和归一化操作在输入上交替执行, 并生成从低级到高级越来越复杂的特征层次结构[7]。
由于数据集中的图像对深度学习训练存在数据量不足的问题, 本研究采用Mixup图像扩增方法进行数据集扩大。各随机选取良恶性图像的3/4进行数据增广, 其余图像作为测试集。增广后的良恶性图像各达30 000张。同时采用迁移学习的方法进行网络预训练。采用ImageNet数据集完成。后采用增广的数据集进行参数优化。学习和训练过程见图 1。
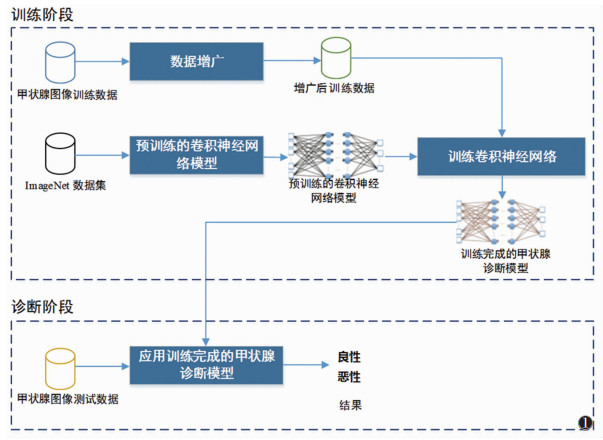 |
| 图 1 基于卷积神经网络的CT甲状腺结节分类方法 |
1.2.4 验证模型
利用测试集测试训练得到的模型, 以此作为评价分类器的性能指标。一般情况下, 训练集迭代次数20或30次, 每次迭代后用测试集验证, 随着迭代次数的增加, 模型精度趋于稳定。
1.3 深度学习选择3名CT医师(初级、中级、高级职称各1名), 独立对测试集图像进行识别和判断, 记录诊断每张图像所需时间。同时记录模型对相同测试集的识别结果。诊断性能由准确率、敏感度、特异度、诊断时间评定[8-9]。
1.4 统计学分析应用SPSS 21.0统计学软件分析数据, 计量资料以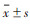
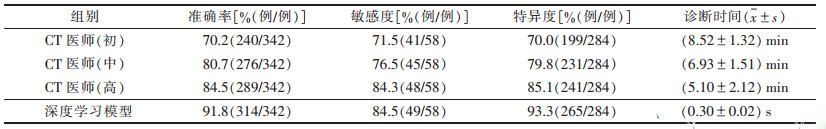
测试集342例, 其中良性结节58例, 恶性结节284例。深度学习模型正确识别314例(准确率91.8%), 其中正确识别良性结节49例, 正确识别恶性结节265例, χ2检验表明, 深度学习模型与3名CT医师的诊断准确率、敏感度和特异度比较, 差异均有统计学意义(均P < 0.05, 表 1)。
| 表 1 深度学习模型与3名CT医师诊断结果对比 |
 |
3 讨论
随着人工智能的飞速发展, 计算机检测与辅助诊断系统也受到广泛关注。本研究初步探索了人工智能图像识别技术在CT甲状腺结节的应用。收集672例甲状腺患者, 整理后投入深度学习模型进行训练和验证, 其诊断敏感度为84.5%, 特异度为93.3%, 准确率为91.8%, 每张图像的诊断时间为(0.30±0.02)s; 表明深度学习模型的诊断准确率、敏感度、特异度均高于CT医师。深度学习模型在甲状腺结节诊断同时可完成结节定位、分割和分类:在结节定位上, 由于CNN具有图像特征位移不变性, 可从图像不同位置中提取学习到的特征, 不会因结节位置多变和体积较小导致检出率下降, 具有较好的泛化能力; 在结节分类上, 深度学习模型实现从原始图像输入到最终分类的映射, 不仅消除了机器学习中手工设计特征对最终分类的影响, 还可自动提取潜在的图像特征。
影响结节检出的因素很多, 对扫描参数相关因素(包括扫描层厚、重建间隔、重建算法、螺距、曝光剂量)需做好质量控制[10]。目前, CT对甲状腺结节良恶性辅助诊断已逐步应用于临床, 可降低漏误诊率, 提高诊断水平[11]。本研究用于训练的图像数据相对较少, 模型的初始构建和训练仍需人工标注, 精度有待进一步提升。本研究不足:①甲状腺结节CT图像是核心资源, 但目前缺乏有效的标准训练数据及统一的行业标准, 无法获得良好的训练效果; ②在临床使用过程中, 虽能避免人为漏诊, 但常检出过多的假阳性结节[12-13]; ③临床医师诊断甲状腺结节时, 需结合超声、临床化验指标, 进一步提高诊断的准确性。针对上述问题, 算法模型仍需改进, 进一步提升产品性能。
总之, 随着算法持续改进、模型不断优化, 以及低剂量CT扫描的普及, 基于人工智能的甲状腺结节检出, 对降低影像科医师工作强度、减少甲状腺结节漏误诊率有明显的临床意义[14]。
| [1] |
金征宇, 薛华丹. 医学放射诊断学新进展[J]. 协和医学杂志, 2011, 2(3): 197-199. |
| [2] |
刘士远, 萧毅. 基于深度学习的人工智能对医学影像学的挑战和机遇[J]. 中华放射学杂志, 2017, 51(12): 899-901. |
| [3] |
张惠茅, 萧毅, 洪楠, 等. 医学影像人工智能产业现状和发展需求调研报告[J]. 中华放射学杂志, 2019, 53(6): 507-511. |
| [4] |
Ma J, Luo S, Dighe M, et al. Differential diagnosis of thyroid nodules with ultrasound elastography based on support vector machines[C]//IEEE International Ultrasonics Symposium, 2010: 1372-1375.
|
| [5] |
明佳蕾, 方向明. 基于人工智能的CT肺结节检出临床应用及研究进展[J]. 中华放射学杂志, 2019, 53(6): 522-525. |
| [6] |
王智杰, 高杰, 孟茜茜, 等. 基于深度学习的人工智能技术在早期胃癌诊断中的应用[J]. 中华消化内镜杂志, 2018, 35(8): 551-556. |
| [7] |
中华医学会消化内镜学分会, 中国抗癌协会肿瘤内镜专业委员会. 中国早期胃癌筛查及内镜诊治共识意见(2014年, 长沙)[J]. 中华消化内镜杂志, 2014, 31(7): 361-377. |
| [8] |
原利晶, 陈武, 黄玉琴, 等. 超声计算机辅助联合造影鉴别诊断甲状腺良恶性结节的研究[J]. 中国超声医学杂志, 2019, 35(4): 299-302. |
| [9] |
王洛伟, 辛磊, 林寒, 等. 中国消化内镜技术发展现状[J]. 中华消化内镜杂志, 2015, 32(8): 501-515. |
| [10] |
王瑛.甲状腺超声与甲状腺功能在老年患者甲状腺良恶性结节鉴别中的价值[J/CD].世界最新医学信息文摘(电子版), 2016, 16(84): 103.
|
| [11] |
Esteva A, Kuprel B, Novoa RA, et al. Dermatologist-level class ification of skin cancer with deep neural networks[J]. Nature, 2017, 542: 115-118. |
| [12] |
Chen PJ, Lin MC, LAI MJ, et al. Accurate classification of dim inutive colorectal polyps using computer-aided analysis[J]. Gastroenterology, 2018, 154: 568-575. |
| [13] |
张敏敏, 金震东, 蔡哲元, 等. 计算机辅助判别超声内镜图像诊断胰腺癌的实验研究[J]. 中华消化内镜杂志, 2009, 26(4): 180-183. |
| [14] |
陈京水, 李业勤, 刘玉, 等. 人工神经网络在图像处理中的应用[J]. 中国医学装备. |
 2020, Vol. 18
2020, Vol. 18


