| 人工血管动静脉内瘘后期闭塞的介入治疗 |
2. 广州中医药大学第一附属医院影像科,广东 广州 510405
近年来, 随着自体动静脉内瘘(autogenous arteriovenous fistulas, AVF)反复闭塞者的不断增多和人工血管材料的长足发展, 在我国接受人工血管动静脉内瘘(arteriovenous graft, AVG)的患者亦逐年增多。但AVG存在使用时间短、阻塞率高的缺点[1], 及时介入干预可有效延长其使用寿命。高州市人民医院自2017年1月至2018年1月对22例AVG闭塞患者进行介入治疗, 取得了良好的临床效果。现报道如下。
1 资料与方法 1.1 一般资料22例中, 男13例, 女9例; 年龄26~77岁, 中位年龄45岁。行AVG后规律血透4个月~2年, 临床发现血管震颤杂音消失, 均经CDFI检查证实为人工血管透析通路内血栓形成并血流中断。从发现、确诊至要求行介入治疗时间在2 d内。
1.2 仪器与方法患者仰卧于DSA导管床上, 患侧上肢外展外旋, 常规消毒铺巾。18G套管针逆向穿刺人工血管“U”形襻的静脉侧侧襻, 导丝交换置入6F导管鞘后, 缓慢注射含肝素30 mg的生理盐水达全身肝素化, 经鞘送入0.035/150 cm超滑导丝和5F椎管过动脉端吻合口, 造影确认后更换高压球囊导管(Boston公司GladiatorTM Elite球囊直径4~6 mm, 长度4 cm), 自人工血管动脉端吻合口至静脉侧侧襻穿刺口以球囊压迹消失为度依次逐段扩张, 每次持续时间30~60 s。经鞘抽栓操作:采用双导丝技术于鞘侧臂接50 mL注射器保持负压抽吸的同时缓慢拔鞘, 冲洗鞘内血栓后再沿短导丝送入导管鞘, 如上重复操作, 直至注射器被血液缓慢推移(即血流已通至静脉侧侧襻穿刺口)并造影确认为止。抽栓期间经椎管脉冲式手推尿激酶10万U+生理盐水10 mL行溶栓治疗。后于人工血管动脉侧侧襻顺向穿刺并置入6F导管鞘, 采用原高压球囊导管对狭窄的引流静脉、阻塞的静脉侧侧襻和静脉端吻合口行球囊扩张成形以开通血管和压碎血栓, 然后插入5F椎管过动脉端吻合口行AVG全程造影:残存狭窄应 < 30%。同时, 血透通路触及持续震颤并听及明显杂音提示介入操作成功。经皮血管球囊成形术(percutaneous transluminal angioplasty, PTA)术后弹性回缩及夹层狭窄>30%者, 置入GORE公司的Viabahn覆膜支架。术后拔鞘行介入入口的缝合以止血。
2 结果所有患者经球囊导管碎栓后, 将自人工血管动脉吻合端至静脉侧侧襻介入入口处的血栓经鞘吸出, 而其远端栓子顺血流流入肺动脉内, 均未出现肺栓塞症状(图 1)。经椎管行尿激酶溶栓治疗均未出现穿刺口、脑和肾等出血。血管彩色多普勒超声和(或)造影提示:单发狭窄者15例中, 引流静脉、人工血管、静脉端和动脉端吻合狭窄分别为4、2、7和2例; 2处及其以上狭窄者7例, 其中2处狭窄者6例, 引流静脉与静脉端吻合口、人工血管与动脉端吻合口狭窄分别为4和2例, 另1例出现引流静脉(肱与腋静脉各1处)和静脉端吻合口3处狭窄。22例行PTA治疗后, 19例狭窄率 < 30%, 提示成功; 3例扩张后狭窄率仍>30%, 狭窄位置见表 1。后均成功置入GORE公司的Viabahn覆膜支架。术后当日和次日均使用人工血管行血透治疗。随访6个月, 1例术后36 d因人工血管静脉端吻合口狭窄加重致血栓栓塞, 再次行介入治疗后一直通畅, 余患者血透通路均通畅。
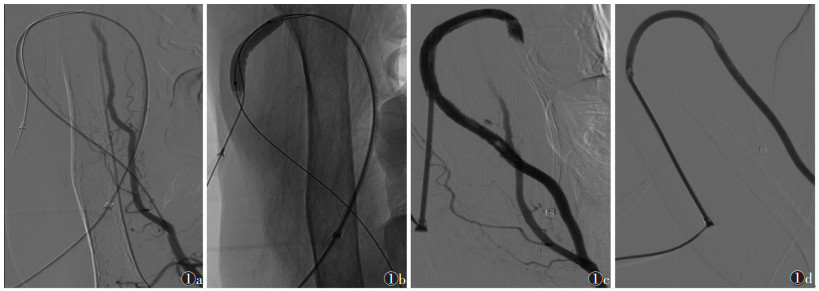 |
| 图 1 女, 52岁, 1年前因尿毒症行左前臂人工血管动静脉内瘘术, 术后一直采用人工血管行血透治疗 图1a 肱动脉造影示人工血管闭塞 图1b, 1c 经球囊扩张碎栓、鞘抽栓后造影示人工血管动脉段开通 图1d 球囊扩张人工血管静脉吻合口和静脉段闭塞后造影复查示已开通 |
| 表 1 22例人工血管动静脉内瘘闭塞PTA结果 |
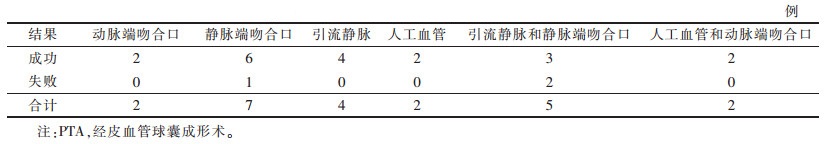 |
3 讨论
近年来, AVG技术不断进步、成熟, 随着专为透析通路设计厚壁、内支撑和可拉伸聚四氟乙稀(PTFE)人工血管的问世, 使得AVG术越来越多地开展, 但相应的并发症发生率也逐渐增多, 其中最常见的是血管闭塞[2-3]。目前, AVG通路闭塞的介入治疗报道较少, 仍是目前临床工作的难点。
介入入路的正确选择是AVG闭塞介入性治疗成功的保障, 可极大降低并发症的发生率。国内报道[4-5]了经肱动脉、股动脉和人工血管单入路(静脉侧或动脉侧侧襻)途径治疗人工血管透析通路狭窄与闭塞病变。本研究表明, 选择人工血管动、静脉侧侧襻双入路作为AVG闭塞病变介入入路的优点有:①介入操作路径短, 可供选择的介入器械, 如长为75 cm高压球囊GladiatorTM Elite等增多; ②碎栓后的栓子顺血流立即冲至鞘管内和附近, 利于血栓的抽吸和减少对人工血管的损伤; ③彩色多普勒超声和血管造影均无法完全显示AVG闭塞血透通路内的情况, 如狭窄的部位、范围和程度等, 人工血管双入路可满足整个AVG闭塞病变的处理; ④术后拔出导管鞘仅行介入入口的局部缝合即可止血, 无需卧床制动或担心压迫介入入口引起血透通路血栓再次形成并闭塞、血肿和出血等并发症。
AVG闭塞可分为早期(即 < 3个月)和后期(即>3个月), 后期主要是人工血管吻合口和人工血管穿刺点的内膜增生, 其次是回流静脉老化等引起狭窄, 并常在狭窄的基础上继发血栓形成以致闭塞[6]。本组所有患者使用人工血管规律血透超过3个月后出现动、静脉端吻合口、人工血管和引流静脉等部位狭窄, 并在狭窄的基础上继发血栓形成而闭塞, 完全符合后期闭塞的原因。国内外专家[6-9]对人工血管透析通路的狭窄伴血栓形成并闭塞病变的共识是:尽快处理, 推荐术中结合影像学表现评价内瘘, 可采用经皮介入技术取栓, 并行血管成形术。文献[7-9]报道的介入取栓方法有:抽栓导管抽栓和Fogarty导管或球囊导管拖栓等。抽栓导管一般为6~8 F, 很难与人工血管的管径(直径一般为5~6 mm)匹配, 抽栓效果有限。Fogarty导管或球囊导管拖栓效果较好, 无法对狭窄段以远管腔内的血栓完全拖出, 也易造成血管撕裂引起夹层、大出血等风险。本组患者术前均全身肝素化, 先对静脉侧侧襻介入入口以前的血透通路球囊扩张以解除狭窄和压碎血栓, 目的是疏通血流使栓子随血流冲至入口附近以利于鞘管抽吸; 然后处理入口以后的血栓, 经管注入尿激酶溶解新鲜的血栓后可能存在微量无法溶解的血栓被球囊导管压碎后流入肺动脉。造影示血透通路管腔内无血栓存留, 虽有微量碎血栓流入肺动脉, 但无肺动脉栓塞症状, 介入治疗血栓效果佳, 并发症极少。PTA被认为是介入治疗AVG狭窄或闭塞的首选, PTA术后狭窄率>30%、血管破裂血液外渗和狭窄频繁复发等可置入支架[10], 覆膜支架在降低再狭窄和提高近远期血管开放率方面比裸支架具有明显优越性[11-12]。本组患者均采用耐高压球囊导管对狭窄处反复多次长时间扩张, 其中19例PTA术后成功, 3例PTA失败后均成功置入GORE公司Viabahn覆膜支架, 术后当日和次日使用人工血管行血透治疗。随访6个月, 1例介入治疗术后36 d因静脉端吻合口狭窄加重致血栓闭塞再次行介入治疗后一直通畅, 其余患者血透通路均通畅。
总之, 介入治疗人工血管透析通道闭塞病变, 具有简单安全、成功率高、创伤小、可重复操作、并发症少的优势, 值得临床推广应用。
| [1] |
吴巍巍, 刘昌伟, 刘暴, 等. 血液透析人工血管动静脉内瘘术及术后闭塞的治疗[J]. 中国医学科学院学报, 2010, 32(3): 324-327. DOI:10.3881/j.issn.1000-503X.2010.03.018 |
| [2] |
闫巍, 张福先, 张昌明, 等. 人造血管动静脉内瘘在血液透析中的应用[J]. 中国实用外科杂志, 2009, 29(11): 918-920. DOI:10.3321/j.issn:1005-2208.2009.11.015 |
| [3] |
万正东, 宋斌, 雷红卫, 等. 人造血管透析通路血栓性狭窄与闭塞的介入治疗探讨[J]. 中国现代医学杂志, 2017, 27(5): 138-140. DOI:10.3969/j.issn.1005-8982.2017.05.030 |
| [4] |
任安, 刘巍, 张雪哲, 等. 血液透析分流通道机能不全和闭塞的造影诊断及介入治疗[J]. 中华放射学杂志, 1999, 33(4): 267-270. DOI:10.3760/j.issn:1005-1201.1999.04.014 |
| [5] |
杨硕菲, 陈佳佺, 张岚, 等. 彩色多普勒超声引导下血透通路狭窄的腔内治疗[J]. 血管与腔内血管外科杂志, 2016, 2(6): 523-526. |
| [6] |
Schild AF. Maintaining vascular access:the management of hemodialysis arteriovenous grafts[J]. J Vasc Access, 2010, 11: 92-99. DOI:10.1177/112972981001100202 |
| [7] |
尹杰, 张宪生, 佘康, 等. 人工血管透析通路闭塞的处理[J]. 中华临床医师杂志, 2015, 9(8): 1312-1316. DOI:10.3877/cma.j.issn.1674-0785.2015.08.008 |
| [8] |
艾鹏, 邓超频, 王华, 等. 血液透析内瘘通路狭窄与闭塞的介入治疗[J]. 温州医科大学学报, 2014, 44(3): 213-215. DOI:10.3969/j.issn.2095-9400.2014.03.014 |
| [9] |
杜伟, 陈磊, 段文帅, 等. 血液透析动静脉内瘘血管狭窄和闭塞的介入治疗[J]. 实用医学影像杂志, 2012, 13(1): 62-64. DOI:10.3969/j.issn.1009-6817.2012.01.020 |
| [10] |
王宾. 血液透析通路狭窄相关问题介入治疗进展[J]. 国际医学放射学杂志, 2017, 40(3): 321-329. |
| [11] |
Kundu S. Review of central venous disease in hemodialysis pa tients[J]. J Vasc Interv Radiol, 2010, 21: 963-968. DOI:10.1016/j.jvir.2010.01.044 |
| [12] |
Haskal ZJ, Trerotola S, Dolmatch B. Stent graft versus balloon angioplasty for failing dialysis-access grafts[J]. N Engl J Med, 2010, 362: 494-503. DOI:10.1056/NEJMoa0902045 |
 2019, Vol. 17
2019, Vol. 17


