迄今,全世界共报道了约280种贝类寄生桡足类[1],记录宿主贝类超过430种,多数是双壳类[2-3]。中国海洋贝类寄生桡足类的研究相对薄弱,仅记录7种,均属于剑水蚤目(Cyclopoida)分别是:Anthessius mytilicolus Reddiah, 1966采自翡翠贻贝(Perna viridis (Linnaeus));Anthessius pinnae Humes, 1959采自双色江珧蛤(Pinna bicolor Gmelin); Panjakus platygyrae Humes & Stock, 1973采自黑旗江珧蛤(Atrina vexillum (Born));高氏牡蛎蚤(Ostrincola koe Tanaka, 1961)采自文蛤(Meretrix meretrix(Linnaeus))(现鉴定为短文蛤(M. petechialis (Lamarck))[4])和丽文蛤(Meretrix lusoria (Röding));拟牡蛎蚤(Ostrincola similis Lin & Ho, 1999)采自长牡蛎(Crassostrea gigas (Thunberg))和翡翠贻贝;Myicola formosanus Lin & Ho, 1999采自青蛤(Cyclina sinensis (Gmelin));黄海章鱼蚤(Octopicola huanghaiensis Du et al., 2018)采自长蛸(Octopus minor (Sasaki))和短蛸(Amphioctopus fangsiao (d′Orbigny))[5-10]。大部分种分布在东海和南海,只有高氏牡蛎蚤和黄海章鱼蚤在黄海有过报道,关于渤海的贝类寄生桡足类尚未见报道。
本研究检查了黄渤海双壳类32种,发现了8种剑水蚤目寄生桡足类,其中7种为中国新记录种。
1 材料和方法于2016年3月至2018年5月在丹东、东港、庄河、大连、瓦房店、营口、锦州、葫芦岛、兴城、寿光、莱州、龙口、烟台、威海、荣成、乳山、海阳、青岛、日照、连云港、盐城、南通共22地对黄渤海双壳类寄生桡足类进行了调查,共检查双壳类32种8 628个体。
双壳贝类样品通过市场购买(确认原产地)或实地采集获得,用过滤海水清洗。打开贝壳,于解剖镜(Zeiss Stemi 508)下检查,先观察外套腔里有无桡足类,然后用解剖刀解剖软体部,检查内部寄生桡足类。如发现寄生桡足类,用吸管吸出,经清水洗净后,用75%酒精或10%海水福尔马林固定。记录宿主、寄生部位、采集时间和地点等。
桡足类解剖前先绘制整体图并测量体长(不包含尾叉上刚毛)。解剖在一个干净的载玻片上进行,将解剖后的各个结构转移到滴有适量乳酚溶液的载玻片上,小心盖上盖玻片,然后用优质指甲油封片。观察和绘图在装有显微绘图仪的显微镜(Nikon E600)下进行。
感染率及平均感染强度按Margolis等[11]的定义计算:
感染率(Prevalence)=被某种寄生虫感染的宿主数/检查的总宿主数×100%。
平均感染强度(Mean intensity)=某种寄生虫总数/被该种寄生虫感染的宿主数。
2 结果与讨论调查的32种双壳类中,下列23种双壳类(908个体)未检查到寄生桡足类:薄壳绿螂(Glauconome angu-lata Reeve),连云港,1批3个;饼干镜蛤(Dosinia biscocta (Reeve)),寿光、连云港,2批43个;长竹蛏(Solen strictus Gould),莱州,1批40个;大竹蛏(Solen grandis Dunker),莱州,1批4个;等边浅蛤(Macridiscus aequilatera (Sowerby)),丹东,1批21个;盾形单筋蛤(Isomonia umbonata (Gould)),日照,1批18个;光滑河蓝蛤(Potamocorbula laevis (Hinds)),连云港,1批125个;黑荞麦蛤(Xenostrobus atratus (Lischke)),葫芦岛,1批7个;滑顶薄壳鸟蛤(Fulvia mutica(Reeve)),丹东、东港,3批74个;加州扁鸟蛤(Keenocardium californiense(Deshayes)),莱州、日照,2批28个;魁蚶(Anadara broughtonii (Schrenck)),丹东、瓦房店、莱州、青岛,5批124个;毛蚶(Anadara kagoshimensis (Tokunaga)),青岛、连云港,2批23个;密鳞牡蛎(Ostrea denselamellosa Lischke),青岛,3批16个;葡萄牙牡蛎(Crassostrea angulata (Lamarck)),莱州,1批5个;青蛤(Cyclina sinensis (Gmelin)),青岛、盐城、南通,5批180个;砂海螂(Mya arenaria Linnaeus),青岛,1批18个;凸壳肌蛤(Arcuatula senhousia (Benson)),连云港,1批60个;虾夷扇贝(Mizuhopecten yessoensis (Jay)),烟台,1批19个;缢蛏(Sinonovacula constricta (Lamarck)),青岛,1批36个;硬壳蛤(Mercenaria mercenaria (Linnaeus)),日照、连云港、盐城,4批55个;栉江珧(Atrina pectinata (Linnaeus)),青岛,1批5个;栉孔扇贝(Azumapecten farreri (Jones & Preston)),青岛,1批2个;中国不等蛤(Anomia chinensis Philippi),青岛,1批2个。
在菲律宾蛤仔(Ruditapes philippinarum(Adams & Reeve))等9种双壳类中发现寄生剑水蚤类8种,隶属1亚目4科8属,详见表 1及下文物种分述。
|
|
表 1 黄渤海双壳类寄生剑水蚤类的采样信息、感染率和感染强度 Table 1 Sampling information and infection levels of cyclopoid copepods parasitic in bivalvian mollusks from the Yellow Sea and the Bohai Sea |
桡足亚纲(Copepoda)
剑水蚤目(Cyclopoida)
鳋亚目(Ergasilida)
闭水蚤科(Clausidiidae Embleton, 1901)
壳蚤属(Conchyliurus Bocquet & Stock, 1957)
负羽壳蚤(Conchyliurus quintus Tanaka, 1961)(见图 1和表 1)
|
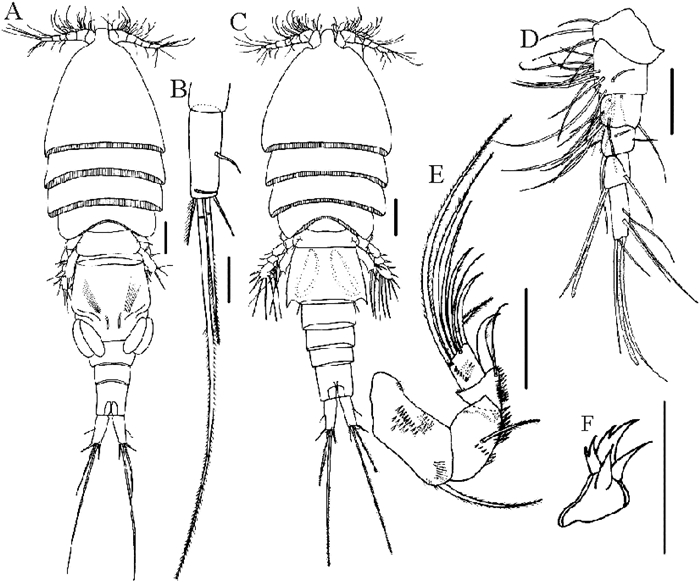
(A:雌虫,背面观;B:雌虫尾叉,背面观;C:雄虫,背面观;D:雌虫第1触角;E:雌虫第2触角;F:雌虫第2小颚第2节。比例尺:A, C=100 μm; B, D, E, F=50 μm。A: Female, dorsal; B: Female caudal ramus, dorsal; C: Male, dorsal; D: Female antennule; E: Female antenna; F: Female second segment of maxilla. Scale bars: A, C=100 μm; B, D, E, F=50 μm.) 图 1 负羽壳蚤 Fig. 1 Conchyliurus quintus Tanaka, 1961 |
宿主、采集地及感染情况:寄生于短文蛤、菲律宾蛤仔、四角蛤蜊(Mactra quadrangularis Reeve)、纹斑棱蛤(Neotrapezium liratum (Reeve))和中国蛤蜊(Mactra chinensis(Philippi))的外套腔和内脏团。采自山东莱州、海阳、青岛,江苏连云港、南通5地。最大感染率33.3%(四角蛤蜊;江苏南通,2016年11月)(宿主个数n≤3未统计在内,下同)。平均感染强度变化范围1.0~14.0,最大感染强度14(菲律宾蛤仔;山东青岛,2016年9月)(见表 1)。
雌虫(n=10;形态描述依据成体标本,下同):身体(见图 1A)背腹扁平,长1.27 mm(1.17~1.41 mm)(平均值,括号内是变化范围;下同),宽0.38 mm(0.34~0.43 mm)。前、后体部长度比0.95(0.88~0.99)。生殖节(见图 1A)长宽比1.24(1.04~1.39)。尾叉(见图 1B)长宽比2.57(2.37~2.73)。第1触角(见图 1D)6节。第2触角(见图 1E)4节。第2小颚(见图 1F)2节,第2节具4个刺状结构,其中2个呈分叉状。
雄虫(n=7):身体(见图 1C)和雌虫相似。长1.06 mm(0.91~1.20 mm),宽0.32 mm(0.27~0.35 mm)。前、后体部长度比0.93(0.88~0.97)。生殖节(见图 1C)长宽比0.79(0.69~0.82)。尾叉长宽比2.46(2.10~2.63)。
负羽壳蚤是中国新记录种。Tanaka(1961)首次在日本的波纹巴非蛤(Paratapes undulatus (Born))外套腔内发现该种,后在日本及韩国其他贝类报道。宿主包括Serratina capsoides (Lamarck)、青蛤、菲律宾蛤仔、中国朽叶蛤(Coecella chinensis(Deshayes))、四角蛤蜊、丽文蛤、缢蛏(Sinonovacula constricta(Lamarck))、Nuttallia japonica(Reeve)、樱蛤(Limecola contabulata (Deshayes))、纹斑棱蛤、脆壳全海笋(Barnea manilensis (Philippi))、粗异白樱蛤(Heteromacoma irus(Hanley))、砂海螂、毛蚶(Anadara kagoshimensis(Tokunaga))、大竹蛏(Solen grandis Dunker)和长竹蛏(Solen strictus Gould)共16种双壳类[3, 12-16]。本文报道的短文蛤和中国蛤蜊为负羽壳蚤的新宿主。本文标本的体长、前后体部长度比、尾叉、第1触角、口器及胸足的结构和前人描述一致[15, 17]。然而,我们并未观测到第2小颚末节其中一个刺状结构上面的2个微刺[15]。
舐皮蚤科(Lichomolgidae Kossmann, 1877)
赫尔曼蚤属(Herrmannella Canu, 1891)
竹蛏赫尔曼蚤(Herrmannella soleni Kim & Ho, 1991)(见图 2和表 1)
|
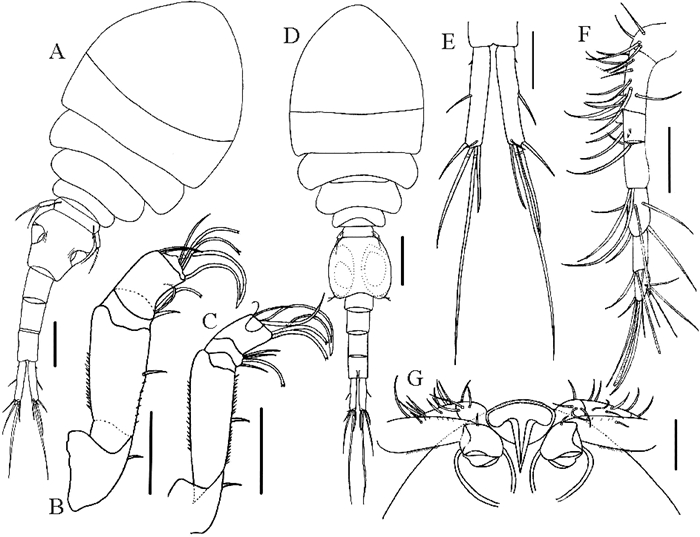
(A:雌虫,背面观;B:雌虫第2触角;C:雄虫第2触角;D:雄虫,背面观;E:雌虫尾叉,背面观;F:雌虫第1触角;G:雌虫额角,腹面观。比例尺:A,D=100 μm; B,C, E, F, G=50 μm。A: Female, dorsal; B: Female antenna; C: Male antenna; D: Male, dorsal; E: Female caudal ramus, dorsal; F: Female antennule; G: Female rostrum, ventral. Scale bars: A, D=100 μm; B, C, E, F, G=50 μm.) 图 2 竹蛏赫尔曼蚤 Fig. 2 Herrmannella soleni Kim & Ho, 1991 |
宿主、采集地及感染情况:寄生于中国蛤蜊和紫石房蛤(Saxidomus purpurata(Sowerby))的外套腔。采自山东荣成、海阳2地。最大感染率50.0%(紫石房蛤;荣成,2017年2月)。平均感染强度变化范围1.5~1.6,最大感染强度3(中国蛤蜊;山东海阳,2017年2月)(见表 1)。
雌虫(n=6):身体(见图 2A)长1.01 mm(0.95~1.10),宽0.37 mm(0.33~0.39 mm)。前、后体部长度比1.17(1.11~1.23)。生殖节(见图 2A)长宽比1.04(0.94~1.13)。尾叉(见图 2E)长宽比5.24(4.64~5.76)。额角(见图 2G)长76 μm(70~83 μm)。第1触角(见图 2F)7节。第2触角(见图 2B)4节,第3节具3个刚毛。
雄虫(n=2):身体(见图 2D)和雌虫相似。长0.77 mm(0.74~0.80 mm),宽0.27 mm(0.27~0.27 mm)。前、后体部长度比1.13(1.13~1.14)。生殖节(见图 2D)长宽比0.87(0.84~0.89)。尾叉长宽比3.91(3.86~3.96)。第2触角(见图 2C)和雌虫相似,但第3节具4个刚毛。
竹蛏赫尔曼蚤是中国新记录种。之前在韩国及日本有过报道。已知宿主包括大竹蛏、四角蛤蜊、长竹蛏和总角截蛏(Solecurtus divaricatus (Lischke))[3, 16, 18]。本文报道的中国蛤蜊和紫石房蛤为竹蛏赫尔曼蚤的新宿主。本文标本雄虫尾叉长宽比(3.91)小于韩国标本(6.8)[18]。本文所测额角长76 μm(70~83 μm),原始描述额角长770 μm[18],疑似笔误或排字错误。
舐皮蚤属(Lichomolgus Thorell, 1859)
拟舐皮蚤(Lichomolgus similis Ho & Kim, 1991)(见图 3和表 1)
|
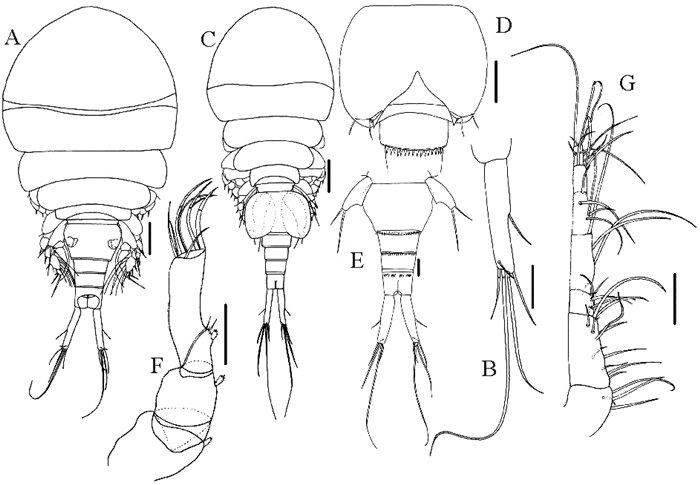
(A:雌虫,背面观;B:雌虫尾叉,背面观;C:雄虫,背面观;D:雄虫生殖节,腹面观;E:雌虫后体部,腹面观;F:雌虫第2触角;G:雌虫第1触角。比例尺:A, C=100 μm; B, D, E, F, G=50 μm。A: Female, dorsal; B: Female caudal ramus, dorsal; C: Male, dorsal; D: Male genital segments, ventral; E: Female urosome, ventral; F: Female antenna; G: Female antennule. Scale bars: A, C=100 μm; B, D, E, F, G=50 μm.) 图 3 拟舐皮蚤 Fig. 3 Lichomolgus similis Ho & Kim, 1991 |
宿主、采集地及感染情况:寄生于短文蛤的外套腔。采自辽宁东港,山东莱州,江苏连云港、盐城、南通5地。最大感染率42.3%(山东莱州,2016年9月)。平均感染强度变化范围1.7~6.0,最大感染强度18(辽宁东港,2017年9月)(见表 1)。
雌虫(n=10):身体(见图 3A)长1.19 mm(1.04~1.38 mm),宽0.56 mm(0.52~0.62 mm)。
前、后体部长度比1.53(1.24~1.73)。生殖节(见图 3E)长宽比0.72(0.60~0.90)。尾叉(见图 3B)长宽比5.02(3.83~5.84)。第1触角(见图 3G)7节,刚毛数分别为4,13,6,3,4,2,7,末3节各具1根感觉毛。第2触角(见图 3F)4节,第4节长宽比2.65(1.96~3.87)。
雄虫(n=10):身体(见图 3C)和雌虫相似。长0.94 mm(0.79~1.07 mm),宽0.38 mm(0.33~0.43 mm)。前、后体部长度比1.22(1.12~1.36)。生殖节(见图 3D)长宽比0.69(0.59~0.85),末端有2个刚毛和2个刺。尾叉长宽比5.51(4.98~6.15)。第1触角7节,第2节比雌虫多2根感觉毛,第4节比雌虫多1根感觉毛。
拟舐皮蚤是中国新记录种。该种最先由Ho & Kim[15]在韩国的丽文蛤和青蛤中发现,后在泰国的文蛤中报道[19]。本文报道的短文蛤为拟舐皮蚤的新宿主。和原始描述[15]对比,本文雄虫标本的第1触角第2节多1个感觉毛、生殖节后方多1个刺。
偏顶蛤蚤属(Modiolicola Aurivillius, 1882)
二分偏顶蛤蚤(Modiolicola bifida Tanaka, 1961)(见图 4和表 1)
|
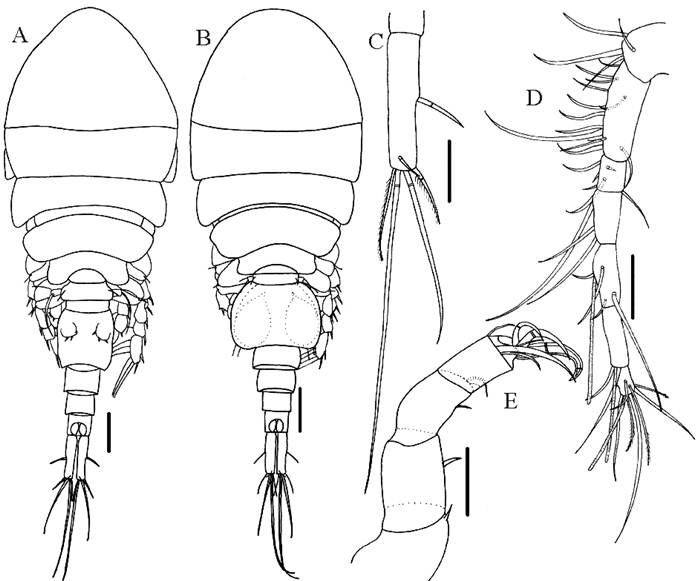
(A:雌虫,背面观;B:雄虫,背面观;C:雌虫尾叉,背面观;D:雌虫第1触角;E:雌虫第2触角。比例尺:A, B=100 μm; C~E=50 μm。A: Female, dorsal; B: Male, dorsal; C: Female caudal ramus, dorsal; D: Female antennule; E: Female antenna. Scale bars: A, B=100 μm; C~E=50 μm.) 图 4 二分偏顶蛤蚤 Fig. 4 Modiolicola bifida Tanaka, 1961 |
宿主、采集地及感染情况:寄生于菲律宾蛤仔、江户布目蛤(Leukoma jedoensis (Lischke))、四角蛤蜊、中国蛤蜊和紫贻贝(Mytilus galloprovincialis(Lamarck))的外套腔和内脏团。采自山东莱州、海阳、青岛,江苏连云港4地。最大感染率18.4%(四角蛤蜊;江苏连云港,2018年5月)。平均感染强度变化范围1.0~7.1,最大感染强度58(菲律宾蛤仔;山东青岛,2017年1月)(见表 1)。
雌虫(n=10):身体(见图 4A)长1.17 mm(1.09~1.28 mm),宽0.45 mm(0.40~0.50 mm)。前、后体部长度比1.29(1.19~1.36)。生殖节(见图 4A)长宽比1.20(1.10~1.31)。尾叉(见图 4C)长宽比4.12(3.80~4.46)。第1触角(见图 4D)7节。第2触角(见图 4E)4节,第4节长宽比1.71(1.38~2.09)。
雄虫(n=10):身体(见图 4B)和雌虫相似,长0.99 mm(0.89~1.15 mm),宽0.35 mm(0.31~0.42 mm)。前、后体部长度比1.17(1.10~1.28)。生殖节(见图 4B)长宽比0.78(0.68~0.90)。尾叉长宽比3.86(3.42~4.49)。
二分偏顶蛤蚤是中国新记录种。该种在日本及韩国均有报道。宿主包括巴菲蛤(Paphia sp.)、中国蛤蜊、菲律宾蛤仔、紫贻贝、青蛤、四角蛤蜊、凸壳肌蛤(Arcuatula senhousia(Benson))、魁蚶(Anadara broughtonii (Schrenck))、毛蚶、远东贻贝(Crenomytilus grayanus (Dunker))、长牡蛎、紫彩血蛤(Nuttallia olivacea (Jay))、宽壳全海笋(Barnea dilatata(Souleyet))、脆壳全海笋和Penitella gabbii (Tryon)共15种双壳类[3, 12-17, 20-22]。本文报道的江户布目蛤为二分偏顶蛤蚤的新宿主。Do和Kajihara[20]详细描述了该种,本文标本与其描述一致。
海螂蚤科(Myicolidae Yamaguti, 1936)
牡蛎蚤属(Ostrincola Wilson, 1944)
高氏牡蛎蚤(Ostrincola koe Tanaka, 1961)(见图 5和表 1)
|
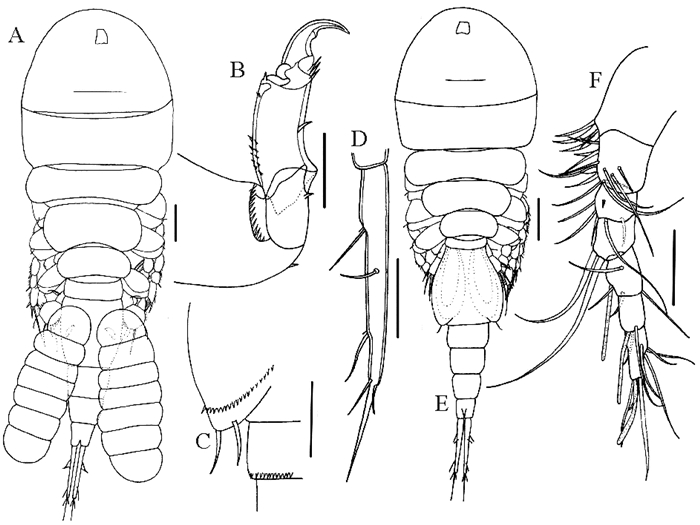
(A:雌虫,背面观;B:雌虫第2触角;C:雄虫生殖节后腹部;D:雌虫尾叉,背面观;E:雄虫,背面观;F:雌虫第1触角。比例尺:A, E=100 μm; B, C, D, F=50 μm。A: Female, dorsal; B: Female antenna; C: Male posteroventral genital segment; D: Female caudal ramus, dorsal; E: Male, dorsal; F: Female antennule. Scale bars: A, E=100 μm; B, C, D, F=50 μm.) 图 5 高氏牡蛎蚤 Fig. 5 Ostrincola koe Tanaka, 1961 |
宿主、采集地及感染情况:寄生于短文蛤和四角蛤蜊的外套腔和鳃。采自山东莱州,江苏连云港、南通3地。最大感染率85.7%(四角蛤蜊;江苏南通,2016年11月)。平均感染强度变化范围1.0~4.9,最大感染强度14(四角蛤蜊;江苏南通,2016年11月)(见表 1)。
雌虫(n=10):身体(见图 5A)长1.27 mm(1.15~1.43 mm),宽0.44 mm(0.42~0.46 mm)。前、后体部长度比1.26(1.09~1.37)。尾叉(见图 5D)长宽比9.07(7.90~10.23)。第1触角(见图 5F)7节,刚毛数分别为4,14,5,3,4,2,7,末3节各具1根感觉毛。第2触角(见图 5B)4节,第1节具1排刺,第3节有5个刚毛,第3节长宽比2.06(1.52~2.66)。
雄虫(n=10):身体(见图 5E)和雌虫相似。长1.00 mm(0.91~1.17 mm),宽0.31 mm(0.28~0.33 mm)。前、后体部长度比1.07(0.97~1.14)。生殖节(见图 5C)后腹部有2个几乎等长的刚毛。尾叉长宽比9.38(8.04~12.37)。第1触角7节,刚毛数分别为4,14,5,3,4,2,7,第2节及末3节各有1根感觉毛,第4节有2根感觉毛。
高氏牡蛎蚤是渤海新记录种。该种在日本、韩国及中国江苏均有报道。宿主包括波纹巴菲蛤、巴菲蛤(Paphia sp.)、日本石咸蛤(Petricola japonica Dun-ker)、中国朽叶蛤、菲律宾蛤仔、丽文蛤、青蛤、四角蛤蜊、透明美丽蛤(Serratina diaphana (Deshayes))、侧扁隐海螂(Cryptomya busoensis Yokoyama)、缢蛏、大竹蛏、长竹蛏和文蛤共14种双壳类[7, 9, 12, 15, 17, 23-24]。其中,Ho & Zheng[7]在中国江苏报道的宿主“文蛤”应该是短文蛤,因为近些年来的研究证明文蛤并不分布在我国的黄海地区[4]。本文标本与之前的报道及之前的有关报道之间存在些细微的形态差异。雌虫第1触角第2节上的刚毛数和之前报道不同(14 vs 15)[9, 15]。雌虫第1触角第3节上的刚毛数和Ho等[9]报道的一致,但不同于Ho和Kim[15](5 vs 6)。雄虫第1触角第2节上的刚毛数和之前报道[15]不同(14 vs 15)。雄虫第1触角第3节上的刚毛数不同于Ho和Kim[15](5 vs 6)。Ho和Kim[15]和Ho等[9]均描述了第2触角第1节上的斜刺,但Ho和Zheng[7]并未提及该特征。第2触角第3节上的刚毛数和Ho等[9]相同,但不同于Ho和Kim[15](5 vs 6)。
伪海螂蚤属(Pseudomyicola Yamaguti, 1936)
多刺伪海螂蚤(Pseudomyicola spinosus (Raffaele & Monticelli, 1885))(见图 6和表 1)
|
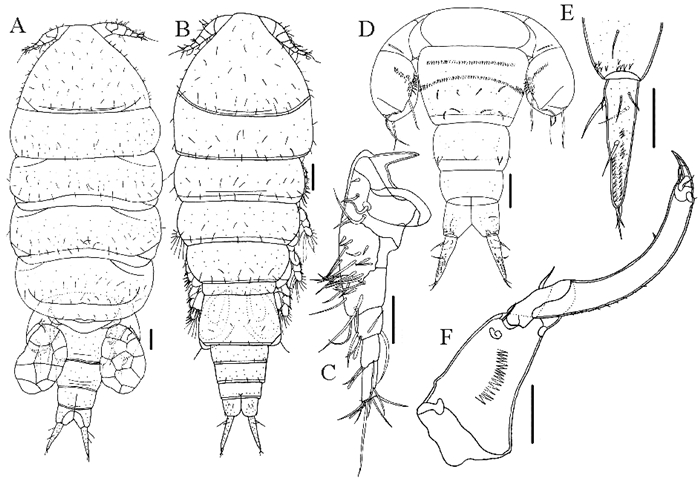
(A:雌虫,背面观;B:雄虫,背面观;C:雌虫第1触角;D:雌虫后体部,腹面观;E:雌虫尾叉,腹面观;F:雌虫第2触角。比例尺:A, B, D=100 μm; C, E, F=50 μm。A: Female, dorsal; B: Male, dorsal; C: Female antennule; D: Female urosome, ventral; E: Female caudal ramus, ventral; F: Female antenna. Scale bars: A, B, D=100 μm; C, E, F=50 μm.) 图 6 多刺伪海螂蚤 Fig. 6 Pseudomyicola spinosus (Raffaele & Monticelli, 1885) |
宿主、采集地及感染情况:寄生于菲律宾蛤仔和紫贻贝的外套腔和鳃。采自辽宁大连,山东青岛两地。最大感染率13.9%(紫贻贝;辽宁大连,2017年9月)。平均感染强度变化范围1.0~1.6,最大感染强度4(紫贻贝;山东青岛,2017年3月)。菲律宾蛤仔感染率极低,在4 376个蛤仔中仅发现1个虫体(见表 1)。
雌虫(n=10):体长(见图 6A)2.18 mm(1.94~2.33 mm),宽0.72 mm(0.62~0.79 mm)。前、后体部长度比1.70(1.49~1.87)。生殖节(见图 6D)长宽比0.69(0.59~0.87)。肛节腹面(见图 6E)有1、2、3或7个(大多数为1)长刚毛,近末端有一些刺。Humes[25](见文献[25]的图29~32)在描述该种肛节末端刺的分布时分了4种类型(Ⅰ, Ⅱ, Ⅲ, Ⅳ),本实验所观察到的10个标本中有9个属于第Ⅰ类型,剩下的1个标本左侧肛节末端刺的分布属于第Ⅱ类型,右侧分布属于第Ⅰ类型。尾叉(见图 6E)长宽比4.27(3.55~5.80)。第1触角(见图 6C)6节。第2触角(见图 6F)3节。
雄虫(n=7):身体(见图 6B)和雌虫相似,长1.47 mm(1.29~1.57 mm),宽0.45 mm(0.38~0.51 mm)。前、后体部长度比1.47(1.27~1.66)。生殖节(见图 6B)长宽比0.70(0.58~0.92)。尾叉长宽比4.94(3.84~7.61)。
多刺伪海螂蚤是中国新记录种。该种在大西洋、太平洋和西印度洋均有分布[26]。全世界目前共在50多种双壳类的外套腔中发现该种[27]。本文标本的宿主为菲律宾蛤仔和紫贻贝。其中,菲律宾蛤仔为新宿主,然而在所检查的4 376个菲律宾蛤仔中,只见到1个虫体,该种桡足类可能是偶然侵入菲律宾蛤仔。本文标本和前人描述[22, 25, 28]没有明显不同。
贻贝蚤科(Mytilicolidae Bocquet & Stock, 1957)
贻贝蚤属(Mytilicola Steuer, 1902)
东方贻贝蚤(Mytilicola orientalis Mori, 1935)(见图 7和表 1)

|
(A:雌虫,背面观;B:雄虫,背面观;C:雌虫尾叉,背面观;D:雌虫第1触角;E:雌虫第2触角;F:雌虫口部结构;G:雌虫第1小颚;H:雌虫第2小颚;I:雄虫颚足;J:雌虫第1胸足;K:雄虫第1胸足;L:雌虫第5胸足。比例尺:A, B=200 μm; C~L=50 μm。A: Female, dorsal; B: Male, dorsal; C: Female caudal ramus, dorsal; D: Female antennule; E: Female antenna; F: Female mouth-parts; G: Female maxillule; H: Female maxilla; I: Male maxilliped; J: Female leg 1; K: Male leg 1; L: Female leg 5. Scale bars: A, B=200 μm; C~L=50 μm.) 图 7 东方贻贝蚤 Fig. 7 Mytilicola orientalis Mori, 1935 |
宿主、采集地及感染情况:寄生于长牡蛎和紫贻贝的外套腔、鳃和内脏团(有些标本确定是从胃,肠和性腺中取出)。采自山东荣成、乳山、青岛3地。最大感染率18.2%(长牡蛎;山东青岛,2017年1月)。平均感染强度变化范围1.0~8.0,最大感染强度8(长牡蛎;山东乳山,2016年4月)(见表 1)。
雌虫(n=10):身体(见图 7A)细长,长7.44 mm(6.18~8.65 mm),宽0.95 mm(0.65~1.14 mm)(位于卵囊连接处)。头部长386 μm(306~416 μm),宽596 μm(493~664 μm)。尾叉(见图 7C)长172 μm(112~213 μm)。第1触角(见图 7D)4节,刚毛数分别为14、5、3和8。第2触角(见图 7E)4节。上唇(见图 7F)呈W型结构。大颚缺失。第1小颚(见图 7G)末端有2个小刚毛。第2小颚(见图 7H)末端具小刚毛结构。颚足退化。胸足1~4(见图 7J)内外肢分别由2节构成。第1~4胸足各节刺的分布详见表 2。
|
|
表 2 东方贻贝蚤雌虫1~4胸足刚毛公式 Table 2 Armature patterns of legs 1~4 of Mytilicola orientalis Mori, 1935 in female |
第5胸足(见图 7L)3个小刚毛。
雄虫(n=6):雄虫(见图 7B)较雌虫身体长度明显变短,长3.07 mm(2.32~3.67 mm),宽0.61 mm(0.47~0.69 mm)。头部长311 μm(255~368 μm),宽447 μm(351~502 μm)。尾叉长107 μm(90~138 μm)。
第1触角、第2触角、上唇、第1小颚、第2小颚和雌虫相似。颚足(见图 7I)末端呈钩状,钩状部位有薄膜状结构。胸足1~4(见图 7K)内外肢分别由2节构成。第1和2胸足内肢的刺较雌虫要长些。第1-4胸足各节刺的分布详见表 3。
|
|
表 3 东方贻贝蚤雄虫1~4胸足刚毛公式 Table 3 Armature patterns of legs 1~4 of Mytilicola orientalis Mori, 1935 in male |
第5胸足和雌虫相似。
东方贻贝蚤是中国新记录种。该种分布在东北大西洋、地中海、黑海、东北太平洋和西北太平洋[29-31]。宿主包括长牡蛎、厚壳贻贝(Mytilus unguiculatus Valenciennes)、欧洲牡蛎(Ostrea edulis Linnaeus)、奥林匹亚牡蛎(Ostrea lurida Carpenter)、油黑壳菜蛤(Mytilus trossulus Gould)、紫贻贝、加利福尼亚贻贝(Mytilus californianus Conrad)、贻贝(Mytilus edulis Linnaeus)、菲律宾蛤仔、Leukoma staminea (Conrad)、朦胧圆滨蛤(Nuttallia obscurata (Reeve))、新石房蛤(Saxidomus gigantea (Deshayes))、大西洋舟螺(Crepidula fornicata (Linnaeus))、Barnea dilatata japonica (Yokoyama)和脆壳全海笋[3, 29, 32-36]。本文标本第1触角第1节的刚毛数及第2触角节数和之前报道不同[21],可能是人为因素导致观察结果不同。该种与肠贻贝蚤(Mytilicola intestinalis Stuer, 1902)极相似,Mori[29]和Elsner等[37]认为胸节背部的凸起状结构是鉴别两个种的有效特征,肠贻贝蚤的背部凸起很短、末端呈圆形,而东方贻贝蚤的背部凸起很长、末端相比肠贻贝蚤尖锐。此外,Mori[29]还指出两个种的上唇结构也有区别,肠贻贝蚤的上唇下边缘为圆形,东方贻贝蚤的上唇下边缘则为有缺刻的三角形。本文标本的特征符合东方贻贝蚤。
蹄螺蚤属(Trochicola Dollfus, 1914)
日本蹄螺蚤(Trochicola japonica Shimura & Kuwabara, 1984)(见图 8和表 1)
|
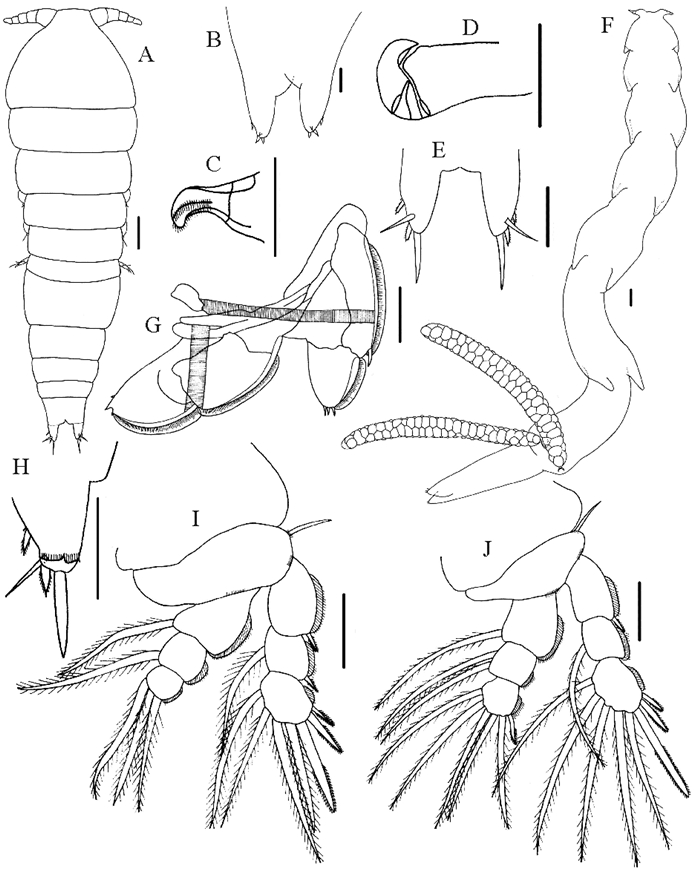
(A:雄虫,背面观;B:雌虫尾叉,背面观;C:雌虫第2小颚末节;D:雄虫颚足;E:雄虫尾叉,背面观;F:雌虫背面观;G:雌虫第1胸足;H:雄虫尾叉,腹面观;I:雄虫第1胸足;J:雄虫第2胸足。比例尺:A=100 μm; B~E, G~J=50 μm; F=200 μm。A: Male dorsal; B: Female caudal ramus, dorsal; C: Tip of female maxilla; D: Male maxilliped; E: Male caudal ramus, dorsal; F: Female, dorsal; G: Female leg 1; H: Male caudal ramus, ventral; I: Male leg 1; J: Male leg 2. Scale bars: A=100 μm; B~E, G~J=50 μm; F=200 μm.) 图 8 日本蹄螺蚤 Fig. 8 Trochicola japonica Shimura & Kuwabara, 1984 |
宿主、采集地及感染情况:寄生于菲律宾蛤仔的外套腔、鳃、体壁和内脏团(有些标本确定是从肠和消化腺中取出)。采自辽宁兴城,山东青岛,江苏连云港、南通4地。最大感染率28.0%(山东青岛,2017年11月)。平均感染强度变化范围1.0~1.7,最大感染强度6(山东青岛,2017年12月)(见表 1)。
雌虫(n=10):身体(见图 8F)细长,长6.20 mm(3.98~8.18 mm),宽0.61 mm(0.48~0.72 mm)(位于卵囊连接处)。头部长395 μm(365~447 μm),宽530 μm(454~645 μm)(不含头部侧面的突起)。尾叉(见图 8B)长158 μm(118~188 μm)。第2小颚(见图 8C)末端具小刚毛结构。胸足1~4(见图 8G)内外肢分别由2节构成。第1~4胸足各节刺的分布详见表 4。
|
|
表 4 日本蹄螺蚤雌虫1~4胸足刚毛公式 Table 4 Armature patterns of legs 1~4 of Trochicola japonica Shimura & Kuwabara, 1984 in female |
雄虫(n=4):雄虫(见图 8A)较雌虫身体长度明显变短。长1.18 mm(0.93~1.31 mm),宽0.34 mm(0.33~0.35 mm)。前、后体部长度比1.35(1.19~1.49)。头部长304 μm(286~323 μm),宽即为体宽。生殖节(见图 8A)长128 μm(114~146 μm),宽255 μm(251~260 μm)。尾叉(见图 8E、H)长53 μm(52~55 μm),尾叉腹面存在两片膜状结构。颚足(见图 8D)末端呈钩状,钩状部位有薄膜状结构。胸足1-4(见图 8I、J)内外肢分别由3节构成。第1~4胸足各节刚毛和刺的分布详见表 5。
|
|
表 5 日本蹄螺蚤雄虫1~4胸足刚毛公式 Table 5 Armature patterns of legs 1~4 of Trochicola japonica Shimura & Kuwabara, 1984 in male |
日本蹄螺蚤是中国新记录种。该种具有明显的宿主特异性,目前仅发现于菲律宾蛤仔[16, 38]。前人报道雄虫第4胸足内肢有2[16]或3节[38],本文标本是3节。本文雌虫标本1~4胸足内外肢末端刺的数目并不固定,与Shimura和Kuwabara[38]的结论一致。本文发现雄虫1~4胸足内外肢刺和刚毛的分布情况也不是固定不变的,而Shimura和Kuwabara[38]及Kim和Sato[16]只描述了一种状态。本文及Kim和Sato[16]的雄虫尾叉上存在两片膜状结构,但Shimura和Kuwabara[38]则未报道该结构。Shimura和Kuwabara[38]报道该种时未提及雄虫颚足末端钩状部位的膜状结构,而本文标本和Kim和Sato[16]报道的雄虫颚足描述一致,末端钩状部位均有膜状结构。Shimura和Kuwabara[38]报道该种时提及第2小颚末节有1个基部小刚毛,而本文和Kim和Sato[16]未观察到该结构。
本研究报道的8种(渤海5种,黄海8种)双壳类寄生桡足类中,高氏牡蛎蚤曾在江苏如东、启东有过报道[7],其余7种为中国新记录种。负羽壳蚤、竹蛏赫尔曼蚤、二分偏顶蛤蚤、高氏牡蛎蚤、拟舐皮蚤和东方贻贝蚤之前在朝鲜半岛西海岸有过报道[3, 39-40]。本研究发现的多刺伪海螂蚤和日本蹄螺蚤为黄海新记录种。此外,Kim[3, 39]和Moon和Kim[40]还在朝鲜半岛西海岸报道了其他13种贝类(包含11种双壳类)寄生桡足类,Du等[10]在青岛报道了黄海章鱼蚤。迄今,黄海海域共记录贝类寄生桡足类22种。渤海海域贝类寄生桡足类尚无报道,本研究发现的负羽壳蚤、拟舐皮蚤、二分偏顶蛤蚤、高氏牡蛎蚤和日本蹄螺蚤均为渤海新记录种。在中国其他海域,仅数篇文献报道了台湾[8-9]和香港[5-6]等少数海区的贝类寄生桡足类,共记录东海4种(Anthessius mytilicolus,Ostrincola simi-lis,Myicola formosanus,Ostrincola koe)[8-9],南海3种(A. mytilicolus,A. pinnae,Panjakus platygyrae)[5-6]。这些物种与黄渤海种类多不相同,提示中国南、北方沿海的贝类寄生桡足类区系或有较大差异。我们的研究中,除检查了黄渤海32种双壳类(8 628个体)外,还检查了多板纲(Polyplacophora)、腹足纲(Gastropoda)和头足纲(Cephalopoda)软体动物32种1 451个体(均未发现寄生桡足类;见附录)。然而,该调查仅涵盖黄渤海约500种贝类[41]中的66种(含Du等[10]检查的2种头足类)。因此,全面系统的调查是中国贝类寄生桡足类研究领域一项亟待开展的基础工作。
关于寄生桡足类对贝类影响的报道尚少,但有研究表明:肠贻贝蚤会造成欧洲紫贻贝的大量死亡[42];Pectinophilus ornatus Nagasawa et al., 1988对虾夷扇贝的感染率可达到100%,并导致虾夷扇贝的肥满度降低[43-44];东方贻贝蚤可使牡蛎肠内壁破损,造成牡蛎死亡减产[45];高氏牡蛎蚤寄生在短文蛤的外套腔,破坏宿主组织,使其遭受病菌感染,大量死亡[7]。本文调查显示,寄生桡足类在黄渤海双壳类的感染率和感染强度一般不高,但高氏牡蛎蚤在短文蛤及四角蛤蜊的感染率,有时可达50%以上,二分偏顶蛤蚤在菲律宾蛤仔中最大感染强度可达58(见表 1),其对宿主贝类的危害值得进一步研究。
3 结语本文对黄渤海双壳类寄生剑水蚤目桡足类进行了调查。共鉴定出8种双壳类寄生剑水蚤类,其中7种为中国新记录种。在渤海发现5种,均为海区新记录种;在黄海发现8种,其中2种为黄海新记录种。这些寄生桡足类在黄渤海感染双壳类的感染率一般不超过50%。黄渤海贝类寄生桡足类的种类组成与东海、南海记录的种类差异较大。研究结果丰富了贝类寄生虫流行病学资料,对海洋贝类寄生虫防控具参考意义。
附录:其他软体动物寄生桡足类的调查情况作者的研究中,除调查了黄渤海32种双壳类外,还对其它32种贝类(1 451个体)进行了调查,但均未检查到寄生桡足类,采样情况如下:多板纲(Polyplacophora):朝鲜鳞带石鳖(Lepidozona coreanica(Reeve)),大连、青岛,2批2个;红条毛肤石鳖(Acanthochitona rubrolineata (Lischke)),青岛,5批106个;双刻鳞带石鳖(Lepidozona bisculpta (Carpenter in Pilsbry)),青岛,1批1个。腹足纲(Gastropoda):半褶织纹螺(Nassarius sinarum(Philippi)),连云港,1批1个;背小节贝(Lottia dorsuosa (Gould)),青岛、日照,2批24个;扁玉螺(Neverita didyma (Rding)),莱州、青岛,2批2个;朝鲜花冠小月螺(Lunella correensis (Récluz)),青岛、日照,6批98个;单齿螺(Monodonta labio(Linnaeus)),大连、葫芦岛、莱州、青岛、日照,8批191个;单一丽口螺(Tristichotrochus unicus (Dunker)),大连,1批4个;短滨螺(Littorina brevicula (Philippi)),大连、葫芦岛、莱州、青岛、日照、连云港,9批417个;方斑东风螺(Babylonia areolata (Link)),南通,1批1个;古氏滩栖螺(Batillaria cumingii (Crosse)),莱州、青岛,2批15个;红带织纹螺(Nassarius succinctus (Adams)),日照,1批1个;嫁虫戚(Cellana toreuma (Reeve)),青岛,3批29个;杰氏裁判螺(Funa jeffreysii(Smith)),青岛,1批8个;口马丽口螺(Calliostoma koma (Shikama & Habe)),青岛,1批1个;蓝无壳侧鳃海牛(Pleurobranchaea maculata (Quoy & Gaimard)),青岛,1批1个;丽小笔螺(Mitrella albuginosa (Reeve)),葫芦岛、青岛、日照,3批54个;脉红螺(Rapana venosa (Valenciennes)),莱州、青岛、日照,6批30个;皮氏蛾螺(Volutharpa perryi (Jay)),青岛,2批25个;日本菊花螺(Siphonaria japonica (Donovan)),青岛,1批1个;润泽角口螺(Ceratostoma rorifluum (Adams & Reeve)),大连,1批20个;史氏背尖贝(Nipponacmea schrenckii(Lischke)),大连、青岛,3批56个;双带小笔螺(Mitrella bicincta(Gould)),青岛,1批10个;托氏琩螺(Umbonium vestiarium(Linnaeus)),莱州、青岛,2批15个;习见织纹螺(Nassarius pyrrhus(Menke)),莱州,1批2个;秀丽织纹螺(Reticunassa festiva (Powys)),青岛、连云港,2批9个;锈凹螺(Tegula rustica (Gmelin)),大连、葫芦岛、龙口、威海、青岛、日照,8批104个;疣荔枝螺(Reishia clavigera (Küster)),大连、葫芦岛、龙口、青岛、日照,10批185个;纵肋织纹螺(Nassarius variciferus(Adams)),莱州,1批2个。头足纲(Cephalopoda):火枪鱿(Loliolus(Nipponololigo) beka (Sasaki)),青岛,2批15个;双喙耳乌贼(Lusepiola birostrata (Sasaki)),青岛,2批21个。
| [1] |
Boxshall G A, O′Reilly M. The first parasitic copepod from a scaphopod mollusc host[J]. Systematic Parasitology, 2015, 90: 113-124. DOI:10.1007/s11230-014-9537-9
(  0) 0) |
| [2] |
Humes A G. How many copepods?[J]. Hydrobiologia, 1994, 292/293: 1-7. DOI:10.1007/BF00229916
(  0) 0) |
| [3] |
Kim I H. Poecilostomatoid copepods associated with bivalves in Korea and their distribution[J]. Zoological Studies, 2004, 43(2): 187-192.
(  0) 0) |
| [4] |
张素萍, 王鸿霞, 徐凤山. 中国近海文蛤属(双壳纲, 帘蛤科)的系统分类学研究[J]. 动物分类学报, 2012, 37(3): 473-479. Zhang S P, Wang H X, Xu F S. Taxonomic study on Meretrix(Bivalvia, Veneridae) from China seas[J]. Acta Zootaxonomica Sinica, 2012, 37(3): 473-479. (  0) 0) |
| [5] |
Humes A G, Lee S Y. The poecilostome copepod Anthessius mytilicolus Reddiah, 1966, associated with the mussel Perna viridis(L.) at Hong Kong[J]. Asian Marine Biology, 1985, 2: 85-92.
(  0) 0) |
| [6] |
Humes A G, Boxshall G A. Poecilostome copepods associated with bivalve molluscs and a brachiopod at Hong Kong[J]. Journal of Natural History, 1988, 22: 537-544. DOI:10.1080/00222938800770361
(  0) 0) |
| [7] |
Ho J S, Zheng G X. Ostrincola koe (Copepoda, Myicolidae) and mass mortality of cultured hard clam(Meretrix meretrix) in China[J]. Hydrobiologia, 1994, 284: 169-173. DOI:10.1007/BF00006888
(  0) 0) |
| [8] |
Lin C L, Ho J S. Poecilostomatoid copepods parasitic in bivalve mollusks of Taiwan[J]. Publications of the Seto Marine Biological Laboratory, 1999, 38(5/6): 201-218.
(  0) 0) |
| [9] |
Ho J S, Liu W C, Lin C L. New record of Ostrincola koe Tanaka, 1961(Copepoda: Poecilostomatoida: Myicolidae) from hard clam(Meretrix lusoria) of Taiwan, with key to species of genus Ostrincola Wilson, 1944[J]. Journal of Fisheries Society of Taiwan, 2012, 39(3): 137-148.
(  0) 0) |
| [10] |
Du X, Dong C, Sun S C. Octopicola huanghaiensis n. sp.(Copepoda: Cyclopoida: Octopicolidae), a new parasitic copepod of the octopuses Amphioctopus fangsiao(d′Orbigny) and Octopus minor(Sasaki)(Octopoda: Octopodidae) in the Yellow Sea[J]. Systematic Parasitology, 2018, 95: 905-912. DOI:10.1007/s11230-018-9819-8
(  0) 0) |
| [11] |
Margolis L, Esch G W, Holmes J C, et al. The use of ecological terms in parasitology[J]. The Journal of Parasitology, 1982, 68(1): 131-133. DOI:10.2307/3281335
(  0) 0) |
| [12] |
Ko Y, Murakami Y, Daiku K. The biology of the commensal copepods in Japanese marine bivalves[J]. Records of the Oceanographic Works in Japan, 1962, 6: 113-119.
(  0) 0) |
| [13] |
Ko Y. On the occurrence of four commensal copepods in the Japanese clam, Tapes japonica[J]. Bulletin of the Faculty of Fisheries, Nagasaki University, 1969, 28: 83-91.
(  0) 0) |
| [14] |
Yoshikoshi K, Ko Y. Food and feeding of three species of cyclopoid copepods associated with marine pelecypods(preliminary note)[J]. Bulletin of the Faculty of Fisheries, Nagasaki University, 1974, 38: 109-115.
(  0) 0) |
| [15] |
Ho J S, Kim I H. Copepod parasites of commercial bivalves in Korea. Ⅱ. Copepods from cultured bivalves[J]. Journal of the Korean Fisheries Society, 1991, 24(6): 369-396.
(  0) 0) |
| [16] |
Kim I H, Sato S I. A review of copepods associated with bivalves in Japan, with description of two new species(Crustacea, Copepoda, Cyclopoida)[J]. Bulletin of the Tohoku University Museum, 2010, 9: 1-22.
(  0) 0) |
| [17] |
Tanaka O. On copepods associated with marine pelecypods in Kyushu[J]. Journal of the Faculty of Agriculture Kyushu University, 1961, 11(3): 249-278. DOI:10.5109/22687
(  0) 0) |
| [18] |
Kim I H, Ho J S. Copepod parasites of commercial bivalves from Korea. I. Two new poecilostomatoid species from Solen grandis Dunker in the Yellow Sea[J]. The Korean Journal of Systematic Zoology, 1991, 7(1): 1-12.
(  0) 0) |
| [19] |
Ho J S, Kim I H. Copepod parasites of a commercial clam(Meretrix meretrix) from Phuket, Thailand[J]. Hydrobiologia, 1995, 308: 13-21. DOI:10.1007/BF00037782
(  0) 0) |
| [20] |
Do T T, Kajihara T. Two poecilostomatoid copepods, Anthessius graciliunguis n. sp. and Modiolicola bifdus Tanaka, 1961 from the blue mussel, Mytilus edulis galloprovincialis Lamarck, in Japan[J]. Fish Pathology, 1984, 19(1): 5-15. DOI:10.3147/jsfp.19.5
(  0) 0) |
| [21] |
Do T T, Kajihara T. Studies on parasitic copepod fauna and biology of Pseudomyicola spinosus, associated with blue mussel Mytilus edulis galloprovincialis in Japan[J]. Bulletin of the Ocean Research Institute, University of Tokyo, 1986(23): 1-63.
(  0) 0) |
| [22] |
Suh H L, Choi S D. Two copepods(Crustacea) parasitic on the blue mussel, Mytilus galloprovincialis, from the Yongsan River Estuary in Korea[J]. Bulletin of the Korean Fisheries Society, 1990, 23(2): 137-140.
(  0) 0) |
| [23] |
Ko Y, Yoshikoshi K, Ito N. External anatomy of a commensal copepod, Ostrincola koe — Ⅱ nauplius stage[J]. Bulletin of the Faculty of Fisheries, Nagasaki University, 1974, 38: 87-93.
(  0) 0) |
| [24] |
Kim I H. Illustrated Encyclopedia of Fauna & Flora of Korea. Vol. 38. Cirripedia, Symbiotic Copepoda, and Pycnogonida[M]. Seoul: Ministry of Education, 1998.
(  0) 0) |
| [25] |
Humes A G. The cyclopoid copepod Pseudomyicola spinosus(Raffaele & Monticelli) from marine pelecypods, chiefly in Bermuda and the West Indies[J]. Beaufortia, 1968, 14(178): 203-226.
(  0) 0) |
| [26] |
Cáceres Martínez C, Chávez Villalba J, Garduño Méndez L. First record of Pseudomyicola spinosus in Argopecten ventricosus in Baja California, Mexico[J]. Journal of Invertebrate Pathology, 2005, 89: 95-100. DOI:10.1016/j.jip.2005.03.004
(  0) 0) |
| [27] |
Ho J S. Phylogenetic analysis of the Myicolidae, a family of poecilostome copepods chiefly parasitic in marine bivalve mollusks[J]. Acta Zoologica Taiwanica, 1992, 3(2): 67-77.
(  0) 0) |
| [28] |
Ho J S. Origin and dispersal of Mytilus edulis in Japan deduced from its present status of copepod parasitism[J]. Publications of the Seto Marine Biological Laboratory, 1980, 25(5-6): 293-313. DOI:10.5134/176009
(  0) 0) |
| [29] |
Mori T. Mytilicola orientalis, a new species of parasitic copepoda[J]. The Zoological Society of Japan, 1935, 47: 687-690.
(  0) 0) |
| [30] |
Lauckner G. Diseases of Mollusca: Bivalvia. In Diseases of Marine Animals. Vol II: Introduction, Bivalvia to Scaphopoda (ed. Kinne, O. )[M]. Hamburg: Biologische Anstalt Helgoland, 1983: 477-802.
(  0) 0) |
| [31] |
Streftaris N, Zenetos A. Alien marine species in the Mediterranean the 100'worst invasives' and their impact[J]. Mediterranean Marine Science, 2006, 7(1): 87-118. DOI:10.12681/mms.180
(  0) 0) |
| [32] |
Bernard F R. The parasitic copepod Mytilicola orientalis in British Columbia[J]. Journal Fisheries Research Board of Canada, 1969, 26(1): 190-191. DOI:10.1139/f69-022
(  0) 0) |
| [33] |
Grizel H. Mytilicola orientalis Mori, parasitism[J]. Fiches D′Identification des Maladies et Parasites des Poissons, Crustacés et Mollusques, 1985, 20: 1-4.
(  0) 0) |
| [34] |
Goater C P, Weber A E. Factors affecting the distribution and abundance of Mytilicola orientalis(Copepoda) in the mussel, Mytilus trossulus, in Barkley Sound, B. C[J]. Journal of Shellfish Research, 1996, 15: 681-684.
(  0) 0) |
| [35] |
Marshall W L, Bower S M, Meyer G R. A comparison of the parasite and symbiont fauna of cohabiting native(Protothaca staminea) and introduced(Venerupis philippinarum and Nuttalia obscurata) clams in British Columbia[J]. Journal of Shellfish Research, 2003, 22(1): 185-192.
(  0) 0) |
| [36] |
Francisco C J, Hermida M A, Santos M J. Parasites and symbionts from Mytilus galloprovincialis (Lamark, 1819)(Bivalves: Mytilidae) of the Aveiro Estuary Portugal[J]. Journal of Parasitology, 2010, 96(1): 200-205. DOI:10.1645/GE-2064.1
(  0) 0) |
| [37] |
Elsner N O, Jacobsen S, Thieltges D W, et al. Alien parasitic copepods in mussels and oysters of the Wadden Sea[J]. Helgoland Marine Research, 2011, 65: 299-307. DOI:10.1007/s10152-010-0223-2
(  0) 0) |
| [38] |
Shimura S, Kuwabara R. Trochicola japonicus sp. nov., a mytilicolid copepod parasitic in the short neck clam(Tapes philippinarum) from Lake Hamana, Japan[J]. Fish Pathology, 1984, 18(4): 191-197. DOI:10.3147/jsfp.18.191
(  0) 0) |
| [39] |
Kim I H. Two new species of Doridicola(Copepoda: Cyclopoida: Rhynchomolgidae) associated with opisthobranch mollusks from Korea[J]. The Korean Journal of Systematic Zoology, 2007, 23(2): 117-126. DOI:10.5635/KJSZ.2007.23.2.117
(  0) 0) |
| [40] |
Moon S Y, Kim I H. Description of Conchyliurus dispar n. sp.(Copepoda, Cyclopoida, Clausidiidae) associated with the bivalve Barnea manilensis(Philippi) from the Yellow Sea with a discussion of the male morphotypes in the genus[J]. Zootaxa, 2014, 3760(3): 471-478. DOI:10.11646/zootaxa.3760.3.14
(  0) 0) |
| [41] |
张素萍, 张均龙, 陈志云, 等. 黄渤海软体动物图志[M]. 北京: 科学出版社, 2016. Zhang S P, Zhang J L, Chen Z Y, et al. Mollusks of the Yellow Sea and Bohai Sea[M]. Beijing: Science Press, 2016. (  0) 0) |
| [42] |
Blateau D, Coguic Y L, Mialhe E, et al. Mussel(Mytilus edulis) treatment against the red copepod Mytilicola intestinalis[J]. Aquaculture, 1992, 107(2-3): 165-169. DOI:10.1016/0044-8486(92)90062-P
(  0) 0) |
| [43] |
Nagasawa K, Nagata M. Effects of Pectenophilus ornatus (Copepoda) on the biomass of cultured Japanese scallop Patinopecten yessoensis[J]. Journal of Parasitology, 1992, 78(3): 552-554. DOI:10.2307/3283669
(  0) 0) |
| [44] |
Suzuki H, Matsutani T. Infection of the parasitic copepod, Pectenophilus ornatus on juvenile Japanese scallop, Patinopecten yessoensis[J]. Aquaculture Science, 2009, 57(3): 513-514.
(  0) 0) |
| [45] |
Holmes J M C, Minchin D. Two exotic copepods imported into Ireland with the Pacific oyster Crassostrea gigas (Thunberg)[J]. Irish Naturalists Journal, 1995, 25(1): 17-20.
(  0) 0) |
 2022, Vol. 52
2022, Vol. 52


