众所周知,鱼粉和鱼油是水产饲料最主要的组成部分,因为两者的营养价值对于鱼类的生长来说是十分理想的[1],但随着水产养殖业的迅速发展,鱼粉、鱼油资源变得日益短缺,致使养殖成本上升,严重抑制了水产养殖业的发展,因此如何合理有效地利用资源以及寻找其替代品就成为亟须解决的问题。
饲料中的脂质是鱼类所需要的重要营养物质,既是鱼体能量的主要来源又是机体的重要组成部分,能为机体提供必需脂肪酸、磷脂、固醇类和脂溶性维生素等重要营养物质以维持体内的各种生物学过程[2-3],在鱼类的生长发育、新陈代谢等生命活动中起到了至关重要的作用。此外,脂肪还具有节约蛋白的作用,在一定范围内,饲料脂肪水平的升高可以提高饲料效率,并通过节约蛋白的作用促进生长。只有当饲料的脂肪水平和脂肪酸组成适宜时,鱼类的生长、发育和繁殖等各项生命活动才能正常进行。由于脂肪的节约蛋白作用,促进了高脂饲料的应用,但是研究发现高脂饲料导致了鱼体肝脏和腹腔脂肪的沉积,造成了可食用面积减少、肉质下降等一系列问题。用植物油高度替代鱼油导致了同样的问题[4-6]。因此,了解饲料中的脂肪水平和脂肪源替代如何影响生长和代谢以及两者之间有什么相互的影响将有利于促进饲料中鱼油的高效节约利用。
大菱鲆(Scophthalmus maximus L.)属鲽形目(Pleuronectiformes)菱鲆科(Scophthalmidae)菱鲆属(Scophthalmus),俗称“多宝鱼”,是一种低温经济鱼类,具有经济价值高、生长迅速、宜于集约化养殖等优点,其养殖产业已发展成为中国北方海水养殖支柱产业[7]。然而,鱼油资源的短缺限制了其养殖业的发展,因此,寻找合理利用鱼油的方法以及寻找鱼油替代品就显得十分必要。本实验探讨了不同脂肪水平及脂肪源的饲料在生长、脂代谢相关基因表达等方面对大菱鲆幼鱼的影响,以期为大菱鲆饲料中鱼油的利用提供更多理论依据。
1 材料与方法 1.1 实验饲料以鱼粉、谷朊粉、大豆浓缩蛋白作为蛋白源,以鱼油、大豆卵磷脂为脂肪源,豆油作为100%替代脂肪源,设计6种实验饲料,饲料干物质的粗蛋白含量为50%,脂肪含量设为8%、12%和16% 3个梯度。所有实验饲料中添加晶体氨基酸以满足大菱鲆对必需氨基酸的需求。添加丙酸钙作为防霉剂;添加乙氧基喹啉作为抗氧化剂;添加海藻酸钠作为黏合剂;添加三氧化二钇作为测定表观消化率的指示剂。饲料配方见表 1。各实验组用到的饲料F8、S8、F12、S12、F16、S16,字母F表示鱼油为脂肪源,字母S表示豆油为替代脂肪源,数字8、12、16表示饲料的脂肪含量为8%、12%、16%。
|
|
表 1 实验饲料的组成及成分分析(干物质) Table 1 Formulas and proximate composition of the experimental diets (dry matter) |
所有原料经粉碎机粉碎并过80目的网筛,然后将粉碎好的原料按照饲料配方从小量到大量逐步混合均匀,此后将大豆卵磷脂混入鱼油和豆油中,根据实验配方将预混料分别与相应量的鱼油或豆油混合均匀,然后将胆碱加入到30%饲料重量的水中混匀,再将水与饲料充分混匀。饲料颗粒(3 mm×4 mm)由制粒机制成,然后在55 ℃的通风风箱中烘干12 h。待饲料颗粒干燥冷却后用双层塑料袋装好并封口,保存在-20 ℃冰箱中待使用。
1.2 饲养管理实验在青岛亿海丰水产品有限公司(山东青岛)进行。大菱鲆幼鱼从养殖厂购买,在实验开始前用商业饲料喂养2周,使鱼适应养殖环境。将初始体质量(13.01±0.01) g的幼鱼挑选出来随机分到18个养殖箱中,每个养殖箱30尾鱼。实验所用海水经过砂滤器过滤后以1.5 L/min的速度注入养殖箱。每个处理组都被分成3个平行进行实验。每天7:00和19:00进行定量投喂(投喂量为鱼体质量的1%),每2周称一次体质量并根据体质量调整投喂量。投喂后将粪便清理干净。养殖实验进行56 d。
1.3 样品收集养殖实验结束后饥饿处理24h,记录每个养殖箱内鱼的数量,并称量每个养殖箱内鱼总体质量。每箱随机选出4尾鱼保存在-20 ℃冰箱中用以进行体成分分析。从每个养殖箱中取4尾鱼,取鱼体的肝、肠、肌肉并用液氮保存。每养殖箱中随机挑选2尾鱼测量体质量、体长、内脏团重量、肝脏重量。取肝脏样品保存在液氮中,再保存在-80 ℃冰箱中用于基因定量分析。
1.4 化学分析将样品置于105 ℃烘箱中烘至恒重以测定水分。粗蛋白的测定通过凯氏定氮法(Kjeltec TM 8400, FOSS, Sweden)。采用索氏提取法(Buchi 36680, Switzerland)用乙醚提取后测定粗脂肪。
1.5 肝脏脂肪含量及脂肪酸组成检测肝脏中脂肪含量方法如下:将肝脏样品冷冻干燥,称取100 mg的样品于10 mL玻璃离心管中,记录下样品的质量w0和对应的试管编号;每个离心管中加入氯仿-甲醇溶液(氯仿:甲醇=2:1,存放在棕色玻璃瓶中4 mL,摇匀后盖好盖子,浸泡24 h。75 ℃下烘干另外一批玻璃离心管至恒重,两次误差不得超过0.001 g,记录下离心管质量w1和对应的编号。将氯仿-甲醇溶液加至6 mL,离心(3 000 g,10 min),再将上清液转入第二批离心管;在沉淀中加入2 mL氯仿-甲醇溶液,静置2 h后离心(3 000 g,10 min);上清液仍转入第二批离心管。在上清液中加入1.2 mL 1.6%的CaCl2,摇匀,盖上盖子静置过夜。过夜后用移液枪小心弃去上层液,再将离心管置于75 ℃烘箱中烘干至恒重,两次误差不得超过0.001 g,记录下质量w2。每个样品两个重复。得到肝脏脂肪含量=(w2-w1) /w0×100%。
检测肝脏中脂肪酸含量方法如下:将肝脏样品冷冻干燥,在研钵中充分磨细,称取100 mg左右的样品于带盖的10 mL刻度试管,加入1 mol/L的KOH-甲醇3 mL,于80 ℃的水浴中加热20 min,放置冷却;再加入2 mol/L HCl-甲醇溶液3 mL,混匀,于80 ℃的水浴中加热20 min,放置冷却;加正己烷1 mL,振荡萃取,静置过夜;过夜后取上清得到样品,使用气相色谱仪(Agilent Technologies Inc., Santa Clara, California, USA)分析样品脂肪酸组成,饲料脂肪酸组成见表 2。
|
|
表 2 饲料中脂肪酸的组成(总脂肪酸) Table 2 Fatty acid composition (total fatty acids) of the experimental diets |
肝脏总RNA参照Trizol试剂盒(Invitrogen, USA)提取,提取肝脏样品中的总RNA。然后利用PrimeScriptTM反转录试剂盒将提取的RNA反转录为cDNA。反转录后检测cDNA的浓度并用DEPC水稀释至80 μg/μL,分装后置于-20 ℃保存备用。利用已有目的基因过氧化物酶体增殖物激活受体α(Peroxisome proliferator-activated receptor alpha,PPARα)、肉毒碱棕榈酰转移酶I(Carnitine palmitoyltransferase I,CPTI)、磷脂酸磷酸化酶1(Lipin 1)、过氧化物酶体增殖物激活受体γ(Peroxisome proliferator-activated receptor gamma,PPARγ)、脂蛋白脂酶(Lipoprotein Lipase,LPL)、肝X受体(Liver X receptors,LXR)、延伸因子1α(Elongation Factor -lα, EF1α)的引物序列合成引物,引物序列如表 3所示。定量PCR的体系为25 μL,其中12.5 μL SYBR. Premix Ex TaqTM、0.5 μL上下游引物(10 μmol/L)、3μL cDNA和9.5 μL的DEPC水。定量仪器为实时定量PCR仪(Mastercycler ep realplex,Eppendorf,Germany)。实时定量PCR的程序为95 ℃持续2 min;95 ℃持续15 s,退火温度持续15 s,72 ℃持续20 s,共计40个循环。得到各基因的CT值,并根据2-ΔΔCt方法测定目的基因的表达量[8]。
|
|
表 3 大菱鲆脂肪代谢相关基因的实时定量PCR引物 Table 3 Real-time quantitative PCR primers for fatty metabolismrelated genes of turbot (Scophthalmus maximus L.) |
大菱鲆摄食率、特定生长率、肥满度等参照以下公式计算:
存活率(Survival rate,SR)=(最终鱼数量/初始鱼数量)×100%;
增重率(Weight gain rate,WGR)=(终体质量-初始体质量)/初始体质量×100%;
特定生长率(Specific growth rate,SGR) =(ln终体质量-ln始体质量)/实验天数×100%;
肥满度(Condition factor,CF)=终体质量(g) /体长3(cm)×100%;
肝体比(Hepatosomatic index,HSI)=肝脏重(g)/体质量(g)×100%;
脏体比(Viscerosomatic index,VSI)=内脏重(g)/体质量(g)×100%。
数据统计分析使用SPSS 19.0。数据采用双因素方差分析(ANOVA)再进行Tukey检验。当P < 0.05时视作有显著性差异。数据以平均值±标准误差表示。
2 结果 2.1 饲料中不同脂肪水平和脂肪源对大菱鲆生长参数影响实验各组的生长数据如表 4所示。随着饲料脂肪水平的升高以及脂肪源的替代,大菱鲆幼鱼的存活率(SR)没有显著差异(P>0.05),但是终末体质量(FBW)、增重率(WGR)和特定生长率(SGR)出现了显著差异(P<0.05)。FBW、WGR和SGR均随饲料脂肪水平的上升而上升,只有S16组下降,而用豆油替代了饲料中的鱼油后FBW、WGR和SGR全部下降(P<0.05),在所有的处理组中,F16组的FBW、WGR和SGR高于其他各组,S16组最低,但与F8、S8组相比没有显著差异(P<0.05),F8、S8、F12和S12组之间没有显著差异(P>0.05),但F8、S8组与F16组有显著差异(P<0.05),F12和S12组则没有显著差异(P>0.05)。
|
|
表 4 饲料脂肪水平和豆油替代对大菱鲆生长的影响 Table 4 Effect of dietary lipid level and fish oil replaced by soybean oil on growth parameters of juvenile turbot |
实验各组肥满度(CF)、脏体比指数(VSI)和肝体比指数(HSI)结果如表 5所示,随着饲料脂肪水平的增加大菱鲆脏体比指数(VSI)和肝体比指数(HSI)均有所上升并且产生了显著差异(P<0.05),但肥满度(CF)没有受到显著影响(P>0.05);而在用豆油替代饲料中的鱼油后,脏体比指数(VSI)和肝体比指数(HSI)没有受到影响(P>0.05),但肥满度(CF)出现了显著差异(P<0.05)。
|
|
表 5 饲料脂肪水平和豆油替代对大菱鲆肝体比、脏体比及肥满度的影响 Table 5 Effect of dietary lipid level and fish oil replaced by soybean oil on hepatosomatic index (HSI), viscerosomatic index (VSI) and condition factor (CF) of juvenile turbot |
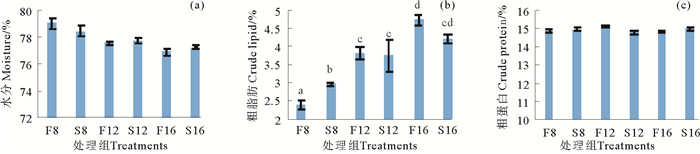
对各处理组的大菱鲆的体组成进行了分析,包括鱼体的水分、粗蛋白和粗脂肪,结果如图 1所示。随着饲料脂肪水平的上升,鱼体水分含量下降但没有显著差异(P>0.05),脂肪含量上升(P<0.05),蛋白含量没有明显的差异(P>0.05);当用豆油替代鱼油后,鱼体的水分、粗蛋白和粗脂肪含量均有所下降,但没有显著的差异(P>0.05)。在所有处理组中,F8组的水分含量最高,F16组的水分含量最低,但各组间没有显著差异(P>0.05);F16组的脂肪含量最高,与S16组相比没有显著差异(P>0.05),但显著高于其他处理组(P<0.05),F8组的脂肪含量最低,显著低于其他处理组(P<0.05),S8组的脂肪含量仅高于F8组,显著低于其他组(P<0.05),F12、S12和S16组的脂肪含量差异不大(P>0.05);F12组的蛋白含量最高,S12组的蛋白含量最低,但各组间没有显著差异(P>0.05)。
|
(同一图中不同小写字母表示组间差异显著(P<0.05)。Significant differences are indicated by different superscript alphabets in each chart(P<0.05). ) 图 1 饲料脂肪水平和豆油替代对大菱鲆体组成的影响 Fig. 1 Effect of dietary lipid level and fish oil replaced by soybean oil on whole body composition of juvenile turbot |
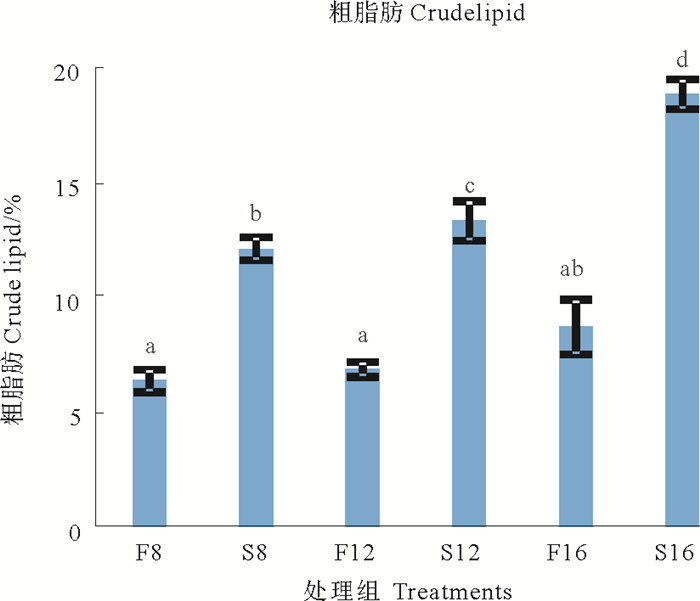
实验各组肝脏脂肪含量如图 2所示。大菱鲆肝脏脂肪含量随着饲料脂肪水平的升高而显著上升(P<0.05),同时豆油的替代也引起了肝脏脂肪含量显著的上升(P<0.05),S16组的肝脏脂肪含量最高,显著高于其他处理组(P<0.05);其次是S12组,显著高于剩余4组(P<0.05),S8和F16组差异不显著(P>0.05),但显著高于F8和F12组(P<0.05)。
|
(同一图中不同小写字母表示组间差异显著(P<0.05)。Significant differences are indicated by different superscript alphabets in each chart(P < 0.05). ) 图 2 饲料脂肪水平和豆油替代对大菱鲆肝脏脂肪含量的影响 Fig. 2 Effect of dietary lipid level and fish oil replaced by soybean oil on the lipid content of the liver in juvenile turbot |
大菱鲆肝脏的脂肪酸组成如表 6所示。肝脏中饱和脂肪酸(Saturated fatty acid,SFA)的含量随着饲料脂肪水平的上升和豆油的替代而出现了下降(P<0.05),n-6系列的多不饱和脂肪酸(n-6 Polyunsaturated fatty acids,n-6 PUFA)的含量受到了饲料脂肪水平和豆油替代的共同影响,在没有豆油替代的3组中,∑n-6 PUFA的含量随脂肪水平的升高而下降(P<0.05),而用豆油替代后,∑n-6 PUFA的含量变化趋势则相反(P<0.05)。二十碳五烯酸(Eicosapentaenoic acid,EPA)和二十二碳六烯酸(Docosahexaenoic acid,DHA)没有受到饲料脂肪水平的显著影响(P>0.05),但在用豆油替代后EPA和DHA含量显著下降(P<0.05)。
|
|
表 6 饲料脂肪水平和豆油替代对大菱鲆肝脏脂肪酸组成(总脂肪酸)的影响 Table 6 Effect of dietary lipid level and fish oil replaced by soybean oil on the fatty acid composition (total fatty acids) in the liver of the juvenile turbot |
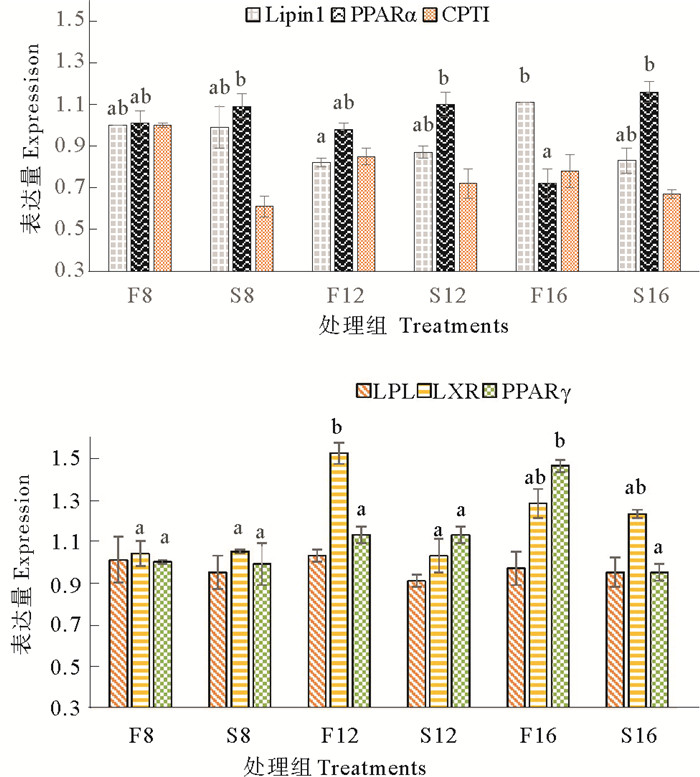
各处理组间肝脏脂肪代谢相关基因的相对表达量如图 3所示。Lipin1和LPL的表达量没有随着饲料脂肪水平和豆油替代的变化而发生显著的差异(P>0.05),但是当有豆油替代时两者的表达量均有下降的趋势。Lipin1表达量最高出现在F16组,最低出现在F12组;F12组LPL表达量最高,S12组表达量最低,但各组间没有显著性差异(P>0.05)。PPARα的表达量受饲料脂肪水平和豆油替代的共同影响,豆油替代上调了PPARα的表达量(P<0.05),而没有豆油替代时,PPARα的表达量随饲料脂肪水平的升高而降低,豆油替代鱼油后其表达量升高,S16组PPARα的表达量最高,显著高于F16组(P<0.05),但与其他组相比没有显著差异(P>0.05)。豆油替代降低了CPT I的表达量,在豆油替代的情况下,CPT I的表达量随着脂肪水平的升高而有所上升,非替代组的变化趋势与此相反。F12组LXR的表达量最高,与F16和S16组没有显著差异(P>0.05),S12组表达量最低,但只与F12组有显著差异(P<0.05)。F16组PPARγ的表达量最高,显著高于其他各组(P<0.05),其余各组没有显著性差异(P>0.05)。
|
(同一图中不同小写字母表示组间差异显著(P<0.05)。Significant differences are indicated by different superscript alphabets in each gene(P < 0.05). ) 图 3 饲料脂肪水平和豆油替代对大菱鲆肝脏脂肪代谢相关基因表达的影响 Fig. 3 Effect of dietary lipid level and fish oil replaced by soybean oil on the lipid metabolism related gene expression in the liver of the juvenile turbot |
在本次实验中,用6种不同的饲料喂养大菱鲆幼鱼,实验进行56 d。大菱鲆幼鱼的存活率(SR)没有随着饲料脂肪水平的提高以及脂肪源的替代而出现显著的差异(P>0.05),但是终末体质量(FBW)、增重率(WGR)和特定生长率(SGR)出现了显著的差异(P<0.05)。从结果可以看出,F16组的FBW、WGR和SGR最高,生长最好;而S16组的生长最差,其余4组的生长没有显著差异(P>0.05)。虽然没有出现显著差异,但是除S16组外的5组FBW、WGR和SGR均随饲料脂肪水平的上升而出现了上升趋势,这是由于当鱼体摄食的饲料脂肪不充足时,鱼体摄入的能量就会不足,就会引起生长的下降,此外,饲料中的脂肪有节约蛋白的作用,当摄入的脂肪充足时,鱼体就可以减少用于产生能量的蛋白质分解,进而提高生长。生长结果表明,当用豆油替代饲料中鱼油时,鱼体的FBW、WGR和SGR均出现了下降,说明用豆油100%替代鱼油会对大菱鲆的生长产生抑制,这与之前的研究相一致[9]。而且从生长结果可以发现,当饲料脂肪水平为8%和12%时,豆油替代虽然抑制了大菱鲆的生长,但是没有出现显著差异(P>0.05),这可能说明当饲料脂肪水平为8%~12%时,在相同的摄食量下,100%的豆油替代不会对大菱鲆的生长造成太大的影响;而当饲料脂肪水平达到16%时,生长出现了显著的下降(P<0.05),这与之前的研究报道相一致[10],这说明当饲料中豆油含量上升时,其抑制鱼体生长的作用就会越明显,进而表现为生长上的差异。之前的研究表明[9],12%脂肪水平下100%的豆油替代会显著抑制大菱鲆的生长,同时也会抑制大菱鲆的摄食率,而在本实验中,在定量投喂的情况下,12%脂肪水平的鱼油组和豆油组生长差异不大,这可能说明豆油替代饲料的适口性是影响大菱鲆生长的原因之一,因此可以考虑提高豆油替代饲料的适口性来增加豆油的利用性。
随着饲料脂肪水平的增加,大菱鲆脏体比指数(VSI)和肝体比指数(HSI)均有所上升并出现了显著差异(P<0.05),这说明了肝脏是大菱鲆体内沉积脂肪的主要器官;而在用豆油替代鱼油后,VSI和HSI均没有出现显著差异(P>0.05),这与在大菱鲆[10]、篮子鱼(Siganus canaliculatus)[11]、军曹鱼(Rachycentron canadum)[12]、欧洲鲈鱼(Dicentrarchus labrax)和虹蹲(Oncorhynchus mykiss)[13]上的研究结果相一致。另外,肥满度(CF)没有受到饲料脂肪水平影响(P>0.05),但当用豆油替代鱼油后,鱼体的CF出现了显著差异(P<0.05)。
实验分析了包括鱼体水分、粗蛋白和粗脂肪在内的各项体组分,结果显示鱼体水分受饲料脂肪水平的影响(P<0.05),随着饲料脂肪水平的上升,鱼体水分含量下降;而豆油替代则没有影响鱼体的水分含量(P>0.05)。大菱鲆鱼体的粗脂肪含量随饲料脂肪含量升高而显著升高(P<0.05),这与大菱鲆[14]、欧洲鲈鱼[15]、金头鲷(Sparus aurata)[16]、异育银鲫(Carassius auratusgibelio)、长吻鮠(Leiocassis longirostris Günther)[17]。等研究结果相一致;而豆油替代对鱼体粗脂肪的含量没有造成显著的差异(P>0.05),这与先前的研究结果相一致[10, 19-21]。鱼体粗蛋白含量没有受到饲料脂肪水平和豆油替代的显著影响(P>0.05),这与先前的研究结果相一致[10, 19-21],这说明饲料脂肪水平和豆油替代不会显著影响蛋白质在大菱鲆体内的沉积。
饲料的脂肪水平和豆油替代情况显著影响了大菱鲆肝脏脂肪含量(P<0.05):随着饲料脂肪水平的升高,大菱鲆肝脏脂肪含量发生了显著的上升(P<0.05),其结果与Gélineau等[22]的研究结果相一致;同时豆油的替代也影响了其肝脏脂肪含量,引起了脂肪含量的显著上升(P<0.05),这也与Bell等[23]在大菱鲆上的研究结果相一致,这可能是与豆油替代后饲料中的n3/n6比值变化有关。n3-PUFA与n6- PUFA之间的不平衡会造成肝脏脂肪含量的增加[24],而在本实验中,当饲料中的鱼油被豆油替代后,n3/n6的比值均出现了下降。本实验中的大菱鲆肝脏脂肪酸组成验证了之前的一些研究结果[11-12, 21, 25-27],反映了饲料中的脂肪酸组成。LC-PUFA的合成是通过Δ6去饱和酶、延长酶和Δ5去饱和酶催化C18底物,如C18:2n-6和C18:3n-3等来完成的,但大菱鲆将C18:3n-3转化为EPA和DHA的能力有限,所以肝脏中EPA和DHA的含量变化并没有与饲料中C18:3n-3含量的变化相一致,甚至表现出完全相反的变化趋势,但与饲料中EPA和DHA的含量变化趋势相近。其结果与Regost等[10]在大菱鲆上的研究一致。这也说明大菱鲆获得EPA和DHA主要靠外界摄食而不是自身合成。
肝脏脂肪的沉积受脂肪的合成与分解两方面的影响。肝脏脂肪沉积的增加不仅与脂肪合成相关基因的表达上调有关,同时与脂肪分解相关基因的表达下调有关。饲料脂肪水平和豆油替代影响了脂肪代谢相关基因的表达,最终会影响肝脏的脂肪沉积。饲料在鱼体肠细胞中形成乳糜微粒后进入血液循环,进而被LPL水解成乳糜残粒(Chylomicron remnants,CMR),LPL可以结合乳糜残粒并将其转运到肝细胞,这是饲料中的脂肪酸进入肝脏的方式[28]。脂肪酸进入细胞后,在CPT I的作用下进入线粒体进行β氧化供能,在氧化供能过程中会生成乙酰辅酶A。此外,饲料中n-3多不饱和脂肪酸会刺激CPT I的活性,进而增加线粒体内的脂肪酸氧化和提高β氧化能力[29]。PPARα可以通过与多不饱和脂肪酸和类视黄醇X受体(Retinoid X receptor,RXR)结合来诱导脂肪酸氧化和线粒体氧化。此外,脂肪酸可以调节PPARα的表达并进一步调节其靶基因的表达,包括LPL和CPT[30]。Lipin 1可以通过诱导PPARα的表达来激活脂肪酸氧化和线粒体氧化,同时可以抑制脂肪合成并降低循环脂质水平[31]。LXR是一种转录因子,可以与配体结合形成二聚体,形成的二聚体与DNA结合,可促进脂肪的生成,而被激活的PPARα则会促进脂肪酸的氧化[32]。PPARγ是脂肪酸摄取和脂肪生成的关键调控因子[33]。
当大菱鲆摄入的能量不足时,体内AMP/ATP的比值就会上升,进而激活AMPK磷酸化,诱导Lipin1的基因表达,进而诱导PPARa的基因表达,从而上调CPT I和LPL的基因表达[34],这样提高了肝脏的脂肪分解能力;同时抑制LXR结合到应答元件上,从而抑制LXR靶基因的转录水平[35-36],抑制脂肪的合成。而随着饲料脂肪水平的上升,鱼体摄入能量逐渐升高,Lipin1、PPARa、CPT I和LPL基因表达量均发生了下降;LXR和PPARγ的基因表达量上升。而豆油中富含亚油酸(18:2n-6),豆油替代对肝脏脂肪代谢相关基因的影响主要原因是饲料中脂肪酸组成的不同。有研究发现饲料中高水平的n-3 LC-PUFA可能会促进脂肪酸氧化相关基因的表达[37-38],饲料中的n-3 PUFA可以通过刺激CPT I的酶活力促进线粒体膜的流动性,进而增加线粒体脂肪酸氧化[29]。因此饲料中较高含量的n-3 PUFA会诱导脂肪分解相关基因的表达,进而导致β-氧化能力增加,降低肝脏的脂肪沉积。当用豆油替代饲料中的鱼油时,饲料中n-3 PUFA的含量明显下降,而n-6 PUFA的含量上升,这就可能引起豆油替代组内脂肪氧化的降低,进而导致肝脏脂肪水平的上升。
各组Lipin1的基因表达量的变化趋势如图 3所示,当饲料中没有豆油替代时,Lipin1的表达量随着饲料脂肪水平的上升先下降然后上升,在16%脂肪水平处上升的原因很可能是鱼体摄入的能量和n-3 PUFA已经超过鱼体需求,这会激活脂肪分解相关基因(如Lipin1)的表达,提高肝脏脂肪分解的能力,避免脂肪过多沉积;而豆油替代组中Lipin1表达量虽然没有出现显著的差异(P>0.05),但有降低的趋势,这可能说明饲料中的n-6 PUFA会抑制Lipin1的基因表达。PPARα的表达也受到了脂肪水平和豆油替代的影响,在鱼油组中PPARα的表达量随着饲料脂肪水平的上升而下降;当有豆油替代时,各脂肪水平下PPARα的表达量均出现了上升,这与之前的研究结果相一致[9],也有研究显示亚油酸可以增加大鼠β细胞的胰岛素分泌[39],而胰岛素会调节大鼠体内PPARα的转录活性[40],可上调PPARα基因表达。由此可见,饲料脂肪水平和豆油中的亚油酸都可上调PPARα的基因表达量。CPT I和LPL的表达量在非替代组中,均随饲料脂肪水平的上升而下降;在各脂肪水平下,豆油的替代抑制了CPT I和LPL的基因表达,而在豆油替代的情况下,随着脂肪水平的上升,两者的表达量没有出现显著的变化,这可能说明饲料中n-3 PUFA的含量会影响CPT I和LPL的基因表达。LXR的表达量随着饲料脂肪水平的上升而上升,随着豆油的替代而下降,该结果与之前的研究结果一致,其研究结果被解释为饲料中n3 LC-PUFA含量的下降会导致LXR表达的下调[41-42],本次的实验结果印证了这一现象,说明n3 LC-PUFA可能会促进LXR的表达,而饲料脂肪水平的上升会促进LXR的表达,进而增加脂肪的合成。PPARγ被认为是脂肪合成和肝脏脂质变性的重要调控因子[43-46]。饲料脂肪水平的上升促进了PPARγ的表达,豆油替代则抑制了其表达,与之前的研究相一致[47],说明亚油酸会抑制PPARγ的表达,而在豆油替代的情况下,随着脂肪水平的上升,PPARγ的表达量没有出现显著的变化,这也可能说明饲料中n-3 PUFA的含量会影响PPARγ的表达量,即PPARγ的表达受饲料脂肪水平、n-3 PUFA的含量和亚油酸含量的共同影响。
总体来说,当鱼体摄入能量不足时,鱼体摄入的脂肪主要用于脂肪分解,此时脂肪分解相关基因表达上升,同时,脂肪合成相关基因表达下降,脂肪合成能力下降。当鱼体摄入能量充足时,脂肪分解相关基因表达就会下降,脂肪合成相关基因表达上升,达到稳定的状态。而在用豆油替代后,各脂肪代谢相关的基因表达就会受到饲料脂肪酸组成变化的影响而表现出不同的变化趋势。
4 结语当饲料主要脂肪源为鱼油时,鱼体生长性能随饲料脂肪水平升高而具有升高趋势。当饲料中脂肪水平为12%~16%时,获得最优的鱼体生长性能。当饲料主要脂肪源为豆油时,大于16%的豆油会抑制鱼体生长。大菱鲆脂肪代谢显著受饲料脂肪水平和脂肪来源的影响。本研究为大菱鲆饲料中脂肪水平及脂肪源的合理选择提供了一定的理论依据。
| [1] |
Watanabe T. Strategies for further development of aquatic feeds[J]. Fisheries Science, 2002, 68(2): 242-252.
(  0) 0) |
| [2] |
Watanabe Y G. An organ culture study on the site of determination of ACTH and LH cells in the rat adenohypophysis[J]. Cell and Tissue Research, 1982, 227(2): 267-275. DOI:10.1007/BF00210885
(  0) 0) |
| [3] |
Turchini G M, Torstensen B E, Ng W, et al. Fish oil replacement in finfish nutrition[J]. Reviews in Aquaculture, 2009, 1(1): 10-57.
(  0) 0) |
| [4] |
Ghioni C, Tocher D R, Bell M V, et al. Low C 18 to C 20 fatty acid elongase activity and limited conversion of stearidonic acid, 18: 4 (n-3), to eicosapentaenoic acid, 20: 5 (n-3), in a cell line from the turbot, Scophthalmus maximus[J]. Biochimica et Biophysica Acta (BBA)-Molecular and Cell Biology of Lipids, 1999, 1437(2): 170-181.
(  0) 0) |
| [5] |
Sargent J R, Tacon A G J. Development of farmed fish: A nutritionally necessary alternative to meat[J]. Proceedings of the Nutrition Society, 1999, 58(2): 377-383. DOI:10.1017/S0029665199001366
(  0) 0) |
| [6] |
Torstensen B E, Bell J G, Rosenlund G, et al. Tailoring of Atlantic salmon (Salmo salar L.) flesh lipid composition and sensory quality by replacing fish oil with a vegetable oil blend[J]. Journal of Agricultural and Food Chemistry, 2005, 53(26): 10166-10178. DOI:10.1021/jf051308i
(  0) 0) |
| [7] |
刘兴旺, 艾庆辉, 麦康森. 大豆浓缩蛋白替代鱼粉对大菱鲆摄食, 生长及体组成的影响[J]. 水产学报, 2015, 38(1): 91. Liu Xing-Wang, Ai Qing-Hui, Mai Kang-Sen. Effects of replacing fish meal with soy protein concentrate on feed intake and growth of turbot(Scophthalmus maximus L.)[J]. Journalof Fisheries of China, 2015, 38(1): 91. (  0) 0) |
| [8] |
Livak K J, Schmittgen T D. Analysis of relative gene expression data using real-time quantitative PCR and the 2-△△Ct method[J]. Methods, 2001, 25(4): 402-408. DOI:10.1006/meth.2001.1262
(  0) 0) |
| [9] |
Peng M, Xu W, Mai K, et al. Growth performance, lipid deposition and hepatic lipid metabolism related gene expression in juvenile turbot (Scophthalmus maximus L.)fed diets with various fish oil substitution levels by soybean oil[J]. Aquaculture, 2014, 433: 442-449. DOI:10.1016/j.aquaculture.2014.07.005
(  0) 0) |
| [10] |
Regost C, Arzel J, Robin J, et al. Total replacement of fish oil by soybean or linseed oil with a return to fish oil in turbot (Psetta maxima): 1. Growth performance, flesh fatty acid profile, and lipid metabolism[J]. Aquaculture, 2003, 217(1): 465-482.
(  0) 0) |
| [11] |
Xu S, Wang S, Zhang L, et al. Effects of replacement of dietary fish oil with soybean oil on growth performance and tissue fatty acid composition in marine herbivorous teleost Siganus canaliculatus[J]. Aquaculture Research, 2012, 43(9): 1276-1286. DOI:10.1111/j.1365-2109.2011.02931.x
(  0) 0) |
| [12] |
Trushenski J, Schwarz M, Lewis H, et al. Effect of replacing dietary fish oil with soybean oil on production performance and fillet lipid and fatty acid composition of juvenile cobia Rachycentron canadum[J]. Aquaculture Nutrition, 2011, 17(2): e437-e447.
(  0) 0) |
| [13] |
Figueiredo‐Silva A, Rocha E, Dias J, et al. Partial replacement of fish oil by soybean oil on lipid distribution and liver histology in European sea bass (Dicentrarchus labrax) and rainbow trout (Oncorhynchus mykiss) juveniles[J]. Aquaculture Nutrition, 2005, 11(2): 147-155.
(  0) 0) |
| [14] |
Regost C, Arzel J, Cardinal M, et al. Dietary lipid level, hepatic lipogenesis and flesh quality in turbot (Psetta maxima)[J]. Aquaculture, 2001, 193(3): 291-309.
(  0) 0) |
| [15] |
Peres H, Oliva-Teles A. Effect of dietary lipid level on growth performance and feed utilization by European sea bass juveniles (Dicentrarchus labrax)[J]. Aquaculture, 1999, 179(1): 325-334.
(  0) 0) |
| [16] |
Vergara J M, Robainà L, Izquierdo M, et al. Protein sparing effect of lipids in diets for fingerlings of gilthead sea bream[J]. Fisheries Science, 1996, 62(4): 624-628.
(  0) 0) |
| [17] |
Pei Z, Xie S, Lei W, et al. Comparative study on the effect of dietary lipid level on growth and feed utilization for gibel carp (Carassius auratus gibelio) and Chinese longsnout catfish (Leiocassislongirostris Günther)[J]. Aquaculture Nutrition, 2004, 10(4): 209-216.
(  0) 0) |
| [18] |
Wang J T, Liu Y J, Tian L X, et al. Effect of dietary lipid level on growth performance, lipid deposition, hepatic lipogenesis in juvenile cobia (Rachycentron canadum)[J]. Aquaculture, 2005, 249(1): 439-447.
(  0) 0) |
| [19] |
Hardy R W, Scott T M, Harrell L W. Replacement of herring oil with menhaden oil, soybean oil, or tallow in the diets of Atlantic salmon raised in marine net-pens[J]. Aquaculture, 1987, 65(3): 267-277.
(  0) 0) |
| [20] |
Greene D H S, Selivonchick D P. Effects of dietary vegetable, animal and marine lipids on muscle lipid and hematology of rainbow trout (Oncorhynchus mykiss)[J]. Aquaculture, 1990, 89(2): 165-182. DOI:10.1016/0044-8486(90)90308-A
(  0) 0) |
| [21] |
Arzel J, Lopez F X M, Métailler R, et al. Effect of dietary lipid on growth performance and body composition of brown trout (Salmo trutta) reared in seawater[J]. Aquaculture, 1994, 123(3-4): 361-375. DOI:10.1016/0044-8486(94)90071-X
(  0) 0) |
| [22] |
Gélineau A, Corraze G, Boujard T, et al. Relation between dietary lipid level and voluntary feed intake, growth, nutrient gain, lipid deposition and hepatic lipogenesis in rainbow trout[J]. Reproduction Nutrition Development, 2001, 41(6): 487-503. DOI:10.1051/rnd:2001103
(  0) 0) |
| [23] |
Bell J G, Tocher D R, MacDonald F M, et al. Effects of diets rich in linoleic (18: 2n-6) and α-linolenic (18: 3n-3) acids on the growth, lipid class and fatty acid compositions and eicosanoid production in juvenile turbot (Scophthalmus maximus L.)[J]. Fish Physiology and Biochemistr, 1994, 13(2): 105-118.
(  0) 0) |
| [24] |
Takeuchi T, Watanabe T. Effect of excess amounts of essential fatty acids on growth of rainbow trout[J]. Bulletin of the Japanese Society of Scientific Fisheries, 1979, 45(12): 1517-1519. DOI:10.2331/suisan.45.1517
(  0) 0) |
| [25] |
Tocher D R, Bell J G, Dick J R, et al. Effects of dietary vegetable oil on Atlantic salmon hepatocyte fatty acid desaturation and liver fatty acid compositions[J]. Lipids, 2003, 38(7): 723-732. DOI:10.1007/s11745-003-1120-y
(  0) 0) |
| [26] |
Sun S, Ye J, Chen J, et al. Effect of dietary fish oil replacement by rapeseed oil on the growth, fatty acid composition and serum non-specific immunity response of fingerling black carp, Mylopharyngodon piceus[J]. Aquaculture Nutrition, 2011, 17(4): 441-450. DOI:10.1111/j.1365-2095.2010.00822.x
(  0) 0) |
| [27] |
Benítez-Dorta V, Caballero M J, Izquierdo M, et al. Total substitution of fish oil by vegetable oils in Senegalese sole (Solea senegalensis) diets: effects on fish performance, biochemical composition, and expression of some glucocorticoid receptor-related genes[J]. Fish Physiology and Biochemistry, 2013, 39(2): 335-349.
(  0) 0) |
| [28] |
Saxena U, Klein M G, Vanni T M, et al. Lipoprotein lipase increases low density lipoprotein retention by subendothelial cell matrix[J]. The Journal of Clinical Investigation, 1992, 89(2): 373-380. DOI:10.1172/JCI115595
(  0) 0) |
| [29] |
Madsen L, Rustan A C, Vaagenes H, et al. Eicosapentaenoic and docosahexaenoic acid affect mitochondrial and peroxisomal fatty acid oxidation in relation to substrate preference[J]. Lipids, 1999, 34(9): 951-963. DOI:10.1007/s11745-999-0445-x
(  0) 0) |
| [30] |
Petrescu A D, Huang H, Martin G G, et al. Impact of L-FABP and glucose on polyunsaturated fatty acid Induction of PPARα-regulated β-oxidative enzymes[J]. American Journal of Physiology-Gastrointestinal and Liver Physiology, 2013, 304(3): 241-256. DOI:10.1152/ajpgi.00334.2012
(  0) 0) |
| [31] |
Finck B N, Kelly D P. PGC-1 coactivators: Inducible regulators of energy metabolism in health and disease[J]. The Journal of Clinical Investigation, 2006, 116(3): 615-622. DOI:10.1172/JCI27794
(  0) 0) |
| [32] |
Goto T, Lee J Y, Teraminami A, et al. Activation of peroxisome proliferator-activated receptor-alpha stimulates both differentiation and fatty acid oxidation in adipocytes[J]. Journal of Lipid Research, 2011, 52(5): 873-884. DOI:10.1194/jlr.M011320
(  0) 0) |
| [33] |
彭墨.饲料脂肪水平和脂肪酸组成对大菱鲆幼鱼脂沉积的影响[D].青岛: 中国海洋大学, 2014. Peng Mo. The effects of dietary lipid level and fatty acids composition on lipid deposition in juvenile turbot (Scophthalmus maximus L.)[D]. Qingdao: Ocean University of China, 2014. http://d.wanfangdata.com.cn/thesis/D548420 (  0) 0) |
| [34] |
Zechner R. The tissue-specific expression of lipoprotein lipase: implications for energy and lipoprotein metabolism[J]. Current Opinion In lipidology, 1997, 8(2): 77-88. DOI:10.1097/00041433-199704000-00005
(  0) 0) |
| [35] |
Sampath H, Ntambi J M. Polyunsaturated fatty acid regulation of genes of lipid metabolism[J]. Annual Review of Nutrition, 2005, 25(1): 317-340. DOI:10.1146/annurev.nutr.25.051804.101917
(  0) 0) |
| [36] |
Schlegel A, Stainier D Y R. Microsomal triglyceride transfer protein is required for yolk lipid utilization and absorption of dietary lipids in zebrafish larvae[J]. Biochemistry, 2006, 45(51): 15179-15187. DOI:10.1021/bi0619268
(  0) 0) |
| [37] |
Jump D B, Clarke S D, Thelen A, et al. Dietary polyunsaturated fatty acid regulation of gene transcription[J]. Progress in Lipid Research, 1996, 35(3): 227-241. DOI:10.1016/S0163-7827(96)00007-0
(  0) 0) |
| [38] |
Jump D B. Fatty acid regulation of gene transcription[J]. Critical Reviews in Clinical Laboratory Sciences, 2004, 41(1): 41-78. DOI:10.1080/10408360490278341
(  0) 0) |
| [39] |
Zhou Y, Song Y, Zhou H, et al. Linoleic acid activates GPR40/FFA1 and phospholipase C to increase[Ca2+]i release and insulin secretion in islet beta-cells[J]. Chinese Medical Sciences Journal, 2012, 27(1): 18-23. DOI:10.1016/S1001-9294(12)60017-0
(  0) 0) |
| [40] |
Shalev A, Siegrist-Kaiser C A, Yen P M, et al. The peroxisome proliferator-activated receptor alpha is a phosphoprotein: Regulation by insulin[J]. Endocrinology, 1996, 137(10): 4499-4502. DOI:10.1210/endo.137.10.8828512
(  0) 0) |
| [41] |
Cruz-Garcia L, Minghetti M, Navarro I, et al. Molecular cloning, tissue expression and regulation of liver X receptor (LXR) transcription factors of Atlantic salmon (Salmo salar) and rainbow trout (Oncorhynchus mykiss)[J]. Comparative Biochemistry and Physiology Part B: Biochemistry and Molecular Biology, 2009, 153(1): 81-88. DOI:10.1016/j.cbpb.2009.02.001
(  0) 0) |
| [42] |
Cruz-Garcia L, Sánchez-Gurmaches J, Gutiérrez J, et al. Regulation of LXR by fatty acids, insulin, growth hormone and tumor necrosis factor-α in rainbow trout myocytes[J]. Comparative Biochemistry and Physiology Part A: Molecular & Integrative Physiology, 2011, 160(2): 125-136.
(  0) 0) |
| [43] |
Yu Y, Correll P H, Heuvel J P V. Conjugated linoleic acid decreases production of pro-inflammatory products in macrophages: Evidence for a PPARγ-dependent mechanism[J]. Biochimica et Biophysica Acta (BBA)-Molecular and Cell Biology of Lipids, 2002, 1581(3): 89-99.
(  0) 0) |
| [44] |
Schadinger S E, Bucher N L R, Schreiber B M, et al. PPARγ2 regulates lipogenesis and lipid accumulation in steatotic hepatocytes[J]. American Journal of Physiology-Endocrinology and Metabolism, 2005, 288(6): 1195-1205. DOI:10.1152/ajpendo.00513.2004
(  0) 0) |
| [45] |
Matsusue K, Kusakabe T, Noguchi T, et al. Hepatic steatosis in leptin-deficient mice is promoted by the PPARγ target gene Fsp27[J]. Cell Metabolism, 2008, 7(4): 302-311.
(  0) 0) |
| [46] |
Morán-Salvador E, López-Parra M, García-Alonso V, et al. Role for PPARγ in obesity-induced hepatic steatosis as determined by hepatocyte-and macrophage-specific conditional knockouts[J]. The FASEB Journal, 2011, 25(8): 2538-2550. DOI:10.1096/fj.10-173716
(  0) 0) |
| [47] |
Escobar E L O, Gomes‐Marcondes M C C, Carvalho H F. Dietary fatty acid quality affects AR and PPARγ levels and prostate growth[J]. The Prostate, 2009, 69(5): 548-558. DOI:10.1002/pros.20905
(  0) 0) |
 2020, Vol. 50
2020, Vol. 50


