2. 中国科学院青岛生物能源与过程研究所,环境资源化与水回用研究组,山东 青岛 266101;
3. 中国海洋大学海洋环境与生态教育部重点实验室,山东 青岛 266100;
4. 中国科学院青岛生物能源与过程研究所,青岛市功能膜材料与膜技术重点实验室,山东 青岛 266101
含甘油高盐废水广泛存在于环氧氯丙烷(ECH)生产、生物质精炼等行业,由于其COD含量和盐含量都较高,难以生化处理,因此属于难降解有机废水。其中,环氧氯丙烷生产所产生的该种废水的处置是目前石化行业面临的突出环保问题[1]。
环氧氯丙烷是一种精细化工产品,可以作为环氧树脂、纺织品、离子交换树脂、某些表面活性剂、医药、农药的生产原料[2]。2012年,全球环氧氯丙烷的产量提高到约9×109 t[3]。
甘油法生产环氧氯丙烷工艺产生的废水主要由高浓度无机盐(8%~16%),和有机化合物(COD15~40 g/L)组成[4],其中有机物主要是甘油。废水中无机盐含量高,一般不能直接生物处理,需要预处理或使用物理化学方法处理:如陈新德[5]用蒸发除盐-Fenton法,帅晓丹等[4, 6]用催化湿式过氧化物氧化法,胡华斌等[7]使用多效蒸发、Fenton催化氧化和生物工艺处理环氧氯丙烷生产废水。然而,多数的高级氧化处理工艺在处理过程中都需要外加试剂或者引入新杂质,既增加了成本,又造成了二次污染。
电渗析(Electrodialysis, ED)是一种以电能作为驱动力的电化学过程。在电位差的作用下,溶液中的阴阳离子穿过阴阳离子交换膜从原溶液迁移到另一种溶液中,达到分离的目的。解利昕等[8]采用电渗析-好氧生物联合法处理环氧氯丙烷废水。经过絮凝沉淀和电渗析脱盐的废水,电导率由36.5 mS/cm降到3.29 mS/cm,COD降至100 mg/L以下。然而,好氧生物处理过程中会产生大量污泥,而污泥处置会增加处理成本。厌氧生物处理技术由于将大部分有机碳转化为甲烷,使污泥产生量大为减少。另外,产生的甲烷可以用于供热或发电,实现废水的资源化利用。厌氧膜生物反应器(Anaerobic Membrane Bioreactor, AnMBR)综合了厌氧生物处理与膜生物反应器的特点,能够提高微生物截留率,提升出水水质,近年来在水处理领域得到了广泛的关注。因此,本研究采用电渗析-厌氧膜生物反应器工艺对含甘油高盐废水进行处理。实验研究了电渗析的脱盐效率,AnMBR对甘油的转化与降解效率,以及盐浓度冲击对AnMBR稳定性的影响。本研究为ED-AnMBR处理含甘油高盐废水提供了理论和优化指导。
1 实验部分 1.1 实验材料硫酸钠、氯化钙、甘油、葡萄糖、氯化铵、磷酸氢二钾均为分析纯,由国药集团化学试剂有限公司提供。
实验所用非均相阳离子交换膜(CM)和阴离子交换膜(AM)由上化水处理材料有限公司提供,参数如表 1所示。电渗析装置单张离子交换膜有效面积为134.67 cm2(20.1 cm×6.7 cm)。
|
|
表 1 离子交换膜特征 Table 1 Characteristic of ion exchange membranes |
电渗析膜堆由21张膜组成,包括10张阴离子交换膜和11张阳离子交换膜。如图 1(a)所示,淡化室(D室)和浓缩室(C室)交替形成堆叠。靠近阳极室和阴极室的两个隔室为“保护室”,用来防止在电极上沉积钙。电极室加入0.5 L 0.1 mol·L-1 Na2SO4溶液,保护室加0.5 L 0.1 mol·L-1 NaCl溶液。D室中加入0.5 L合成含甘油高盐废水,组成与山东某环氧氯丙烷企业生产废水主要物质相同,为12.34 g/L甘油(COD为15 000 mg/L)和150 g/L CaCl2。自来水加入C室,避免纯水电阻过大的情况。在实验中使用3.5A的恒定电流(电流密度260 A/m2)。C室和D室的流速设定为0.42 L/min。电渗析脱盐实验前,C室和D室都使用超纯水预运行半小时以确保装置无泄漏。由于电渗析膜堆、管道死体积中超纯水的稀释作用,电渗析实验中D室甘油浓度降到了8.0 g/L,电导率降到了114 mS/cm。
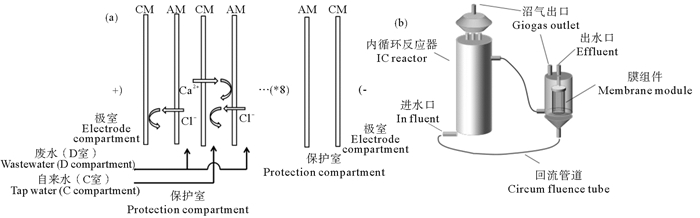
|
图 1 电渗析装置和厌氧膜生物反应器示意图 Fig. 1 Configuration of ED and AnMBR |
厌氧膜生物反应器构造如图 1(b)所示:反应器采用外置式膜组件,主体生物反应器为内循环反应器(IC),有效容积10 L。膜组件采用厦门鲲扬膜科技有限公司生产的微滤膜,孔径0.2 μm,整个膜组件表面积0.093 2 m2。反应器运行期间采用蠕动泵控制流速,保持出水流量7 L/m2·h(LMH)。且每出水0.5 h,对膜进行反洗,反洗持续2 min,流量为7 LMH,与出水相同。出水时采用真空压力表测量跨膜压差。反应器采用半连续方式运行,为了方便研究甘油在AnMBR下的降解效率,反应器进水中不含CaCl2。在实验1~15 d为污泥稳定期,以葡萄糖作为底物,水力停留时间(HRT)为5 d,有机负荷(OLR)为1.5 g/L·d,化学需氧量(COD)为7 500 mg/L。第16~23天为底物变化阶段,HRT=5 d,OLR=0.75 g/L·d,COD=3 750 mg/L。此阶段以葡萄糖和甘油作为混合底物,葡萄糖/甘油混合比例每两天调整一次,分别为4:1,2:3,3:2,1:4。第24~38天,以甘油作为底物,HRT=5 d,OLR=0.75 g/L·d。整个过程按COD:N:P=200:5:1的比例添加氯化铵和磷酸氢二钾,为微生物成长提供必要的N、P元素。当每阶段结束时,对膜组件进行清洗。清洗时首先用清水冲去表面污泥,再将膜组件浸入pH=10的0.01 mol·L-1次氯酸钠溶液中处理30 min。
为研究CaCl2浓度与COD厌氧降解和转化关系,进行了批处理实验。实验总共分为8组,采用250 mL培养瓶,每瓶加入80 mL污泥,20 mL不同盐度的含油的废水。污泥在装瓶之前在厌氧环境下放置5 d以上以消耗底物。每组小瓶初始COD浓度均为40 g/L,分别收到不同盐度的冲击,初始CaCl2浓度分别为0,2%,4%,6%,8%,10%,12%,15%,每组设置3个平行实验。装瓶完毕后,用N2曝气2 min创造厌氧环境,封口,在37 ℃摇床中进行培养,每天每瓶取样2 mL。
1.3 测量方法电导率和pH值采用电导率仪(FG3-ELK,梅特勒-托利多国际有限公司)和pH计(FG2,梅特勒-托利多国际有限公司)测量。甘油与挥发性有机酸(VFA)通过装有BIO-RID柱的液相色谱仪(安捷伦N2700,美国)。流动相是0.01 mol·L-1 H2SO4,流速0.6 mL/min。COD采用国家标准方法重铬酸钾法(GB11914-89)检测。沼气分析使用固定式二合一气体(CH4,CO2)检测仪(深圳市科尔诺电子科技有限公司,中国)检测。体积采用排饱和碳酸氢钠溶液测量。
1.4 计算方法电渗析过程的能耗根据公式
| $ E = \int U I{\rm{d}}t $ |
计算。其中:E为电渗析过程的能耗(J);U为电渗析膜堆两侧电压(V);I为电渗析电流(A);t为运行时间(s)。
电流效率根据公式
| $ \eta = \frac{{zcV{\rm F}}}{{nIt}} \times 100\% $ |
计算。其中:η为电流效率(%);z为离子电荷量;c为离子浓度(mol/L);V为体积(L);F为法拉第常数(C/moL);n为电渗析膜对数;I为电流(A);t为运行时间(s)。
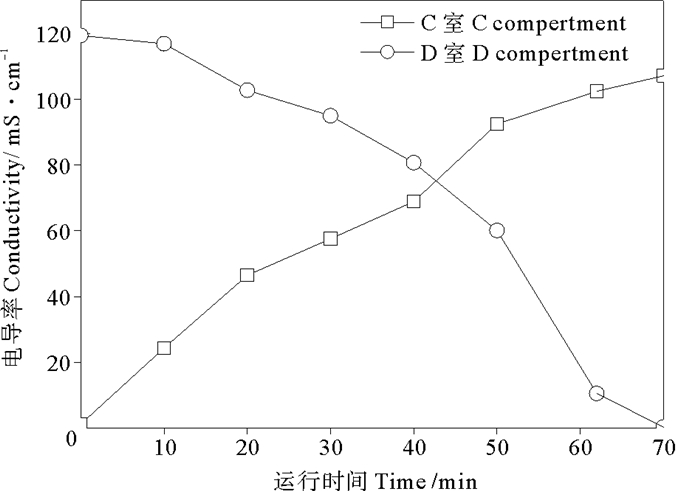
2 结果与讨论 2.1 电渗析脱除CaCl2效率与能耗电渗析处理废水取得了良好的脱盐效果。电渗析运行70 min后,D室电导率由119.4 mS/cm下降至0.321 mS/cm,脱盐率达到99%以上(见图 2)。在脱盐的同时,D室和C室的水体积也在发生变化,D室中的水在电渗析过程中会向C室迁移,造成甘油在D室中浓缩,浓度由8.0 g/L增大到11.24 g/L(见图 3)。电渗析过程在恒流3.5A条件下运行,电压也稳定在19.4~21 V范围内(见表 2),该过程平均能耗为616 kJ/L,电流效率为91.4%。电流效率高,其原因在于进水浓度高,部分离子可以在浓度梯度下进行扩散。
|
图 2 电渗析过程中电导率变化 Fig. 2 Conductivityin ED process |

|
图 3 渗析过程中甘油浓度与体积变化 Fig. 3 Glycerol concentration and volume changes in electrodialysis |
|
|
表 2 电渗析过程中电压与电流变化 Table 2 Voltage and current change in electrodialysis |
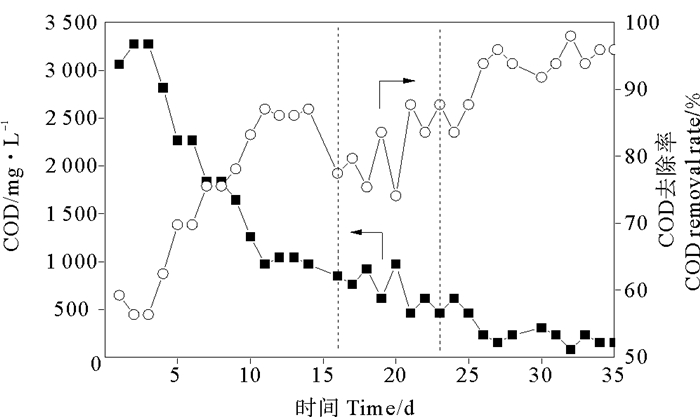
如图 4,反应器运行初始1~3 d,出水COD在3 000 mg/L以上,去除率仅56%。反应器运行第3~10 d,出水COD浓度逐渐下降,COD去除率逐渐升高。在第11天,COD去除率就达到90%。在第16~23 d,底物由葡萄糖逐渐变为甘油,此时COD去除率略有下降,但是很快恢复。运行30 d后,AnMBR出水水质保持在250 mg/L以下,达到了95%以上COD去除效果。
|
图 4 AnMBR出水COD浓度及COD去除率 Fig. 4 Effluent COD concentration and COD removal in AnMBR |
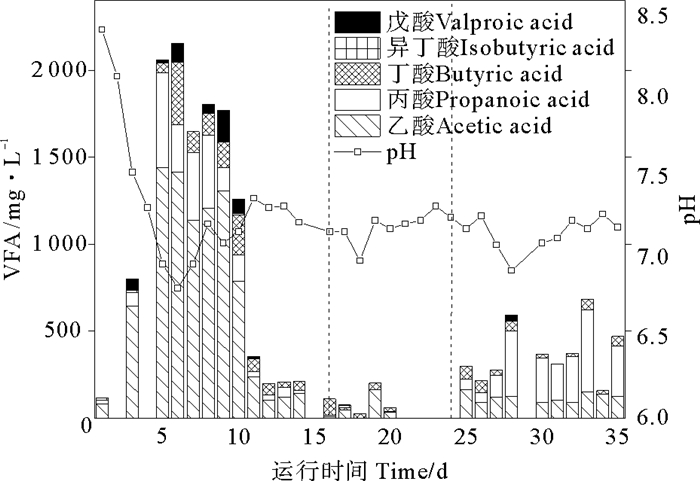
反应器运行过程中,AnMBR系统pH基本保持7.00以上(见图 5),表明反应器运行期间没有出现严重酸化现象,一直保持厌氧微生物适宜生存的环境。反应器启动期间出水中VFA成分和浓度数据表明,造成pH波动的原因主要是由于VFA的积累和利用。在反应器刚开始启动的1~5 d,反应器中VFA浓度不断上升,最高达到大约2 200 mg/L。此时正对应反应器pH快速下降的过程。此阶段反应器受到负荷冲击,甲烷菌的活性下降,因此VFA略有积累。此时反应器以葡萄糖为底物,VFA种类以乙酸、丙酸、丁酸等小分子酸为主,尤其是乙酸含量,占据VFA产量的65%以上。第10天之后,VFA浓度降低至400 mg/L以下,表明甲烷菌活性恢复,相应COD去除率升高,达到85%以上。25天后完全以甘油为底物,反应器内VFA浓度上升至300 mg/L左右,其原因在于底物转变造成微生物不适应,代谢不彻底。在第25~35天内,VFA含量基本在200~500 mg/L之间波动,表明底物有葡萄糖转变为甘油对污水处理效率和甲烷菌活性影响不大。甘油为底物时,有机酸产物以丙酸为主,乙酸丁酸的比例相对降低。这与丙酸是甘油厌氧降解的主要产物有关。据报道,厌氧条件下甘油先转化为二羟基丙酮。随后二羟基丙酮在厌氧条件下被氧化,转化为磷酸烯醇丙酮酸盐,最终转化为丙酸等VFA[9]。VFA尤其是丙酸的积累会成为厌氧消化的限速步骤,抑制产甲烷菌活性[10-11]。
|
图 5 AnMBR中pH和VFA成分和浓度变化 Fig. 5 pH and VFA changes in AnMBR |
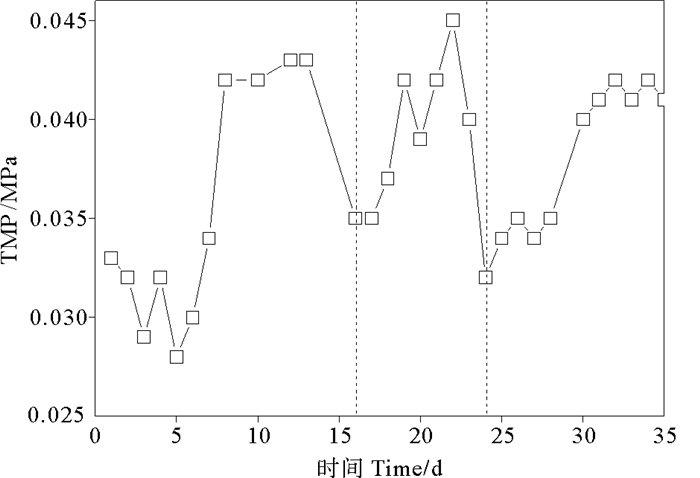
在反应器运行期间,跨膜压差(TMP)变化如图 6所示。反应器运行初期(第5~8天)跨膜压差上升很快,第8天即达到0.040 MPa,并在随后第8~11天内达到稳定在0.040~0.043 MPa。这个规律符合一般MBR反应器中的膜污染规律,其原因在于膜污染有3个阶段[12-13]:(1)初始污染阶段:小颗粒物质附着膜表面,造成膜孔堵塞。该过程膜通量降低迅速,跨膜压快速升高。(2)缓慢污染阶段:膜表面不断吸附悬浮固体,并形成滤饼层。此阶段跨膜压上升较慢。(3)跨膜压快速上升阶段:此阶段滤饼层被压实,膜污染迅速增加。实验在第16天和第24天对膜进行离线清洗,清洗时膜污染达到第二阶段尚未进行第三阶段。在化学清洗后,跨膜压差分别从0.043和0.040 MPa恢复到0.035和0.032 MPa。实验结果证明,化学清洗能有效控制AnMBR膜的污染,降低跨膜压差。
|
图 6 AnMBR跨膜压差变化 Fig. 6 TMP changes in AnMBR |
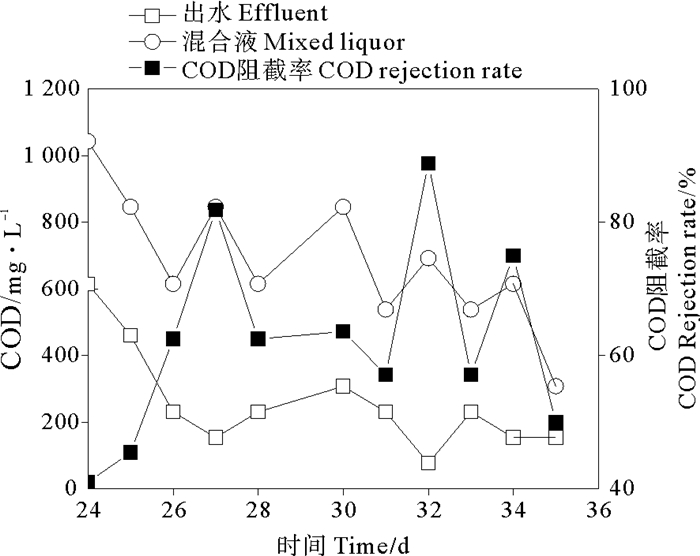
以甘油为底物的AnMBR反应器内部混合液COD与透过液的COD浓度进行比较,其结果如图 7所示。反应器内部溶解性COD浓度从1 043 mg/L降至307 mg/L,与此同时,膜透过液的溶解性COD浓度从615 mg/L降至153 mg/L。说明膜对溶解性COD也有截留作用,其截留率为41%~81%。
|
图 7 AnMBR第24~35天内反应器中混合液溶解性COD与膜透过液COD比较 Fig. 7 Comparison of soluble COD and effluent COD on day 24~35 in AnMBR |
除此以外,AnMBR处理有机废水的优势还在于有机物资源化,即在污水处理的同时将有机物转化为甲烷。对AnMBR运行期间收集的沼气成分进行分析,以葡萄糖为底物时,其CH4与CO2分别占78.30%和21.70%,而以甘油为底物时,CH4与CO2分别占80.42%,19.58%。这说明在AnMBR系统中,甲烷比例高于58%的理论计算数值。在甘油为底物时,AnMBR的比产甲烷速率平均为0.252 L CH4/g甘油。该值与Hutnan等[14]报道的未经酸化的粗甘油比产甲烷率0.328 L/gCOD以及Vlassis等[15]采用CSTR反应器降解甘油时比产甲烷速率0.3 L CH4/gCOD都略低。说明部分有机物仍存在于反应器内部参与污泥自生生长。
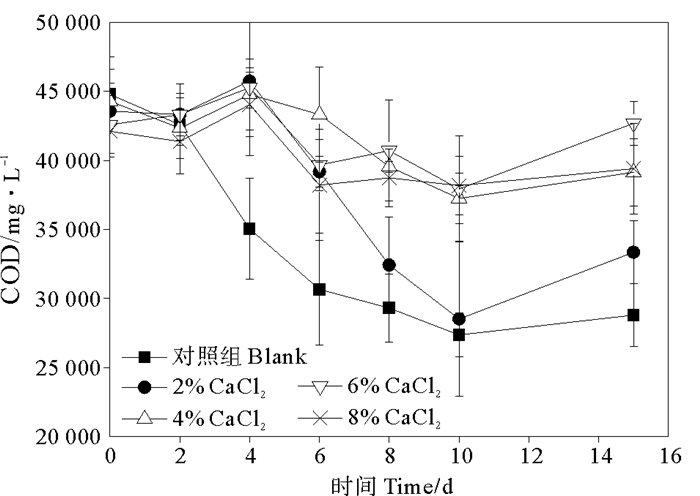
2.3 CaCl2浓度与COD厌氧降解和转化关系在8组不同盐浓度的批处理小瓶实验中,COD浓度变化如图 8所示:在高有机负荷状态下,对照组中COD在1~10 d内快速下降,但是第10天下降速度逐渐减缓,COD去除率达39%。这主要是由于微生物酸化作用降低了系统pH,因此微生物活性降低。在2%盐度的实验组中,COD在4天后才迅速下降,同样在第10天达到稳定,COD去除35%。在4%的盐度及以上盐度中,COD只有稍许下降,去除率只有不到20%。在4%盐度以下,厌氧污泥仍然具有处理COD降解能力。但是在高盐度(6%以上)冲击下,厌氧污泥几乎丧失了处理能力。因此,进入生物处理的含盐废水浓度不宜高于4%。
|
图 8 不同CaCl2浓度下COD浓度变化 Fig. 8 COD concentration changes in different CaCl2 concentration |
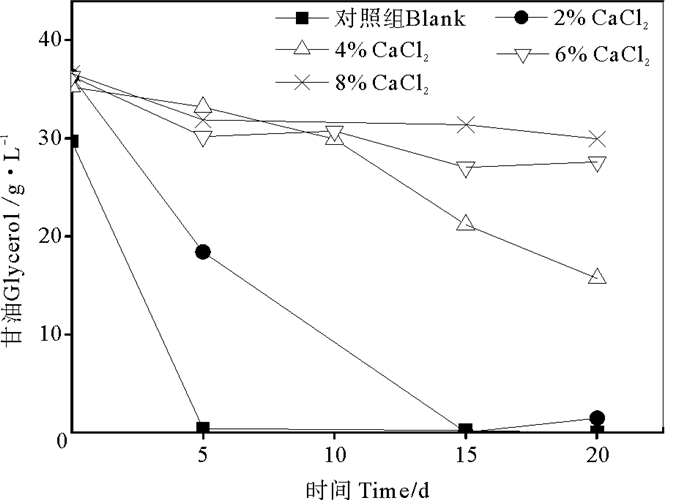
由图 9所示,通过液相色谱对瓶中甘油含量进行分析,发现在对照组中甘油成分迅速下降,5天内即已完全降解,而在盐度2%条件下,甘油降解的过程需要15天。在4%条件下,甘油20天内降解55%。而对于6%盐度以上的条件,甘油只降解了24%。另外,液相色谱数据显示,在甘油减少的过程中,有其他醇类物质生成。根据Biebl等[16]的报道,甘油可能在1,3-丙二醇脱氢酶的作用下,在厌氧环境中首先被还原,生成3-羟基丙醛,然后转化为1,3-丙二醇。
|
图 9 不同CaCl2浓度下甘油浓度 Fig. 9 Glycerol concentration changes in different CaCl2 concentration |
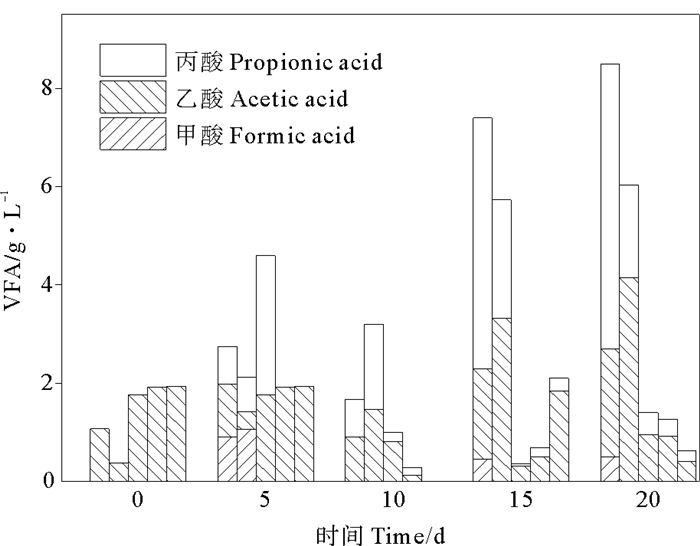
图 10显示了CaCl2浓度与VFA成分和浓度的变化关系。通过VFA成分和浓度的分析发现,在实验最初只有乙酸存在于原始污泥中。在加入甘油之后,有机酸浓度和种类都有增加。在实验第5天,各组乙酸浓度基本保持不变,对照组和2%盐度实验组中出现甲酸和丙酸,4%盐度实验组中只出现了丙酸。随着时间增加,在对照组和2%盐度实验组中VFA不断积累,主要包括甲酸、乙酸和丙酸,并且丙酸的数量最多。这个规律符合之前的报道[17]。当处理甘油有机负荷过高时,VFA尤其是丙酸的降解会成为厌氧消化的限速步骤,抑制产甲烷菌活性。因此,反应器需要控制盐浓度和有机负荷以提高甲烷的产率。
|
(当天数据从左至右依次是空白组,2%,4%,6%,8%盐度实验组。From left to right in order of blank, 2%, 4%, 6%, 8% group for each day. ) 图 10 不同CaCl2浓度下VFA成分和浓度变化关系图 Fig. 10 VFA concentration changes in different CaCl2 concentration |
经过CaCl2浓度与COD厌氧降解和转化实验发现,厌氧降解甘油的过程适宜在低盐度条件下进行,如果受到4%以下盐度冲击,仍然能够在一定时间内恢复处理效果。而更高盐度冲击较难恢复活性。因此,电渗析工艺作为厌氧生物处理的前处理,需要保证处理盐度在4%以内。
3 结语本研究表明,电渗析-AnMBR集成工艺可以高效处理高盐高COD含量的模拟环氧氯丙烷生产废水。在电渗析过程中,CaCl2的脱除效率达到99%。AnMBR工艺对甘油进行厌氧降解时,达到95%以上的COD去除率。膜在COD去除中发挥了重要作用,其COD截留率为41%~81%。TMP在膜放入反应器后经历了快速上升阶段,最终稳定在0.040~0.043 MPa。AnMBR沼气中甲烷比例为78.3%,甘油比产甲烷速率0.252 L CH4/g甘油。厌氧污泥可以耐受高达2%的盐度,高于6%污泥活性受损严重。甘油厌氧降解主要产物为丙酸,盐度越高,VFA总产量及VFA中丙酸所占比例越低,说明微生物活性受到高盐环境抑制。但是高浓度丙酸被认为不利于甲烷菌生长,因此在厌氧处理甘油的过程中,要注意系统的有机负荷不宜过大,否则会造成严重的VFA积累,尤其要注意丙酸的积累。
| [1] |
Myszkowski J, Milchert E. Recovery of chloroorganic compounds from waste waters of glycerine epichlorohydrin production[J]. Polish Journal of Chemical Technology, 2001, 3(2): 17-19.
(  0) 0) |
| [2] |
Bell B M, Briggs J R, Campbell R M, et al. Glycerin as a renewable feedstock for epichlorohydrin production. The GTE process[J]. Clean-Soil Air Water, 2008, 36(8): 657-661. DOI:10.1002/clen.v36:8
(  0) 0) |
| [3] |
Almena A, Mart N M. Techno-economic analysis of the production of epichlorhydrin from glycerol[J]. Industrial & Engineering Chemistry Research, 2016, 38(12): 49-54.
(  0) 0) |
| [4] |
帅晓丹.甘油法环氧氯丙烷高盐废水处理技术研究[D].上海: 华东理工大学, 2014. Shuai X D. Treatment the High Salinity Wastewater Generated During Epichlorohydrin Synthesis with Glycerol[D]. Shanghai: East China University of Science, 2014. http://cdmd.cnki.com.cn/Article/CDMD-10251-1014255846.htm (  0) 0) |
| [5] |
陈新德. 蒸发与Fenton试剂联用处理环氧氯丙烷废水的研究[J]. 上海化工, 2012, 37(12): 1-4. Chen X D. Study on treatment of epichlorohydrin wastewater by evaporation combined with fenton reagent[J]. Shanghai Chemical Industry, 2012, 37(12): 1-4. DOI:10.3969/j.issn.1004-017X.2012.12.001 (  0) 0) |
| [6] |
帅晓丹, 曹国民, 洪芳, 等. 环氧氯丙烷生产废水的资源化处理技术[J]. 化工环保, 2013, 33(6): 518-522. Shuai X D, Cao G M, Hong F, et al. Reutilization technology of epichlorohydrin production wastewater[J]. Environmental Protection of Chemical Industry, 2013, 33(6): 518-522. DOI:10.3969/j.issn.1006-1878.2013.06.010 (  0) 0) |
| [7] |
胡华斌, 胡芳, 马永利. 环氧氯丙烷生产废水的物化-生化处理[J]. 广东化工, 2014, 41(4): 70-71. Hu H B, Hu F, Ma Y L. Physicochemical and biochemical treatment of epichlorohydrin production wastewater[J]. Guangdong Chemical Industry, 2014, 41(4): 70-71. DOI:10.3969/j.issn.1007-1865.2014.04.036 (  0) 0) |
| [8] |
解利昕, 李慧, 余海晨. 环氧氯丙烷生产过程高含盐水的处理研究[J]. 工业水处理, 2015, 35(3): 75-78. Xie L X, Li H, Yu H C. Study on the treatment of the high-salinity wastewater from epichlorohydrin production[J]. Industrial Water Treatment, 2015, 35(3): 75-78. (  0) 0) |
| [9] |
Biebl H, Menzel K, Zeng A P, et al. Microbial production of 1, 3-propanediol[J]. Appl Microbiol Biotechnol, 1999, 52(3): 289-297. DOI:10.1007/s002530051523
(  0) 0) |
| [10] |
Lawrence A W. Application of process kinetics to design of anaerobic processes[J]. Anaerobic Biological Treatment Processes, 1971, 27(105): 163-189.
(  0) 0) |
| [11] |
Viana M B, Freitas A V, Leitao R C, et al. Anaerobic digestion of crude glycerol: A review[J]. Environmental Technology Reviews, 2012, 1(1): 81-92. DOI:10.1080/09593330.2012.692723
(  0) 0) |
| [12] |
肖椿.膜生物反应器中SMP特性及对膜污染影响研究[D].南京: 南京大学, 2014. Xiao C. Study on the Characteristics of Soluble Microbial Products and Its Effect on the Membrane Fouling in Membrane Bioreactor[D]. Nanjing: Nanjing Univerisity, 2014. http://cdmd.cnki.com.cn/article/cdmd-10284-1015502929.htm (  0) 0) |
| [13] |
Ognier S, Wisniewski C, Grasmick A. Influence of macromolecule adsorption during filtration of a membrane bioreactor mixed liquor suspension[J]. Journal of Membrane Science, 2002, 209(1): 27-37. DOI:10.1016/S0376-7388(02)00123-0
(  0) 0) |
| [14] |
Hutnan M, Kolesárová N, Bodik I. Anaerobic digestion of crude glycerol as sole substrate in mixed reactor[J]. Environmental Technology, 2013, 34(13-16): 2179-2187.
(  0) 0) |
| [15] |
Vlassis T, Stamatelatou K, Antonopoulou G, et al. Methane production via anaerobic digestion of glycerol: A comparison of conventional (CSTR) and high-rate (PABR) digesters[J]. Journal of Chemical Technology & Biotechnology, 2013, 88(11): 2000-2006.
(  0) 0) |
| [16] |
Biebl H, Menzel K, Zeng A P, et al. Microbial production of 1, 3-propanediol[J]. Applied Microbiology & Biotechnology, 1999, 52(3): 289-297.
(  0) 0) |
| [17] |
Dharmadi Y, Murarka A, Gonzalez R. Anaerobic fermentation of glycerol by Escherichia coli: A new platform for metabolic engineering[J]. Biotechnology & Bioengineering, 2010, 94(5): 821-829.
(  0) 0) |
2. Waste Valorization and Water Reuse Group (WVWR), Qingdao Institute of Bioenergy and Bioprocess Technology, Chinese Academy of Sciences, Qingdao 266101, China;
3. Key Laboratory of Marine Environment and Ecology, Ministry of Education, Qingdao 266100, China;
4. Qingdao Key Laboratory of Functional Membrane Material and Membrane Technology, Qingdao Institute of Bioenergy and Bioprocess Technology, Chinese Academy of Sciences, Qingdao 266101, China
 2019, Vol. 49
2019, Vol. 49


