海草床作为近岸三大典型海洋生态系统之一,拥有极强的固碳能力,其固碳速率高达83 g·m-2·a-1,约为森林的20倍,每年的固碳总量约占海洋总固碳量的三分之一[1-2]。海草床还具有加速颗粒物沉降、吸收和封存重金属、防风固堤等重要的生态作用,以及为众多海洋动物提供产卵、育幼和索饵等优良栖息地的资源养护作用[3-4]。然而受自然环境变化和人类活动影响,自1980年以来全球范围内超过30%的海草床已完全退化,我国海草床的状况也不容乐观,海南南部、广州合浦地区及山东半岛的桑沟湾、芙蓉岛等海区的海草床退化面积超过1 300 ha[5-6]。目前海草床的退化速率达到7%·a-1,是其自然再生速率的30倍,因此仅靠海草的自然生长已无法达到海草床自然恢复的目的[7]。
种子播种法是一种适用于规模化实践的海草床修复方法,主要通过种子撒播、掩埋或经人工培养成幼苗后移栽到海区等措施达到恢复或构建海草床的目的,具有成本低、受限小,不易对供体海草床造成破坏,能够增加遗传多样性等优点[8]。种子播种法主要包括种子采集、保存和播种等环节,其中种子保存是种子播种法的关键环节。与陆生植物不同,海草属于高等水生植物,其种子的保存需要浸泡在海水中,极易出现提前萌发、活力下降等问题。休眠是种子应对外界环境变化的重要方式,有研究表明大部分的海草种子均有休眠期,但其休眠期从几周到几年不等[9-10]。因此,可以通过延长种子休眠,在维持种子活力的基础上抑制种子萌发,有效解决储存过程中种子质量下降的问题,为规模化海草床修复提供理论基础。
对陆生植物的研究显示,比较有效的延长种子休眠方法主要有高渗保存法、超低温保存法和抑制剂保存法。高渗保存法是指通过外部盐离子的添加使种子处于高渗透压的环境中,抑制种子吸收水分,从而延长种子休眠,该方法成本较低但由于离子作用易使种子失活,所以应用范围较窄[11]。超低温保存法是指将种子保存在-196 ℃的超低温环境中,从而达到延长休眠及种质保护的作用,该方法操作简单,能实现种子长期保存,但成本较高,仅适合少量种子的长期保存[12]。抑制剂保存法是指通过添加萌发抑制剂延长种子休眠,该方法操作简单、成本低,效果好,适合大批量种子的保存,是目前最常用的延长种子休眠方法,其中脱落酸(Abscisic acid, ABA)是常用的抑制剂之一[13]。
ABA是植株体内的重要激素,主要存在于胚及胚乳中,具有调节种子休眠的作用[14]。对水稻(Oryza sativa)种子的研究发现,外源添加ABA能够在保持种子活力的前提下调节种子的休眠时间,其中低浓度ABA(0~20 mg·L-1)将打破水稻种子休眠,而高浓度ABA(20~90 mg·L-1)能够延长种子休眠[13-14]。以此为基础,Hong等[15]对秋茄(Kandelia candel)的研究发现,高浓度ABA能够显著延长秋茄种子的休眠时间,其中ABA浓度为120和150 mg·L-1时延长效果显著。目前,有关外源ABA对海草种子休眠时间调节作用的研究尚未见报道,促使海草种子延长休眠的适宜ABA浓度范围亦不清楚。因海草与红树同属滨海高等植物,因此推测高浓度ABA可能促进海草种子延长休眠。
为验证该假设,本研究以我国温带海域海草优势种——鳗草(Zostera marina)为对象,分别设置浓度为0(对照)、3、15、30和300 mg·L-1的ABA处理组,通过综合分析种子休眠延长期的种子萌发率和种子活力以及去休眠时种子的再萌发率,查明外源ABA对鳗草种子延长休眠的影响,明确促进鳗草种子延长休眠的适宜ABA浓度范围;并通过各时期种子水分、可溶性糖及淀粉等内部贮存物质含量的测定与分析,弄清鳗草种子应对外源ABA作用的营养物质响应过程,以期为鳗草种质长期保存及其种子修复理论与技术提供参考。
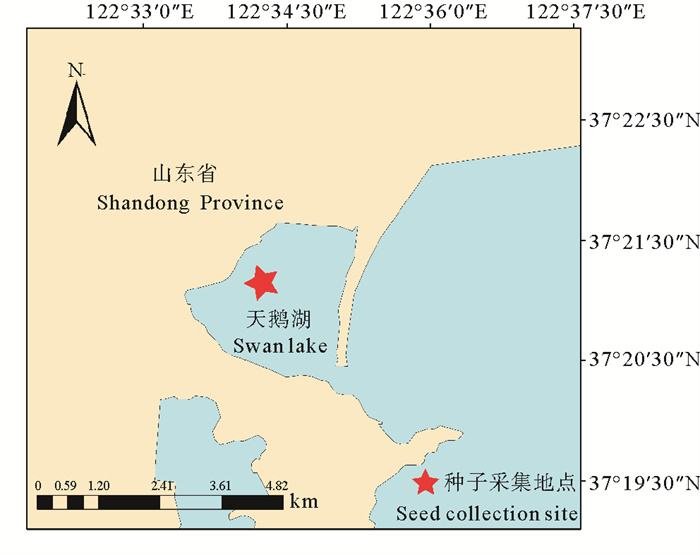
1 材料与方法 1.1 实验材料实验用鳗草种子于2019年7月采集于山东省荣成市天鹅湖海域(37°20′18″N —37°21′32″N, 122°33′18″E—122°34′45″E,见图 1)。在鳗草分布较多的区域采集生殖枝,将佛焰苞摘下后放入网目孔径为1.0 mm的尼龙网袋中,置于自然海域1个月。待种子成熟脱落后,移入处理箱中加入海水搅拌,除去上层有机碎屑及贝壳等杂质,收集至广口瓶中带回实验室,于4 ℃、盐度30的海水中保存。为减少真菌的生成,保存期间每两天换水一次。
|
图 1 种子采集地点 Fig. 1 Seed collection site |
以陆生植物及红树种子延长休眠常用的ABA浓度为基础[13-15],设置5个不同ABA浓度处理组:0(对照)、3、15、30和300 mg·L-1。将25 mg ABA粉末溶于0.5 mL甲醇,无菌水定容至20 mL配置成浓度为1 250 mg·L-1的ABA母液。通过计算,取0、2.4、12、24和240 mL ABA母液分别加入1 000、997.6、988、976和760 mL海水中配置成上述5种不同ABA浓度的海水。采用高效液相色谱法(HPLC)测定海水中的ABA浓度,确保海水中ABA的实际浓度与计算一致。
1.3 实验过程从种子中挑选颗粒饱满、纵肋清晰、褐色或墨绿色的成熟种子45 000粒,平均分为45组,分别置于500 mL烧杯中,每组为1个重复,每个处理组含9个重复。向各烧杯中添加300 mL相应ABA浓度的海水,然后随机置于光照培养箱(GXZ-0288,宁波江南仪器厂)的载物托架上,于15 ℃、黑暗条件下培养90 d。为了保证海水中ABA浓度恒定,每天以相同ABA浓度的海水对烧杯中的海水进行替换。
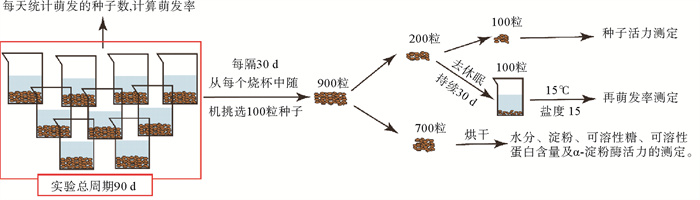
1.4 样品采集与测定各处理组的取样流程如图 2所示。实验总周期为90 d,实验期间每天对萌发的种子进行统计,计算萌发率。每隔30 d进行1次取样,取样时从每个烧杯中随机挑选100粒种子,每个处理组共计挑选900粒种子,从中随机挑选200粒,平均分成2份,分别用于种子活力及再萌发率的测定。种子活力的测定采用四唑法[16]。种子再萌发率测定时,将种子置于15 ℃、盐度15的海水中进行30 d的去休眠,每天统计萌发的种子数,计算萌发率。萌发率及种子活力的计算方法如下:
|
图 2 实验流程图 Fig. 2 Flowchart of experiment |
萌发率=萌发的种子数/种子总数×100%;
种子活力=被染色种胚数/种子总数×100%。
样品中剩余的700粒种子,用于种子内部储藏物质的测定。其中水分含量的测定采用烘干法[17],可溶性糖及淀粉含量的测定采用蒽酮法[18],可溶性蛋白含量的测定采用凯氏定氮法[19],α-淀粉酶活力的测定采用碘-淀粉比色法[20],每组样品的同一指标重复测定3次。
1.5 数据分析对所有指标进行方差齐性检验,将方差不齐的指标进行对数或开根号转换,使其满足方差齐性。然后对所有指标进行单因素方差分析(ANOVA),以P < 0.05作为显著差异水平,以P < 0.01作为极显著差异水平,利用Duncan多重比较分析组间差异。采用R语言FactoMineR包对萌发率、种子活力和再萌发率等生态学指标进行PCA分析,Corrplot包对种子的可溶性糖、淀粉和水分含量等生理学指标进行Speraman相关性分析。数据统计分析使用SPSS 25.0软件进行,分析结果使用OriginLab 2020b、R语言进行绘图。
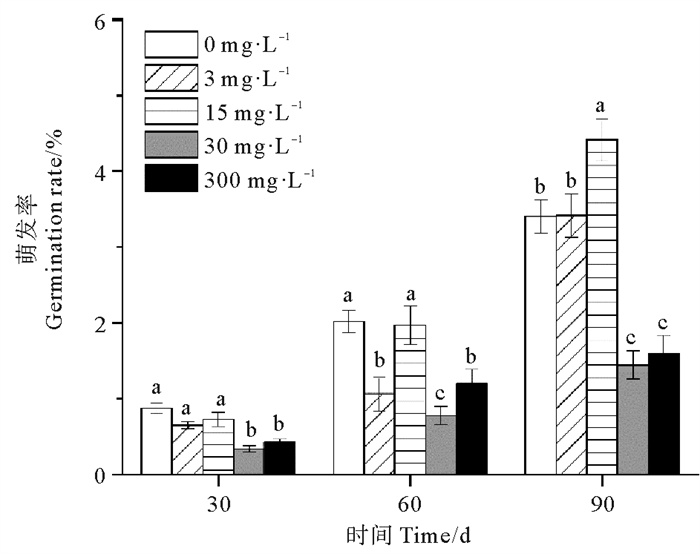
2 实验结果 2.1 休眠延长期的种子萌发率各处理组鳗草种子的累积萌发率随时间延长呈现逐渐升高趋势,至90 d时达到最大值(见图 3)。单因素方差分析表明,实验结束时,30和300 mg·L-1处理组的种子累积萌发率显著低于其它处理组,分别仅为对照组的41%和51%(P<0.05),而15 mg·L-1处理组累积萌发率最高,是对照组的1.1倍。
|
图 3 不同ABA浓度对鳗草种子萌发率的影响 Fig. 3 The effect of different ABA concentrations on the germination rate of eelgrass seed |
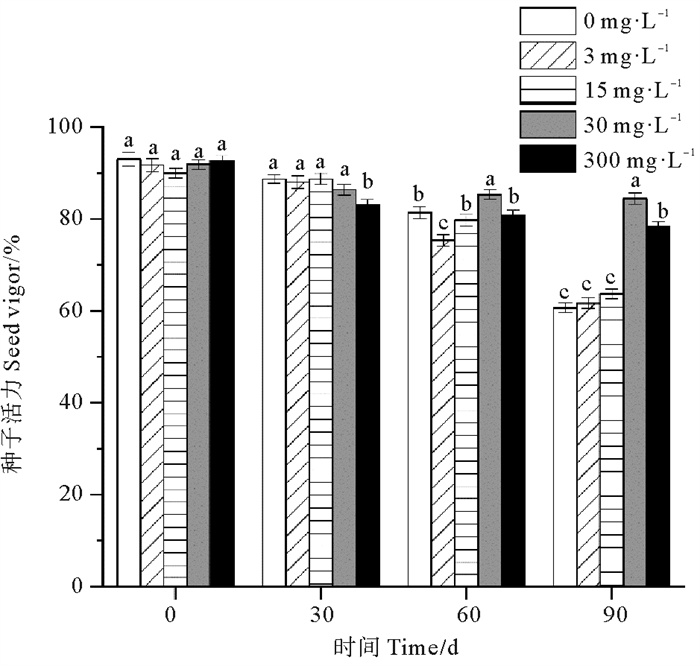
各处理组鳗草种子的种子活力随时间推移呈现逐渐下降趋势(见图 4)。单因素方差分析表明,至实验结束,30 mg·L-1处理组种子活力最高,显著高于其它处理组(P<0.05),为对照组的1.4倍;3和15 mg·L-1处理组种子活力较低,与对照组无显著差异(P>0.05)。
|
图 4 不同ABA浓度对鳗草种子活力的影响 Fig. 4 The effect of different ABA concentrations on the seed vigor of eelgrass |
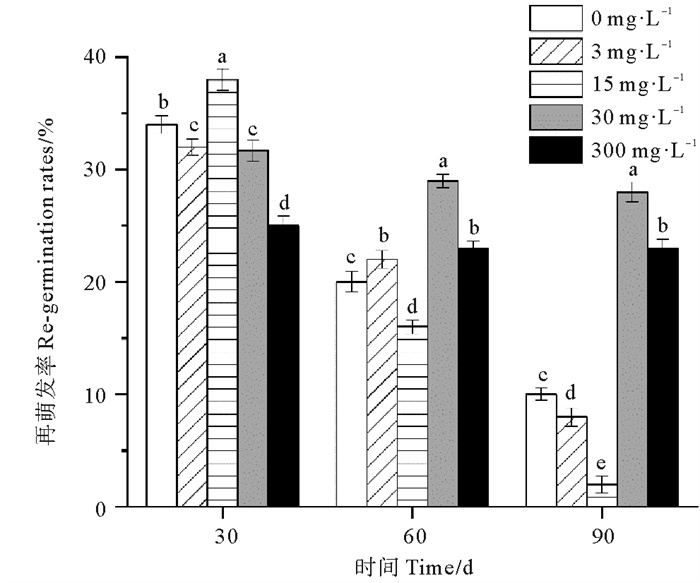
各处理组鳗草种子的再萌发率随时间延长呈现下降趋势(见图 5)。单因素方差分析表明,实验结束时,30 mg·L-1处理组的再萌发率最高,显著高于其它处理组,为对照组的2.8倍。15 mg·L-1处理组的再萌发率最低,显著低于其它处理组(P<0.05),仅为对照组的20%。
|
图 5 不同ABA浓度对鳗草种子再萌发率的影响 Fig. 5 The effect of different ABA concentrations on the seed regermination rate of eelgrass |
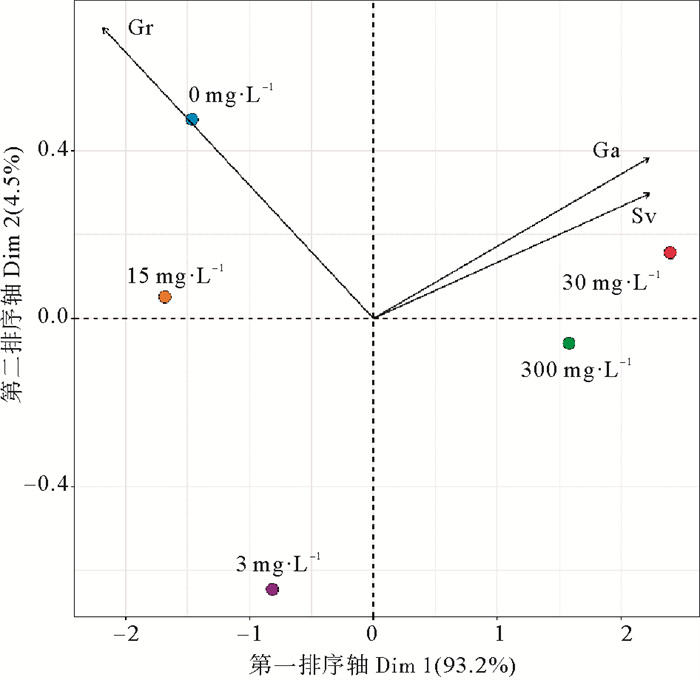
对各处理组萌发率、种子活力和再萌发率进行PCA分析,结果显示第一排序轴的特征值大于1,对各指标的解释量高达93.2%(见图 6)。种子活力、再萌发率与第一排序轴聚成一簇,呈正相关关系,萌发率呈负相关关系。对各指标进行排序后发现30 mg·L-1处理组对种子延长休眠的效果较好,期间种子萌发率最低,而种子活力和再萌发率最高。
|
( Gr为萌发率;Ga为再萌发率;Sv为种子活力。Gr is germination rate; Ga is regermination rate; Sv is seed vigor. ) 图 6 不同ABA浓度与鳗草种子各指标的排序图 Fig. 6 Sequence diagram of different ABA concentrations and various indexes of eelgrass seeds |
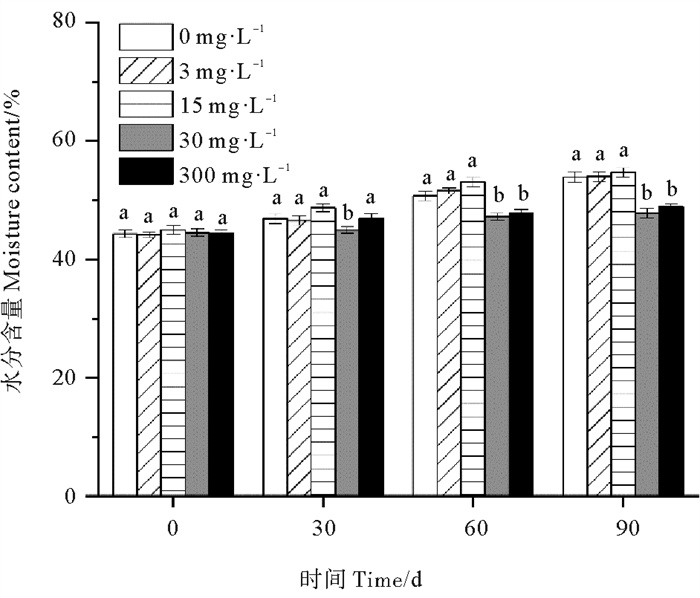
各处理组鳗草种子的水分含量随时间推移总体呈上升趋势,至90 d时达到最大值,其中30和300 mg·L-1处理组种子水分含量上升不明显(见图 7)。单因素方差分析表明,至实验结束,30和300 mg·L-1处理组鳗草种子的种子水分含量最低,显著低于其它处理组(P<0.05),分别为对照组的88%和91%,而3和15 mg·L-1处理组水分含量最高,与对照组无显著差异(P>0.05)。
|
图 7 不同ABA浓度对鳗草种子水分含量的影响 Fig. 7 The effect of different ABA concentrations on the water content of eelgrass seeds |
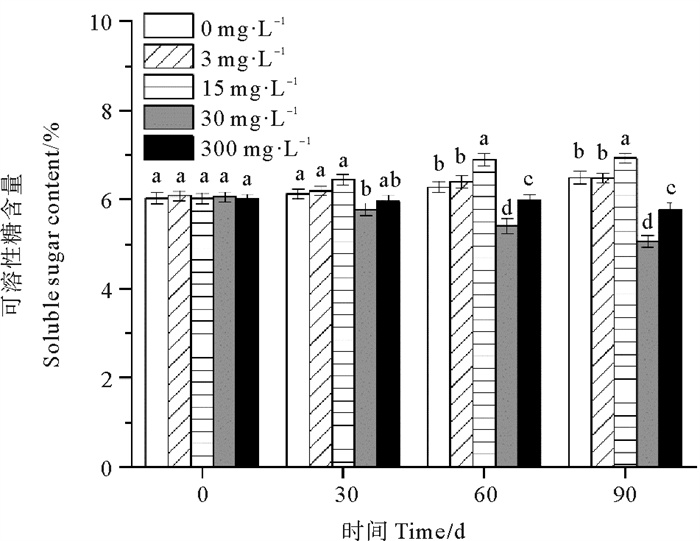
0、3和15 mg·L-1处理组鳗草种子的可溶性糖含量随时间延长呈上升趋势,而30和300 mg·L-1处理组鳗草种子的可溶性糖含量随时间延长呈现下降趋势(见图 8)。单因素方差分析表明,至实验结束时,30 mg·L-1处理组可溶性糖含量最低,显著低于其它处理组(P<0.05),为对照组的78%,15 mg·L-1处理组的可溶性糖含量最高,显著高于其它处理组(P<0.05),为对照组的1.1倍。
|
图 8 不同ABA浓度对鳗草种子可溶性糖含量的影响 Fig. 8 The effect of different ABA concentrations on the soluble sugar content of eelgrass seeds |
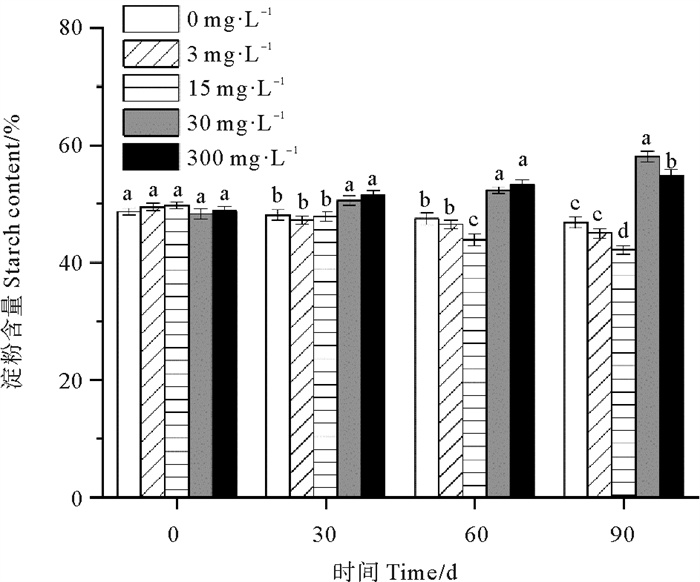
30和300 mg·L-1处理组鳗草种子的淀粉含量随时间延长呈上升趋势,而0、3和15 mg·L-1处理组鳗草种子的淀粉含量随时间延长呈下降趋势(见图 9)。单因素方差分析表明,至实验结束,30 mg·L-1处理组淀粉含量最高,显著高于其它处理组(P<0.05),为对照组的1.2倍,15 mg·L-1处理组的淀粉含量最低,显著低于其它处理(P<0.05),为对照组的90%。
|
图 9 不同ABA浓度对鳗草种子淀粉含量的影响 Fig. 9 The effect of different ABA concentrations on the starch content of eelgrass seeds |
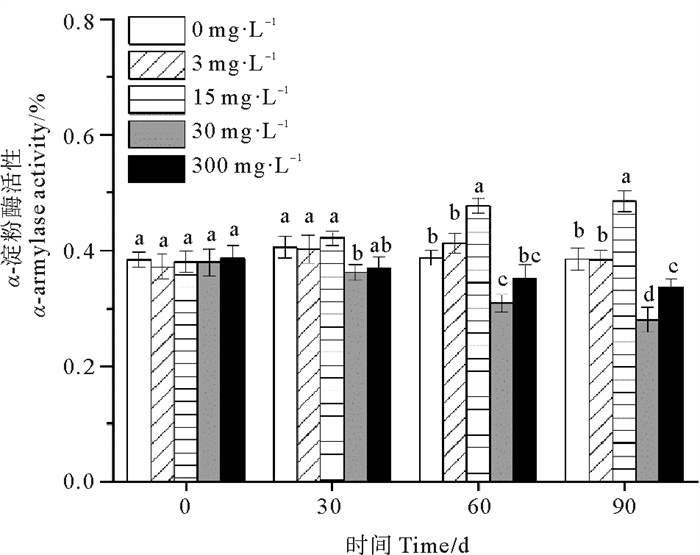
休眠延长期内30和300 mg·L-1处理组鳗草种子的α-淀粉酶活性随时间延长呈现下降趋势,而0、3和15 mg·L-1处理组鳗草种子的α-淀粉酶活性随时间延长呈上升趋势(见图 10)。单因素方差分析表明,至实验结束时,30 mg·L-1处理组α-淀粉酶活性最低,显著低于其它处理组(P<0.05),为对照组的72%,15 mg·L-1处理组α-淀粉酶活性最高,显著高于其它处理(P<0.05),为对照组的1.3倍。
|
图 10 不同ABA浓度对鳗草种子α-淀粉酶活性的影响 Fig. 10 The effect of different ABA concentrations on the α-amylase activity of eelgrass seeds |
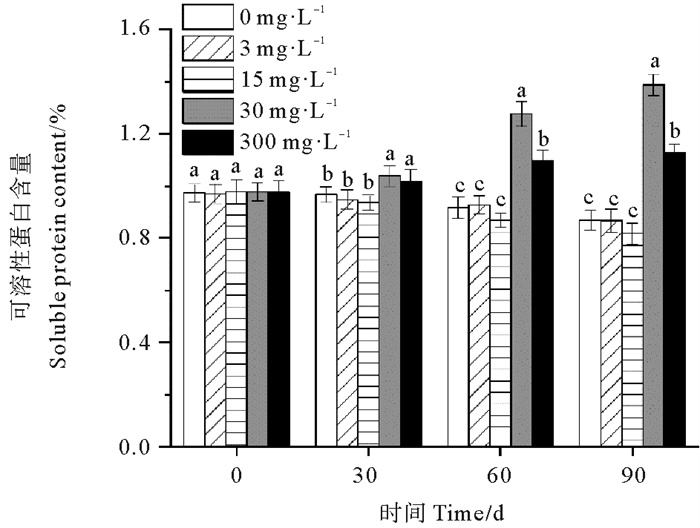
休眠延长期内30和300 mg·L-1处理组鳗草种子的可溶性蛋白含量随时间延长呈现上升趋势,而0、3和15 mg·L-1处理组鳗草种子的淀粉含量随时间延长呈现下降趋势(见图 11)。单因素方差分析表明,至实验结束时,30 mg·L-1处理组可溶性蛋白含量最高,显著高于其它处理组(P<0.05),为对照组的1.6倍,15 mg·L-1处理组淀粉含量最低,与对照组无显著差异(P>0.05)。
|
图 11 不同ABA浓度对鳗草种子可溶性蛋白含量的影响 Fig. 11 The effect of different ABA concentrations on the soluble protein content of eelgrass seeds |
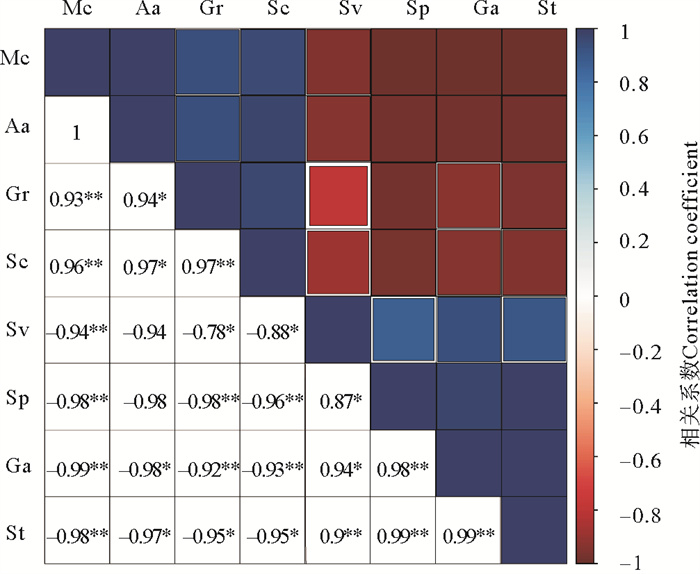
将萌发率、种子活力等生态学指标与水分含量、淀粉含量等生理学指标进行相关性分析,发现萌发率、种子活力及再萌发率与植株体内各类营养物质均有显著相关性,其中与水分含量的相关性最强(见图 12)。结果显示,水分与萌发率、种子活力呈极显著正相关(相关系数均大于0.9),与再萌发率呈极显著负相关(相关系数小于-0.9)。综合显示,水分含量是延长鳗草种子休眠的关键因素,其对种子的萌发率与再萌发率,以及种子活力均有显著影响。
|
( Mc代表水分含量(%),Aa代表α-淀粉酶活性活性(%),Gr代表萌发率(%),Sc代表可溶性糖含量(%),Sv代表种子活力(%),Sp代表可溶性蛋白(%),Ga代表再萌发率(%),St代表淀粉含量(%)。代表差异显著,代表差异极显著。Mc represents moisture content(%); Aa represents α-amylase activity(%); Gr represents germination rate(%); Sc represents soluble sugar content(%); Sv represents seed vigor(%); Sp represents soluble protein(%); Ga represents regermination rate(%); St represents starch content(%). represents significant difference, and represents very significant difference. ) 图 12 鳗草种子萌发的生态学指标与生理学指标的相关性分析 Fig. 12 Correlation analysis of ecological and physiological indexes of seed germination in eelgrass |
外源ABA的添加能有效抑制种子萌发,延长种子休眠时间,但休眠的延长效果受外源ABA浓度影响显著。大量研究表明,低浓度ABA将打破种子休眠,而高浓度ABA将延长种子休眠[13-15, 21]。Hong等[15]研究发现,150 mg·L-1的ABA能显著延长秋茄种子的休眠时间,休眠延长期内高浓度组(150 mg·L-1)的种子成熟度仅为对照组的60%。黄益洪等[22]研究发现,白小麦(Triticum aestivum)种子经80~100 mg·L-1ABA溶液浸泡后,种子的休眠时间显著延长,延长休眠期种子萌发率仅为对照组的42%。周述波[23]研究发现,ABA浓度为70~110 mg·L-1时能显著延长水稻种子的休眠时间,休眠延长期内,种子萌发率仅为对照组的40%。本研究也发现高浓度ABA(30和300 mg·L-1) 的添加能够有效延长鳗草种子的休眠时间,从而验证了高浓度ABA能够促进鳗草种子延长休眠的假设。其中ABA浓度为30 mg·L-1的休眠延长效果最好,延长休眠期间种子的累积萌发率仅为对照组的37%,种子活力和再萌发率为对照组的1.4和2.8倍。该ABA浓度显著低于陆生植物和红树植物种子延长休眠所需的ABA浓度,这可能是由于种子保存方式的不同。Chen等[24]对秋茄的研究发现,海水浸泡对种子内部的ABA含量具有显著影响,其与浸泡时间呈正比。鳗草种子需要浸泡在海水中保存,种子内部的ABA含量高于陆生植物和红树植物种子的ABA含量,因此对外源ABA的需求浓度可能更低。
3.2 休眠延长期海草种子内部贮存物质响应过程萌发是指种子打破休眠,胚芽突破种皮向外伸展的过程。萌发时种子需大量吸水,从而活跃细胞内的生理生化过程。此时种子吸水膨胀,种子内部的水分含量增加[25]。同时淀粉酶将淀粉分解为可溶性糖,为种子萌发提供能量,种子内部淀粉含量下降,可溶性糖含量升高[26]。蛋白质能够维持种子活力,提高种子的萌发潜力,也是种子萌发过程中不可缺少的物质,萌发过程中蛋白质在蛋白酶的作用下分解为氨基酸,为幼苗建植提供物质基础,蛋白质含量显著降低。
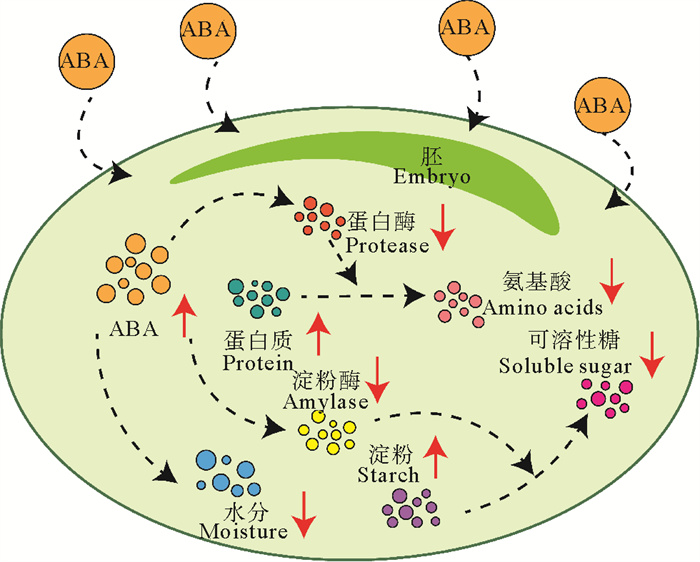
对陆生植物来讲,ABA主要通过抑制α-淀粉酶活性来延长种子休眠。雍太文[13]通过70 mg·L-1的ABA溶液浸泡水稻种子发现,水稻种子内部的α-淀粉酶活性与对照组相比降低了90%以上,可溶性糖含量降低61.3%,可溶性蛋白含量增加37.1%。本研究发现,ABA对鳗草种子的延长休眠作用,是多种因素共同作用的结果,其中水分含量是主要因素。外源ABA的添加能够抑制种子的吸胀作用,降低种子的水分含量,与对照组相比ABA浓度为30 mg·L-1处理组种子含水量在90 d内降低12%。造成该差异的主要原因可能是种子内部营养物质的合成方式不同,在萌发初期,鳗草种子内部营养物质的合成需要溶解在水中,对水分的需求量高于陆地植物,所以抑制种子吸水更能延长种子休眠。ABA的添加还能够通过降低α-淀粉酶活性,减缓淀粉的分解速率,降低可溶性糖含量,提升可溶性蛋白含量来达到延长休眠的目的,具体过程如图 13所示。至实验结束,30 mg·L-1处理组的α-淀粉酶活性及可溶性糖含量分别降低18%和22%,淀粉含量升高20%,可溶性蛋白含量升高60%。
|
图 13 ABA处理下鳗草种子内部生理响应示意图 Fig. 13 Schematic diagram of internal physiological response of eelgrass seeds to ABA treatment |
本研究通过设置不同浓度脱落酸(ABA)处理组,探究了外源ABA对延长鳗草种子休眠的作用,分析了鳗草种子应对外源ABA的生理响应过程。结果发现,15 ℃、黑暗条件下,30 mg·L-1外源ABA的添加能够显著延长鳗草种子的休眠时间。休眠延长期间,鳗草种子吸胀作用减弱,种子内部水分含量上升不明显,α-淀粉酶活性降低,淀粉转化速率减缓,可溶性糖含量降低,淀粉和可溶性蛋白含量上升。由于外源ABA对种子延长休眠的作用不仅受浓度影响,还与光照和温度等外界环境因素密切相关,因此未来的研究还需进一步探究光照和温度等环境因子对ABA延长休眠的影响。
| [1] |
Mcleod E, Chmura G L, Bouillon S, et al. A blueprint for blue carbon: Toward an improved understanding of the role of vegetated coastal habitats in sequestering CO2[J]. Frontiers in Ecology and the Environment, 2011, 9(10): 552-560. DOI:10.1890/110004
(  0) 0) |
| [2] |
Fourqurean J W, Duarte C M, Kennedy H, et al. Seagrass ecosystems as a globally significant carbon stock[J]. Nature Geoscience, 2012, 5(7): 505-509. DOI:10.1038/ngeo1477
(  0) 0) |
| [3] |
Horinouchi M. Distribution patterns of benthic juvenile gobies in and around seagrass habitats: Effectiveness of seagrass shelter against predators[J]. Estuarine, Coastal and Shelf Science, 2007, 2007(72): 657-664.
(  0) 0) |
| [4] |
Rooker J R, Holt G J, Holt S A. Vulnerability of newly settled red drum(Sciaenops ocellatus) to predatory fish: Is early-life survival enhanced by seagrass meadows?[J]. Marine Biology, 1998, 131(1): 145-151. DOI:10.1007/s002270050305
(  0) 0) |
| [5] |
王道儒, 吴钟解, 陈春华, 等. 海南岛海草资源分布现状及存在威胁[J]. 海洋环境科学, 2012, 31(1): 34-38. Wang D R, Wu Z J, Chen C H, et al. Distribution of seagrass resources and existing threat in Hainan Island[J]. Marine Environmental Science, 2012, 31(1): 34-38. DOI:10.3969/j.issn.1007-6336.2012.01.008 (  0) 0) |
| [6] |
郑凤英, 邱广龙, 范航清, 等. 中国海草的多样性、分布及保护[J]. 生物多样性, 2013, 21(5): 517-526. Zheng F Y, Qiu G L, Fan H Q, et al. Diversity, distribution and conservation of Chinese seagrass species[J]. Biodiversity Science, 2013, 21(5): 517-526. (  0) 0) |
| [7] |
Waycott M, Duarte C M, Carruthers T J, et al. Accelerating loss of seagrasses across the globe threatens coastal ecosystems[J]. Proceedings of the National Academy of Sciences of the United States of America, 2009, 106(30): 12377-12381. DOI:10.1073/pnas.0905620106
(  0) 0) |
| [8] |
Pickerell C H, Schott S, Wyllie-Echeverria S. Buoy-deployed seeding: Demonstration of a new eelgrass(Zostera marina L.) planting method[J]. Ecological Engineering, 2005, 25(2): 127-136. DOI:10.1016/j.ecoleng.2005.03.005
(  0) 0) |
| [9] |
Reed D C, Holbrook S J, Solomon E, et al. Studies on germination and root development in the surfgrass Phyllospadix torreyi: Implications for habitat restoration[J]. Aquatic Botany, 1998, 62(2): 71-80. DOI:10.1016/S0304-3770(98)00088-6
(  0) 0) |
| [10] |
Mc Millan C. Seed germination in Halodule wrightii and Syringodium filiforme from Texas and the U. S. Virgin Islands[J]. Aquatic Botany, 1983, 15(2): 217-220. DOI:10.1016/0304-3770(83)90033-5
(  0) 0) |
| [11] |
Mador B M, Guilar R L, Kaya C, et al. Comparative effects of NaCl and polyethylene glycol on germination, emergence and seedling growth of cowpea[J]. Journal of Agronomy & Crop Science, 2010, 188(4): 235-247.
(  0) 0) |
| [12] |
Engelmann F. Plant cryopreservation: Progress and prospects[J]. In Vitro Cellular & Developmental Biology-Plant, 2004, 40(5): 427-433.
(  0) 0) |
| [13] |
雍太文, 杨文钰, 王小春. 外源ABA对杂交水稻种子萌发的生理效应[J]. 种子, 2002, 1(5): 26-30. Yong T W, Yang W Y, Wang X C. The Physiological effect of exogenous ABA on germination of hybrid rice seed[J]. Seed, 2002, 1(5): 26-30. DOI:10.3969/j.issn.1001-4705.2002.05.013 (  0) 0) |
| [14] |
丁君辉, 李耀国, 童建华. 脱落酸对水稻种子萌发的影响[J]. 作物研究, 2012, 26(4): 328-330. Ding J H, Li Y G, Tong J H. Effect of ABA on germination of rice seeds[J]. Crop Research, 2012, 26(4): 328-330. DOI:10.3969/j.issn.1001-5280.2012.04.04 (  0) 0) |
| [15] |
Hong L, Su W, Zhang Y, et al. Transcriptome profiling during mangrove viviparity in response to abscisic acid[J]. Scientific Reports, 2018, 8(1): 1-12.
(  0) 0) |
| [16] |
王建林. 高级作物生理学[M]. 北京: 中国农业大学出版社, 2013: 135-136. Wang J L. Advanced Crop Physiology[M]. Beijing: China Agricultural University Press, 2013: 135-136. (  0) 0) |
| [17] |
杨敏. 种子生产与管理[M]. 合肥: 合肥工业大学出版社, 2013: 163-167. Yang M. Seed Production and Management[M]. Hefei: Hefei University of Technology Press, 2013: 163-167. (  0) 0) |
| [18] |
Lewis M A, Dantin D D, Chancy C A, et al. Florida seagrass habitat evaluation: A comparative survey for chemical quality[J]. Environmental Pollution, 2007, 146(1): 206-218. DOI:10.1016/j.envpol.2006.04.041
(  0) 0) |
| [19] |
陈智慧, 史梅, 王秋香, 等. 用凯氏定氮法测定食品中的蛋白质含量[J]. 新疆畜牧业, 2008, 18(5): 22-24. Chen Z H, Shi M, Wang Q X, et al. The protein content in food determined by Kjeldahl method[J]. Animal Husbandry in Xinjiang, 2008, 18(5): 22-24. DOI:10.3969/j.issn.1003-4889.2008.05.010 (  0) 0) |
| [20] |
荣俊, 杨待建, 伍晓雄. 加酶饲料中淀粉酶总活力的测定—碘淀粉比色法[J]. 饲料工业, 1994, 15(3): 40-42. Rong J, Yang D J, Wu X X. Determination of total amylase activity in enzymatic feeds-iodide starch colorimetric method[J]. Feed industry, 1994, 15(3): 40-42. (  0) 0) |
| [21] |
张宜麟, 赵帆, 赵洁. 脱落酸对水稻种子萌发及相关基因表达的影响[J]. 武汉植物学研究, 2005, 23(3): 203-210. Zhang Y L, Zhao F, Zhao J. Effects of exogenous ABA on the seed germination of rice(Oryza sativa L.) and the expression of relative genes[J]. Journal of Wuhan Botanical Research, 2005, 23(3): 203-210. (  0) 0) |
| [22] |
黄益洪, 汤日圣, 叶晓青. 脱落酸(ABA)对白粒小麦种子萌发及幼苗生长的影响[J]. 麦类作物学报, 2009, 3(29): 503-507. Huang Y H, Tang R S, Ye X Q. Effect of ABA on the germination of white-grain wheat seeds and growth of its seedlings[J]. Journal of Triticeae Crops, 2009, 3(29): 503-507. (  0) 0) |
| [23] |
周述波, 林伟, 萧浪涛, 等. 外源GA3和ABA对杂交水稻种子萌发的影响[J]. 湖南农业大学学报, 2005, 31(3): 270-271. Zhou S B, Lin W, Xiao L T, et al. The effect of exogenous GA3 and ABA on germination of hybrid rice seeds[J]. Journal of Hunan Agricultural University, 2005, 31(3): 270-271. (  0) 0) |
| [24] |
Chen L Z, Wang W Q, Lin P. Photosynthetic and physiological responses of Kandelia candel L. Druce seedlings to duration of tidal immersion in artificial seawater[J]. Environmental and Experimental Botany, 2005, 54(3): 256-266. DOI:10.1016/j.envexpbot.2004.09.004
(  0) 0) |
| [25] |
Bradford K J. A water relations analysis of seed germination rates[J]. Plant Physiology, 1990, 94(2): 840-849.
(  0) 0) |
| [26] |
Steinbach H, Benech Arnold R, Sanchez R A. Hormonal regulation of dormancy in developing sorghum seeds[J]. Plant Physiology, 1997, 113(1): 149-154. DOI:10.1104/pp.113.1.149
(  0) 0) |
 2021, Vol. 51
2021, Vol. 51


