2. 青岛农业大学海都学院,山东 烟台 265100;
3. 青岛根源生物技术集团有限公司,山东 青岛 266000
凡纳滨对虾(Litopenaeus vannamei)又称南美白对虾、白对虾,因其高产量、广盐性、良好的适应能力与良好的营养价值被广泛养殖。益生菌的定义是能够改善肠道菌群生态平衡,对宿主有益的活微生物制剂[1]。益生菌具有拮抗病原菌、与病原菌竞争黏附位点和营养物质、调节免疫等特点而最初应用在猪和牛等陆生动物的饲料添加剂中[2]。益生菌在水产养殖中的应用最早始于30多年前,但是受到重视却是在21世纪之后[3]。
在过去的30多年,有一些菌株已经被鉴定认为是益生菌并在在水产养殖中有一些应用,Noor Uddin等评估了在越南对虾养殖中常用的7种益生菌产品中的细菌种类含量,其中以枯草芽孢杆菌(Bacillus subtilis)、地衣芽孢杆菌(B. licheniformis)、苏云金芽孢杆菌(B. thuringiensis)和嗜酸乳杆菌(Lactobacillus acidophilus)为主[4],芽孢杆菌和乳酸菌是使用最为广泛的益生菌[5]。对于益生菌的筛选,其对致病菌的抑制能力与对肠黏膜的黏附能力是潜在益生菌重要的预筛指标[2]。Tepaamorndech等通过对多株弧菌致病菌的抑制作用筛选出B. aryabhattai TBRC8450,将其添加到饲料中发现其可以提高对哈维氏弧菌(Vibrio harveyi)的抵抗能力并减少凡纳滨对虾肠道弧菌的丰度[6],Zokaeifar等发现对哈维氏弧菌和副溶血弧菌(V. parahemolyticus)有抑制作用的枯草芽孢杆菌L10和枯草芽孢杆菌G1能提高凡纳滨对虾胃肠道中的芽孢杆菌数量并减少弧菌数量,并提高其生长表现与对病原菌的抵抗能力[7]。凡纳滨对虾生活盐度较广,其在盐度5~50下均可存活[8],而有些益生菌在高盐度下并不能存活,因而将盐度也作为一个评价指标。与一些在水产养殖中控制疾病方法的单一机制模式不同,益生菌可以从多方面给宿主带来好处,这在水产养殖应用中存在着巨大的潜力[9]。
水产品的健康状况依赖于或受制于直接生存环境,因为它们与各种各样的微生物密切接触,包括可以在动物外部和内表层定植的致病菌和条件致病菌,而肠道菌群形成一个天然的防御屏障,对肠道上皮细胞的结构和代谢起着保护作用,因此,建立正常或保护性微生物群是排除潜在的入侵者和维持机体健康状态的关键因素[10-11]。Luis-Villasenor等发现芽孢杆菌的混合物可提高白对虾存活率和促进幼虾的生长发育,还可提高幼虾肠道菌群的多样性和均匀度,帮助保持对虾肠道内菌群的平衡[12]。
为从实验室前期研究的潜在益生菌中筛选出对凡纳滨对虾有益生功能的菌株,本研究从对凡纳滨对虾常见致病菌的抑制作用、对凡纳滨对虾肠黏液的黏附能力和对盐度的耐受性三方面进行评价,并探讨其对凡纳滨对虾肠道菌群的影响。
1 材料与方法 1.1 菌株来源与活化22株乳酸菌由哈尔滨工业大学乳科学与发酵工程实验室馈赠,鼠李糖乳杆菌LGG购于美国ATCC;致病菌菌哈维氏弧菌(CGMCC NO. 1.1601)和副溶血弧菌(CGMCC NO. 1.1997)购于中国普通微生物菌种保藏中心。
乳酸菌用含20%甘油的MRS在-80 ℃下保存,用MRS液体培养基在37 ℃条件下静置培养20 h活化,接种量为2%,活化第二代后用于实验。
弧菌用含20%甘油的2216E液体培养基在-80 ℃下保存,用2216E液体培养基在30 ℃条件下静置培养20 h活化,接种量为2%,活化第二代后用于实验。
1.2 潜在益生菌代谢产物的抑菌实验 1.2.1 无菌上清液抑菌活性的测定将培养好的细菌悬液在8 000 r/min离心5 min得到上清液,取上清液后用0.22 μm滤膜过滤以除去残留的菌体和其他杂质,得到无菌上清液并用pH计测定其pH。采用牛津杯琼脂扩散法进行具有抑菌活性的细菌筛选实验。将1.5%琼脂培养基倾倒在无菌培养皿(按每平皿10 mL)中待其凝固,水平放置以形成平面,凝固后在其上放置牛津杯。
制备2216E半固体培养基(即琼脂浓度为0.6%的2216E培养基)15 mL,冷却至40 ℃左右加入8 μL指示菌倒入含牛津杯的琼脂平皿上,待其凝固后取出牛津杯,在孔洞中加入150 μL无菌上清液,静置扩散2 h后置于30 ℃培养箱中培养20 h,观察加入无菌上清液的孔洞周围有无抑菌圈的形成,并抑菌圈的大小来初步判断抑菌活性的强弱,每株菌做3个平行实验[13]。
1.2.2 排除有机酸的发酵上清液实验将培养好的细菌悬液在8 000 r/min离心5 min,取上清液后用5 mol/L的NaOH调pH至6.0后用0.22 μm滤膜过滤以除去残留的菌体和其他杂质,得到排除有机酸后的无菌上清液备用。然后按照1.2.1中方法进行抑菌实验,观察排除有机酸后无菌上清液的抑菌效果,每株菌做3个平行实验。
1.3 潜在益生菌对南美白对虾肠黏液的黏附 1.3.1 对虾肠道粗黏液的获取小心刮取凡纳滨对虾肠道黏液置于预冷的PBS缓冲液(每1.5 L含十二水磷酸氢二钠4.32 g、氯化钠12.0 g、氯化钾0.3 g、磷酸二氢钾0.3 g)中,于4 ℃,12 000 r/min条件下离心10 min后取上清以去除不溶解物质。凡纳滨对虾肠道粗黏液蛋白浓度用Bradford的方法进行测定后用PBS缓冲液将终浓度调至1 mg/mL[2]。
1.3.2 细菌的荧光标记将CFDA-SE用二甲基亚砜溶解配制成1 mmol/L的母液,用0.22 μm滤膜过滤后分装,避光储存于-20 ℃待用。
将细菌培养液于4 ℃,8 000 r/min条件下离心5 min后去除上清液,用无菌PBS缓冲液将沉淀洗涤3次后悬浮于PBS缓冲液中,最终细菌浓度调至109 CFU/mL。于1 mL细菌菌悬液添加20 μL CFDA-SE母液混匀,37 ℃避光孵育15 min后于4 ℃,8 000 r/min条件下离心5 min去除上清液,用无菌PBS缓冲液将沉淀洗涤3次去除多余的染液。细菌重悬于无菌PBS,采用流式细胞仪在488 nm条件下分析其标记率[2]。
1.3.3 细菌对肠黏液的黏附在无菌96孔板中添加100 μL对虾粗黏液后于4 ℃过夜固定,用无菌PBS缓冲液洗涤3次96孔板,除去未固定的黏液。将100 μL经过荧光标记的细菌分别添加至固定过黏液的孔中,37 ℃孵育1 h。用PBS冲洗96孔板3次,去除未固定的细菌后用100 μL 0.05%胰蛋白酶室温处理10 min。将100 μL预冷的无菌BHI(Brain-heart infusion)添加至96孔板中以终止胰蛋白酶反应后收集样品,用荧光分光光度计测其荧光值,测定条件为:激发波长488 nm,发射波长518 nm,狭缝宽度2.5 nm。黏附率用黏附菌与初始菌的荧光强度比值表示,每株菌测定3个平行[2]。
1.4 潜在益生菌在不同盐浓度下的生长将活化后的细菌分别接种到添加有不同盐分的MRS中,即在添加0%~5%的氯化钠的MRS肉汤中接种2%活化好的乳酸菌,37 ℃培养20 h后,以MRS培养基为空白,用酶标仪测乳酸菌菌悬液的OD600来评估盐度对细生长的影响,每株菌做3个平行实验[14]。
1.5 菌株的16 S测序鉴定将菌株进行DNA提取,PCR扩增,送至上海生工生物工程有限公司进行测序,将得到的拼接序列在NCBI上进行比对,从比对结果中选择同源性较高的菌株的16S rDNA序列作为参比用MEGA7来构建进化树,将其鉴定到种水平。
1.6 潜在益生菌对凡纳滨对虾肠道菌群的影响 1.6.1 饲料的准备通过对抑菌活性、对凡纳滨对虾肠道的黏附性以及对盐度耐受性等体外实验,选出性能较好菌株,37 ℃静置培养20 h后,于4 000 r/min离心15 min后用无菌生理盐水洗涤3次,并重悬于无菌生理盐水中使得乳酸菌的浓度为1×109 CFU/mL,按照1:1:1的比例混合后备用。
将处理好的潜在益生菌加入到商业饲料中混匀,最终使每克基础饲料中含有1×108 CFU益生菌,空白对照组用等量无菌生理盐水与饲料混合。配制完成的饲料在室温自然晾干后于4 ℃储存,饲料每周配制一次[2]。
1.6.2 凡纳滨对虾的分组与饲养凡纳滨对虾由威海许家村养殖场购买,运送至根源生物公司水产养殖实验室进行养殖。将凡纳滨对虾随机平均分配于12个50 L(39 cm×39 cm×33 cm)的水族箱中暂养驯化10 d,暂养结束后将所有对虾混合,挑选大小一致的对虾称重随机分组,此时对虾均重约为2.13 g,分为2组,每组3个平行,分别为植物乳杆菌组(P组)和空白对照组(B组)。所有对虾均饲养于盐度24的人工海水中,温度为(26±1)℃, 每日饲喂对虾5%体重的基础饲料,持续通气,循环水饲养,及时排污换水,饲养4周。
1.6.3 凡纳滨对虾肠道的收集及测序饲养结束后将对虾饥饿处理一天,用无菌手术剪将肠道取出,每个养殖缸取9尾对虾肠道合并,每个处理3个平行, 用液氮速冻后于-80℃下保存备用。
将样品送至上海锐翌公司进行检测,使用QIAamp PowerFecal DNA Kit DNA提取试剂盒(QIAGEN公司)提取DNA,使用通用引物341F和806R进行16S rDNA扩增,扩增区域为V3~V4区,在通用引物的5’端加上适合Illumina Miseq PE250测序的index序列和接头序列。以稀释后的基因组DNA为模板,使用KAPA HiFi Hotstart ReadyMix PCR kit高保真酶进行PCR。用2%琼脂糖凝胶电泳检测PCR产物,并用AxyPrep DNA凝胶回收试剂盒(AXYGEN公司)切胶回收PCR产物。使用Qubit进行文库定量,并根据每个样品的数据量要求,进行相应比例的混合。使用Illumina Miseq PE250进行上机测序。
将得到的基因序列利用Usearch在0.97相似度下进行聚类,对聚类后的序列进行嵌合体过滤后,得到用于物种分类的OTU (Operational Taxonomic Units,操作分类单元),然后进行肠道菌群结构α多样性分析,并对不同处理组的肠道菌群结构进行比较,分析组间差异菌群,研究肠道菌群结构的变化。
1.7 实验数据处理实验结果表示平均值±标准偏差,用SPSS 22.0进行单因素ANOVA分析,P < 0.05为显著性差异。
2 结果 2.1 潜在益生菌对致病菌的抑制效果将实验室前期贮藏的23株乳酸菌,经培养取无菌发酵上清液进行抑菌实验,这23株乳酸菌对2株弧菌均有明显抑菌效果,其酸碱度和抑菌圈直径(包含牛津杯形成的孔洞直径7.8 mm)见表 1。
|
|
表 1 乳酸菌无菌发酵上清液酸碱度及其对弧菌的抑菌效果 Table 1 The pH of supernatant of lactic acid bacteria and its antibacterial effect on Vibrio |
其中YRL863和KTZ对2株弧菌的抑菌效果显著较高,其次是YRL577、SB27和KTP(C-2)对2株弧菌的抑菌效果也明显较好,T1对2株弧菌的抑菌效果显著较低,其余菌株对2株弧菌的抑菌效果各有差异,而23株乳酸菌的无菌发酵上清液的pH最高的为T1,最低的为Q7。并且经过排酸实验后,此23株乳酸菌均无明显抑菌圈产生,表明这23株乳酸菌的抑菌活性物质均为有机酸。
2.2 乳酸菌对凡纳滨对虾肠黏液的黏附率取对哈维氏弧菌和副溶血弧菌有抑菌效果的乳酸菌,研究其对凡纳滨对虾肠黏液的黏附性,结果见表 2。23株乳酸菌的黏附率在1.581%~7.292%之间,其中D-嗜酸乳杆菌、YRL45和KTP(C-2)的黏附性最好,其次是QL、YRL577、K14的黏附性较好,而T1的黏附性最差。
|
|
表 2 乳酸菌对凡纳滨对虾肠黏液的黏附率 Table 2 Adhesion rate of lactic acid bacteria to intestinal mucus of L. vannamei |
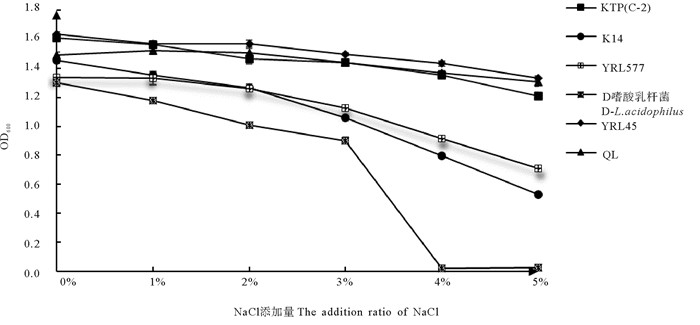
将黏附性最好的6株乳酸菌进行盐度耐受性实验,结果见图 1。其中D-嗜酸乳杆菌对盐度比较敏感,当NaCl添加量大于1%时,其OD600值急剧下降,当培养基NaCl添加量大于4%时,其几乎不生长;K14和YRL577对盐度的耐受性较好,当NaCl添加量超过2%时,其OD600下降变快,当NaCl添加量到5%时,相较于未添加NaCl时,K14和YRL577还能生长,但是其OD600值下降很多,表明其生长状态受到较大影响;其中KTP(C-2)、YRL45和QL对盐度的耐受性最好,当NaCl添加量不超过5%时,其OD600呈缓慢下降趋势,一直到添加5% NaCl时,但是这3株乳酸菌仍有良好的生长状况,并且其发酵终点的发酵液仍为酸性。
|
图 1 盐度对乳酸菌生长的影响 Fig. 1 Effect of salinity on the growth of lactic acid bacteria |
将在不同盐度下生长的KTP(C-2)、YRL45和QL这3株乳酸菌无菌发酵液进行对副溶血弧菌和哈维氏弧菌的抑菌实验,其抑菌直径见表 3,结果中抑菌圈的直径包括牛津杯孔的直径7.8 mm。
|
|
表 3 不同盐度乳酸菌无菌发酵上清液对弧菌的抑菌圈直径 Table 3 Inhibition zone diameter of sterile supernatant of lactic acid bacteria growing in different salinity against Vibrio |
通过对盐度耐受性实验发现KTP(C-2)、YRL45和QL对盐度的耐受性最好,并且其在不同盐度下的无菌发酵上清液对哈维氏弧菌和副溶血弧菌仍旧存在明显的抑菌效果。
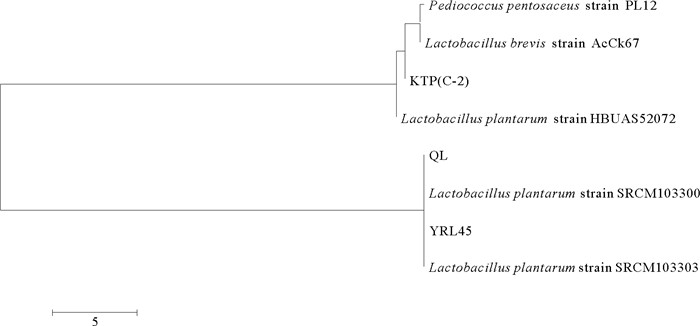
2.4 菌株的16S rDNA鉴定结果将KTP(C-2)、YRL45和QL的16S rDNA拼接序列在NCBI网站上利用BLAST进行比对,发现这3株菌均为植物乳杆菌,QL与L. plantarum strain SRCM103303的相似性达到99.81%,YRL45与L. plantarum strain SRCM103300相似性达到99.45%,KTP(C-2)与L. plantarum strain HBUAS52072相似性达到了99.93%。用MEGA7.0软件进行核酸比对,用比邻法构建进化树,结果见图 2。
|
图 2 YRL45、QL和KTP(C-2)的系统发育树 Fig. 2 Phylogenetic tree of YRL45, QL and KTP(C-2) |
本实验利用QIIME软件计算样品的Alpha多样性指数的值,分别从Chao1指数、Shannon指数和Simpson指数分析。凡纳滨对虾肠道菌群OTU数和α多样性见表 4,不同样本OTU韦恩图见图 3。
|
|
表 4 不同处理组凡纳滨对虾肠道菌群多样性指数 Table 4 Intestinal flora diversity index of L.Vannamei in different treatment groups |
|
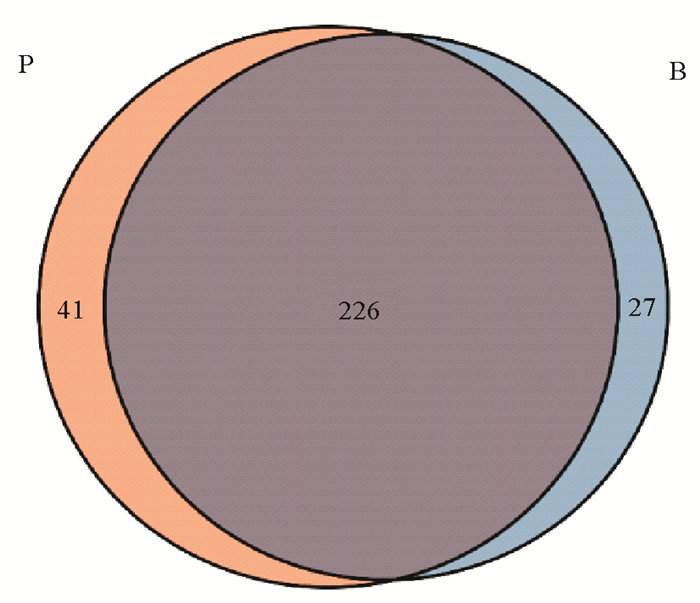
图 3 不同处理组OTUs韦恩图 Fig. 3 Venn diagram showing the unique and shared OTUs between the different treatment groups |
表 4结果显示,植物乳杆菌组抽平处理后的OTU数量比对照组多,而chao1指数、Shannon指数和Simpson指数较低,但是其标准偏差较大,说明相同处理的平行样本间差异略大,4个指数在2个处理组之间均没有显著差异。
图 3中Venn图显示,P组和B组共有的OTU数有226个,其共有OTU在门水平上分类的丰度最高的6类从大到小依此为变形菌门、拟杆菌门、厚壁菌门、梭杆菌门、疣微菌门和放线菌门,其中P组独有的OTU有41个,占总OTU数的15.36%,高于B组独有的10.67%。由此可知,植物乳杆菌(L. plantarum YRL45、L. plantarum QL、L. plantarum KTP(C-2))干预后,凡纳滨对虾肠道菌群独有物种较多,α多样性有所降低,但无显著影响。
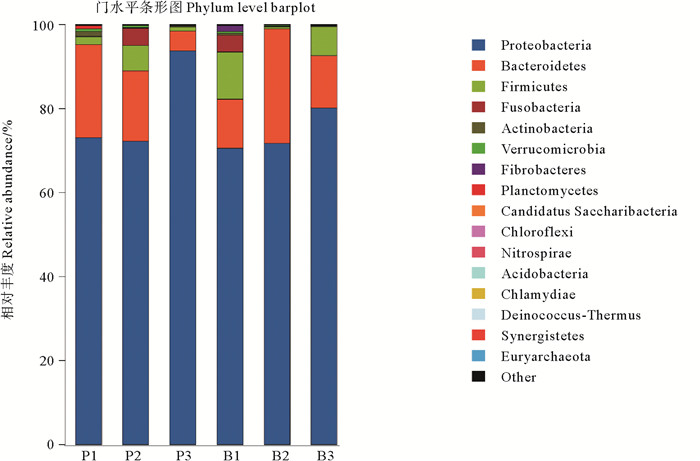
2.5.2 凡纳滨对虾肠道菌群结构根据OTU物种注释结果,各个样品在门的水平上物种相对丰度图见图 4。由图 4可知,在门水平上,变形菌门和拟杆菌门为凡纳滨对虾肠道优势菌门,共超过肠道菌群90%的比例,其次是厚壁菌门。P组的变性菌门丰度较高,但和B组之间没有显著差异,但是P3样本中变形菌门的丰度较为异常,有可能是样本在采集至检测过程中有偶然污染或保存过程中发生变化。B组的厚壁菌门丰度较高,但是两组之间没有显著性差异,大多益生菌比如乳酸菌、芽孢杆菌都属于厚壁菌门,从此处看来,植物乳杆菌干预后对厚壁菌门的丰度没有提高作用。P组中的放线菌门有所提高(平均丰度由0.289提高到0.500),虽然没有达到显著性差异,但是放线菌门中也有如节杆菌和双歧杆菌类益生菌,植物乳杆菌处理组均能提高肠道菌群中放线菌门的丰度。由此可见,植物乳杆菌(KTP(C-2)、YRL45和QL)对凡纳滨对虾肠道菌群没有显著改变,但是对其中一些物种的相对丰度有一定的调节作用。
|
图 4 不同处理组肠道菌群结构 Fig. 4 Gut flora structure in different treatment groups |
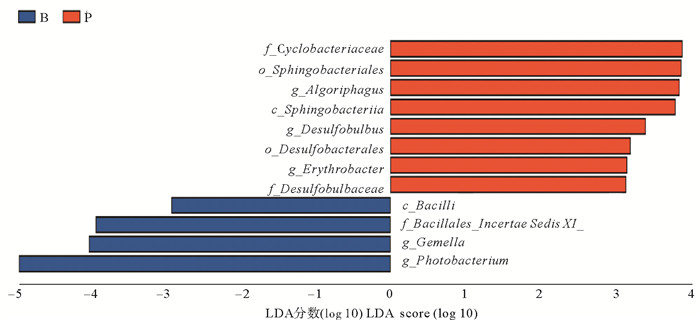
通过LEfSe分析,分析不同处理组的凡纳滨对虾肠道菌群种特有物种,结果见图 5。从属水平上分析,Photobacterium(发光杆菌属)和Gemella在B组中显著上调,Algoriphagus、Desulfobulbus(脱硫球茎菌属)和Erythrobacter(赤杆菌属)在P组中显著上调。
|
(c代表纲,o代表目,f代表科,g代表属。c means Class, o means Order, f means Family, g means Genus. ) 图 5 不同处理组凡纳滨对虾肠道微生物LDA分数 Fig. 5 LDA scores of intestinal microbial in different treatment groups |
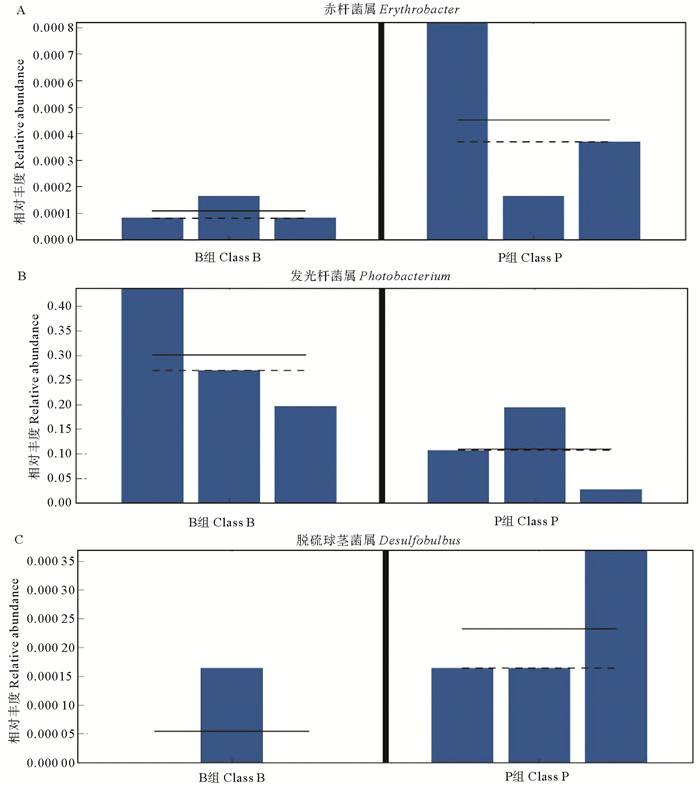
赤杆菌属、发光杆菌和脱硫球茎菌属的组内相对丰度分布见图 6A、6B和6C,其中P组的赤杆菌属平均丰度约为0.000 45,显著高于B组的约0.000 10,并且P组中每个样本中赤杆菌属的丰度均比B组高。而P组中发光杆菌的丰度约为0.10,显著低于B组的0.30,并且P组中发光杆菌的丰度均比B组低。P组中的脱硫球茎菌属丰度比B组高,但是在2.5.2中发现P3样本中肠道菌群变形菌门异常多,在这里P3的脱硫球茎菌属丰度较高可能与之有关,但总体而言P组的脱硫球茎菌属还是相对B组较高。
|
(组内三个柱形图表示组内3个平行样本。The three bars in the each group represent 3 parallel samples in the group. ) 图 6 差异性物种的组内分布 Fig. 6 Intra-group distribution of differential species |
以上结果表明植物乳杆菌YRL45、KTP(C-2)和QL干预对凡纳滨对虾肠道微生物结构有一定的调节作用,干预过后提高了赤杆菌属和脱硫球茎菌属的丰度,降低了发光杆菌的丰度。
3 讨论近年来,益生菌在水产养殖中受到广泛的关注与研究,但其在凡纳滨对虾等无脊椎动物中的研究仍非常有限[15]。益生菌可以产生对病原菌有抑制或者杀灭作用的物质如有机酸、过氧化氢、细菌素等物质[16],本研究以对凡纳滨对虾养殖中常见致病菌为指示菌评价受试菌的抑菌能力,发现23株乳酸菌对哈维氏弧菌和副溶血弧菌均有较明显的抑制效果,分析上清液的酸碱度与其抑菌圈直径,发现其抑菌效果与pH有一定的联系,比如T1的抑菌效果最差,其上清液pH最高,但是YRL863和KTZ的抑菌效果最好,其pH并不是最低的,并且经过排酸实验后,此23株乳酸菌均无明显抑菌圈产生,表明这23株乳酸菌的抑菌活性物质均为有机酸,但其抑菌圈直径与上清液pH并不是绝对成负相关的,这可能是由于不同有机酸的抑菌效果不同。益生菌通过对肠上皮的黏附位点的竞争而产生益生活性,细菌能黏附并定植于肠道上皮层而阻碍病原菌的黏附是益生菌筛选的理想标准,这种对位点的作用机制称为“竞争性抑制”[17-18],本研究再以凡纳滨对虾肠黏液为对象评价受试菌的黏附潜力,发现黏附性较好的为D-嗜酸乳杆菌、YRL45、KTP(C-2)、QL、YRL577和K14这6株乳酸菌;并且针对凡纳滨对虾广盐性的特点进一步对受试菌进行盐度耐受性,发现YRL45、KTP(C-2)和QL对盐度的耐受性最好。对YRL45、KTP(C-2)和QL进行16S rDNA测序比对,发现这3株乳酸菌均为植物乳杆菌。
肠道菌群与生物体的健康有着密切的关系,并且对宿主的营养吸收、免疫应答和肠黏膜的形态都有影响[19]。本研究将植物乳杆菌YRL45、KTP(C-2)和QL混合后饲喂凡纳滨对虾, 发现变形菌门和拟杆菌门为凡纳滨对虾肠道优势菌门,其次是厚壁菌门,与之类似的是Huang等研究发现凡纳滨对虾肠道中优势菌群是变形菌门、拟杆菌门与放线菌门或厚壁菌门[20]。Sha等研究戊糖乳杆菌(L. pentosus)及其上清液对凡纳滨对虾肠道菌群的影响发现戊糖乳杆菌上清液能显著提高对虾肠道内放线菌的丰度[19],这与本研究有相似结果。
通过LEfSe分析发现,植物乳杆菌YRL45、KTP(C-2)和QL能提高赤杆菌属的丰度,降低了发光杆菌属对肠道菌群的影响力。发光杆菌属是凡纳滨对虾养殖中的条件致病菌,Amoah等发现添加凝结芽孢杆菌(B. coagulans)可以减少凡纳滨对虾肠道菌群中发光杆菌属的丰度[21],Huynh等发现添加合生元(植物乳杆菌和低聚半乳糖)可以减少肠道中美人鱼发光杆菌(Photobacterium damselae)[22],Hu等也发现低聚果糖的添加可以改善对虾肠道微生物多样性,抑制肠道中P. damselae-like strains[23]。脱硫球茎菌属为潜在病原体[24],在植物乳杆菌组中也有所增加,但是其中有一个样本的脱硫球茎菌属丰度异常,总体而言有一定的增加。但是赤杆菌属是光合细菌的一种,属于功能性菌的一种,在本实验中,植物乳杆菌处理组中能增加赤杆菌属。与之相似的是,Hu等发现相比较对照组,添加芽孢杆菌和糖蜜的混合物的对虾肠道菌群中赤杆菌属较为突出[25]。
从肠道菌群结构与差异分析综合来看,植物乳杆菌YRL45、KTP(C-2)和QL的添加对凡纳滨对虾肠道菌群结构有一定的调节作用,并且在提高赤杆菌属和降低发光杆菌属方面有一定的效果。
4 结语本研究通过评价乳酸菌对凡纳滨对虾致病菌的抑制作用与对其肠黏液的黏附作用来筛选凡纳滨对虾的潜在益生菌,并根据其养殖盐度范围来评价乳酸菌的耐盐性,进一步选出耐盐性能更好的植物乳杆菌YRL45、KTP(C-2)和QL作为凡纳滨对虾潜在益生菌来饲喂凡纳滨对虾,发现其对凡纳滨对虾肠道菌群的结构中放线菌门的丰度有一定改善,且能提高赤杆菌属丰度,降低发光杆菌属丰度,对肠道菌群一定的调节作用,本研究为益生菌在凡纳滨对虾中的筛选应用提供了理论基础。
| [1] |
Fuller R. Probiotics in man and animals[J]. J Appl Bacteriol, 1989, 66(5): 365-378. DOI:10.1111/j.1365-2672.1989.tb05105.x
(  0) 0) |
| [2] |
Sha Y J, Wang L, Liu M, et al. Effects of lactic acid bacteria and the corresponding supernatant on the survival, growth performance, immune response and disease resistance of Litopenaeus vannamei[J]. Aquaculture, 2016, 452: 28-36. DOI:10.1016/j.aquaculture.2015.10.014
(  0) 0) |
| [3] |
Zorriehzahra M J, Delshad S T, Adel M, et al. Probiotics as beneficial microbes in aquaculture: An update on their multiple modes of action: A review[J]. Vet Q, 2016, 36(4): 228-241. DOI:10.1080/01652176.2016.1172132
(  0) 0) |
| [4] |
Noor Uddin G M, Larsen M H, Christensen H, et al. Identification and antimicrobial resistance of bacteria isolated from probiotic products used in shrimp culture[J]. Plos One, 2015, 10(7): e132338.
(  0) 0) |
| [5] |
Hao K, Liu J, Ling F, et al. Effects of dietary administration of Shewanella haliotis D4, Bacillus cereus D7 and Aeromonas bivalvium D15, single or combined, on the growth, innate immunity and disease resistance of shrimp, Litopenaeus vannamei[J]. Aquaculture, 2014, 428-429: 141-149. DOI:10.1016/j.aquaculture.2014.03.016
(  0) 0) |
| [6] |
Tepaamorndech S, Chantarasakha K, Kingcha Y, et al. Effects of Bacillus aryabhattai TBRC8450 on vibriosis resistance and immune enhancement in Pacific white shrimp, Litopenaeus vannamei[J]. Fish and Shellfish Immunology, 2019, 86: 4-13. DOI:10.1016/j.fsi.2018.11.010
(  0) 0) |
| [7] |
Zokaeifar H, Balcázar J L, Saad C R, et al. Effects of Bacillus subtilis on the growth performance, digestive enzymes, immune gene expression and disease resistance of white shrimp, Litopenaeus vannamei[J]. Fish and Shellfish Immunology, 2012, 33(4): 683-689. DOI:10.1016/j.fsi.2012.05.027
(  0) 0) |
| [8] |
Ponce-Palafox J, Martinez-Palacios C A, Ross L G. The effects of salinity and temperature on the growth and survival rates of juvenile white shrimp, Penaeus vannamei, Boone, 1931[J]. Aquaculture, 1997, 157(1): 107-115.
(  0) 0) |
| [9] |
Hai N V. The use of probiotics in aquaculture[J]. Journal of Applied Microbiology, 2015, 119(4): 917-935. DOI:10.1111/jam.12886
(  0) 0) |
| [10] |
Gomez G D, Balcazar J L. A review on the interactions between gut microbiota and innate immunity of fish[J]. FEMS Immunol Med Microbiol, 2008, 52(2): 145-154.
(  0) 0) |
| [11] |
Shanahan F, O Hara A M. The gut flora as a forgotten organ[J]. EMBO Reports, 2006, 7(7): 688-693. DOI:10.1038/sj.embor.7400731
(  0) 0) |
| [12] |
Luis Villasenor I E, Voltolina D, Gomez Gil B, et al. Probiotic modulation of the gut bacterial community of juvenile Litopenaeus vannamei challenged with Vibrio parahaemolyticus CAIM 170[J]. Latin American Journal of Aquatic Research, 2015, 43(4): 766-775.
(  0) 0) |
| [13] |
杨艳艳.源于植物乳杆菌的抗菌肽Lac-B23的筛选、分离纯化及抗菌特性的研究[D].哈尔滨: 哈尔滨工业大学, 2014. Yang Y Y. Isolation, Purification and antibacterial Properties of Bacteriocin Lac-B23 Producing by Lactobacillus plantarum[D]. Harbin: Harbin Institute of Technology, 2014. http://cdmd.cnki.com.cn/Article/CDMD-10213-1014083144.htm (  0) 0) |
| [14] |
Zuo Z, Shang B, Shao Y, et al. Screening of intestinal probiotics and the effects of feeding probiotics on the growth, immune, digestive enzyme activity and intestinal flora of Litopenaeus vannamei[J]. Fish and Shellfish Immunology, 2019, 86: 160-168. DOI:10.1016/j.fsi.2018.11.003
(  0) 0) |
| [15] |
Kumar V, Roy S, Meena D K, et al. Application of probiotics in shrimp aquaculture: Importance, mechanisms of action, and methods of administration[J]. Reviews in Fisheries Science and Aquaculture, 2016, 24(4): 342-368. DOI:10.1080/23308249.2016.1193841
(  0) 0) |
| [16] |
Servin A L. Antagonistic activities of Lactobacilli and Bifidobacteria against microbial pathogens[J]. FEMS Microbiology Reviews, 2004, 28(4): 405-440. DOI:10.1016/j.femsre.2004.01.003
(  0) 0) |
| [17] |
Lazado C C, Caipang C M A, Brinchmann M F, et al. In vitro adherence of two candidate probiotics from Atlantic cod and their interference with the adhesion of two pathogenic bacteria[J]. Veterinary Microbiology, 2011, 148(2-4): 252-259. DOI:10.1016/j.vetmic.2010.08.024
(  0) 0) |
| [18] |
Balcázar J L, De Blas I, Ruiz-Zarzuela I, et al. The role of probiotics in aquaculture[J]. Veterinary Microbiology, 2006, 114(3-4): 173-186. DOI:10.1016/j.vetmic.2006.01.009
(  0) 0) |
| [19] |
Sha Y J, Liu M, Wang B, et al. Bacterial population in intestines of Litopenaeus vannamei fed different probiotics or probiotic supernatant[J]. Journal of Microbiology and Biotechnology, 2016, 26(10): 1736-1745. DOI:10.4014/jmb.1603.03078
(  0) 0) |
| [20] |
Huang Z, Li X, Wang L, et al. Changes in the intestinal bacterial community during the growth of white shrimp, Litopenaeus vannamei[J]. Aquaculture Research, 2016, 47(6): 1737-1746. DOI:10.1111/are.12628
(  0) 0) |
| [21] |
Amoah K, Huang Q, Tan B, et al. Dietary supplementation of probiotic Bacillus coagulans ATCC 7050, improves the growth performance, intestinal morphology, microflora, immune response, and disease confrontation of Pacific white shrimp, Litopenaeus vannamei[J]. Fish and Shellfish Immunology, 2019, 87: 796-808. DOI:10.1016/j.fsi.2019.02.029
(  0) 0) |
| [22] |
Huynh T, Hu S, Chiu C, et al. Bacterial population in intestines of white shrimp, Litopenaeus vannamei fed a synbiotic containing Lactobacillus plantarum and galactooligosaccharide[J]. Aquaculture Research, 2019, 50(3): 807-817. DOI:10.1111/are.13951
(  0) 0) |
| [23] |
Hu X, Yang H, Yan Y, et al. Effects of fructooligosaccharide on growth, immunity and intestinal microbiota of shrimp (Litopenaeus vannamei) fed diets with fish meal partially replaced by soybean meal[J]. Aquaculture Nutrition, 2019, 25(1): 194-204.
(  0) 0) |
| [24] |
Duan Y F, Wang Y, Dong H B, et al. Changes in the intestine microbial, digestive, and immune-related genes of Litopenaeus vannamei in response to dietary probiotic Clostridium butyricum supplementation[J]. Front Microbiol, 2018, 9: 2191. DOI:10.3389/fmicb.2018.02191
(  0) 0) |
| [25] |
Hu X, Cao Y, Wen G, et al. Effect of combined use of Bacillus and molasses on microbial communities in shrimp cultural enclosure systems[J]. Aquaculture Research, 2017, 48(6): 2691-2705. DOI:10.1111/are.13101
(  0) 0) |
2. Haidu College, Qingdao Agricultural University, Yantai 265100, China;
3. Qingdao Genyuan Biotech Group, Qingdao 266000, China
 2020, Vol. 50
2020, Vol. 50


