2. 烟台市海洋经济研究院,山东 烟台 264034;
3. 海阳市黄海水产有限公司,山东 烟台 265122
鲟鱼是一类大型而又古老的硬骨鱼类,多数品种和杂交种具有重要的经济价值、营养价值和科研价值[1]。我国的鲟鱼人工养殖产业已经形成了完整的养殖技术[2]。但传统养殖方式对水质要求高、占地多、易受环境因素影响,而工厂化循环水养殖模式可节约水90%以上,实现节能减排、环境友好型生产[3]。生物滤池作为循环水养殖系统(Recirculating aquaculture system,RAS)中水处理单元的核心, 其主要通过硝化细菌的硝化作用将养殖水体中的有机氮、总氨氮(TAN)、亚硝酸氮(NO2--N)等有毒物质转化为低毒性的硝酸氮(NO3--N)[4]。生物过滤器内部的微生物群落结构及组成决定了生物过滤功能的特性和效率,但微生物群落结构复杂,相较于其他水质指标并不容易直接观测,可将现代分子生物学应用到生物滤池的研究中,通过学科交叉来寻求新突破、新发现[5]。黄志涛等[6]通过16S rRNA高通量测序研究了生物滤池内微生物群落结构及多样性,发现池内起硝化作用的主要细菌是亚硝化单胞菌(Nitrosomonas)和硝化螺菌(Nitrospira)。吴越等[7]研究发现细菌群落结构会受磷酸盐、pH等环境因子的影响。现代分子生物学技术的应用正逐步揭开生物净化的神秘面纱。
循环水养殖系统稳定运行期间生物滤池中硝化细菌的数量是动态变化的,但影响其时空分布的主要环境因子目前尚未明确。本研究以杂交鲟(施氏鲟Acipenser schrenckii ♀×西伯利亚鲟Acipenser baerii ♂)循环水养殖系统的四级生物滤池为研究对象,运用16S rRNA高通量测序手段研究微生物的群落结构、种群稳定性以及功能菌在生物滤池中所起的作用。探究循环水养殖系统的生物滤池中微生物群落结构、微生物群落对水质变化的响应及生物滤池的运行参数,为鲟鱼及其他名贵鱼类的循环水养殖系统生物滤池的设计与运行提供技术支撑和理论数据。
1 材料与方法 1.1 养殖系统实验系统位于山东省海阳市黄海水产有限公司7号养殖车间,整个系统由9个养殖池(养殖面积50 m2,有效水深1 m)、转鼓式微滤机、生物滤池、充氧池和紫外线杀菌消毒装置等组成。养殖用水盐度13,日补充水量约占总水量的15%,循环率为8次/d。生物滤池分为四级(1~4级生物滤池),其中2级为MBBR,生物滤料为比表面积600 m2/m3的多孔塑料环,其余3级为固定床,生物滤料为比表面积316 m2/m3的立体弹性填料,均采用自然挂膜。
2019年6月开始鲟鱼养殖,初始养殖密度为42.5 kg/m3,鲟鱼平均体长为(74.58±4.24)cm、平均体质量为(3.87±0.56)kg,鱼体健康状况良好。养殖过程中投喂鲟鱼专用颗粒饲料(升索牌G8饵料,粗蛋白含量44%),每天投饵2次,时间为7:30和16:30,日投喂量为鱼体质量的0.36%。
1.2 水质检测方法实验期间,每5天测定1次各级生物滤池进、出水水质。水温、溶解氧、pH采用YSI多参数水质分析仪于现场检测;总氨氮、亚硝酸氮、硝酸氮、化学需氧量等指标在实验室根据《海洋监测规范第4部分:海水分析》(GB17378.4—2007)操作规范进行检测,每个指标测定3次, 结果取平均值。
1.3 样品采集和高通量测序将四级生物滤池按水流方向依次标为A~D,并在实验第1、11、21、31、41天分别从4个滤池中以五点取样法剪取滤料样品,混合样品约15 g分别放入编号A~D的50 mL取样管中[8],加40 mL无菌水后放入-80 ℃冰箱中保存,并将样品送至上海美吉生物医药科技有限公司在Illumina-MiSeq平台上进行测序分析。
1.4 分析方法使用Microsoft Excel和SPSS 26.0软件对各级生物滤池的水质数据进行统计分析和单因素方差分析。根据Index序列区分各样本的数据,将其以fasta格式保存,利用Qiime(version 1.9.1)对数据进行检测并去除嵌合体序列[9]。利用Uparse软件(version 7.0.1090)按照97%相似性进行OTUs聚类(不含单序列),形成OTUs列表[10]。用RDP Classifier(version 2.11)对OTUs代表序列进行比对分析,在不同分类学水平上注释其群落的物种信息[11]。基于OTU聚类的结果,利用R语言工具计算Shannon和Chao1指数[12],对微生物群落与测定的各环境理化指标进行主成份分析(PCA)和冗余分析(RDA)[13]。
2 结果与分析 2.1 四级生物滤池水处理性能及分析实验期间,循环水养殖系统运行稳定,四级生物滤池进、出水的水质参数如表 1所示,生物滤池进、出水的总氨氮浓度、COD浓度存在显著性差异(P<0.05),水温18.2 ℃、溶解氧6.24 mg/L、pH 7.0。总氨氮、亚硝态氮和化学需氧量的去除率为60.23%、15.56%和33.77%。生物滤池总进水与1、2、3级生物滤池出水的总氨氮浓度依次显著降低(P<0.05),说明前3级生物滤池对氨氮去除效果明显;相反,3级生物滤池出水和生物滤池总出水总氨氮浓度相差不大,即4级生物滤池的氨氮去除率较差;而2级生物滤池出水COD浓度显著低于1级生物滤池出水COD浓度(P<0.05),说明COD的去除主要发生在2级生物滤池。
|
|
表 1 各级生物滤池进、出水的水质参数 Table 1 Water quality parameters of inlet and outlet water at all levels of biological filter |
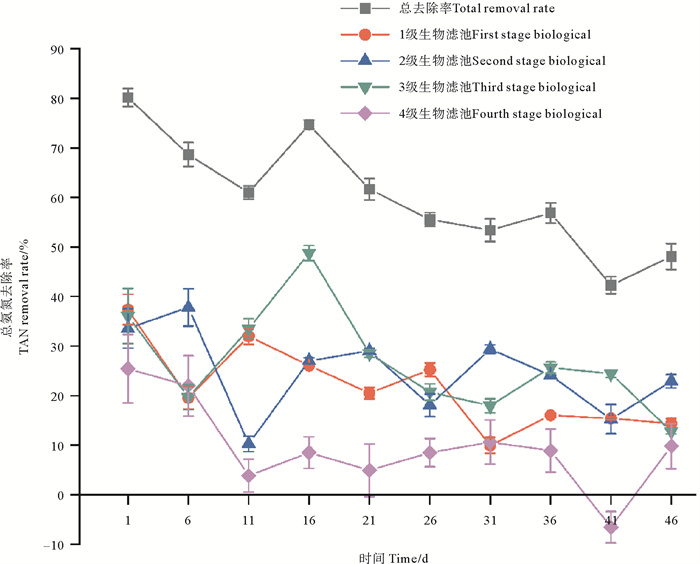
生物滤池总进水的TAN浓度为0.209~0.369 mg/L,总出水的TAN浓度为0.047~0.164 mg/L,TAN总去除率平均为60.23%(见图 1),生物滤池可有效去除养殖水中的氨氮,且水质稳定在一定范围内。其中,1级生物滤池的TAN去除率为21.65%,占总去除率的36.81%;2级生物滤池的TAN去除率为24.74%,占总去除率的31.21%;3级生物滤池的TAN去除率为26.80%;占总去除率的26.00%;4级生物滤池的TAN去除率为9.5%,占总去除率的5.98%。1、2、3级生物滤池对TAN的去除率显著高于4级生物滤池(P < 0.05,见表 2),4级生物滤池对TAN去除效果不明显。
|
图 1 实验期间各级生物滤池TAN去除率 Fig. 1 TAN removal rates of various biofilters during the experiment |
|
|
表 2 各级生物滤池去除率 Table 2 Removal rate of various biological filters |
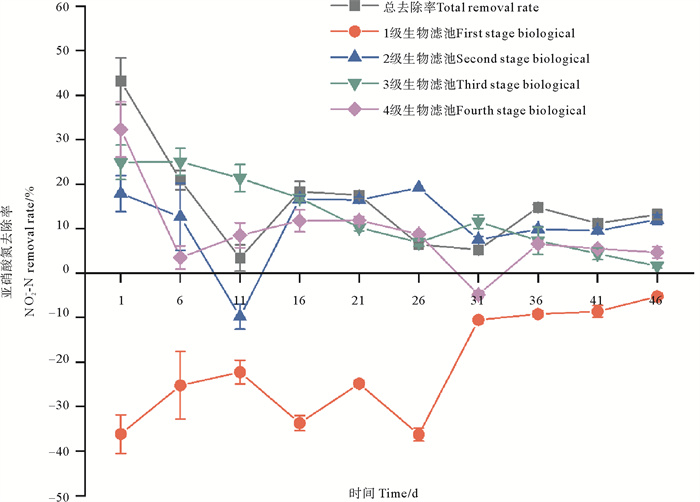
生物滤池进水NO2--N浓度为0.013~0.037 mg/L,经生物滤池水处理后NO2--N浓度降低为0.007~0.032 mg/L,去除率为15.56%。其中,1级生物滤池对亚硝酸氮的去除率显著低于其他3级生物滤池(P<0.05,见表 2)。如图 2所示,1级生物滤池的NO2--N去除率为-21.19%,2级生物滤池的NO2--N去除率为11.20%,3级生物滤池的NO2--N去除率为13.02%,4级生物滤池的NO2--N去除率为9.03%。其中,1级生物滤池NO2--N去除率为负值,即生物滤池内的NO2--N浓度先升高再降低。
|
图 2 实验期间各级生物滤池NO2--N去除率变化 Fig. 2 NO2--N removal rates of various biofilters during the experiment |
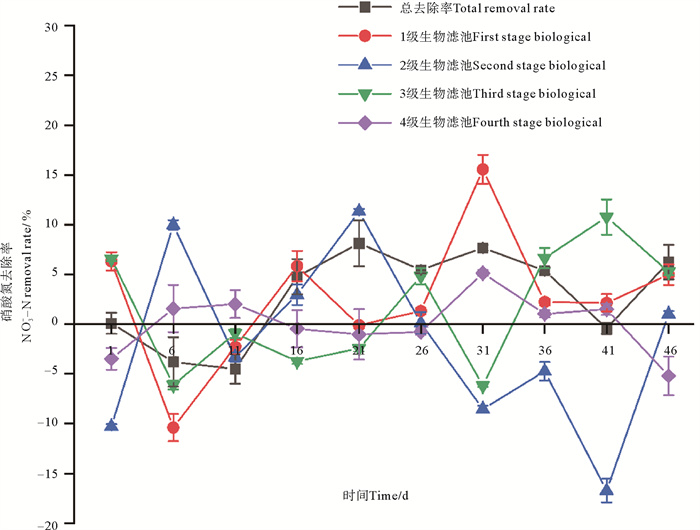
生物滤池进水硝酸氮浓度稳定在11.38~13.93 mg/L,平均为12.63 mg/L;出水浓度在10.76~13.67 mg/L,平均为12.24 mg/L,去除率为2.9%。硝酸氮去除率变化如图 3所示。其中,各级生物滤池间硝酸氮的去除率无显著性差异(P>0.05,见表 2),1级生物滤池的NO3--N去除率为2.56%,2级生物滤池的NO3--N去除率为-1.83%,3级生物滤池的NO3--N去除率为1.47%,4级生物滤池的NO3--N去除率为0.03%。
|
图 3 实验期间各级生物滤池NO3--N去除率变化 Fig. 3 NO3--N removal rates of various biofilters during the experiment |
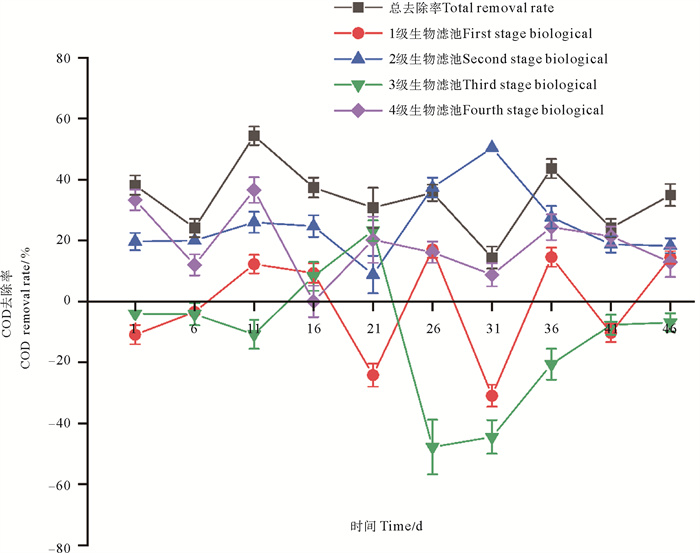
生物滤池总进、出水的COD浓度存在显著性差异(P < 0.05,见表 1),总进水的COD浓度为2.43~4.43 mg/L,出水的COD为1.39~2.88 mg/L,去除率为33.77%。试验期间COD去除率变化如图 4所示。其中,1级生物滤池的COD去除率为-1.21%,2级生物滤池的COD去除率为25.18%,3级生物滤池的COD去除率为-11.49%,4级生物滤池的COD去除率为18.59%。2、4级生物滤池的COD去除率显著高于1、3级生物滤池(P<0.05,见表 2),2、4级生物滤池的COD去除效果更明显。
|
图 4 实验期间各级生物滤池COD去除率变化 Fig. 4 COD removal rates of various biofilters during the experiment |
20个生物膜样品均得到原始序列数和多样性指数(见表 3),样本覆盖率(Coverage)为100%。通过比较5个时间点生物滤池的多样性指数发现,第3个时间点整个生物滤池平均Shannon指数为5.650,高于其他4个时期。微生物群落丰富度和多样性在第3、4、5个时间点时依次降低。
|
|
表 3 微生物群落多样性指数 Table 3 Microbial community diversity index |
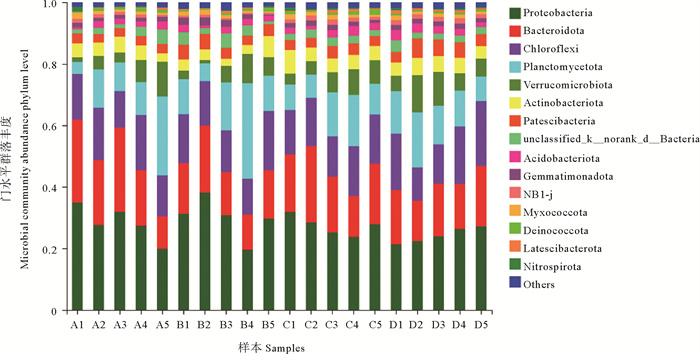
20个生物膜样品中微生物群落结构组成相似(见图 5),微生物主要隶属于37个门,561个属,926个种,其优势菌为变形菌门(Proteobacteria, 19.4%~38.1%)、拟杆菌门(Bacteroidetes, 10.6%~27.3%)、绿弯菌门(Chloroflex,10.7%~21.1%)、浮霉菌门(Planctomycetes,3.9%~30.9%)、疣微菌门(Verrucomicrobiota,1.0%~12.1%),其组成分布在门水平上与先前报道的结果相似[14-16]。
|
( A~D分别表示1~4级生物滤池,1~5分别表示5个取样时间点。图示中unclassified_knorank_dBacteria表示数据库中没有类似序列的一个细菌门。A~D respectively represent 1~4 biological filters, and 1~5 respectively represent 5 sampling time points.In figure unclassified_knorank_dBacteria represents a phylum of bacteria with no similar sequence in the database. ) 图 5 生物滤池微生物在门水平的群落结构 Fig. 5 Community structure of microorganisms in biofilter at phylum level |
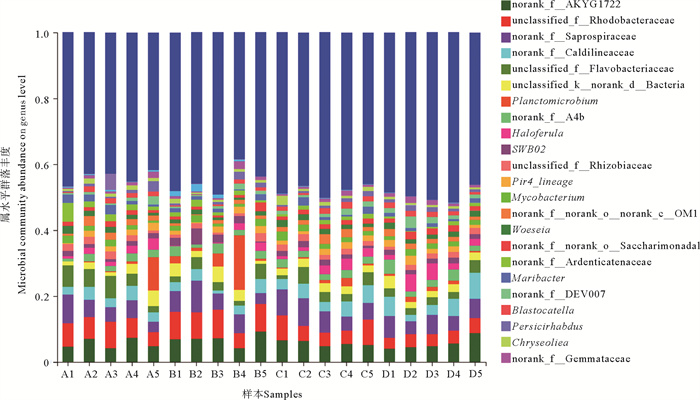
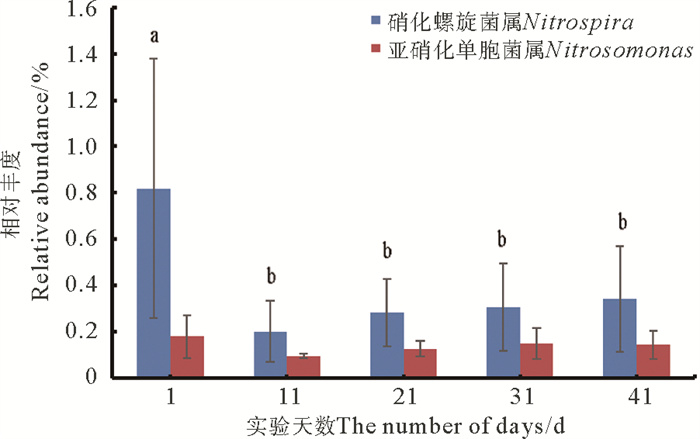
优势菌属(见图 6)分别为:norank_fAKYG1722(4.11%~9.31%)、unclassified_fRhodobacteraceae(3.21%~8.85%)、norank_fSaprospiraceae(3.25%~9.63%)、norank_fCaldilineaceae(0.97%~7.90%)、unclassified_fFlavobacteriaceae(1.10%~6.81%)、unclassified_knorank_dBacteria(0.87%~4.66%)、浮霉菌属(Planctomicrobium,0.048%~16.50%)。它们分别属于AKYG1722科、红杆菌科(Rhodobacteraceae)、腐螺旋菌科(Saprospiraceae)、暖绳菌科(Caldilineaceae)、黄杆菌科(Flavobacteriaceae)等。在生物滤池中起硝化作用的主要细菌是氨氧化细菌和亚硝化细菌[17],此生物滤池中的相关细菌有硝化螺旋菌属(Nitrospira, 0.037%~1.43%)和亚硝化单胞菌属(Nitrosomonas,0.054%~0.21%)细菌。其中,硝化螺旋菌属在时间上相对丰度显著性降低(见图 7),虽然这些菌属的丰度不高,但其是水处理过程中起十分重要作用的功能性细菌[18]。
|
( A~D分别表示1~4级生物滤池,1~5分别表示5个取样时间点。norank表示数据库中没有具体分类学信息;unclassified表示数据库中没有类似序列;f_表示科(Family),o_表示目(Order),c_表示纲(Class),k_表示界(Kingdom),d_表示域(Domain),例如f_Rhodobacteraceae表示红杆菌科。A~D respectively represent 1~4 biological filters, and 1~5 respectively represent 5 sampling time points. Norank indicates that there is no specific taxonomy information in the database; unclassified indicates that there is no similar sequence in the database; f_stands for Family, o_stands for Order, c_stands for Class, k_stands for Kingdomla, d_stands for Domain, for example, f_Rhodobacteraceae stands for Rhodobacteraceae. ) 图 6 生物滤池微生物在属水平的群落结构 Fig. 6 Community structure of microorganisms in biofilter at genus level |
|
( 图中字母不同表示二者之间存在显著性差异(P<0.05)。Different letters in the figure indicate significant differences between the two (P < 0.05). ) 图 7 硝化细菌属水平相对丰度变化 Fig. 7 Changes in relative abundance of Nitrifying bacteria at genus level |
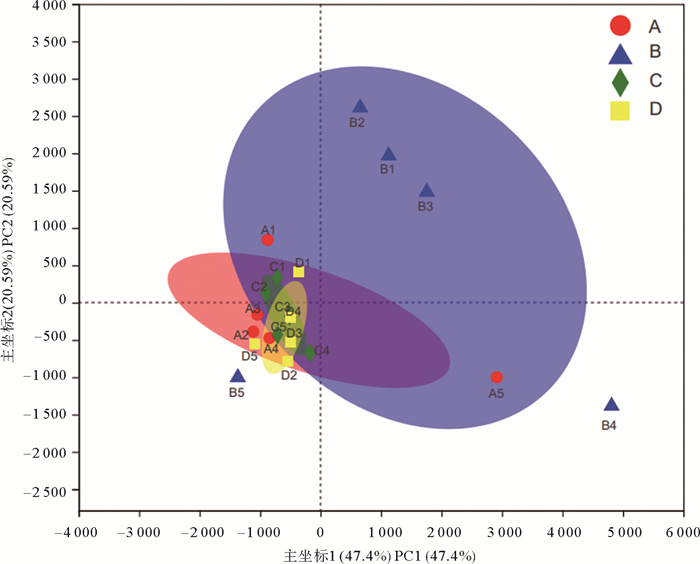
OTU(Operational taxonomic unit)水平PCA分析(见图 8)所示,两轴的总贡献率为67.99%。其中,主坐标1的方差贡献率为47.40%,主坐标2的方差贡献率为20.59%。在空间上,1、3、4级生物滤池各样本点之间的相似度较高,与2级生物滤池样本点之间相似度较低,说明1、3、4级生物滤池中微生物群落有更高的相似性;在时间上,2级生物滤池3个时间点(B1、B2、B3)的相似度较高,与B4、B5之间相似度较低。结果表明,不同样品的微生物群落差异较大,即各级生物滤池中不同时期的微生物群落差异较大。
|
( A~D分别表示1~4级生物滤池,1~5分别表示5个取样时间点。A~D respectively represent 1~4 biological filters, and 1~5 respectively represent 5 sampling time points. ) 图 8 生物滤池微生物群落OTU水平主成分分析 Fig. 8 Principal component analysis of microbial community in biofilter on OTU level |
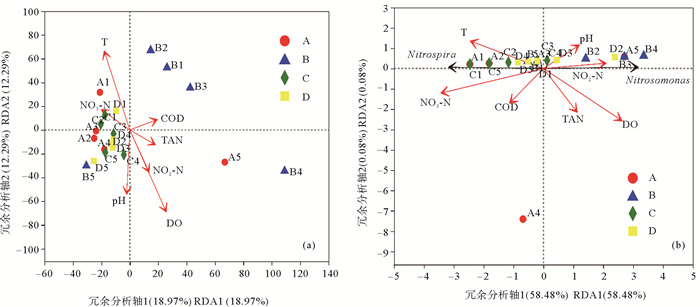
OTU水平微生物群落与水环境因子冗余分析如图 9(a)所示,第一主轴解释比例为18.97%,第二主轴解释比例为12.29%,共解释31.16%的方差变化。采用蒙特卡洛置换检验P<0.05的有:DO(P=0.001)、T(P=0.02)、pH(P=0.027),这3种环境因子是影响微生物OTU分布的关键因子,而其他4种水环境因子:NO2--N(P=0.251)、NO3--N(P=0.584)、TAN(P=0.749)、COD(P=0.763)对细菌OTU分布也会产生一定的影响。本实验系统用水为盐度13的半咸水,故氨氧化细菌主要为亚硝化单胞菌属,而硝化细菌主要为硝化螺旋菌属[19]。因此,以亚硝化单胞菌属和硝化螺旋菌属为例进一步分析环境因子与硝化细菌间的动态响应(见图 9(b))。第一主轴和第二主轴对硝化细菌群落相对丰度方差的解释比例分别为58.48%和0.08%,共解释58.56%的方差变化。在第一主轴上,NO2-N、NO3-N和T是主要的影响因子,相关系数分别为0.999、-0.982和-0.845;第二主轴上COD和TAN是主要影响因子,相关系数分别为-0.861和-0.837。其中,硝化螺旋菌属细菌丰度与NO3-N有较强正相关性,亚硝化单胞菌属细菌丰度与NO2-N有较强正相关性。
|
( A~D分别表示1~4级生物滤池,1~5分别表示5个取样时间点;Nitrospia:硝化螺旋菌属;Nitrosomonas:亚硝化单胞菌属;T:温度;DO:溶解氧浓度;TAN:总氨氮浓度;NO2-N:亚硝酸氮浓度;NO3-N:硝酸氮浓度;COD:化学需氧量。A~D respectively represent 1~4 biological filters, and 1~5 respectively represent 5 sampling time points; Nitrospia: Nitrospia; Nitrosomonas: Nitrosomonas; T: Temperature; DO: Dissolved oxygen concentration; TAN: Total ammonia nitrogen concentration; NO2-N: Nitrite nitrogen concentration; NO3-N: Nitrate nitrogen concentration; COD: Chemical oxygen demand. ) 图 9 微生物群落OTU水平(a)、硝化细菌(b)与水环境因子的冗余分析 Fig. 9 Redundancy analysis of OTU level microbial community(a) and Nitrifying bacteria genera(b) and water environmental factors |
生物过滤作为循环水养殖系统水处理技术的关键环节,对维持循环水养殖系统的稳定性和提高系统的承载力起着十分重要的作用[20]。本研究中4级生物滤池对TAN、NO2--N、NO3--N和COD等主要污染物的平均去除率分别为60.23%、15.56%和2.9%和33.77%,各级生物滤池的去除率存在显著差异(P < 0.05,见表 2)。其中,4级生物滤池TAN去除率显著低于前3级,这可能是由水体经前3级生物滤池处理后TAN浓度降低导致的[21],相关研究[4]表明生物滤池分级过多可能会导致整体运行效率降低;1级生物滤池NO2--N去除率显著低于后三级生物滤池,其原因可能是1级生物滤池内氨化作用明显,氨氮首先转化为亚硝酸氮,亚硝酸氮作为硝化过程的中间产物会有一定的积累;1、3级生物滤池对COD去除率为负值的原因可能与实验期间观察到的生物滤池内微生物膜脱落有关[22]。
微生物群落结构并非一成不变,其在时间和空间上存在一定的变化,可能影响生物滤池的处理效果。在空间上,1、3、4级生物滤池的微生物群落结构有较高的相似性(见图 8),但A5和B4分别与同级滤池样本距离较远,这可能是由于浮霉菌门(Planctomycetes)在A5以及B4的比例明显高于其他时间点(见图 5)。在时间上,以B4、B5为例(见图 6),2级生物滤池内的生物多样性因浮霉菌属(Planctomyces)细菌丰度过高而降低,而后又因浮霉菌属(Planctomyces)细菌丰度减少而升高(见表 3),即2级滤池内微生物群落结构的稳定性为先降低后恢复,多样性高的微生物群落结构更稳定[23]。而微生物群落结构的变化与生物滤池的处理能力存在一定的联系:微生物群落丰富度和多样性降低(见表 3)可能对生物滤池TAN和NO2--N的总去除率呈下降趋势有一定的影响,其中,生物滤池TAN总去除率缓慢下降(见图 1)可能与亚硝化单胞菌属的相对丰度减少有关(见图 7);NO2--N去除效果较差(见图 2)可能与硝化螺菌属的相对丰度显著减少有关(P<0.05,见图 7),若NO2--N持续积累将会破坏鱼体血液中的血红蛋白,导致鱼类缺氧甚至死亡[24, 25]。
微生物群落结构对水质变化存在一定程度的动态响应。试验结果表明,微生物群落结构与溶解氧(DO)、水温(T)和pH呈显著相关性(P<0.05,见图 9(a)),同时也受TAN浓度、NO3--N浓度和COD浓度的影响。秦宇等[26]认为溶解氧浓度过高会抑制厌氧菌的代谢产生, 而溶解氧浓度过低将影响好氧菌的活性。硝化细菌最适温度为30~35 ℃[27],适当升高温度有利于硝化细菌的繁殖,但考虑到养殖对象的适宜水温不宜超过26 ℃[28]。王新为等[29]发现氨氧化细菌更适应于弱碱性的环境,适当提高pH有利于促进氨氧化细菌的生长,这与本研究结果相似。此外,硝化细菌主要还受COD浓度的影响(见图 9(b)),试验结果表明,随着COD浓度的升高,硝化细菌的相对丰度降低,即COD浓度对硝化细菌有一定程度的抑制作用。有研究[30]表明COD浓度越高,对硝化细菌的抑制作用时间越长。在实际生产中,及时清理脱落的生物膜并兼顾生物滤池内COD浓度的日常变化,降低COD浓度有利于增加硝化螺旋菌属、亚硝化单胞菌属等功能性细菌的丰度从而提高生物滤池的水处理效率。
4 结论(1) 本实验发现生物滤池对总氨氮、亚硝酸盐和化学需氧量的去除率分别达到60.23%、15.56%和33.77%,整个过程对亚硝酸氮去除不明显。其中,4级生物滤池进、出水的总氨氮、亚硝酸盐和COD浓度相差不大,相较于前3级生物滤池对氨氮的去除效果不明显,其可能存在功能上的浪费。
(2) 通过高通量测序,本次实验生物滤池中微生物隶属于37个门,100个纲,240个目,369个科和561个属的细菌,其主要为变形菌门、绿弯菌门和拟杆菌门。1、3、4级生物滤池的微生物群落组成相似,且在时间、空间尺度上存在动态变化。
(3) 受生物滤池的水环境因子的影响微生物群落结构并非一成不变,即其对水质变化有一定程度的动态响应。在实际生产中可以合理调节生物滤池内COD浓度来稳定生物滤池运行期的微生物群落结构,增加硝化螺旋菌属、亚硝化单胞菌属细菌的丰度,从而提高生物滤池的水处理效率。
| [1] |
孙大江, 曲秋芝, 张颖, 等. 中国的鲟鱼养殖[J]. 水产学杂志, 2011, 24(4): 67-70. Sun D J, Qu Q Z, Zhang Y, et al. Sturgeon aquaculture in China[J]. Chinese Journal of Fisheries, 2011, 24(4): 67-70. DOI:10.3969/j.issn.1005-3832.2011.04.018 (  0) 0) |
| [2] |
刘晓勇, 李鸶鸶, 赵明军. 中国鲟鱼养殖产业发展战略思考[J]. 中国渔业经济, 2013, 31(6): 69-76. Liu X Y, Li S S, Zhao M J. The aquaculture industry and development strategy of sturgeon in China[J]. Chinese Fisheries Economics, 2013, 31(6): 69-76. DOI:10.3969/j.issn.1009-590X.2013.06.012 (  0) 0) |
| [3] |
张宇雷, 吴凡, 王振华, 等. 超高密度全封闭循环水养殖系统设计及运行效果分析[J]. 农业工程学报, 2012, 28(15): 151-156. Zhang Y L, Wu F, Wang Z H, et al. Engineering design and performance evaluation of super high density recirculating aquaculture system[J]. Transactions of the Chinese Society of Agricultural Engineering, 2012, 28(15): 151-156. (  0) 0) |
| [4] |
柳婷婷, 李丽, 蒋雯雯, 等. 循环水养殖系统六级生物滤池运行效果分析[J]. 环境工程学报, 2019, 13(4): 902-909. Liu T T, Li L, Jiang W W, et al. Performance evaluation of a six-stage bio-filter in recirculating aquaculture system[J]. Chinese Journal of Environmental Engineering, 2019, 13(4): 902-909. (  0) 0) |
| [5] |
宋协法, 李华龙. 养殖污水中主要分解氨氮微生物的分离鉴定[J]. 渔业现代化, 2013, 40(1): 1-6. Song X F, Li H L. Research of nitrifying bacteria from cultivation wastewater[J]. Fishery Modernization, 2013, 40(1): 1-6. (  0) 0) |
| [6] |
黄志涛, 宋协法, 李勋, 等. 基于高通量测序的石斑鱼循环水养殖生物滤池微生物群落分析[J]. 农业工程学报, 2016, 32(S1): 242-247. Huang Z T, Song X F, Li X, et al. Analysis of microbial diversity of submerged biofilters in recirculating aquaculture system(RAS) for grouper(Epinehelus moara) based on high-throughput DNA sequencing[J]. Transactions of the Chinese Society of Agricultural Engineering, 2016, 32(S1): 242-247. (  0) 0) |
| [7] |
吴越, 马建忠, 郑伊诺, 等. 石斑鱼循环水养殖系统微生物群落结构[J]. 中国水产科学, 2017, 24(5): 1045-1054. Wu Y, Ma J Z, Zheng Y N, et al. Analysis of microbial community structure in recirculating aquaculture system for groupers(Epinephelus)[J]. Journal of Fishery Sciences of China, 2017, 24(5): 1045-1054. (  0) 0) |
| [8] |
张皓天, 宋协法, 刘兴震, 等. 斑石鲷循环水养殖系统生物滤池微生物群落对水质变化的动态响应[J]. 环境工程学报, 2020, 14(8): 2176-2185. Zhang H T, Song X F, Liu X Z, et al. Dynamic response of microbial community to water quality change in biofilter for recirculating aquaculture system of Oplegnathus punctatus[J]. Chinese Journal of Environmental Engineering, 2020, 14(8): 2176-2185. (  0) 0) |
| [9] |
Edgar R C. Search and clustering orders of magnitude faster than BLAST[J]. Bioinformatics, 2010, 26(19): 2460. (  0) 0) |
| [10] |
Edgar R. UPARSE: highly accurate OTU sequences from microbial amplicon reads[J]. Nature Methods, 2013, 10(10): 996. (  0) 0) |
| [11] |
Wang Q, Garrity G M, Tiedje J M. Naive Bayesian classifier for rapid assignment of rRNA sequences into the new bacterial taxonomy[J]. Applied and environmental microbiology, 2007, 73(16): 5261-5267. (  0) 0) |
| [12] |
Maughan H, Wang P W, Caballero J D, et al. Analysis of the Cystic Fibrosis Lung Microbiota via Serial Illumina Sequencing of Bacterial 16S rRNA Hypervariable Regions[J]. PLoS One, 2012, 7(10): e45791. (  0) 0) |
| [13] |
唐婧, 徐小蓉, 商传禹, 等. 南明河城区河段细菌多样性与环境因子的关系[J]. 微生物学报, 2015, 55(8): 1050-1059. Tang J, Xu X R, Shang C Y, et al. Association of bacterial diversity in city of Nanming river with enviromental factors[J]. Acta Microbiologica Sinica, 2015, 55(8): 1050-1059. (  0) 0) |
| [14] |
张皓. 养殖环境微生物群落的动态变化及与水环境的互作[D]. 苏州: 苏州大学, 2015. Zhang H. The Dynamic Changes of Microbial Communities in Aquaculture Environment and Interactions with Water Environment[D]. Suzhou: Soochow University, 2015. (  0) 0) |
| [15] |
邱楚雯, 施永海, 王韩信. 暗纹东方鲀不同养殖模式下的微生物群落结构[J]. 水产学报, 2021, 45(2): 209-220. Qiu C W, Shi Y H, Wang H X. Microbial community structure in different cultural patterrns of Talifugu obscures[J]. Journal of Fisheries of China, 2021, 45(2): 209-220. (  0) 0) |
| [16] |
Xin X, Liu S Q, Qin J W, et al. Performances of simultaneous enhanced removal of nitrogen and phosphorus via biological aerated filter with biochar as fillers under low dissolved oxygen for digested swine wastewater treatment[J]. Bioprocess and Biosystems Engineering, 2021, 44(8): 1741-1753. (  0) 0) |
| [17] |
方精云, 沈泽昊, 唐志尧, 等. "中国山地植物物种多样性调查计划"及若干技术规范[J]. 生物多样性, 2004(1): 5-9. Fang J Y, Shen Z H, Tang Z Y, et al. The protocol for the survey plan for plant species diversity of China's Mountains[J]. Biodiversity Science, 2004(1): 5-9. (  0) 0) |
| [18] |
罗国芝, 吴慧芳, 谭洪新. 自养硝化过程去除循环水养殖系统水体中氨氮的研究进展[J]. 淡水渔业, 2019, 49(2): 78-83. Luo G Z, Wu H F, Tan H X. Progress on removing ammonia nitrogen from autotrophicnitrification in recirculating aquaculture system[J]. Freshwater Fisheries, 2019, 49(2): 78-83. (  0) 0) |
| [19] |
Gonzalez-Silva B M, Jonassen K R, Bakke I, et al. Nitrification at different salinities: Biofilm community composition and physiological plasticity[J]. Water Research, 2016, 95: 48-58. (  0) 0) |
| [20] |
傅雪军, 马绍赛, 朱建新, 等. 封闭式循环水养殖系统水处理效率及半滑舌鳎养殖效果分析[J]. 环境工程学报, 2011, 5(4): 745-751. Fu X J, Ma S S, Zhu J X, et al. Analysis of the efficiency of water treatment and the cultured effect of Cynoglossus semilaevis Günther in closed re-circulating aquaculture systems[J]. Chinese Journal of Environmental Engineering, 2011, 5(4): 745-751. (  0) 0) |
| [21] |
刘飞, 胡光安, 韩舞鹰. 水力停留时间、水温与氨氮浓度对浸没式生物滤池氨氮去除速率的效应[J]. 淡水渔业, 2004(1): 3-5. Liu F, Hu G A, Han W Y. Effects of hydraulic retention time, water temperature and ammonia concentration on ammonia nitrogen removal rate in a submerged biofilter[J]. Freshwater Fisheries, 2004(1): 3-5. (  0) 0) |
| [22] |
王海燕, 吴军年, 李兆光, 等. 抑制条件下好氧生物膜模型的建立及模拟[J]. 工业水处理, 2006(12): 63-66. Wang H Y, Wu J N, Li Z G, et al. Establishment and simulation of aerobic bio-film under inhibited conditions[J]. Industrial Water Treatment, 2006(12): 63-66. (  0) 0) |
| [23] |
Cyrus, A. Resource pulses can alleviate the biodiversity-invasion relationship in soil microbial communities[J]. Ecology, 2015, 96(4): 915-926. (  0) 0) |
| [24] |
张晓莹, 么宗利, 来琦芳, 等. 亚硝酸盐胁迫下异育银鲫呼吸代谢生理响应[J]. 海洋渔业, 2018, 40(2): 189-196. Zhang X Y, Yao Z L, Lai Q F, et al. Physiological response of respiration and metabolism in Carassius auratus gibelio under nitrite stress[J]. Marine Fisheries, 2018, 40(2): 189-196. (  0) 0) |
| [25] |
马青山, 李艳. 水产养殖中好氧反硝化细菌的筛选及评价研究进展[J]. 动物营养学报, 2021, 33(1): 20-32. Ma Q S, Li Y. Advances in screening and evaluation of aerobic microbes in aquaculture[J]. Chinese Journal of Animal Nutrition, 2021, 33(1): 20-32. (  0) 0) |
| [26] |
秦宇, 郭劲松, 方芳, 等. 溶解氧及曝停比对单级自养脱氮系统微生物群落结构的影响[J]. 环境科学, 2009, 30(2): 493-498. Qin Y, Guo J S, Fang F, et al. Effect of DO and aeration/ non-aeration ratio on the microbial community structure in one-step SBBR completely autotrophic nitrogen removal process[J]. Environmental Science, 2009, 30(2): 493-498. (  0) 0) |
| [27] |
Herman, Bouwer. Ground water recharge with sewage effluent[J]. Water Science & Technology, 1991, 23(10): 2099-2108. (  0) 0) |
| [28] |
李大鹏, 刘松岩, 谢从新, 等. 水温对中华鲟血清活性氧含量及抗氧化防御系统的影响[J]. 水生生物学报, 2008(3): 327-332. Li D P, Liu S Y, Xie C X, et al. Effects of water temperature on serum content of reactive oxygen species and antioxidant defense system in Chinese sturgen, Acipenser sinensis[J]. Acta Hydrobiologica Sinica, 2008(3): 327-332. (  0) 0) |
| [29] |
王新为, 孔庆鑫, 金敏, 等. pH值与曝气对硝化细菌硝化作用的影响[J]. 解放军预防医学杂志, 2003(5): 319-322. Wang X W, Kong Q X, Jin M, et al. Effect of pH and aeration on nitrification of nitrobacteria[J]. Journal of Preventive Medicine of Chinese People's Liberation Army, 2003(5): 319-322. (  0) 0) |
| [30] |
王春英. 碱度、氨氮负荷和COD对独立硝化的影响[J]. 四川环境, 2009, 28(4): 4. Wang C Y. Effect of basicity, ammonia-N and COD on independent nitrification[J]. Sichuan Environment, 2009, 28(4): 4. (  0) 0) |
2. Yantai Marine Economic Research Institute, Yantai 264034, China;
3. Haiyang Yellow Sea Aquatic Product Limited Company, Yantai 265122, China
 2022, Vol. 52
2022, Vol. 52


