淡水资源短缺是当今社会急需解决的问题之一。近年来,为了更加充分利用水资源,人们研究开发了诸多方法。膜分离技术作为一种节能、环保的新兴技术,具有低消耗、高效率、环境友好、便于模块化放大等优点,在水处理领域受到了广泛的关注。纳滤(NF)是一种操作压力较低的压力驱动膜分离技术,主要用于软化水体,即脱除水体中二价盐,其中纳滤膜是纳滤技术的关键,它的孔径介于超滤(UF)和反渗透(RO)之间,一般在2 nm以下,截留分子量的范围一般在100~500 Da[1-3],在污水处理、苦咸水及海水的淡化、制药、食品工业和饮用水纯化等领域被广泛应用[4-7]。
用于评估膜分离性能的一个重要参数是膜选择性,它量化了目标溶质与进料溶液的其他成分分离的程度。理想的膜可以有效地选择性地去除不需要的溶质,同时保留或富集某些溶质。硫酸盐作为一种重要的化工原料,有必要在化工生产过程中开发一种高效的提纯浓缩方法[8]。例如,在氯碱工业中,去除盐水溶液中的SO42-可以提高电极电流的效率,延长阳极的使用寿命[9]。目前纳滤膜市场主要以哌嗪(Piperazine, PIP)和均苯三甲酰氯(Trimesoyl chloride, TMC)为单体制备的商品化聚酰胺PIP-TMC纳滤膜为主。纳滤膜分离机理通常是由孔道筛分效应和道南(Donnan)效应解释[10-14]。在商品化聚酰胺NF膜制备过程中,以NF270为例,由于TMC反应不完全,膜表面大量未反应的酰氯基团会在水中水解为羧酸,使得膜表面带有大量的负电荷。根据Donnan效应,该膜对SO42-有较好的截留效果。但是由于过于较小的孔径以及表面过高的电荷密度,使得其对单价盐(NaCl)的截留率50%,二价/一价阴离子选择性仅为1.9[15]。因此,亟需制备一种能够兼具优异的二价/一价阴离子选择性和良好的水通量的NF膜。
近年来,许多报道的文献正致力于这一工作。Zhang等[16]设计了聚多巴胺/聚乙二醇纳米胶囊作为PIP与TMC界面聚合法制备纳滤膜的填料。纳米胶囊的内腔可以作为额外的水输送通道,从而降低对NaCl的截留,Na2SO4/NaCl选择性为4.4。Xiao等[17]以聚醚砜为基膜,通过PIP和TMC的界面聚合制备聚酰胺纳滤膜,再通过6 h的氨基酸离子液体的后修饰改性,使纳滤膜的孔径变大,增加其对二价/一价阴离子的选择性和通量。Ji等[18]提出一步法将两性离子胺分子与多巴胺通过氧化聚合法制备一种新型两性离子多巴胺纳米颗粒,然后在多孔支撑层上进行界面聚合制备了纳滤膜。该两性离子多巴胺颗粒与聚酰胺之间产生较松的交联结构和额外的界面空间,增加了膜的孔径,减小了对NaCl的截留率,Na2SO4/ NaCl选择性为4.5。Liu等[19]通过改变PIP浓度,使PIP-TMC膜表面负电密度降低,对Cl-道南排斥减弱,从而使膜对NaCl截留率降低了6%。然而这些方法均过于复杂,大大增加了其工业化生产的难度。因此需要一种制备方法简单,兼具优异的二价/一价阴离子选择性和良好的水通量的NF膜,该膜可能具有较大的孔径以及较低膜表面的负电密度等特性。
本文分别以二元胺PIP和二元酰氯对苯二甲酰氯(Terephthaloyl chloride, TPC)为水相、有机相单体,通过界面聚合在聚砜(Polysulfone, PSf)基膜上制备了由PIP-TPC线性聚合物交织而成聚酰胺纳滤膜,以此来构建具有更大孔径尺寸的PIP-TPC皮层。此外,与TMC相比,TPC分子只有两个酰氯基团,界面聚合后膜表面未反应的酰氯基团减少,因此由酰氯基团水解的羧基减少[20],这会降低膜表面的负电密度。通过红外、扫描电镜及Zeta电位等对膜的结构和理化性质进行表征,同时考察了TPC浓度对膜性能的影响,并与传统的PIP-TMC纳滤膜进行对比,以期制备的膜具兼具优异的二价/一价阴离子选择性和良好的水通量。
1 实验部分 1.1 试剂及材料聚砜(PSf)超滤膜(切割分子量50 000 Da),国初科技(厦门)有限公司;哌嗪(PIP, 99.0%),对苯二甲酰氯(TPC,99.0%),均苯三甲酰氯(TMC,99.0%),美国Sigma-Aldrich公司;硫酸钠(Na2SO4,99.0%),正己烷(98.0%),丙三醇(99.0%),聚乙二醇-200(PEG-200,99.0%),麦芽糖(99.0%),聚乙二醇-600(PEG-600,99.0%),国药集团化学试剂有限公司;氯化钠(NaCl,99.0%),天津市鼎盛鑫化工有限公司;去离子水,实验室自制。
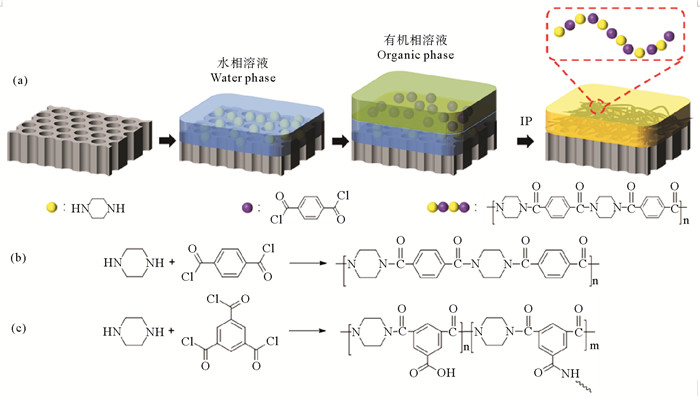
1.2 聚酰胺纳滤膜的制备图 1是复合纳滤膜制备的流程图。首先,将用去离子水冲洗过的PSf超滤基膜固定在聚四氟乙烯模具中。在晾干基膜表面残留的水分后,将0.1 wt% PIP的水相溶液倒在PSf超滤基膜上,浸泡2 min,然后将水相溶液倒掉,并用橡胶滚筒除去膜表面多余的水相溶液。随后将含有一定质量分数的TPC或TMC的正己烷溶液倒在PSf基膜上界面聚合1 min。除去表面多余的有机相溶液后,将界面聚合反应后的膜放入80 ℃的烘箱中热固化1 min。最后用正己烷清洗膜表面以去除未反应的有机相单体,将制备的纳滤膜保存在去离子水中直至使用。以TPC和TMC为有机相单体制备的纳滤膜分别记为PIP-TPC和PIP-TMC。
|
图 1 (a) PIP-TPC膜制备的流程示意图;(b)PIP-TPC纳滤膜聚酰胺层结构式;(c) PIP-TMC纳滤膜聚酰胺层结构式 Fig. 1 (a) Schematic of the fabrication process for PIP-TPC NF membranes by IP; (b) Structure of the PA layer of PIP- TPC NF membranes; (c) Structure of the PA layer of PIP- TMC NF membranes |
采用傅里叶变换红外光谱仪(FTIR,Tensor,德国布鲁克仪器公司)表征PSf基膜和PIP-TPC复合纳滤膜表面的化学结构和组成;采用扫描电子显微镜(SEM,S4800,日本日立公司)表征PSf基膜和PIP-TPC复合纳滤膜的表面形貌;采用流动电位测试仪(Zeta,SF-SD,杭州赛菲膜分离有限公司)在pH=7时,表征膜的表面电位;采用水接触角测试仪(DSA100,德国克吕士公司)表征膜表面的亲疏水性。
膜的切割分子量(Molecular weight cut-off, MWCO)是通过测定丙三醇(94 Da)、聚乙二醇(200 Da)、麦芽糖(340 Da)和聚乙二醇(600 Da)等中性溶质分子的截留率确定的。切割分子量定义为纳滤膜对中性溶质分子截留率为90.0%时,对应的溶质相对分子质量。进料液中性溶质分子浓度为50 mg·L-1。测试过程与膜分离性能评价相同(见1.4)。中性溶质分子截留率根据公式(1)计算:
| $ R = \frac{{{C_{\rm{f}}} - {C_{\rm{p}}}}}{{{C_{\rm{f}}}}} \times 100\% 。$ | (1) |
其中:Cf和Cp分别为进料液和渗透液中中性溶质分子的浓度(mg·L-1),中性溶质分子的浓度由总有机碳分析仪(TOC)测定。
在测试膜的切割分子量的基础上,对膜进行孔径分析。平均几何半径(μs)定义为中性溶质截留率为50%时对应的斯托克斯(Stokes)半径。几何标准偏差(σg)是根据中性溶质截留率为84.13%和50%时对应的Stokes半径之比计算得出。忽略中性溶质与膜孔之间的相互作用,平均有效孔半径(μp)和几何标准差(σp)被视为与μs和σg相同,通过公式(2)对孔径分布与溶质斯托克斯半径的关系进行数学拟合[21]。
| $ \frac{{{\rm{d}}R\left( {{r_{\rm{p}}}} \right)}}{{{\rm{d\, }}{r_{\rm{p}}}}} = \frac{1}{{{r_{\rm{p}}}\ln {\sigma _{\rm{p}}}\sqrt {2{\rm{ \mathit{ π} }}} }}\exp \left[ { - \frac{{{{\left( {\ln {r_{\rm{p}}} - \ln {\mu _{\rm{p}}}} \right)}^2}}}{{2{{\left( {\ln {\sigma _{\rm{p}}}} \right)}^2}}}} \right]。$ | (2) |
其中rp是膜的平均孔径。
1.4 膜分离性能评价通过实验室自制的错流纳滤装置来测试膜的性能,膜的测试有效面积为11.34 cm2,室温稳定在25 ℃。在0.8 MPa测试压力下,使用实验室自制去离子水进行预压30 min,将聚酰胺层压实后,改为0.6 MPa的测试压力,通过公式(3)来评估膜的纯水通量:
| $ J = \frac{Q}{{A \times \Delta t}}。$ | (3) |
其中:Q为一定压力一定过滤时间下渗透过膜的水的体积(L);A为膜的有效面积(m2);Δt为接取渗透液的时间(h)。
膜的截留率以去离子水配置的浓度为2 000 mg·L-1NaCl和Na2SO4的进料液进行测试,通过公式(4)来评估膜的截留率:
| $ R = \frac{{{C_{\rm{f}}} - {C_{\rm{p}}}}}{{{C_{\rm{f}}}}} \times 100\% 。$ | (4) |
其中Cf和Cp分别为进料液和渗透液中NaCl和Na2SO4的电导率(μs/cm)。
通过公式(5)来计算膜的离子选择性:
| $ S\left( {{\rm{N}}{{\rm{a}}_{\rm{2}}}{\rm{S}}{{\rm{O}}_{\rm{4}}}/{\rm{NaCl}}} \right) = {R_{{\rm{N}}{{\rm{a}}_{\rm{2}}}{\rm{S}}{{\rm{O}}_{\rm{4}}}}}/{R_{{\rm{NaCl}}}}。$ | (5) |
其中RNa2SO4和RNaCl由公式(4)计算可得。
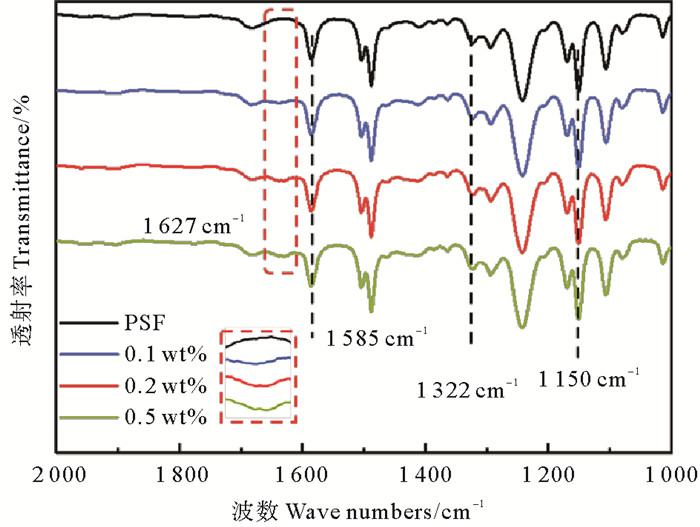
2 结果与讨论 2.1 膜结构及性质表征图 2是PSf基膜和PIP与不同浓度的TPC制备的纳滤膜的傅里叶红外谱图。聚砜基膜分别在1 585和1 322 cm-1处出现PSf的O=S=O不对称伸缩振动强吸收的特征峰,在1 150 cm-1处出现聚砜的O=S=O对称伸缩振动的强吸收[22-24];界面聚合之后,在1 627 cm-1处出现了新的吸收峰,对应着酰胺I带中C=O键伸缩振动峰[25],这归因于PIP中的-NH-与TPC中的-COCl-反应生成的酰胺键-CON-,这表明PIP和TPC成功的在聚砜基膜上发生界面聚合形成了聚酰胺层。此外,随着TPC浓度的提高,酰胺键的特征峰吸收强度也不断增加,表明酰胺键的含量增加。
|
( TPC浓度为0.1 wt%、0.2 wt%、0.5 wt%。TPC concentration are 0.1 wt%, 0.2 wt%, 0.5 wt%. ) 图 2 PSf基膜和PIP-TPC纳滤膜的傅里叶红外谱图 Fig. 2 Fourier transform infrared spectrum of PSf substrate and PIP-TPC composite nanofiltration membrane |
图 3为不同有机相浓度的PIP-TPC纳滤膜和PIP-TMC纳滤膜的SEM图。图 3(a)~(e)为不同TPC浓度的PIP-TPC纳滤膜表面形貌变化。当TPC浓度为0.1 wt%时,聚砜基膜表面未被PIP-TPC皮层完全覆盖,表明当TPC浓度较低时,反应生成的低聚物数量较少,无法形成连续的聚酰胺层,膜表面存在缺陷。当TPC浓度的增加到0.2 wt%时,膜表面与PIP-TMC膜表面相似的结节状形貌。这是因为在界面聚合的过程中,反应发生在有机相一侧,PIP扩散到有机相中与TPC和TMC反应造成的[26]。与PIP-TMC纳滤膜相比,PIP-TPC纳滤膜表面较为光滑,这是因为TPC酰氯基团较少,与PIP的反应相对温和。随着TPC浓度继续增加,膜表面的结节变大,逐渐出现团聚现象。这是因为,TPC浓度增加,与PIP的反应加剧,生成的线性聚合物链大量重叠堆积。

|
( (a)0.1 wt%;(b)0.2 wt%;(c)0.3 wt%;(d)0.4 wt%;(e)0.5 wt%;(f)PIP-TMC。) 图 3 不同TPC浓度的PIP-TPC纳滤膜和PIP纳滤膜的SEM形貌图 Fig. 3 SEM morphologies of PIP-TPC with different TPC concentrations |
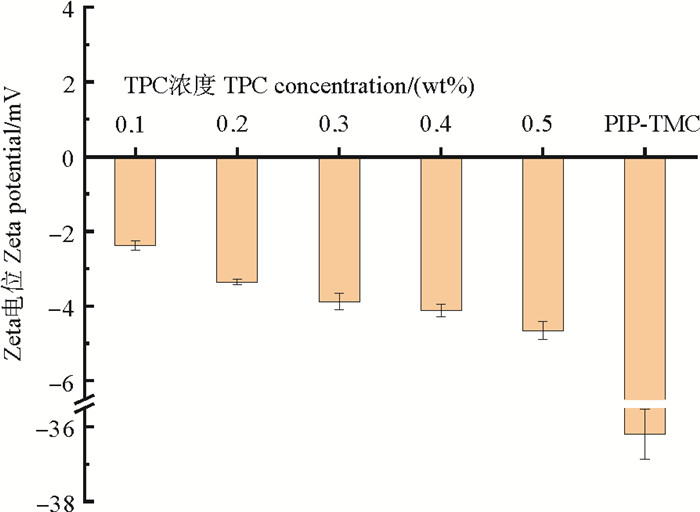
图 4为在pH=7的条件下PIP-TPC纳滤膜表面的Zeta电位,这是由于分离性能测试的进料液是pH=7的盐溶液。从图中可以看出,PIP-TPC是典型的负电纳滤膜,这是因为界面聚合后,TPC中未反应的酰氯基团会水解成羧基,使膜表面表现出负电的特性。由于Donnan效应,膜表面的负电荷会对阴离子产生排斥作用,阴离子的价态越高,受到的排斥作用越强,这有助于对二价阴离子SO42-的截留,同时为了保持溶液呈现电中性,Na2SO4中的Na+会被一同截留。在相同测试条件下与传统的PIP-TMC纳滤膜相比,PIP-TPC纳滤膜表面呈现出较弱的电负性,这是因为TPC是二元酰氯,在和PIP进行充分界面聚合反应后,会生成线性的聚合物,只有末端会发生未反应的酰氯水解为羧基,因此膜表面的负电密度较低。而三元酰氯TMC和PIP,界面聚合会生成网络状聚合物链,这使得膜表面会残留大量未反应的酰氯,从而产生高负电密度的表面。随着TPC浓度的提高,膜表面未反应的酰氯基团增加,膜表面的负电荷密度不断升高[27-28]。较高的负电密度,会加强对Cl-道南排斥作用,不利于NaCl的渗透[17]。因此,高浓度的TPC可能不适合制备高二价/一价阴离子分离性能的纳滤膜。
|
图 4 不同TPC浓度(0.1 wt%~0.5 wt%)的PIP-TPC纳滤膜和PIP-TMC膜在pH=7时Zeta电位图 Fig. 4 Zeta potential diagram of PIP-TPC composite nanofiltration membranes with different TPC concentrations (0.1 wt%~0.5 wt%) and PIP-TMC membrane at pH=7 |
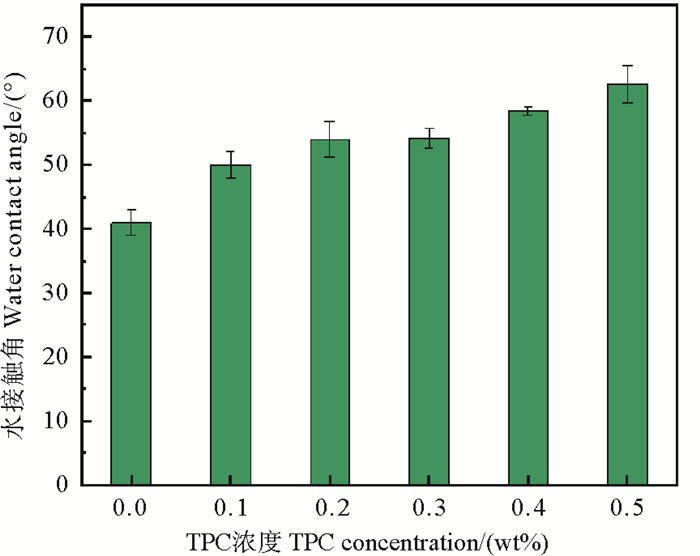
图 5为PSf基膜和不同浓度的PIP-TPC复合纳滤膜的接触角。在TPC膜制备浓度下,PIP-TPC纳滤膜的接触角在50(°)~60(°)范围内。随着TPC浓度增大,PIP-TPC纳滤膜的接触角逐渐变大,这是因为更多TPC分子参与了界面聚合反应,TPC分子内苯环基团的疏水性增大了膜表面接触角[29]。膜表面接触角的增大不利于水通量的提高,因此,高浓度TPC有可能不利于制备高性能纳滤膜。
|
图 5 PSf基膜和不同浓度TPC(0.1 wt%~0.5 wt%)的PIP-TPC复合纳滤膜的接触角 Fig. 5 Contact angle between PSf substrate and PIP-TPC composite nanofiltration membrane with different TPC concentrations (0.1 wt%~0.5 wt%) |
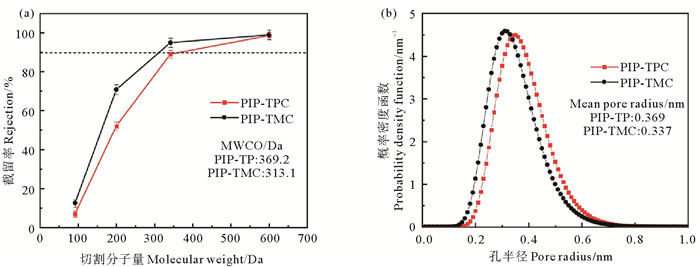
为了探究不同有机单体对膜孔结构的影响,因此进一步分析了PIP-TPC膜和PIP-TMC膜的切割分子量(MWCO)和孔径分布。用不同分子量的中性有机溶质测定MWCO,当溶质截留率为90%时得到MWCO。如图 6(a)所示,PIP-TPC膜和PIP-TMC膜的MWCO分别为369.2和313.1 Da。根据图 6(a)中的数据,计算膜对中性溶质截留率分别为50%和84.13%的相对分子质量以及与之对应的Stokes半径,得到PIP-TPC膜和PIP-TMC膜的孔径分布(见图 6(b))。PIP-TPC膜和PIP-TMC膜的平均孔径分别为0.369和0.337 nm。PIP-TPC膜具有更大孔尺寸,这是因为PIP和TPC界面聚合生成的线性聚合物链间相互交织缠绕构建了相对疏松的PIP-TPC皮层。较大的孔径有利于NaCl的渗透。同时PIP-TPC膜的平均孔径小于SO42-(水合半径为0.379 nm[30]),这使得PIP-TPC膜在孔径略大的情况下,依然对SO42-具有较高截留率(见2.2)。
|
图 6 最优条件PIP-TPC膜和PIP-TMC膜的MWCO(a)和孔径分布(b) Fig. 6 MWCO (a) and pore size distribution curves (b) of the optimal PIP-TPC and PIP-TMC membranes |
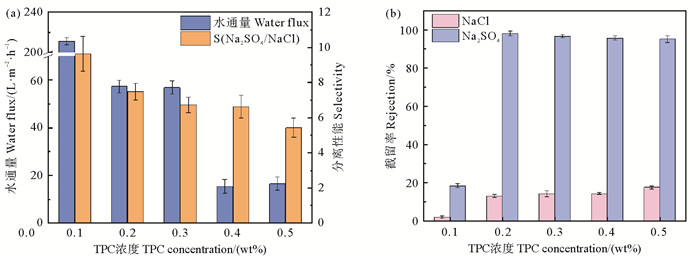
图 7为不同TPC浓度PIP-TPC复合纳滤膜的分离性能。当TPC浓度为0.1 wt%时,由于低浓度下反应生成的聚酰胺层没有完全覆盖PSf基膜,PIP-TPC膜表面存在缺陷,不具有截留性能,这与SEM的结果一致。随着TPC浓度增加,膜表面的聚酰胺层逐渐完整。当TPC浓度为0.2 wt%时,制备的膜具有最佳分离性能,对Na2SO4的截留率98.2%,对NaCl的截留率仅13.1%,Na2SO4/ NaCl选择性为7.5,纯水通量为57.3 L·m-2·h-1。随着TPC浓度继续提高,纯水通量大幅度下降,对NaCl的截留率提高,选择性下降,这是因为TPC浓度提高后,界面聚合反应加剧,线性聚合物链出现大量堆积,重叠,使聚酰胺层孔径减少,厚度增加。较小的孔径会增加对NaCl的截留率,较厚的皮层不利于水的渗透。
|
图 7 (a) TPC浓度对膜水通量和选择性的影响;(b) TPC浓度对膜截留率的影响 Fig. 7 (a) Effect of TPC concentration on water flux and selectivity of PIP-TPC membranes; (b) Effect of TPC concentration on rejection of PIP-TPC membranes |
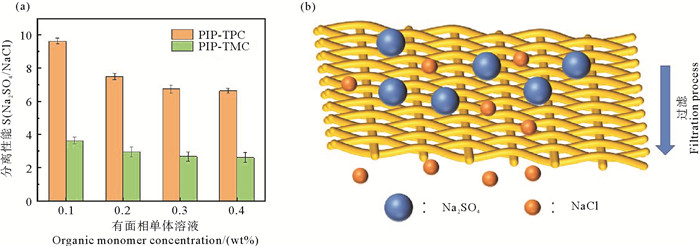
如图 8(a)所示,在相同的制备条件下,PIP-TPC纳滤膜和PIP-TMC纳滤膜的选择性存在很大的差异,相同浓度下PIP-TPC纳滤膜在保持二价盐高截留率的同时,对一价盐具有更低的截留率,因而表现出优异的选择性,而PIP-TMC纳滤膜始终对一价盐有着较高的截留率,选择性较差。这可以通过筛分效应和Donnan效应来进行解释。PIP和TPC都只有两个反应基团,界面聚合形成线性聚合物,线性聚合物链间相互交织缠绕构建了具有较大孔径尺寸的PIP-TPC皮层,减少对NaCl的截留,但孔径小于SO42-的水合半径,依然可以保持对二价阴离子的高截留率,如图 8(b)所示。另一方面,相较于PIP-TMC纳滤膜,PIP-TPC纳滤膜表面负电荷较弱,对Cl-的道南排斥效应减弱, 有利于NaCl的渗透[19],膜表面的负电荷使膜仍对二价阴离子有较强的排斥作用。因此PIP-TPC膜对二价阴离子和一价阴离子具有更高的选择性。
|
图 8 不同有机相浓度(0.1~0.4 wt%)PIP-TPC膜的选择性和PIP-TMC膜的选择性(a)及PIP-TPC纳滤膜过滤过程示意图(b) Fig. 8 Selectivity of PIP-TPC membrane and PIP-TMC membrane at different organic phase concentrations (0.1 wt%~0.4 wt%)(a), and Schematic diagram of PIP-TPC nanofiltration membrane filtration process (b) |
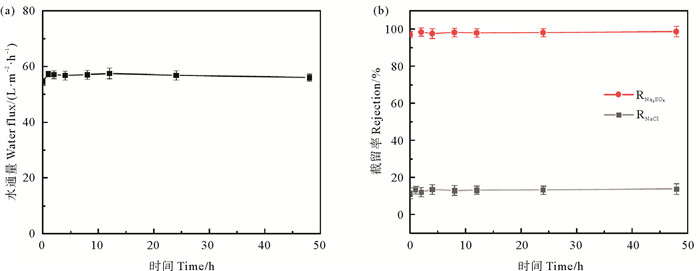
除了水通量、截留率和选择性外,纳滤膜在长时间运行的稳定性也是评价膜性能的重要因素。图 9为PIP-TPC膜48 h运行稳定性测试结果,选取运行时间为0、1、2、4、8、12、24和48 h时进行取样测试。如图 9(a)所示,PIP-TPC膜水通量呈现先略微上升后逐渐稳定的趋势。这是因为测试初期,PIP-TPC皮层较厚,增加了水渗透通过膜的阻力,水通量略低。随着运行测试时间的增加,聚酰胺层被压实,膜厚度减小,跨膜压差降低,使得水通量增加,由54.5 L·m-2·h-1增加到57.6 L·m-2·h-1。运行时间继续增加,水通量趋于稳定。如图 9(b)所示,PIP-TPC膜对Na2SO4和NaCl截留率基本趋于稳定,截留率分别为98.0%和14.2%。膜的水通量和盐截留率在48 h运行测试中,变化在5%以内,证明膜的长时间运行稳定性良好。
|
( (a)水通量;(b)截留率。(a)Water flux; (b)Rejection. ) 图 9 最优制备条件下PIP-TPC膜48h运行稳定性测试 Fig. 9 Stability test of PIP-TPC membrane under optimal preparation conditions for 48h operation |
本文以PIP和TPC分别为水相单体和有机相单体,在PSf基膜上进行界面聚合,生成的线性聚合物链间相互交织缠绕构建了具有较大孔径和较低负电密度的聚酰胺纳滤膜。此外通过各种表征和调控TPC的浓度,来探究PIP-TPC复合纳滤膜的分离性能。当TPC浓度为0.2 wt%时,PIP-TPC纳滤膜具有最优性能,纯水通量为57.3 L·m-2·h-1,对Na2SO4的截留率为98.2%,对NaCl的截留率仅13.1%,Na2SO4/NaCl选择性为7.5,较传统商业聚酰胺纳滤膜PIP-TMC提高了158.6%,并在48 h运行测试中具有较好的稳定性。本研究对二元酰氯TPC与二元胺PIP之间的界面聚合,进行系统的探究,提出了可以制备高二价/一价阴离子选择性纳滤膜的方法,且方法简单,有望满足工业化生产需求。
| [1] |
Tul M S, Kausar A, Siddiq M. Advances in polymeric nanofiltration membrane: A review[J]. Polymer-Plastics Technology and Engineering, 2017, 56(8): 841-856. DOI:10.1080/03602559.2016.1233562 (  0) 0) |
| [2] |
Oatley-Radcliffe D L, Walters M, Ainscough T J, et al. Nanofiltration membranes and processes: A review of research trends over the past decade[J]. Journal of Water Process Engineering, 2017, 19: 164-171. DOI:10.1016/j.jwpe.2017.07.026 (  0) 0) |
| [3] |
Labban O, Liu C, Chong T H, et al. Fundamentals of low-pressure nanofiltration: Membrane characterization, modeling, and understanding the multi-ionic interactions in water softening[J]. Journal of Membrane Science, 2017, 521: 18-32. DOI:10.1016/j.memsci.2016.08.062 (  0) 0) |
| [4] |
Van der B, Vandecasteele C. Removal of pollutants from surface water and groundwater by nanofiltration: Overview of possible applications in the drinking water industry[J]. Environmental Polluton, 2003, 122: 435-445. DOI:10.1016/S0269-7491(02)00308-1 (  0) 0) |
| [5] |
Buonomenna M G, Bae J. Organic solvent nanofiltration in pharmaceutical industry[J]. Separation and Purification Reviews, 2015, 44(2): 157-182. DOI:10.1080/15422119.2014.918884 (  0) 0) |
| [6] |
Röhricht M, Krisam J, Weise U, et al. Elimination of carbamazepine, diclofenac and naproxen from treated wastewater by nanofiltration[J]. Clean-Soil, Air, Water, 2009, 37(8): 638-641. DOI:10.1002/clen.200900040 (  0) 0) |
| [7] |
Sereewatthanawut I, Boam A T, Livingston A G. Polymeric membrane nanofiltration and its application to separations in the chemical industries[J]. Macromolecular Symposia, 2008, 264(1): 184-188. DOI:10.1002/masy.200850429 (  0) 0) |
| [8] |
Liu Meihong, Yu Sanchuan, Zhou Yong, et al. Study on the thin-film composite nanofiltration membrane for the removal of sulfate from concentrated salt aqueous: Preparation and performance[J]. Journal of Membrane Science, 2008, 310(1-2): 289-295. DOI:10.1016/j.memsci.2007.11.002 (  0) 0) |
| [9] |
Fane A G, Wang R, X Hu M. Synthetic membranes for water purification: Status and future[J]. Angewandte Chemie International Edition Engl, 2015, 54(11): 3368-3386. DOI:10.1002/anie.201409783 (  0) 0) |
| [10] |
Anderson J L, Quinn J A. Restricted transport in small pores: A model for steric exclusion and hindered particle motion[J]. Biophysical Journal, 1974, 14(2): 130-150. DOI:10.1016/S0006-3495(74)70005-4 (  0) 0) |
| [11] |
Paul D. Reformulation of the solution-diffusion theory of reverse osmosis[J]. Journal of Membrane Science, 2004, 241(2): 371-386. DOI:10.1016/j.memsci.2004.05.026 (  0) 0) |
| [12] |
Wesolowska K, Koter S, Bodzek M. Modelling of nanofiltration in softening water[J]. Desalination, 2004, 162: 137-151. DOI:10.1016/S0011-9164(04)00037-2 (  0) 0) |
| [13] |
Ren T, Han L, Liu R, et al. Influence of inorganic salt on retention of ibuprofen by nanofiltration[J]. Separation and Purification Technology, 2017, 189: 382-388. DOI:10.1016/j.seppur.2017.08.035 (  0) 0) |
| [14] |
Childress A E, Elimelech M. Relating nanofiltration membrane performance to membrane charge (electrokinetic) characteristics[J]. Environmental Science & Technology, 2000, 34(17): 3710-3716. (  0) 0) |
| [15] |
Ang M B M Y, Tang C L, De Guzman M R, et al. Improved performance of thin-film nanofiltration membranes fabricated with the intervention of surfactants having different structures for water treatment[J]. Desalination, 2020, 481: 114352. DOI:10.1016/j.desal.2020.114352 (  0) 0) |
| [16] |
Zhang L, Zhang M, Lu J, et al. Highly permeable thin-film nanocomposite membranes embedded with PDA/PEG nanocapsules as water transport channels[J]. Journal of Membrane Science, 2019, 586: 115-121. (  0) 0) |
| [17] |
Xiao H F, Chu C H, Xu W T, et al. Amphibian-inspired amino acid ionic liquid functionalized nanofiltration membranes with high water permeability and ion selectivity for pigment wastewater treatment[J]. Journal of Membrane Science, 2019, 586: 44-52. DOI:10.1016/j.memsci.2019.05.038 (  0) 0) |
| [18] |
Ji Y L, Qian W J, An Q F, et al. Mussel-inspired zwitterionic dopamine nanoparticles as building blocks for constructing salt selective nanocomposite membranes[J]. Journal of Membrane Science, 2019, 572: 140-151. DOI:10.1016/j.memsci.2018.11.019 (  0) 0) |
| [19] |
Liu Y L, Zhao Y Y, Wang X M, et al. Effect of varying piperazine concentration and post-modification on prepared nanofiltration membranes in selectively rejecting organic micropollutants and salts[J]. Journal of Membrane Science, 2019, 582: 274-283. (  0) 0) |
| [20] |
Hilal N, Al-Zoubi H, Darwish N A, et al. A comprehensive review of nanofiltration membranes: Treatment, pretreatment, modelling, and atomic force microscopy[J]. Desalination, 2004, 170(3): 281-308. DOI:10.1016/j.desal.2004.01.007 (  0) 0) |
| [21] |
Wang K, Chung T. Fabrication of polybenzimidazole (PBI) nanofiltration hollow fiber membranes for removal of chromate[J]. Journal of Membrane Science, 2006, 281(1-2): 307-315. (  0) 0) |
| [22] |
Xu X X, Zhou C L, Zeng B R, et al. Structure and properties of polyamidoamine/polyacrylonitrile composite nanofiltration membrane prepared by interfacial polymerization[J]. Separation and Purification Technology, 2012, 96: 229-236. (  0) 0) |
| [23] |
An Q F, Sun W D, Zhao Q, et al. Study on a novel nanofiltration membrane prepared by interfacial polymerization with zwitterionic amine monomers[J]. Journal of Membrane Science, 2013, 431: 171-179. DOI:10.1016/j.memsci.2012.12.043 (  0) 0) |
| [24] |
Setiawan L, Wang R, Li K, et al. Fabrication and characterization of forward osmosis hollow fiber membranes with antifouling NF-like selective layer[J]. Journal of Membrane Science, 2012, 394-395: 80-88. (  0) 0) |
| [25] |
Davood A F M H, Hua D, Chung T S. Cross-linked mixed matrix membranes consisting of carboxyl-functionalized multi-walled carbon nanotubes and P84 polyimide for organic solvent nanofiltration (OSN)[J]. Separation and Purification Technology, 2017, 186: 243-254. (  0) 0) |
| [26] |
Xu L, Xu J, Shan B, et al. Novel thin-film composite membranes via manipulating the synergistic interaction of dopamine and m-phenylenediamine for highly efficient forward osmosis desalination[J]. Journal of Materials Chemistry A, 2017, 5(17): 7920-7932. (  0) 0) |
| [27] |
Ahmad A L, Ooi B S, Wahab Mohammad A, et al. Effect of constricted polymerization time on nanofiltration membrane characteristic and performance: A study using the Donnan Steric Pore Flow Model[J]. Journal of Applied Polymer Science, 2004, 94(1): 394-399. (  0) 0) |
| [28] |
Tang C Y, Kwon Y, Leckie J O. Effect of membrane chemistry and coating layer on physiochemical properties of thin film composite polyamide RO and NF membranes[J]. Desalination, 2009, 242(1-3): 149-167. (  0) 0) |
| [29] |
Zhang N, Huang Z, Yang N, et al. Nanofiltration membrane via EGCG-PEI co-deposition followed by cross-linking on microporous PTFE substrates for desalination[J]. Separation and Purification Technology, 2020, 232. (  0) 0) |
| [30] |
Nightingale E R. Phenomenological theory of ion solvation effective radii of hydrated ions[J]. Journal of Physical Chemistry, 2002, 63(9): 1381-1387. (  0) 0) |
 2022, Vol. 52
2022, Vol. 52


