2. 上海海洋大学,上海201306
鸢乌贼隶属于柔鱼科(Ommastrephidae)、鸢乌贼属(Symtectoteuthis),广泛分布在印度洋和西太平洋等海域[1],覆盖南北半球的热带和温带海域[2]。鸢乌贼胴体呈圆锥形,后部瘦凹,头部背面左右两侧和腕部中央的颜色近紫褐色,体表具有大小相间的近圆形色素斑[3],胴背部中央紫褐色宽带延伸至肉鳍后端,头部顶端具有十个腕,分别为左右第一腕、第二腕、第三腕、第四腕和触腕等,尾部具有鳍,且鳍宽大于鳍长。鸢乌贼种群分类的依据主要是胴长组成和产卵时间的差异。Nesis[7]对太平洋和印度洋海域的鸢乌贼进行了研究,认为2个海域的鸢乌贼主要由3个主要种群和2个次要种群组成,其中大型群和中型单轴群分布于印度洋、阿拉伯海等海域,中型双轴群、小型群和微型群则出现在太平洋[4]。
鸢乌贼在中国主要分布于南海海域,主要存在中型群和微型群2个种群,分类依据为背部发光器的有无[5]。目前对南海鸢乌贼的关注度日益提升,张鹏[6]等、颜云榕[7]等和李朋[8]等分别从形态学、地理因素以及分子等角度对其种群结构进行了分析和验证,将其初步分为微型群、中型群以及各地理种群等;王雪辉[9]等估算了其自然死亡率等;张宇美[10]等和颜云榕[11]等对其繁殖和食性做了分析,认为4—7月为其繁殖高峰期,以摄食中上层鱼类为主,且具有自食性。张俊[12]等利用声学对其资源总量进行了估算,认为南海鸢乌贼的现存量总量大约为2×104万t,具有较大开发潜力;范江涛[13]等利用栖息地指数模型对其与环境因素的关系做了相关探讨;吴燕燕[14]等对其重金属含量等做了分析;江艳娥[15]等将其耳石的形态学特征应用于种群分类。形态学研究作为物种的认识和鉴定的基础,对其生长过程中的发育规律以及管理、保护与利用均有重要意义,在其他海域鸢乌贼的研究中,已经有学者对其腕长等形态指标进行了分析[16],而在南海海域该研究较少涉及,已有研究[17]证实利用形态学指标可以对南海鸢乌贼微型群和中型群2个种群取得较好的分类效果,但并未对2个种群在形态指标上的具体差异进行描述。本文根据2012—2013年采集和测量的样本,首先将南海中南部鸢乌贼进行分类,对中型群和微型群进行辨别,然后对2个种群的各腕长、鳍长和鳍宽等参数与胴长进行了函数方程拟合,以此明确各形态指标与胴长之间的最佳函数关系,利用幂函数对两个种群的各参数与胴长之间的关系进行比较,并进行函数各参数的显著性比较,结合性腺成熟度对各参数的数值变化进行了探讨,以得到2个群体的形态学差异和各参数随性腺的发育而发生的变化,旨在为南海鸢乌贼的形态学和种群研究提供参考。
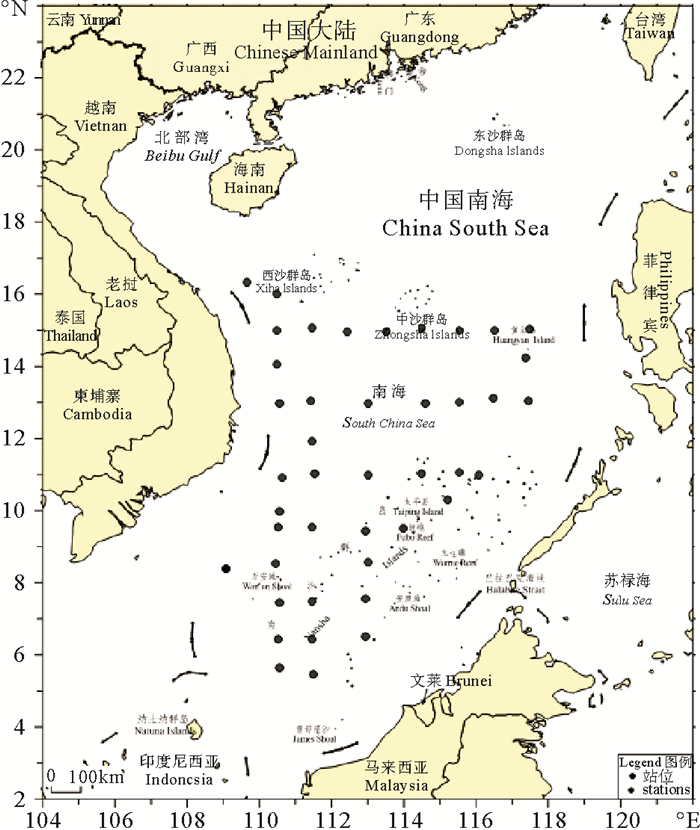
1 样品处理与分析方法 1.1 采样站位与样品处理样品采集时间为2012年9—12月和2013年3—5月,采样站位位于南海中南部海域(见图 1)。作业船采用主尺度为281.60 m×80.18 m的灯光罩网船,作业渔具的网衣最大网目尺寸为35 mm,网囊最小网目2.0 mm。在2个航次共计43个站位的采样过程中,共获得3 437(雄性1 723尾,雌性1 714尾)尾鸢乌贼,样品性别比例:微型群雌雄比为2:1,中型群雌雄比为1:1。样品冷冻保存后运至实验室测定,长度数据精度为1 mm,共测定了胴长(Mantle Length, ML)、右第一腕长(Arm Length-Ⅰ, AL1)、右第二腕长(Arm Length-Ⅱ, AL2)、右第三腕长(Arm Length-Ⅲ, AL3)、右第四腕长(Arm Length-Ⅳ, AL4)、右触腕长(Tentacle Length, TL)、鳍长(Fin Length, FL)和鳍宽(Fin Width, FW)等8个形态指标,微型群雌性、雄性胴长分布范围分别为59~126和56~95 mm。中型群雌性、雄性胴长分布范围分别为78~266和80~160 mm。
|
图 1 采样站位示意图 Fig. 1 Sampling stations |
依据发光器的有无以及性腺发育对样品进行种群鉴别,样品分属微型群与中型群2个种群。分析各形态指标与胴长的关系,分别应用线性、幂、指数、对数、增长和逻辑斯蒂等函数拟合两者之间的关系,根据相关性系数和F值均为最大的准则进行最优模型的筛选。利用幂函数对2个种群的各形态指标与胴长的关系进行比较分析,对2个种群不同性成熟度的各形态指标进行分析。差异性检验采用t检验和anova检验。所有分析均在Excel2007和Spss18.0软件中实现。
拟合模型:
线性函数(Linear function):y=a+bx;
幂函数(Power function):y=axb;
指数函数(Exponential function):y=aebx;
对数函数(Logarithmic function): y=a ln(x)+b;
增长函数(Growth function):y=ea+b/x;
逻辑斯蒂函数(Logistic function):
模型拟合结果的检验使用赤池信息量准则(Akaike information criterion、简称AIC),AIC值最小的模型即为最佳模型。
2 结果 2.1 模型拟合结果本研究中分别以雌性和雄性建模样本的AL1、AL2、AL3、AL4、TL、FL和FW为因变量, ML作为自变量作散点图并进行曲线模型拟合。雌性样本曲线模型拟合结果列于表中(见表 1、2)。可以看出雌性样本个体的各形态指标与体质量的拟合结果中所有模型拟合结果都呈差异极显著(P<0.01),说明所有拟合均有意义。
|
|
表 1 南海中南部中型群建模样本形态指标与体质量模型曲线估计结果 Table 1 Model curve estimation results of seven morphological indicators and ML for medium form of Sthenoteuthis oualaniensis in the central and southern South China Sea |
|
|
表 2 南海中南部微型群建模样本形态性状与体质量模型曲线估计结果 Table 2 Model curve estimation results of seven morphometric traits and ML for dwarf form of S. oualaniensis in the central and southern South China Sea |
中型群雌性AL1、AL2、AL3、AL4和FW与ML的拟合都是线性函数曲线拟合的相关性系数均为最大,分别为0.793、0.872、0.866、0.799和0.940;TL和FL与ML的拟合结果中对数函数曲线拟合的相关性系数均为最大,分别为0.857和0.927。
微型群雌性AL1、AL2、AL3、AL4、TL、FL和FW与ML的拟合结果中幂函数曲线拟合的相关性系数均为最大,分别为0.557、0.722、0.771、0.727、0.753和0.864;FL与ML的拟合结果中对数函数曲线拟合的相关性系数为最大,为0.857。
中型群雄性AL1、AL2、AL3、AL4、TL、FL和FW与ML的拟合结果中幂函数曲线拟合的相关性系数均为最大,分别为0.384、0.587、0.617、0.563、0.593、0.782和0.798。
微型群雄性AL1、AL2、AL3、AL4、TL和FW与ML的拟合结果中幂函数曲线拟合的相关性系数均为最大,相关性系数分别为0.537、0.586、0.606、0.521、0.513和0.715;FL与ML的拟合是对数函数曲线拟合的相关性系数为最大,为0.711。
除微型群雄性FL与ML外,2个种群雌雄个体的AL1、AL2、AL3、AL4、TL、FL和FW与ML的拟合结果中幂函数曲线拟合的AIC值均为最大,微型群雄性FL与ML的拟合结果中增长、指数和逻辑斯蒂函数的AIC值为最大。结果表明,鸢乌贼AL1、AL2、AL3、AL4、TL、FL和FW与ML (除微型群雄性FL与ML外)的模型拟合结果以幂函数最为适合。
2.2 胴长与各形态指标幂函数拟合主成分分析结果表明,第1主成分贡献率均大于40%,且AL1/ML、AL2 /ML、AL3/ML、AL4/ML、FL/ML和FW/ML的特征值处于相近水平,体现了腕与鳍的总体生长状况。在鸢乌贼个体生长的过程中, 胴长与各形态指标都随着个体的发育而发生了明显的变化,由各形态指标与胴长的方程拟合结果可知,在共计28个方程中,相关性系数最高的模型中幂函数、线性函数、对数函数分别占到了68%、18%和14%。各形态指标与胴长(除微型群雄性FL与ML外)的拟合结果中幂函数的AIC值均为最小,即模型拟合结果以幂函数为最佳,且利用幂函数拟合各形态指标与胴长的关系在印度洋海域鸢乌贼中型群和微型群个体的分析中取得了较好的效果,因此为比较南海海域鸢乌贼两个种群各形态指标的差异,统一使用幂函数模型对各形态指标和胴长的关系进行拟合,其结果见图 2和3。
|
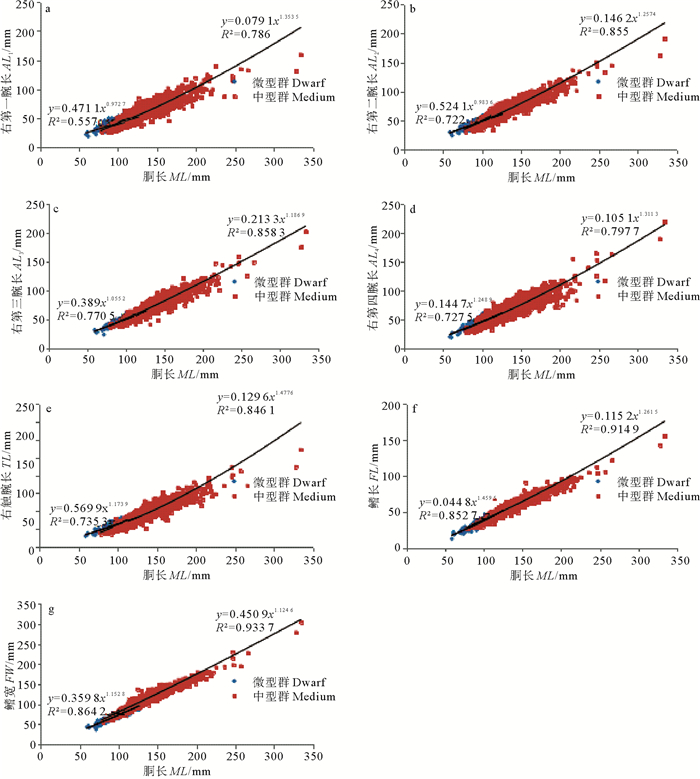
(a.右第一腕长-胴长; b.右第二腕长-胴长; c.右第三腕长-胴长; d.右第四腕长-胴长; e.右触腕长-胴长; f.鳍长-胴长; g.鳍宽-胴。a.AL1-ML; b. AL2-ML; c.AL3-ML; d.AL4-ML; e. TL-ML; f. FL-ML; g.FW-ML) 图 2 南海中南部鸢乌贼微型群与中型群中雌性各形态性状与胴长的关系 Fig. 2 Seven morphological indicators and ML relationship in dwarf and medium forms for females of S. oualaniensis in the central and southern South China Sea |
|
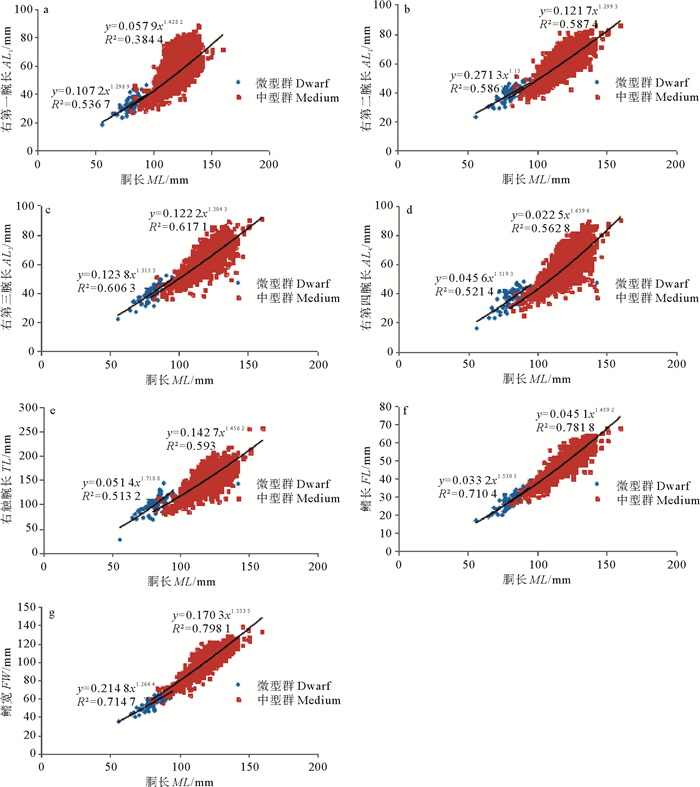
(a.右第一腕长-胴长; b.右第二腕长-胴长; c.右第三腕长-胴长; d.右第四腕长-胴长; e.右触腕长-胴长; f.鳍长-胴长; g.鳍宽-胴长。a. AL1-ML; b. AL2-ML; c. AL3-ML; d.AL4-ML; e. TL-ML; f. FL-ML; g.FW-ML.) 图 3 南海中南部鸢乌贼微型群与中型群中雄性各形态性状与胴长的关系 Fig. 3 Seven morphometric traits and ML relationship in dwarf and medium forms for females of S. oualaniensis in the central and southern South China Sea |
中型群和微型群雌性第一腕长与胴长关系式分别为:MLM=0.079 1×AL11.353 5(R2 = 0.786); MLD=0.471 1×AL10.972 7(R2 = 0.557),2个函数幂指数与常数项差异均为极显著(P<0.01)。
中型群和微型群雌性第二腕长与胴长关系式分别为:MLM=0.146 2×AL21.2574(R2 = 0.855); MLD=0.524 1×AL20.983 6(R2 = 0.722),2个函数幂指数与常数项差异均为极显著(P<0.01)。
中型群和微型群雌性第三腕长与胴长关系式分别为:MLM=0.213 3×AL31.186 9(R2 = 0.858); MLD=0.389×AL31.055 2(R2 = 0.771),2个函数幂指数差异显著(P<0.05),常数项差异极显著(P<0.01)。
中型群和微型群雌性第四腕长与胴长关系式分别为:MLM=0.105 1×AL41.311 3(R2 = 0.798); MLD=0.144 7×AL41.248 9(R2 = 0.728),2个函数幂指数差异不显著(P=0.323),常数项差异显著(P<0.01)。
中型群和微型群雌性触腕长与胴长关系式分别为:MLM=0.129 6×TL1.477 6(R2 = 0.846); MLD=0.569 9×TL1.173 9(R2 = 0.735),2个函数幂指数与常数项差异均为极显著(P<0.01)。
中型群和微型群雌性鳍长与胴长关系式分别为:MLM=0.115 2×FL1.261 5(R2 = 0.915); MLD=0.044 8×FL1.459 5(R2 = 0.853),2个函数幂指数与常数项差异均为极显著(P<0.01)。
中型群和微型群雌性鳍宽与胴长关系式分别为:MLM=0.450 9×FW1.124 6(R2 = 0.934); MLD=0.359 8×FW1.152 8(R2 = 0.864),2个函数幂指数差异不显著(P=0.341),常数项差异显著(P<0.01)。
中型群和微型群雄性第一腕长与胴长关系式分别为:ML=0.057 9×AL11.428 2(R2 = 0.384); ML=0.107 2×AL1ⅹ1.298 9(R2 = 0.537),2个函数幂指数差异不显著(P=0.527),常数项差异显著(P<0.01)。
中型群和微型群雄性第二腕长与胴长关系式分别为:ML=0.121 7×AL21.299 3(R2 = 0.587); ML=0.271 3×AL21.13(R2 = 0.586),2个函数幂指数差异不显著(P=0.420),常数项差异显著(P<0.01)。
中型群和微型群雄性第三腕长与胴长关系式分别为:ML=0.122 2 ×AL31.304 3(R2 = 0.617); ML=0.123 8×AL31.315 3(R2 = 0.606),2个函数幂指数差异不显著(P=0.060),常数项差异显著(P<0.01)。
中型群和微型群雄性第四腕长与胴长关系式分别为:ML=0.022 5×AL41.639 6(R2 = 0.563); ML=0.045 6×AL41.519 3(R2 = 0.521),2个函数幂指数差异不显著(P=0.462),常数项差异显著(P<0.01)。
中型群和微型群雄性触腕长与胴长关系式分别为:ML=0.142 7×TL1.456 2(R2 = 0.593); ML=0.051 4×TL1.718 8(R2 = 0.513),2个函数幂指数差异不显著(P=0.925),常数项差异显著(P<0.01)。
中型群和微型群雄性鳍长与胴长关系式分别为:ML=0.045 1×FL1.459 2(R2 = 0.782); ML=0.033 2×FL1.530 5(R2 = 0.710),2个函数幂指数差异不显著(P=0.167),常数项差异显著(P<0.01)。
中型群和微型群雄性鳍宽与胴长关系式分别为:ML=0.170 3×FW1.333 5(R2 = 0.798); ML=0.214 8×FW1.264 4(R2 = 0.715),2个函数幂指数差异不显著(P=0.527),常数项差异显著(P<0.01)。
2.3 各形态指标与性腺成熟度分析(见图 4、5)
|
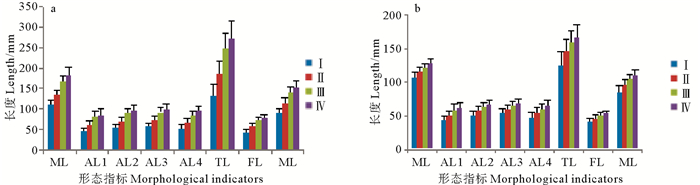
图 4 南海中南部鸢乌贼中型群雌性(a)和雄性(b)在不同性腺成熟度下各形态指标的平均值和标准差变化 Fig. 4 Mean and standard deviation values of eight morphological indicators during different sexual maturity stages in female (a) and males (b) for medium form of S. oualaniensis in the central and southern South China Sea |
|
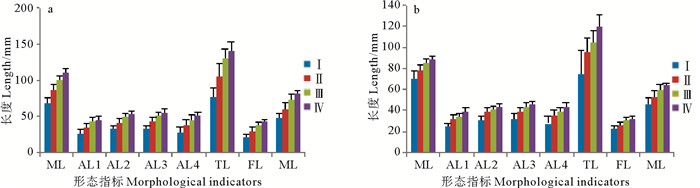
图 5 南海中南部鸢乌贼微型群雌性(a)和雄性(b)在不同性腺成熟度下各形态指标的平均值和标准差变化 Fig. 5 Mean and standard deviation values of eight morphological indicators during different sexual maturity stages in female (a) and males (b) for dwarf form of S. oualaniensis in the central and southern South China Sea |
鸢乌贼个体各形态性状平均值大小依次为FL、AL1、AL4、AL2、AL3、FW、ML与TL,在生长过程中,其胴长与各形态指标随着性腺的发育而产生了明显的变化, 且随着性腺成熟度的增加而增加。中型群雌性各形态性状Ⅰ~Ⅱ期、Ⅱ~Ⅲ期和Ⅲ~Ⅳ期增长率的分布范围分别为20.04(ML)~40.37(TL)、23.99(FW)~32.98(TL)及3.58(AL1)~13.30(AL4);微型群雌性各形态性状Ⅰ~Ⅱ期、Ⅱ~Ⅲ期和Ⅲ~Ⅳ期增长率的分布范围分别为24.79(ML)~42.13(FL)、15.92(ML)~27.60(FL)及3.58(AL1)~13.30(FL);中型群雄性各形态性状Ⅰ~Ⅱ期、Ⅱ~Ⅲ期和Ⅲ~Ⅳ期增长率的分布范围分别为7.66(ML)~18.83(AL1)、5.31(ML)~13.78(AL1)及4.46(TL)~7.24(AL4);微型群雄性各形态性状Ⅰ~Ⅱ期、Ⅱ~Ⅲ期和Ⅲ~Ⅳ期增长率的分布范围分别为11.78(ML)~29.02(AL1)、5.61(AL2)~17.87(FL)及4.44(FL)~15.22(TL)。因此,雌性个体中2个种群的增长率较为接近,雄性个体中两个种群增长率差异明显,表现为微型群的增长率的分布范围较大;中型群和微型群内部,雌性和雄性的增长率差异明显,雌性增长率的分布范围较大,且雌性相邻性成熟度胴长的平均值之间的差均大于雄性。
在微型群雄性中,Ⅱ期与Ⅲ期的AL1、Ⅲ期与Ⅳ期的ML、AL2、AL3、FL与FW差异不显著(P>0.05);Ⅰ期与Ⅱ期的FL与FW、Ⅲ期与Ⅳ期的AL1差异均为显著(P<0.05);其他各相邻性成熟期的参数间差异均为极显著(P<0.01)。在微型群雌性中,除Ⅲ期与Ⅳ期的AL1为差异不显著(P>0.05),其他各相邻性成熟期的参数间差异均为极显著(P<0.01)。在中型群雌性中,除Ⅲ期与Ⅳ期的AL1为差异不显著(P>0.05),其他各相邻性成熟期的参数间差异均为极显著(P<0.01)。在中型群雄性中,各相邻性成熟期的参数间差异均为极显著(P<0.01)。
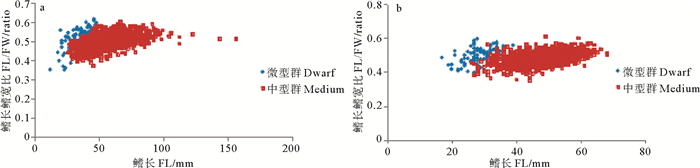
2.4 鳍长鳍宽比与鳍长的关系样品中,中型群的鳍长鳍宽比为1:2.45,微型群的鳍长鳍宽比为1:1.99。Chembian[16]在印度洋西北海岸也发现中型群与微型群的鳍部存在形态学上的差异,并建议可以将这种差异作为区别2个种群的依据。通过南海鸢乌贼胴长与鳍宽鳍长比的散点图可知(见图 6),胴长越小差异越明显,即生长早期的差异更加明显。微型群的鳍宽鳍长比要小于中型群,且该比值随这胴长的增加逐渐减小并趋向于稳定。
|
图 6 南海中南部鸢乌贼两个种群雌性和雄性鳍长鳍宽比与鳍长的关系 Fig. 6 FL/FW ratio and FL relationship in dwarf and medium forms for female and males of S. oualaniensis in the central and southern South China Sea |
Chembian[16]等研究表明印度洋西北海域中型群和微型群的背部胴长范围分别为98~195和92~134 mm,2个种群的TL和FW与ML的表达式在斜率和截距上均具有显著性差异。本次研究中两者胴长的分布范围分别为78~225和59~126 mm。因为本身背部胴长比胴长测量的范围大10%~14%,经过换算后比较发现南海鸢乌贼中型群与微型群比印度洋西北海域的相同种群的胴长分布范围更大,而2个种群雄性个体TL和FW与ML的表达式在斜率上无显著性差异,雌性个体FW和FW与ML的表达式上在无显著性差异。
通过比较2个种群雌性和雄性各形态指标与ML幂函数关系式中的系数可知,中型群雌性各幂函数的幂指数除TL外均大于雄性,而其常数项除TL外均小于雄性;微型群雌性各幂函数的幂指数均大于雄性,常数项均小于雄性。中型群雌雄间除AL1、AL2外,其余各幂函数的幂指数之间均存在显著性差异;除AL3外各幂函数的幂指数之间均存在极显著性差异。微型群中,除AL2和FL外各幂函数的幂指数和常数项中至少有一个系数在性别间均存在显著性差异。通过比较发现,中型群雌雄间存在的差异大于微型群,这可能与其生活周期有关,头足类是分批次产卵[18],中型群尤其是雌性的生命周期更长,性腺发育过程中其形态变化不能确定,而雄性则可能在交配后死亡。雌性个体的各形态指标与ML幂函数表达式中,中型群腕长与ML的表达式中幂指数大于微型群,而其常数项则小于微型群;中型群鳍长、鳍宽与ML的表达式中幂指数要小于微型群,常数项要大于微型群。而在雄性个体中,仅鳍宽、第一腕长、第二腕长、第四腕长与ML的表达式符合上述规律。除中型群的AL5外,中型群和微型群个体其余各形态指标与ML的幂函数关系式中,幂指数为雄性大于雌性,常数项则相反。
3.2 不同性成熟度的各参数比较研究[19]表明,性别和性腺成熟度均可对头足类的生长造成影响。在南海鸢乌贼生长过程中,各性状在性腺成熟度的增加过程中呈现出增长的趋势,且Ⅰ~Ⅱ期的增长率最高,Ⅱ~Ⅲ期的增长率次之,Ⅲ~Ⅳ期的增长率最小。但2个种群以及各自内部雌性和雄性各性状的增长趋势具有差异,首先微型群和中型群间具有差异,微型群个体性状生长过程中,Ⅰ~Ⅱ期的增长值最高,且远高于其他相邻性腺成熟度之间的差值,与Ⅱ~Ⅲ期的增长值的差值分别为20和31 mm,而中型群雄性个体Ⅰ~Ⅱ期的增长值仍为最高,但与Ⅱ~Ⅲ期的增长值的差值较小,仅为13 mm,且中型群雌性个体性状生长过程中,Ⅱ~Ⅲ期的增长值最高。其次,各种群内部雌性和雄性间两个性腺成熟度之间的各参数的增长值具有差别,表现为雌性各性状的增长大于雄性,尤其以中型群更为明显。其中中型群雌性为雄性各性状增长值的2.22~3.42倍,微型群雌性为雄性各性状增长值的1.34~2.30倍。微型群较早进入繁殖期,且在早期专注于生长,腕长等性状发育较为迅速,而在后期生长减慢;中型群生长周期较长,在性腺发育成熟的过程中其生长速率变化不大。
3.3 进一步研究腕与鳍的形态指标与角质颚[20-21]、内壳[22]、耳石[23]等形态分析具有相似性,在角质颚的研究中发现其各形态学参数与ML之间符合线性或者幂函数模型。在耳石形态学的研究中同样发现耳石形态学参数与ML之间符合幂函数等模型,各形态学参数分析均被用来进行种群辨别[11, 21]。相比于角质颚、内壳、耳石,腕与鳍的形态指标分析测量方法简单,但不能长久保存。4种形态学载体的获取难易程度分别为耳石、内壳、角质颚、腕形态指标,其中耳石的形态最为稳定,角质颚由于参与捕食运动会受到不同程度的磨损,内壳在保存和采取过程中易断裂,而腕与鳍的形态指标则是最易获取但也是最易受到损伤。对鸢乌贼耳石、内壳和角质颚等的生长轮纹等进行分析可以得出年龄和洄游路径等内容,耳石[24]、角质颚[25]和内壳[26]等的研究已经可以得到鸢乌贼个体的日龄数据,相对于各性腺成熟度之间的增长分析,基于日龄的各形态指标的生长率将更加准确,结合日龄可以对各性状的生长进行定量描述。故形态学研究应在外部参数分析的基础上,结合硬组织的微量元素和显微结构,对其年龄生长和洄游等进行进一步研究。
实验人员主要依据鸢乌贼外部形态对其进行种群分类,其中中型群与微型群的鉴别则是通过发光器的有无,中型群种群结构的研究还需要更加深入的数据分析,此次研究可以明确两个种群在外部形态上存在的差异,也为进一步的种群划分积累基础资料。鸢乌贼的摄食以头足类和鱼类为主,食物组成比例随胴长的增长而变化[27],其渔场分布与浮游动物的生物量关系显著[28],南海鸢乌贼中型群与微型群两个种群胴长大小差异较大,对两者的食物选择以及摄食洄游应进行进一步的分析。头足类个体的生长率除受生物因素影响外还会受到非生物因素的作用,例如温度[29]、纬度[30]和栖息水层[31]等,而鸢乌贼在生命周期中具有的洄游行为[32]也为其生存环境的规律性变化提供了条件,鸢乌贼中心渔场与环境因素之间存在相关关系,例如对盐度和温度等具有一定的要求,其产卵场环境也需要进行观测,因此应结合基于地理位置改变造成的环境因素、食物和性腺发育等变化,对鸢乌贼的生长率、洄游和生殖等进行深入研究。
| [1] |
王尧耕, 陈新军. 世界大洋性经济柔鱼类资源及其渔业[M]. 北京: 海洋出版社, 2005. Wang Y G, Chen X J. The World Ocean Economic Squid Resources and Fisheries[M]. Beijing: China Ocean Press, 2005. (  0) 0) |
| [2] |
Basir S. Biological feature of an oceanic squid, Sthenoteuthis oualaniensis in the South China Sea, Area Ⅲ: Western Philippines[C]. //Proceedings of the SEAFDEC Seminar on Fishery Resources in the South China Sea, Area Ⅲ: Western Philippines. Malaysia. 2000: 135-147.
(  0) 0) |
| [3] |
陈新军, 刘必林, 王尧耕. 世界头足类[M]. 北京: 海洋出版社, 2009. Chen X J, Liu B L, Wang Y G. The World Cephalopods[M]. Beijing: China Ocean Press, 2009. (  0) 0) |
| [4] |
Nesis K N. Population structure of oceanic ommastrephids, with particular reference to Sthenoteuthis oualaniensis: A review[J]. Recent Advances in Cephalopod Fisheries Biology, 1993, 375-383.
(  0) 0) |
| [5] |
刘金立.利用形态学和RAPD方法鉴定印度洋西北部海域鸢乌贼的种群结构[D].上海: 上海海洋大学, 2006. Liu J L. Identifying Population Structure in the Northwestern Indian Ocean Using Morphological and RAPD Analysis of the Purpleback Flying Squid Symplectoteuthis oualaniensis[D]. Shanghai: Shanghai Ocean University, 2006. http://med.wanfangdata.com.cn/Paper/Detail?id=DegreePaper_Y918053 (  0) 0) |
| [6] |
张鹏, 晏磊, 杨炳忠, 等. 春季南沙海域鸢乌贼种群结构特征的研究[J]. 南方水产科学, 2015, 11(5): 11-19. Zhang P, Yan L, Yang B Z, et al. Population structure of purpleback flying squid (Sthenoteuthis oualaniensis) in Nansha area in spring[J]. South China Fisheries Science, 2015, 11(5): 11-19. DOI:10.3969/j.issn.2095-0780.2015.05.002 (  0) 0) |
| [7] |
颜云榕, 冯波, 卢伙胜, 等. 南沙群岛北部海域鸢乌贼(Sthenoteuthis oualaniensis)夏季渔业生物学研究[J]. 海洋与湖沼, 2012, 43(6): 1177-1187. Yan Y R, Feng B, Lu H S, et al. Fishery biology of purpleback flying squid Sthenoteuthis oualaniensis in northern sea areas around nansha islands in summer[J]. Oceanologia et Limnologia Sinica, 2012, 43(6): 1177-1187. (  0) 0) |
| [8] |
李朋.南海鸢乌贼的种群遗传结构[D].上海: 上海海洋大学, 2014. Li P. Population Genetic Structure of Sthenoteuthis oualaniensis in South China Sea[D]. Shanghai: Shanghai Ocean University, 2014. (  0) 0) |
| [9] |
Wang X H, Qiu Y S, Zhang P, et al. Natural mortality estimation and rational exploitation of purpleback flying squid Sthenoteuthis oualaniensis in the southern South China Sea[J]. Chinese Journal of Oceanology and Limnology, 2017, 35(4): 1-10.
(  0) 0) |
| [10] |
张宇美, 颜云榕, 卢伙胜, 等. 西沙群岛海域鸢乌贼摄食与繁殖生物学初步研究[J]. 广东海洋大学学报, 2013, 33(3): 56-64. Zhang Y M, Yan Y R, Lu H S, et al. Study on feeding and reproduction biology of purple flying squid, Sthenoteuthis oualaniensis in the Western South China Sea[J]. Journal of Guangdong Ocean University, 2013, 33(3): 56-64. DOI:10.3969/j.issn.1673-9159.2013.03.010 (  0) 0) |
| [11] |
颜云榕, 易木荣, 冯波, 等. 南海鸢乌贼3个地理群体形态差异与判别分析[J]. 广东海洋大学学报, 2015, 35(3): 43-50. Yan Y R, Yi M R, Feng B, et al. Morphological variations and discriminant analysis of three different geographic cohorts of Sthenoteuthis oualaniensis in the South China Sea[J]. Journal of Guangdong Ocean University, 2015, 35(3): 43-50. DOI:10.3969/j.issn.1673-9159.2015.03.007 (  0) 0) |
| [12] |
张俊, 陈国宝, 张鹏, 等. 基于渔业声学和灯光罩网的南海中南部鸢乌贼资源评估[J]. 中国水产科学, 2014, 21(4): 822-831. Zhang J, Chen G B, Zhang P, et al. Estimation of purpleback flying squid (Sthenoteuthis oualaniensis) resource in the central and southern South China Sea based on fisheries acoustics and light-falling net[J]. Journal of Fishery Sciences of China, 2014, 21(4): 822-831. (  0) 0) |
| [13] |
范江涛, 张俊, 冯雪, 等. 基于栖息地模型的南沙海域鸢乌贼渔情预报研究[J]. 南方水产科学, 2015, 11(5): 20-26. Fan J T, Zhang J, Feng X, et al. Fishery forecast research of purpleback flying squid in Nansha area based on Habitat model[J]. South China Fisheries Science, 2015, 11(5): 20-26. DOI:10.3969/j.issn.2095-0780.2015.05.003 (  0) 0) |
| [14] |
Wu Y Y, Shen Y, Huang H, et al. Trace element accumulation and tissue distribution in the purpleback flying squid Sthenoteuthis oualaniensis from the central and southern South China Sea[J]. Biological Trace Element Research, 2016, 175(1): 1-9.
(  0) 0) |
| [15] |
Jiang Y E, Chen Z Z, Zhang P, et al. Statolith Morphology of the Sthenoteuthis oualaniensis in the Central South China Sea[J]. Animal Husbandry and Feed Science, 2015, 7(5): 30-35.
(  0) 0) |
| [16] |
Chembian A J, Mathew S. Population structure of the purpleback squid Sthenoteuthis oualaniensis (Lesson, 1830) along the south-west coast of India[J]. Indian Journal of Fisheries, 2014, 61(3): 20-28.
(  0) 0) |
| [17] |
朱凯, 王雪辉, 张鹏, 等. 南海南部鸢乌贼中型群与微型群形态学差异及其判别分析[J]. 热带海洋学报, 2016, 35(6): 82-88. Zhu K, Wang X H, Zhang P, et al. A study on morphological variations and discrimination of medium and dwarf forms of purple flying squid Sthenoteuthis oualaniensis in the southern South China Sea[J]. Journal of Tropical Oceanography, 2016, 35(6): 82-88. (  0) 0) |
| [18] |
Lin D, Chen X, Chen Y, et al. Sex-specific reproductive investment of summer spawners of Illex argentinus in the southwest Atlantic[J]. Invertebrate Biology, 2015, 134(3): 203-213. DOI:10.1111/ivb.2015.134.issue-3
(  0) 0) |
| [19] |
González A F, Castro B G, Guerra A. Age and growth of the short-finned squid Illex coindetii in Galician waters (NW Spain) based on statolith analysis[J]. ICES Journal of Marine Science: Journal du Conseil, 1996, 53(5): 802-810. DOI:10.1006/jmsc.1996.0101
(  0) 0) |
| [20] |
Fang Z, Xu L, Chen X, et al. Beak growth pattern of purpleback flying squid Sthenoteuthis oualaniensis in the eastern tropical Pacific equatorial waters[J]. Fisheries Science, 2015, 81(3): 443-452. DOI:10.1007/s12562-015-0857-8
(  0) 0) |
| [21] |
范江涛, 邱永松, 陈作志, 等. 南海鸢乌贼两个群体间角质颚形态差异分析[J]. 中国海洋大学学报(自然科学版), 2015, 45(10): 42-49. Fan J T, Qiu Y S, Chen Z Z, et al. Morphological difference of the beak between two stocks of Sthenoteuthis oualaniensis inhabiting South China Sea[J]. Periodical of Ocean University of China, 2015, 45(10): 42-49. (  0) 0) |
| [22] |
贡艺.基于内壳稳定同位素信息的秘鲁外海茎柔鱼摄食与洄游研究[D].上海海洋大学, 2015. Yi Gong. The Study on Foraging Strategies and Migration Patterns of Jumbo Squid (Dosidicus gigas) off Peru Based on the Stable Isotopic Information in Gladius[D]. Shanghai: Shanghai Ocean University, 2015. http://cdmd.cnki.com.cn/Article/CDMD-10264-1015974808.htm (  0) 0) |
| [23] |
江艳娥, 张鹏, 林昭进, 等. 南海外海鸢乌贼耳石形态特征分析[J]. 南方水产科学, 2015, 11(5): 27-37. Jiang Y E, Zhang P, Lin Z J, et al. Statolith morphology of purpleback flying squid (Sthenoeuthis oualaniensis) in the offshore south china sea[J]. South China Fisheries Science, 2015, 11(5): 27-37. DOI:10.3969/j.issn.2095-0780.2015.05.004 (  0) 0) |
| [24] |
Chen X J, Liu B L, Tian S Q, et al. Fishery biology of purpleback squid, Sthenoteuthis oualaniensis, in the northwest Indian Ocean[J]. Fisheries Research, 2007, 83(1): 98-104. DOI:10.1016/j.fishres.2006.09.005
(  0) 0) |
| [25] |
Liu B L, Chen X J, Chen Y, et al. Determination of squid age using upper beak rostrum sections: Technique improvement and comparison with the statolith[J]. Marine Biology, 2015, 162(8): 1685-1693. DOI:10.1007/s00227-015-2702-0
(  0) 0) |
| [26] |
Bizikov V A. Growth of Sthenoteuthis oualaniensis, using a new method based on gladius microstructure[C]//ICES Marine Science Symposia. Copenhagen, Denmark: International Council for the Exploration of the Sea, 1995, 199: 445-458.
(  0) 0) |
| [27] |
龚玉艳, 詹凤娉, 杨玉滔, 等. 南海鸢乌贼摄食习性的初步研究[J]. 南方水产科学, 2016, 12(4): 80-87. Gong Y Y, Zhan F P, Yang Y T, et al. Feeding habits of Symplectoteuthis oualaniensis in the South China Sea[J]. South China Fisheries Science, 2016, 12(4): 80-87. DOI:10.3969/j.issn.2095-0780.2016.04.010 (  0) 0) |
| [28] |
钱卫国, 陈新军, 刘必林, 等. 印度洋西北海域秋季鸢乌贼渔场分布与浮游动物的关系[J]. 海洋渔业, 2006, 28(4): 265-271. Qian W G, Chen X J, Liu B L, et al. The relationship between fishing ground distribution of Symlectoteuthis oualaniensis and zooplankton in the northwestern Indian Ocean in autumn[J]. Marine Fisheries, 2006, 28(4): 265-271. DOI:10.3969/j.issn.1004-2490.2006.04.001 (  0) 0) |
| [29] |
Villanueva R. Effect of temperature on statolith growth of the European squid Loligo vulgaris during early life[J]. Marine Biology, 2000, 136(3): 449-460. DOI:10.1007/s002270050704
(  0) 0) |
| [30] |
Huuskonen H. Is otolith microstructure affected by latitude?[J]. Marine Ecology-Progress Series, 1999, 177: 309-310. DOI:10.3354/meps177309
(  0) 0) |
| [31] |
Arkhipkin A I. Age and growth of the mesopelagic squid Ancistrocheirus lesueurii (Oegopsida: Ancistrocheiridae) from the central-east Atlantic based on statolith microstructure[J]. Marine Biology, 1997, 129(1): 103-111. DOI:10.1007/s002270050151
(  0) 0) |
| [32] |
杨德康. 两种鱿鱼资源和其开发利用[J]. 上海水产大学学报, 2002, 11(2): 176-179. Yang D K. The resources and its exploitation and utilization of two spcies of squid[J]. Journal of Shanghai Fisheries University, 2002, 11(2): 176-179. (  0) 0) |
2. Shanghai Ocean University, Shanghai 201306, China
 2019, Vol. 49
2019, Vol. 49


