2. 中国海洋大学海洋环境与生态教育部重点实验室,山东 青岛 266100;
3. 中国海洋大学化学化工学院,山东 青岛 266100
近年来,纳米金粒子(Gold nanoparticles, AuNPs)已被证明是众多氧化还原反应的高效催化剂,包括CO的低温氧化,醇类、醛类和环己烷的选择性氧化,丙烯的环氧化,硝基的还原以及不饱和羰基的氢化反应[1-3]。然而,游离AuNPs由于其高表面能而容易聚集[4],在一定程度上导致了催化活性的降低。将AuNPs固定在合适的载体上不仅可以防止AuNPs的聚集,还可以利用载体的特殊结构与性质以及AuNPs与载体界面之间的相互作用改善其催化活性,是制备高效AuNPs催化剂的有效方法。
常用的AuNPs负载载体主要有金属氧化物[5]、硅基材料[6]、聚合物[7]、黏土矿物[8]和碳材料[9]等。氧化石墨烯(Graphene oxide, GO)是一种由sp2杂化碳原子组成的二维单层石墨片,具有大的比表面积,良好的机械、热和电性能,是良好的催化剂载体[10]。一般认为,在GO上有多种亲水的含氧官能团,包括基底平面上的羟基和环氧基,片状边缘的羧基、酚、醌和内酯基[11]。已经证明,与GO相比,GO表面的含氧官能团被还原得到的还原氧化石墨烯(Reduced graphene oxide, rGO)兼具了石墨烯和氧化石墨烯的各种特性,是理想的AuNPs负载载体[12]。在GO的还原过程中,石墨烯的sp2域可以得到部分恢复,剩余的含氧基团可以与AuNPs相结合,限制了AuNPs的聚集,并使得AuNPs可以均匀稳定地分散在rGO上。此外,rGO利用其表面的2D π-π共轭作用,可以充当电子受体来增强锚定在其表面的AuNPs的催化活性[13]。
AuNPs的负载方法也决定着催化剂的结构,最终对催化性能产生重要影响。以GO和氯金酸为原料,采用化学还原方法,在GO和氯金酸被还原的同时,将AuNPs负载于rGO上是制备rGO/AuNPs复合物的理想方法。用肼、抗坏血酸和硼氢化钠[13-15]等常用还原剂制备rGO/AuNPs复合物,反应条件较为复杂,反应过程难以控制,难以制备催化性能稳定的rGO/AuNPs复合物,阻碍纳米复合材料的大规模生产[16]。因此,简单、绿色、反应过程易于控制的rGO/AuNPs制备方法引起了人们的广泛关注。
本文中在未添加任何还原剂和稳定剂的条件下,通过简单地控制反应体系pH值成功制备了rGO/AuNPs复合物。在此过程中,GO上的—OH将Au(III)还原为AuNPs并沉积在GO上,同时GO在强碱性条件下转化为rGO[17]。所合成的rGO/AuNPs复合物通过紫外-可见吸收光谱(Ultraviolet and visible absorption spectroscopy, UV-vis)、X-射线衍射光电子能谱分析(X-ray photoelectron spectroscopy, XPS),扫描电镜(Scanning electron microscopy, SEM),透射电镜(Transmission electron microscopy, TEM),傅里叶红外变换光谱(Fourier transform infrared spectroscopy, FT-IR)和X-射线衍射(X-ray diffraction patterns, XRD)进行表征。以rGO/AuNPs复合物为催化剂,以4-硝基苯酚(4-nitrophenol, 4-NP)的催化还原反应为探针反应,考察了其催化还原性能。本研究为具有高催化活性的rGO/AuNPs复合物的制备提供了一种简单、绿色的制备方法。
1 材料与方法 1.1 实验材料GO为分析纯,购自山东利特纳米技术有限公司;HAuCl4和4-NP购自国药集团化学试剂有限公司;CH3COOH、NaOH均为分析纯,在所有实验中使用去离子水。
1.2 研究方法 1.2.1 rGO的制备将30 mg GO分散到100 mL去离子水中,室温下超声处理2 h,形成均匀的分散液。用1 mol/L的NaOH溶液将GO分散液的pH值调节至10,90 ℃下加热9 h制备rGO。
1.2.2 rGO/AuNPs复合物的制备rGO/AuNPs复合物依照如下条件制备:将30 mg GO分散到100 mL去离子水中,室温下超声处理2 h后,将5 mL GO分散液与1.5 mL 3 mmol/L HAuCl4溶液混合,用1 mol/L的NaOH溶液调节混合溶液pH至10,在90 ℃下加热9 h制备rGO/AuNPs。考察了其他反应条件不变时,改变单一条件,包括反应体系pH值、反应温度、反应时间和HAuCl4浓度对rGO/AuNPs复合物制备的影响。
1.3 分析测试方法TU-1810紫外可见分光光度计记录rGO和rGO/AuNPs复合物的UV-Vis图。日立S-4800扫描电子显微镜(SEM)和H-7650透射电子显微镜(TEM)表征rGO及rGO/AuNPs复合物的表面形态、尺寸和形貌。Tensor 27傅里叶变换红外光谱仪(FT-IR)表征rGO和rGO/AuNPs复合物的化学结构。X射线衍射(XRD)分析用Bruker D8 Advance X射线衍射仪记录,CuKα为射线源,λ=1.54Å。PHI 1600 ESCA System X射线光电子能谱仪(XPS)表征GO、rGO及rGO/AuNPs复合物的元素组成及官能团,使用Advantage软件对XPS光谱进行拟合。
1.4 数据分析方法以4-NP的催化还原为模型反应,研究rGO/AuNPs复合物的催化还原活性。在30 ℃下,将一定量的rGO/AuNPs复合物加入到含有20 mL浓度为0.2 mmol/L的4-NP和20 mL浓度为0.1 mol/L的NaBH4混合溶液中。在预定的时间间隔内,记录催化还原体系的UV-Vis光谱图。
通过测定4-硝基酚阴离子(4-NPi)在400 nm处的吸光度,依公式(1)计算4-NP的转化率:
| $ \text { Conversion }(\%)=\left(1-A / A_0\right) \times 100。$ | (1) |
式中: A0为4-NPi溶液的初始吸光度;A为反应t时刻4-NPi溶液的吸光度。
在反应体系中,NaBH4大量过量,可用伪一级反应动力学方程(公式(2))来描述4-NP的催化反应动力学:
| $ \ln \left(A_0 / A\right)=k t。$ | (2) |
式中:k为催化反应速率常数,min-1;t为反应时间,min;A0为4-NPi溶液的初始吸光度;A为反应t时刻4-NPi溶液的吸光度。
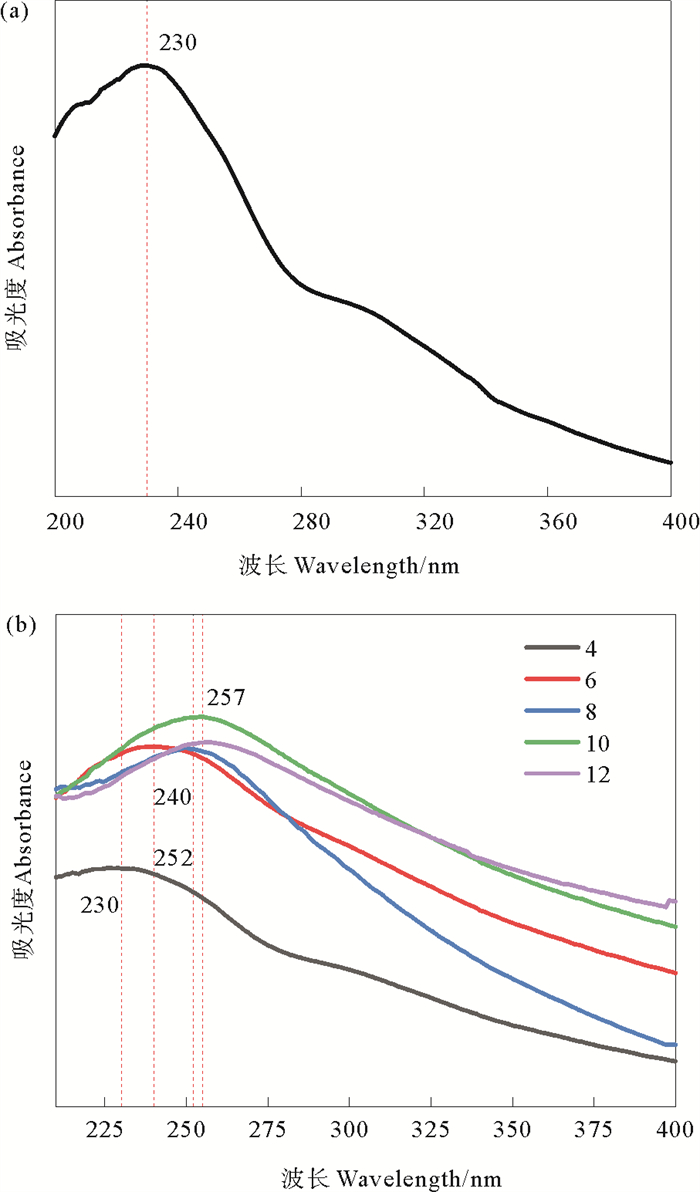
2 结果与讨论 2.1 pH对rGO制备的影响反应体系的pH值在GO的还原反应中发挥着极其重要的作用。GO的UV-Vis图(见图 1(a))显示了两个特征峰。在230 nm处的特征峰对应于芳香族C—C键的π→π*跃迁,而约300 nm处的肩峰可以归因于CO键的n→π*跃迁[6]。
|
图 1 GO分散液的UV-vis图(a)和pH值对GO还原的影响(b) Fig. 1 UV-Vis spectrum of GO (a) and effect of pH on GO reduction (b) |
分别用1%(v/v)CH3COOH溶液和1 mol/L的NaOH溶液调节GO分散液的pH,考察反应体系的pH值对GO还原的影响。在GO还原为rGO的过程中,因为含氧官能团的去除和石墨烯内电子共轭体系的恢复,GO在230 nm处的吸收峰会发生红移,利用吸收峰的位置可以评估GO的还原程度[18-19]。吸收峰的最大吸收波长λmax越大,GO的被还原程度越高[20]。如图 1(b)所示,当体系pH值为4时,λmax出现在230 nm处,与GO的UV-Vis图一致,说明GO没有被还原。当pH值为6时,λmax红移至240 nm。当pH值为8时,λmax红移至252 nm。pH值增加到10时,λmax红移至257 nm。继续增大pH值至12时,λmax不再发生变化。根据以上结果可知,90 ℃时,在碱性条件下,GO可以被成功还原,且rGO的还原程度随着pH的升高而增加。在碱性加热条件下,GO上的环氧基会发生开环反应导致C—O键断裂,羧基也会与OH-发生脱羧反应,GO被还原为rGO[17]。
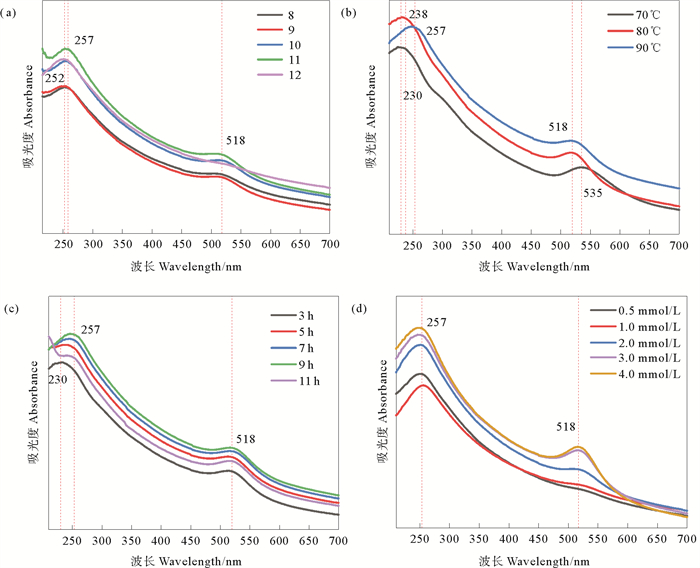
2.2 rGO/AuNPs复合物的制备 2.2.1 pH值的影响图 2(a)为不同pH下制备rGO/AuNPs复合物的UV-Vis图。在pH=8~11的范围内,518 nm处出现了球形、小粒径AuNPs的特征吸收峰。吸收峰强度随着pH值的增加而不断增强,pH值为10时,吸收峰强度最大,此时生成的AuNPs数量最多。在碱性条件下,Au(III)与OH-形成了低氧化还原电位的AuCl(OH)3-或Au(OH)4-,使得Au(III)的还原更为容易。同时,GO及rGO分子中的—OH与六角基面相连,使其成为酚类实体,酚质子是弱酸性的,在碱性条件下,酚类物质去质子化,生成酚盐阴离子。酚盐阴离子被强烈活化并通过将电子转移到Au(III)进行亲电芳香取代被还原为AuNPs并负载在rGO上,同时rGO上的—OH被氧化为半醌[21]。当反应体系的pH为12时,过多的OH-吸附在Au原子簇表面而限制了AuNPs的形成,同时,Na+的高反应活性也导致了Au(OH)4-转变为了NaAuO2,阻碍了AuNPs的形成。
|
图 2 不同pH(a),不同反应温度(b),不同反应时间(c)和不同HAuCl4浓度(d)下制备rGO/AuNPs的UV-Vis图 Fig. 2 UV-Vis spectra of rGO/AuNPs prepared at different pH (a), reaction temperatures (b), reaction time (c) and HAuCl4 concentration (d) |
图 2(b)为不同反应温度下制备rGO/AuNPs复合物的UV-Vis图。当反应温度为70 ℃时,230 nm处GO的特征峰没有发生移动,说明70 ℃下在pH=10的反应体系中也无法还原GO得到rGO。出现在535 nm处的吸收峰证明了粒径较大的AuNPs的生成[22]。在此条件下,GO缺陷处的羟基可能是还原HAuCl4的主要基团[23]。当反应温度升高到80 ℃时,GO的吸收峰红移到了238 nm处,GO被成功还原。518 nm处的吸收峰证明了球形、小粒径AuNPs的生成。继续升高反应温度到90 ℃时,rGO的吸收峰红移至257 nm,说明GO的还原程度随着反应温度的升高而增加,而AuNPs的特征吸收峰位置没有发生变化,表明高温下仍可制备粒径较小的AuNPs。
2.2.3 反应时间的影响图 2(c)为不同反应时间下制备rGO/AuNPs的UV-Vis图。在90 ℃, pH=10的反应体系中,随着反应时间的增加,GO的吸收峰逐渐红移,反应进行到9 h时,吸收峰红移至257 nm,证实了GO的被还原程度会随着反应时间的延长而增加。AuNPs的吸收峰均出现在518 nm处,吸收峰强度随反应时间的延长而增加,证明rGO上负载了更多的AuNPs。
2.2.4 HAuCl4浓度的影响不同HAuCl4浓度下制备rGO/AuNPs的UV-Vis图如图 2(d)所示。当HAuCl4浓度较低(0.5~1.0 mmol/L)时,没有出现AuNPs的特征吸收峰。HAuCl4浓度为2.0 mmol/L时,在518 nm处观察到AuNPs的特征吸收峰。HAuCl4浓度增加到3.0 mmol/L时,AuNPs的吸收峰逐渐增强且峰位置未发生改变。HAuCl4浓度增大到4.0 mmol/L时,AuNPs的吸收峰强度不再增加。以上结果证明,随着HAuCl4浓度的增加,负载于rGO上的AuNPs逐渐增多,且没有发生团聚。这可能是因为rGO上残留的含氧基团可以为AuNPs提供锚定位点,增强了AuNPs在rGO上的稳定性和分散性[24]。
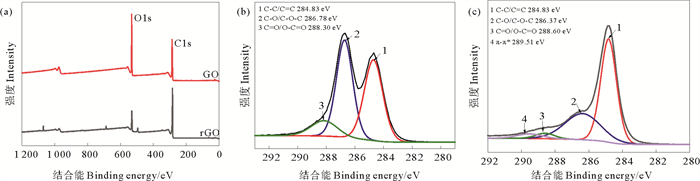
2.3 表征 2.3.1 化学元素分析通过XPS对GO和rGO上不同元素的化学形态及存在的官能团进行了分析。图 3(a)为GO和rGO的XPS全谱分析图。GO谱图中286.12和531.94 eV处的峰分别对应于C 1s和O 1s。rGO的谱图中531.94 eV处的O 1s峰强度明显降低,说明GO中含氧官能团被大量去除,rGO成功制备。
|
图 3 GO和rGO的XPS光谱(a)和GO(b)、rGO(c)的高分辨率典型C1s XPS光谱 Fig. 3 The XPS spectra for GO and rGO(a), and high-resolution core-level C1s XPS spectra for GO (b) and rGO (c) |
图 3(b)—(c)为GO和rGO的高分辨率典型C 1s光谱。如图 3(b)所示,GO的C 1s光谱可以被分为三个峰,分别位于284.83、286.78和288.30 eV,分别归属为石墨化的C—C/C=C、C—O/C—O—C和CO/O—CO,证明了GO中含氧基团的存在。图 3(c)中,除了GO的特征峰,rGO在289.51 eV处出现了一个新峰,对应于π-π*的结合,这可以归因于rGO中sp2共轭体系的恢复[25-26]。与GO相比,rGO中石墨化C—C/C=C峰的变窄证实了存在更均匀的化学环境和有序结构[27]。此外,rGO光谱中C—C/C—O峰的强度比的增加也为rGO中含氧官能团的大量减少提供了有力证据。
使用Advantage软件对GO和rGO的XPS数据进行处理,计算得知GO和rGO的C/O比分别为2.38和5.89。C/O比的增加证实了GO的成功还原。使用甲胺基亚磺酸、硼氢化钠和肼还原GO制备的rGO C/O比分别为5.15[28]、5.80[29]和10.20[15]。本文中,在碱性条件下制备的rGO还原程度低于由肼制备的rGO,但高于由甲胺基亚磺酸和硼氢化钠制备的rGO,说明在碱性条件下还原GO是一种有效的方法。
2.3.2 形态分析图 4为rGO和rGO/AuNPs复合物的SEM图像。如图 4(a)所示,在rGO中可以清楚地观察到分层和褶皱结构,这对于防止由范德华力引起的rGO聚集和保持高的比表面积具有重要作用。在图 4(b)中可以清楚地看到大量的AuNPs成功分散在rGO表面,rGO/AuNPs被成功制备。

|
图 4 rGO(a)及rGO/AuNPs(b)的SEM图 Fig. 4 SEM image of rGO (a) and rGO/AuNPs (b) |
图 5为rGO/AuNPs的TEM图像。如图 5(a)所示,rGO的褶皱和分层结构清晰可见,且AuNPs在其表面分布均匀。从rGO/AuNPs的高倍TEM图像可以看出,成功制备了球形或准球形的AuNPs。结果显示,以rGO做载体可以有效的防止AuNPs的聚集。从AuNPs的粒径分布柱状图(见图 5(b))可以得知,AuNPs的平均粒径为(14.79±3.86) nm。

|
图 5 rGO/AuNPs的TEM图像(a)和AuNPs的粒径分布直方图(b) Fig. 5 TEM image of rGO/AuNPs (a) and histogram of particle size distribution of AuNPs (b) |
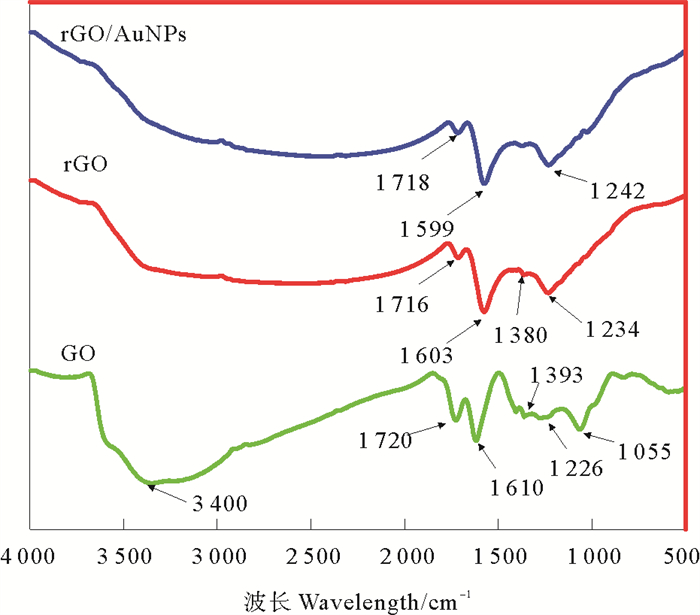
图 6在GO的FT-IR光谱中,3 400 cm-1附近的宽吸收峰是由O—H的伸缩振动引起的。1 720和1 610 cm-1处的吸收峰可分别归属为羰基和羧基的CO伸缩振动以及芳香环上碳骨架的C=C弯曲振动[30]。1 393 cm-1处的峰则与O—H的变形振动有关[25]。1 226和1 055 cm-1处的吸收峰分别对应于环氧基团中C—O的伸缩振动[20]和烷氧基中C—O的伸缩振动[31]。以上结果证实GO中存在着大量的含氧基团。rGO的FT-IR光谱中,与含氧基团相关的特征吸收峰强度急剧下降,包括O—H (3 400 cm-1)、CO (1 720 cm-1) 和C—O (1 226 cm-1),而在1 055 cm-1处C—O伸缩振动的特征吸收峰消失,表明许多含氧基团被去除。在1 603 cm-1处C=C弯曲振动的特征峰峰强增加,证实了rGO中sp2共轭体系的恢复[32]。以上结果证明,rGO被成功制备。与rGO相比,rGO/AuNPs的FT-IR光谱中没有明显变化,相关峰位置的移动证实了AuNPs在rGO上的成功负载。
|
图 6 GO、rGO和rGO/AuNPs的FT-IR光谱 Fig. 6 FT-IR spectra of GO, rGO and rGO/AuNPs |
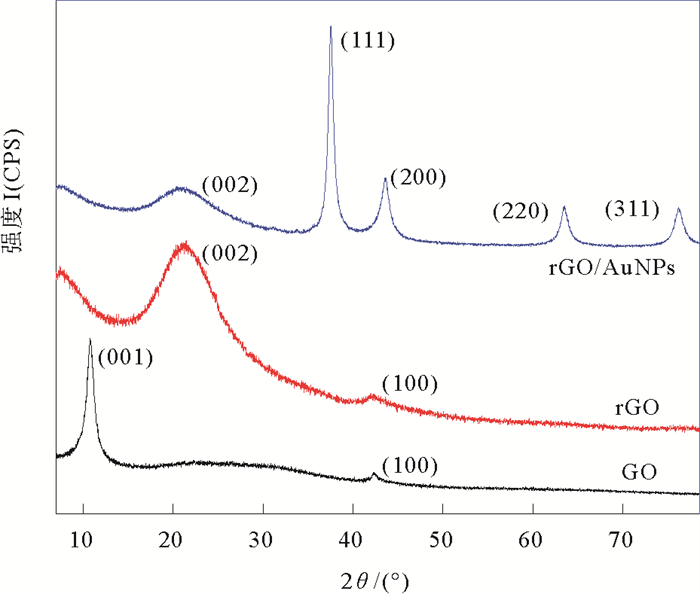
图 7中GO的特征峰出现在10.27°和42.42°,分别对应于GO的(001)和(100)晶面。rGO在10.27°处的峰消失,而在21.07°处出现了代表石墨烯(002)晶面的新的衍射峰,证明了GO已被成功还原。对(001)和(002)特征峰,可利用Bragg方程和Scherrer方程分别评估堆叠的石墨烯层的层间距和堆叠的石墨烯层的平均高度[30]。由计算可知,GO的平均高度为7.78 nm,层间距为0.82 nm,由8~9个石墨烯层组成。rGO的平均高度为1.01 nm,层间距为0.42 nm,由2~3层石墨烯层组成。GO和rGO分别出现在42.42°和41.93°的衍射峰,显示出堆叠的石墨烯层中存在短程秩序[33]。
|
图 7 GO、rGO和rGO/AuNPs的XRD图谱 Fig. 7 XRD patterns of GO, rGO and rGO/AuNPs |
rGO/AuNPs复合物在38.11°、44.23°、64.52°和77.45°出现衍射峰则分别与(111)、(200)、(220)和(311)晶面相对应,这与AuNPs(JCPDS 04-0784)面心立方(FCC)结构相一致。此外,在rGO/AuNPs的XRD图谱也出现了rGO在24.54°的特征峰,这些结果证实了rGO/AuNPs的成功制备。rGO/AuNPs中(111)晶面的衍射峰强度最高,表明AuNPs主要沿着(111)方向生长。由Debye-Scherrer公式[31]根据(111)晶面计算出的AuNPs的平均粒径尺寸为14.74 nm,这与之前的TEM结果一致。
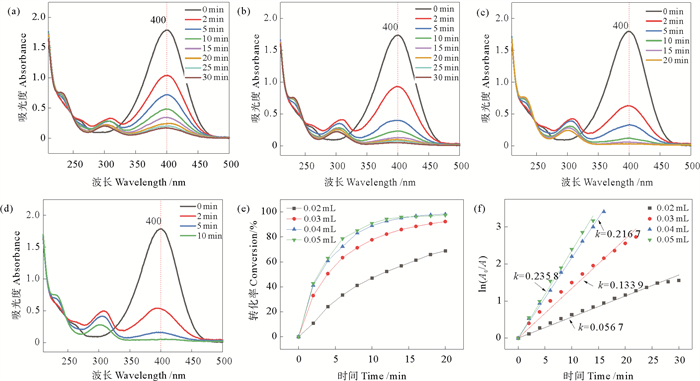
2.3.5 rGO/AuNPs复合物催化还原性能评价在30 ℃下,rGO/AuNPs添加量对催化还原4-NP的影响如图 8所示。如图 8(a)所示,当催化剂添加量为0.02 mL时,400 nm处4-NPi的吸收峰峰强度随着反应时间的延长而逐渐下降,并在297 nm处出现了4-氨基酚(4-aminophenol, 4-AP)的吸收峰,反应进行20 min后400 nm处的吸收峰强度随时间的变化不明显,表明此催化剂添加量条件下rGO/AuNPs复合物对4-NP还原能力有限。随着催化剂添加量的增大,如图 8(b)—(d)所示,催化反应完成所需的时间明显缩短。
|
图 8 0.02 mL(a), 0.03 mL (b), 0.04 mL (c), 0.05 mL (d)催化剂添加量下4-NP催化还原的UV-vis图,4-NP转化率随时间t变化图(e)及不同催化剂添加量下催化还原4-NP的lnA0/A随时间t变化图(f) Fig. 8 UV-vis spectra of the catalytic reduction of 4-NP with 0.02 mL (a), 0.03 mL (b), 0.04 mL (c) and 0.05 mL (d) rGO/AuNPs, 4-NP conversion versus time t (e) and ln(A0/A) versus time t for the catalytic reduction of 4-NP with different catalyst additions(f) |
图 8(e)为在不同催化剂添加量下4-NP转化率随时间的变化图。如图所示,4-NP的转化率随着催化剂添加量的增加而提高,当催化剂添加量为0.02、0.03、0.04和0.05 mL时,反应20 min时4-NP的转化率分别达到68.8%、92.2%、98.2%和98.9%。
图 8(f)为不同催化剂添加量下4-NP催化还原的动力学方程拟合图。如图所示,ln(A0/A)与反应时间t呈现较好的线性关系,R2均大于0.98,催化反应符合伪一级反应动力学方程。反应速率常数k随着催化剂添加量的增加而增大,催化剂添加量由0.02增加到0.04 mL时,k值由0.056 7增大至0.216 7 min-1,增加催化剂添加量至0.05 mL时,k仅增长至0.235 8 min-1。随着催化剂添加量的增加,催化还原效率增加,这可能是因为催化剂添加量会影响比表面积和活性位点的数量[34],当催化剂添加量增加时,有更多的可利用的活性位点,使AuNPs与反应底物的接触机会更多。
在NaBH4存在下,4-NP的催化还原发生在AuNPs的表面[16]。AuNPs催化还原4-NP可能主要包括四个步骤:第一步,4-NP吸附到rGO/AuNPs表面后扩散至AuNPs的表面活性位点;第二步,硼氢根离子(BH4-)与水反应形成偏硼酸盐(BO2-)和活性氢,活性氢转移至AuNPs表面形成活性表面氢Au-H;第三步,AuNPs的活性表面氢Au-H攻击4-NP的硝基,将4-NP还原为4-AP;第四步,产物4-AP从催化剂表面解吸。以rGO/AuNPs复合物为催化剂时,4-NP会通过π-π堆积作用吸附到rGO表面,从而增加AuNPs周围的4-NP浓度,使它们之间的接触更加有效[35],同时,rGO的高导电性,使电子能够更快地从rGO传输到AuNPs,增加局部电子浓度,从而导致4-NP的电子吸收增强[25],这可能也是rGO/AuNPs具有较高催化活性的原因。
3 结语在碱性条件下热处理GO和HAuCl4的混合溶液可以成功制备rGO/AuNPs复合物。在rGO/AuNPs复合物中,小粒径的球形AuNPs均匀分散在rGO上。通过调节pH、反应温度和时间可以控制rGO的还原程度。负载在rGO上AuNPs的粒径与数量也受到反应温度、时间及HAuCl4浓度的控制。催化还原结果表明,rGO/AuNPs复合物对4-NP表现出优异的催化还原性能。本研究提供了一种简单的rGO/AuNPs复合物制备方法,为催化还原硝基酚类化合物的高效催化剂的制备提供了一种新的思路。
| [1] |
Hashmi A S K. Gold-catalyzed organic reactions[J]. Chemical Reviews, 2007, 107(7): 3180-3211. DOI:10.1021/cr000436x (  0) 0) |
| [2] |
Li D, Kaner R B. Graphene-based materials[J]. Science, 2008, 320(5880): 1170-1171. DOI:10.1126/science.1158180 (  0) 0) |
| [3] |
Lim S H, Ahn E-Y, Park Y. Green synthesis and catalytic activity of gold nanoparticles synthesized by Artemisia capillaris water extract[J]. Nanoscale Research Letters, 2016, 11(1): 1-11. DOI:10.1186/s11671-015-1209-4 (  0) 0) |
| [4] |
Sharma A S, Kaur H, Shah D. Selective oxidation of alcohols by supported gold nanoparticles: Recent advances[J]. RSC Advances, 2016, 6(34): 28688-28727. DOI:10.1039/C5RA25646A (  0) 0) |
| [5] |
Zakaria M B, Malgras V, Nagata T, et al. Gold nanoparticles anchored on mesoporous zirconia thin films for efficient catalytic oxidation of carbon monoxide at low temperatures[J]. Microporous and Mesoporous Materials, 2019, 288: 109530. DOI:10.1016/j.micromeso.2019.05.055 (  0) 0) |
| [6] |
Sun L, Jiang L, Peng S, et al. Preparation of Au catalysts supported on core-shell SiO2/polypyrrole composites with high catalytic performances in the reduction of 4-nitrophenol[J]. Synthetic Metals, 2019, 248: 20-26. DOI:10.1016/j.synthmet.2018.12.024 (  0) 0) |
| [7] |
Ilgin P, Ozay O, Ozay H. A novel hydrogel containing thioether group as selective support material for preparation of gold nanoparticles: Synthesis and catalytic applications[J]. Applied Catalysis B: Environmental, 2019, 241: 415-423. DOI:10.1016/j.apcatb.2018.09.066 (  0) 0) |
| [8] |
祝琳华, 李奉隆, 司甜, 等. 层状粘土负载的金催化剂制备及其常温催化氧化活性[J]. 分子催化, 2016, 30(1): 46-53. Zhu L H, Li F L, Si T, et al. Preparation of layered clay-supported gold catalysts and catalytic activity for CO oxidation at room temperature[J]. Journal of Molecular Catalysis, 2016, 30(1): 46-53. DOI:10.16084/j.cnki.issn1001-3555.2016.01.006 (  0) 0) |
| [9] |
Balakumar V, Kim H, Ryu J W, et al. Uniform assembly of gold nanoparticles on S-doped g-C3N4 nanocomposite for effective conversion of 4-nitrophenol by catalytic reduction[J]. Journal of Materials Science & Technology, 2020, 40: 176-184. (  0) 0) |
| [10] |
Li Z, Brouwer C, He C. Gold-catalyzed organic transformations[J]. Chemical Reviews, 2008, 108(8): 3239-3265. DOI:10.1021/cr068434l (  0) 0) |
| [11] |
Compton O C, Nguyen S T. Graphene oxide, highly reduced graphene oxide, and graphene: Versatile building blocks for carbon-based materials[J]. Small, 2010, 6(6): 711-723. DOI:10.1002/smll.200901934 (  0) 0) |
| [12] |
Gao Y, Ma D, Wang C, et al. Reduced graphene oxide as a catalyst for hydrogenation of nitrobenzene at room temperature[J]. Chemical Communications, 2011, 47(8): 2432-2434. DOI:10.1039/C0CC04420B (  0) 0) |
| [13] |
Ge L, Zhang M, Wang R, et al. Fabrication of CS/GA/RGO/Pd composite hydrogels for highly efficient catalytic reduction of organic pollutants[J]. RSC Advances, 2020, 10(26): 15091-15097. DOI:10.1039/D0RA01884H (  0) 0) |
| [14] |
Dhara K, Ramachandran T, Nair B G, et al. Au nanoparticles decorated reduced graphene oxide for the fabrication of disposable nonenzymatic hydrogen peroxide sensor[J]. Journal of Electroanalytical Chemistry, 2016, 764: 64-70. DOI:10.1016/j.jelechem.2016.01.011 (  0) 0) |
| [15] |
Stankovich S, Dikin D A, Piner R D, et al. Synthesis of graphene-based nanosheets via chemical reduction of exfoliated graphite oxide[J]. Carbon, 2007, 45(7): 1558-1565. DOI:10.1016/j.carbon.2007.02.034 (  0) 0) |
| [16] |
Wu J, Zhu B, Zhao Y, et al. One-step eco-friendly synthesis of Ag-reduced graphene oxide nanocomposites for antibiofilm application[J]. Journal of Materials Engineering and Performance, 2020, 29(4): 2551-2559. DOI:10.1007/s11665-020-04742-9 (  0) 0) |
| [17] |
Qin X, Li Q, Asiri A M, et al. One-pot synthesis of Au nanoparticles/reduced graphene oxide nanocomposites and their application for electrochemical H2O2, glucose, and hydrazine sensing[J]. Gold Bulletin, 2014, 47(1): 3-8. (  0) 0) |
| [18] |
Cao X, Yan S, Hu F, et al. Reduced graphene oxide/gold nanoparticle aerogel for catalytic reduction of 4-nitrophenol[J]. RSC advances, 2016, 6(68): 64028-64038. DOI:10.1039/C6RA09386H (  0) 0) |
| [19] |
Darabdhara G, Das M R, Singh S P, et al. Ag and Au nanoparticles/reduced graphene oxide composite materials: synthesis and application in diagnostics and therapeutics[J]. Advances in Colloid and Interface Science, 2019, 271: 101991. DOI:10.1016/j.cis.2019.101991 (  0) 0) |
| [20] |
Fernández-Merino M J, Guardia L, Paredes J, et al. Vitamin C is an ideal substitute for hydrazine in the reduction of graphene oxide suspensions[J]. The Journal of Physical Chemistry C, 2010, 114(14): 6426-6432. DOI:10.1021/jp100603h (  0) 0) |
| [21] |
Pasricha R, Gupta S, Srivastava A K. A facile and novel synthesis of Ag-graphene-based nanocomposites[J]. Small, 2009, 5(20): 2253-2259. DOI:10.1002/smll.200900726 (  0) 0) |
| [22] |
Sun L, Li J, Cai J, et al. One pot synthesis of gold nanoparticles using chitosan with varying degree of deacetylation and molecular weight[J]. Carbohydrate Polymers, 2017, 178: 105-114. DOI:10.1016/j.carbpol.2017.09.032 (  0) 0) |
| [23] |
魏刚, 顾峥烨, 龚水水, 等. 红外光谱法氧化石墨烯表面氧化度的测定[J]. 光谱学与光谱分析, 2020, 40(6): 1722-1727. Wei G, Gu Z Y, Gong S S, et al. Determination of the oxidizability on the surface of the graphene oxide layer by infrared spectroscopy[J]. Spectroscopy and Spectral Analysis, 2020, 40(6): 1722-1727. (  0) 0) |
| [24] |
Jasuja K, Berry V. Implantation and growth of dendritic gold nanostructures on graphene derivatives: Electrical property tailoring and Raman enhancement[J]. ACS Nano, 2009, 3(8): 2358-2366. DOI:10.1021/nn900504v (  0) 0) |
| [25] |
Xu C, Shi X, Ji A, et al. Fabrication and characteristics of reduced graphene oxide produced with different green reductants[J]. PLoS One, 2015, 10(12): e0144842. DOI:10.1371/journal.pone.0144842 (  0) 0) |
| [26] |
Kosowska K, Domalik-Pyzik P, Nocuń M, et al. Chitosan and graphene oxide/reduced graphene oxide hybrid nanocomposites-evaluation of physicochemical properties[J]. Materials Chemistry and Physics, 2018, 216: 28-36. DOI:10.1016/j.matchemphys.2018.05.076 (  0) 0) |
| [27] |
Cobos M, González B, Fernández M J, et al. Study on the effect of graphene and glycerol plasticizer on the properties of chitosan-graphene nanocomposites via in situ green chemical reduction of graphene oxide[J]. International Journal of Biological Macromolecules, 2018, 114: 599-613. DOI:10.1016/j.ijbiomac.2018.03.129 (  0) 0) |
| [28] |
Ma Q, Song J, Jin C, et al. A rapid and easy approach for the reduction of graphene oxide by formamidinesulfinic acid[J]. Carbon, 2013, 54: 36-41. DOI:10.1016/j.carbon.2012.10.067 (  0) 0) |
| [29] |
Shin H J, Kim K K, Benayad A, et al. Efficient reduction of graphite oxide by sodium borohydride and its effect on electrical conductance[J]. Advanced Functional Materials, 2009, 19(12): 1987-1992. DOI:10.1002/adfm.200900167 (  0) 0) |
| [30] |
Zhao F, Kong W, Hu Z, et al. Tuning the performance of Pt-Ni alloy/reduced graphene oxide catalysts for 4-nitrophenol reduction[J]. RSC Advances, 2016, 6(82): 79028-79036. DOI:10.1039/C6RA16045J (  0) 0) |
| [31] |
Sahoo P K, Panigrahy B, Bahadur D. Facile synthesis of reduced graphene oxide/Pt-Ni nanocatalysts: their magnetic and catalytic properties[J]. RSC Advances, 2014, 4(89): 48563-48571. DOI:10.1039/C4RA07686A (  0) 0) |
| [32] |
Guo Y, Sun X, Liu Y, et al. One pot preparation of reduced graphene oxide (RGO) or Au (Ag) nanoparticle-RGO hybrids using chitosan as a reducing and stabilizing agent and their use in methanol electrooxidation[J]. Carbon, 2012, 50(7): 2513-2523. DOI:10.1016/j.carbon.2012.01.074 (  0) 0) |
| [33] |
Stobinski L, Lesiak B, Malolepszy A, et al. Graphene oxide and reduced graphene oxide studied by the XRD, TEM and electron spectroscopy methods[J]. Journal of Electron Spectroscopy and Related Phenomena, 2014, 195: 145-154. DOI:10.1016/j.elspec.2014.07.003 (  0) 0) |
| [34] |
Gangapuram B R, Bandi R, Alle M, et al. Microwave assisted rapid green synthesis of gold nanoparticles using Annona squamosa L peel extract for the efficient catalytic reduction of organic pollutants[J]. Journal of Molecular Structure, 2018, 1167: 305-315. DOI:10.1016/j.molstruc.2018.05.004 (  0) 0) |
| [35] |
Yeh C C, Chen D H. Ni/reduced graphene oxide nanocomposite as a magnetically recoverable catalyst with near infrared photothermally enhanced activity[J]. Applied Catalysis B: Environmental, 2014, 150: 298-304. (  0) 0) |
2. The Key Laboratory of Marine Environmental and Ecology, Ministry of Education, Ocean University of China, Qingdao 266100, China;
3. College of Chemistry and Chemical Engineering, Ocean University of China, Qingdao 266100, China
 2023, Vol. 53
2023, Vol. 53


