2. 中国海洋大学海洋环境与生态教育部重点实验室,山东 青岛 266100;
3. 中国海洋大学化学化工学院,山东 青岛 266100
芳香硝基化合物(Nitroaromatic compounds,NACs)是一类重要的化工原料,广泛应用于染料、塑料、农药和医药等领域[1]。NACs化学结构稳定,难以生物降解,因此,在相关行业废水中常见较高浓度NACs[2]。因传统的生物处理工艺很难将其有效去除[3],NACs在水体、土壤和空气中均已被检出[4-6]。NACs具有“致癌、致畸、致突变”效应,是我国水体优先控制黑名单中的危险化合物[7]。因此,有效去除废水中的NACs对环境和人体健康至关重要。在供氢体的存在下,将NACs转变为相应的芳香胺类化合物的催化还原方法不仅具有操作简单、室温转化率高等优点,还在去除NACs的同时产生了高附加值的芳香胺类化合物,可作为重要化工产品重复使用[8],是符合绿色化学理念的NACs处理方法。
贵金属纳米粒子是NACs催化还原反应中常用的催化剂。其中,纳米银粒子(Silver nanoparticles,AgNPs)因其比表面积大、催化效率高等优点而受到广泛关注[9-10]。而具有高表面能的AgNPs在使用过程中极易团聚,导致其利用率和催化效率大打折扣。以淀粉[11]、壳聚糖[12]、细菌纤维素[13]和木质素[14]等天然聚合物同时为还原剂和稳定剂的AgNPs绿色制备方法,不仅避免了制备过程中使用有毒有害化学物质,还有效防止了AgNPs的团聚[15]。壳聚糖(Chitosan,CS)是甲壳素脱乙酰基产物,是自然界中唯一大量存在的碱性多糖[16]。而CS仅能溶解于酸性溶液中,这在一定程度上限制了由其制备的AgNPs的应用。
在CS分子链上引入—CH2COOH基团制备的羧甲基壳聚糖(Carboxymethyl chitosan,CMC)与CS相比具有更优异的溶解性[17]、生物降解性[18]和生物相容性[19]。碱性条件下,Ag(Ⅰ)的氧化还原电位降低,可以在不引入任何其他还原剂的条件下,利用CMC分子链上大量存在的氨基、羟基及半缩醛羟基实现Ag(Ⅰ)的还原和AgNPs的稳定[20-21]。CMC的取代度(Degree of substitution,DS)和分子量(Molecular weight,MW)决定了其分子链构象和电荷密度[22-23],从而影响了其在AgNPs制备中的还原性和稳定性。充分认识CMC的分子参数对制备AgNPs的形貌及产量的影响,对实现AgNPs的控制合成非常重要。
本文在不添加任何化学还原剂的情况下,以不同取代度及分子量的CMC同时为还原剂和稳定剂制备AgNPs。AgNPs的尺寸和产量受实验条件(如反应温度和时间)和CMC分子参数的控制。通过紫外-可见吸收光谱(Ultraviolet and visible absorption spectroscopy,UV-vis)、傅里叶变换红外光谱(Fourier transform infrared spectroscopy,FT-IR)、透射电子显微镜(Transmission electron microscopy,TEM)和X-射线衍射(X-ray diffraction patterns,XRD)对AgNPs的尺寸形貌进行表征。以AgNPs为催化剂,以水溶液中4-硝基苯酚(4-nitrophenol,4-NP)的催化还原反应为模型反应,探究其催化还原性能。深入认识制备条件对制备AgNPs尺寸形貌的影响及不同条件下制备AgNPs的催化活性,可为AgNPs的可控制备及其构效关系的研究提供依据。
1 材料与仪器 1.1 材料和试剂壳聚糖(CS,分子量473.5 kDa,脱乙酰度93.1%)购自山东奥康生物科技有限公司。氯乙酸(ClCH2COOH) 购自天津市巴斯夫化工有限公司,硝酸银(AgNO3)、异丙醇((CH3)2CHOH)、4-硝基苯酚(4-nitrophenol,4-NP)购自国药集团化学试剂有限公司。其他化学试剂均为分析纯,实验中均使用去离子水。
1.2 实验仪器UV-2100P紫外可见分光光度计(上海菁华科技仪器有限公司),RE-5230旋转蒸发器(上海亚荣生化仪器厂),B-260恒温水浴锅(上海亚荣生化仪器厂),pH计(上海仪电科学仪器股份有限公司)。
2 实验部分 2.1 不同取代度CMC的制备以NaOH为碱化试剂,氯乙酸为羧甲基化试剂,异丙醇为反应溶剂制备CMC。将10 g CS分别加入12 mL浓度为35%(w/w),40%(w/w)和50%(w/w)的NaOH溶液中,置于-20 ℃的冰箱中过夜。自然解冻后转入三口烧瓶中,加入120 mL异丙醇搅拌均匀。分次加入12 g氯乙酸,室温下反应2 h,恒温水浴升温至60 ℃后继续反应2 h。产物透析3天后,减压蒸馏浓缩,用无水乙醇沉淀、洗涤、真空干燥后即得不同取代度的CMC,标记为CMC1,CMC2和CMC3。
2.2 不同分子量CMC的制备采用H2O2氧化降解法制备不同分子量CMC。将1 g CMC2溶解于50 mL去离子水中,加入一定量H2O2后反应一定时间。产物经浓缩、沉淀、真空干燥后即得不同分子量的CMC,反应条件列于表 1中。
|
|
表 1 不同取代度和不同分子量羧甲基壳聚糖的制备条件及分子参数 Table 1 Preparation conditions and molecular parameters of different degree of substitution carboxymethyl chitosan and low molecular weight carboxymethyl chitosan |
无特殊说明时,将3 mL 0.1%(w/v)的CMC3水溶液与1 mL 0.25 mol/L的NaOH溶液及1 mL 1 mmol/L的AgNO3溶液混合,在60 ℃下反应1 h,制备AgNPs。将不同分子参数CMC制备的AgNPs标记为CMC*-Ag。研究某一反应条件对AgNPs制备的影响时,保持其他条件不变。
2.4 表征将0.1 g CMC溶解于10 mL 0.1 mol/L HCl溶液中,用0.1 mol/L NaOH标准溶液滴定,利用电位滴定法测定CMC的取代度(degree of substitution,DS)[24]和脱乙酰度(degree of deacetylation,DD)[25]。
利用粘度法测定CMC的粘均分子量[26]。将CMC溶于0.1 mol/L NaCl溶液中,在(30±0.5) ℃下,用乌氏粘度计测定CMC的相对粘度[η],根据公式(1)计算CMC的粘均分子量(Mv):
| $ [\eta]=7.92 \times 10^{-4} M_V^{1.0}(\mathrm{~mL} / \mathrm{g}) 。$ | (1) |
使用UV-2100P紫外分光光度计(UV-vis)表征AgNPs的表面等离子体共振峰。利用H-7650型透射电子显微镜(TEM)观察AgNPs的形貌。利用Tensor 27傅里叶变换红外光谱仪(FT-IR)表征样品官能团及分子间的相互作用。使用Bruker D8 Advance X射线衍射仪,以CuKα为射线源,在管电流为500 mA和管电压为40 kV下进行X-射线衍射(XRD)分析,表征AgNPs的晶体结构。
2.5 催化性能研究在水溶液中,以4-NP催化还原为4-氨基苯酚(4-aminophenol,4-AP)的反应为模型反应,以NaBH4为供氢体,考察AgNPs的催化活性。
在30 ℃下,将0.1 mL AgNPs溶胶加入20 mL 0.2 mmol/L的4-NP和20 mL 0.1 mol/L现配的NaBH4混合溶液。在固定的时间间隔内,记录4-NP催化还原过程的紫外-可见光谱,考察AgNPs对水溶液中4-NP的催化还原活性。空白对照实验:在30 ℃下,将20 mL 0.2 mmol/L的4-NP和20 mL 0.1 mol/L现配的NaBH4溶液混合,反应30 min,记录4-NP催化还原过程的紫外-可见光谱。
使用UV-Vis仪每隔一段时间记录反应溶液。通过测定4-硝基酚阴离子(4-NPi)在400 nm处的吸光度,按公式(2)计算水溶液中4-NP的转化率:
| $ \text { Conversion }(\%)=\left(1-\frac{A_t}{A_0}\right) \times 100 \% 。$ | (2) |
式中A0和At分别为4-NPi溶液的初始吸光度和反应t时刻的吸光度。
由于反应体系中NaBH4过量,4-NP的催化反应符合准一级反应动力学,拟合方程见公式(3):
| $ \ln \left(\frac{A_0}{A_t}\right)=k t \text { 。} $ | (3) |
式中:k为催化反应速率常数,min-1;t为反应时间,min;A0为4-NPi溶液的初始吸光度;At为反应t时刻4-NPi溶液的吸光度。
3 结果与讨论 3.1 羧甲基壳聚糖的制备不同取代度及不同分子量CMC的分子参数列于表 1中。如表 1所示,通过控制NaOH的浓度,可制备不同取代度的CMC。当NaOH浓度由35%(w/w)增加到50%(w/w)时,CMC的取代度从0.392增加至0.628,且不同取代度的CMC具有相近的粘均分子量(约890 kDa)和脱乙酰度(约94%)。
以CMC2为底物,通过控制H2O2的投加量和降解反应时间可制备不同分子量的CMC。如表 1所示,CMC的分子量随着H2O2投加量的增加和降解反应时间的延长而降低。制备了粘均分子量分别为612.2、133.9和97.1 kDa的低分子量CMC,低分子量CMC与CMC2具有相近的取代度(约0.5)和脱乙酰度(约94%)。
3.2 纳米银粒子的制备 3.2.1 反应温度及时间的影响利用紫外-可见光谱技术判断AgNPs是否成功制备。根据表面等离子体共振峰(SPR)的位置推测AgNPs粒径大小[27-29],SPR最大吸收波长的蓝移表示AgNPs粒径减小,红移则表示AgNPs粒径增大。吸收峰强度越高,则表示制备的AgNPs数量越多,半峰宽越窄表示合成AgNPs的粒径分布越小。
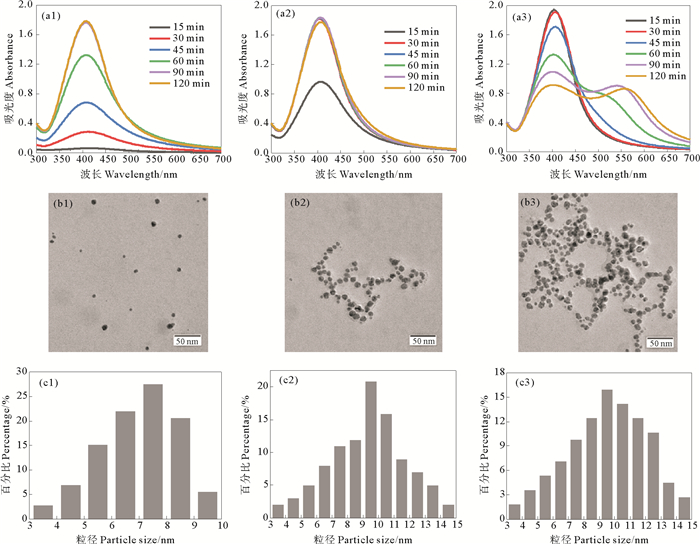
以CMC3同时为还原剂和稳定剂,在不同反应温度及时间下制备AgNPs的UV-Vis光谱如图 1(a)所示。60 ℃(见图 1(a1))下反应15 min后,没有出现AgNPs的SPR峰,说明在此条件下,无法有效制备AgNPs。反应30 min后,在411 nm处出现了较宽的AgNPs的SPR峰。随着反应时间的延长,SPR峰的强度逐渐增加,且半峰宽逐渐变窄,表明AgNPs的数量随着反应时间的延长而增加,且粒径分布逐渐变小。反应90 min后,AgNPs的SPR峰强度不再随反应时间的变化而变化。70 ℃时(见图 1(a2)),反应进行15 min后,在407 nm处出现了AgNPs的SPR峰。反应30 min时,吸收峰强度即达到最大,且不再随反应时间的变化而变化。相较于60 ℃,反应温度的升高加快了AgNPs的生成速率。温度升高,粒子间的碰撞几率增大,还原速率提高,使银核能够快速生成。反应时间延长至120 min时,AgNPs的吸收峰强度略有下降。可能是由于反应时间的延长,粒子间的碰撞聚集几率增加,与此同时在晶粒的生成过程中可能发生了Oswald熟化现象[30],即易溶解的小尺寸晶粒,溶解后释放出的Ag(0)重新在大尺寸晶粒表面生长,导致AgNPs的数量减少。结果表明,在60和70 ℃时,SPR峰强度随反应时间延长而增加,但峰位置无明显变化,说明在此温度下,反应时间决定了AgNPs的数量,而对所制备AgNPs的尺寸无明显影响。
|
((a1) 60 ℃; (a2) 70 ℃; (a3) 80 ℃; (b1) 15 min; (b2) 60 min; (b3) 120 min; (c1) 15 min; (c2) 60 min; (c3) 120 min. ) 图 1 不同温度和反应时间下制备纳米银粒子的UV-Vis光谱(a),80 ℃下反应不同时间制备纳米银粒子的TEM图像(b)和粒径分布直方图(c) Fig. 1 UV-Vis spectra of AgNPs synthesized at different temperatures and reaction time(a), TEM images(b) and particle size distribution histogram(c) of AgNPs synthesized at 80 ℃ for different reaction time |
80 ℃时(见图 1(a3)),反应15 min时即在407 nm处出现了AgNPs的SPR峰,且吸收峰强度明显高于70 ℃下得到的AgNPs的吸收峰。由图 1(b1)所示的TEM图像可知,此时制备了平均粒径为(7.1±1.3) nm且分散性良好的球形AgNPs。随着反应时间的延长,407 nm处的SPR峰强度逐渐降低且半峰宽增加。反应至60 min时,在540 nm处出现了肩峰。由图 1(b2)可知,此时制备的平均粒径为(9.3±2.5) nm的球形AgNPs彼此连接成链状。反应至90 min时,分别在402和543 nm处出现两个吸收峰。反应时间延长至120 min,第二个吸收峰由543 nm红移至557 nm。由图 1(b3)可知,此时生成了平均粒径为(9.5±2.6) nm的AgNPs,且彼此连接成网状,可能是在高温下相邻粒子之间形成网状结构以降低表面能[31]。
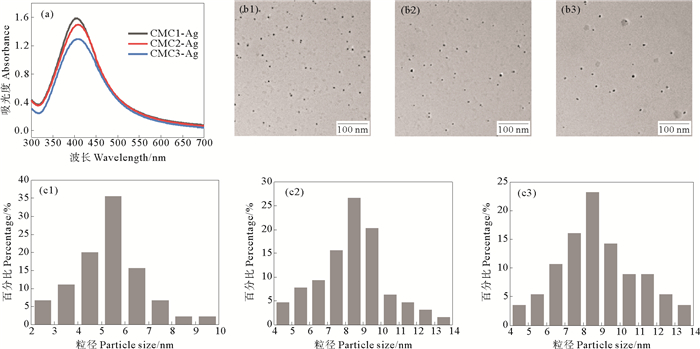
3.2.2 羧甲基壳聚糖取代度的影响图 2(a)为不同取代度的CMC制备AgNPs溶胶的UV-Vis图。如图所示,由CMC1、CMC2和CMC3制备的AgNPs溶胶的SPR峰分别出现在404、408和409 nm,且吸收峰强度逐渐减小,表明CMC对Ag(Ⅰ)的还原能力随着其取代度的增大而降低。以CMC为还原剂和稳定剂制备AgNPs时,CMC的6-OH和2-NH2参与了Ag(Ⅰ)的还原[32-33]。高取代度的CMC3中大量存在的—COO-之间的静电斥力使分子链更加伸展,使得—NH2和—OH之间有更多机会形成氢键,从而降低了其对Ag(Ⅰ)的还原能力。而低取代度的CMC1分子链中的还原基团有更多机会与Ag(Ⅰ)相互作用,生成数量较多的AgNPs。由图 2(b)可知,以CMC1、CMC2和CMC3为还原剂和稳定剂制备的AgNPs均为球形或近球形,平均粒径分别为(5.4±1.5)、(8.3±1.7)和(8.7±2.1) nm(见图 2(c))。结果表明,可通过控制CMC的取代度制备的不同尺寸的AgNPs。
|
((b1, c1) CMC1; (b2;c2) CMC2; (b3, c3) CMC3. ) 图 2 不同取代度的羧甲基壳聚糖制备纳米银粒子的UV-Vis光谱(a), TEM图像(b)和粒径分布直方图(c) Fig. 2 UV-Vis spectra(a), TEM images(b) and particle size distribution histogram(c) of prepared by CMC with different degree of substitution |
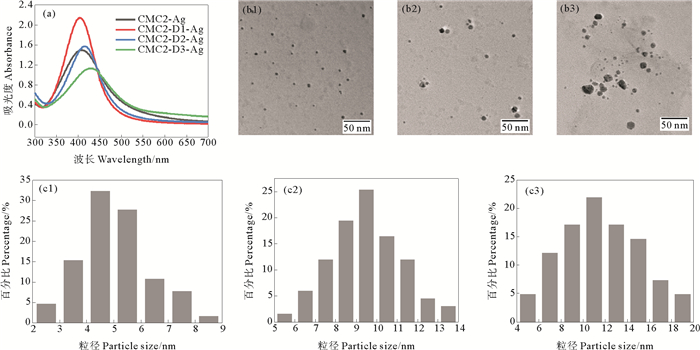
图 3(a)为不同分子量CMC制备AgNPs溶胶的UV-Vis图。如图所示,以CMC2、CMC2-D1、CMC2-D2和CMC2-D3为还原剂和稳定剂制备的AgNPs溶胶的最大吸收波长分别出现在408、405、417和429 nm,且由CMC2-D1制备的AgNPs溶胶吸收峰强度最大。由图 3(b)和(c)可知,由CMC2-D1、CMC2-D2和CMC2-D3分别制备了平均粒径为(5.1±1.2)、(9.5±1.7)和(11.7±3.4) nm的AgNPs。就四种不同分子量CMC而言,以CMC2-D1为还原剂和稳定剂可制备分散性良好的小尺寸球形AgNPs,且产量最高,表明CMC2-D1在AgNPs的制备中具有最高的还原性和稳定性。这可能是因为CMC2经过H2O2氧化降解后β-1, 4糖苷键断裂,产生了更多具有还原活性的半缩醛羟基,形成了更多的还原活性位点。但随着CMC降解程度的加深,氧化程度加重,部分半缩醛羟基被氧化成羧基[34],使CMC2-D2和CMC2-D3的还原活性逐渐降低。同时,CMC分子量的改变也导致溶液中CMC构象的转变[35],从而影响其还原性和稳定性。相较于CMC2-D2,高分子量CMC2的分子链更易缠绕而形成较强的分子内氢键,降低了对Ag(Ⅰ)的还原性和稳定性。
|
((b1, c1) CMC2-D1; (b2, c2) CMC2-D2; (b3, c3) CMC2-D3. ) 图 3 不同分子量羧甲基壳聚糖制备纳米银粒子的UV-Vis光谱(a), TEM图像(b)和粒径分布直方图(c) Fig. 3 UV-Vis spectra(a), TEM images(b) and particle size distribution histogram(c) of AgNPs prepared by CMC with different molecular weight |
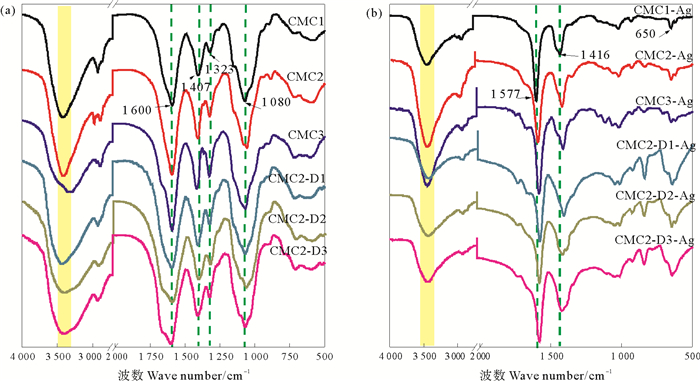
图 4(a)为不同分子参数CMC的FT-IR图。CMC在3 300~3 500 cm-1处的吸收峰为—OH和—NH基的重叠伸缩振动[36]。位于1 600和1 407 cm-1处的特征吸收峰属于—COO-的不对称和对称伸缩振动峰[21],随着CMC取代度的增加,分子链上—COO-的对称伸缩振动峰向高波数方向移动。1 323和1 080 cm-1处的特征吸收峰分别归属于酰胺Ⅲ中N—H的弯曲振动和C—O的伸缩振动[37]。CMC2经H2O2氧化降解后得到的低分子量CMC具有相似的FT-IR光谱。
|
图 4 不同分子参数的羧甲基壳聚糖(a)和不同分子参数羧甲基壳聚糖制备的纳米银(b)的红外光谱图 Fig. 4 FT-IR spectra of CMC(a) with different molecular parameters and synthesized AgNPs (b) |
在CMC1-Ag的红外光谱中,CMC1位于3 300~3 500 cm-1处的—OH和—NH基团的伸缩振动峰向低波数方向移动,—COO-的不对称和对称伸缩振动峰分别由1 600 cm-1位移至1 577 cm-1,由1 407 cm-1移至1 416 cm-1,表明CMC分子中—OH、—NH和—COO-参与了Ag(Ⅰ)的还原及AgNPs的稳定[38]。在650 cm-1处归属于AgNPs的特征吸收峰,证实了AgNPs的成功制备[39]。
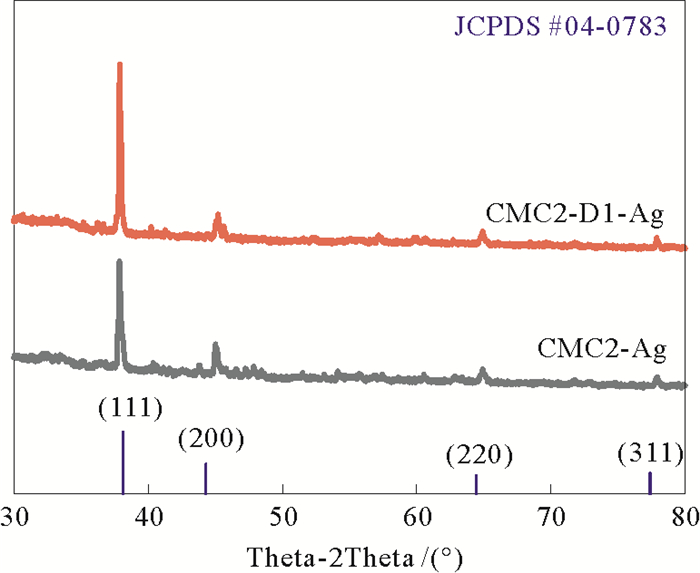
3.3.2 X-射线衍射AgNPs的X-射线衍射图谱如图 5所示。CMC2-Ag和CMC2-D1-Ag在37.9°、45.2°、64.9°和77.9°处的衍射峰分别对应于AgNPs(111)、(200)、(220)和(311)晶面相,与其面心立方(FCC)结构一致(JCPDS 04-0783)[40]。AgNPs(111)晶面的衍射峰最强,表明AgNPs主要沿着(111)方向生长。由Debye-Scherrer公式[41]计算得知CMC2-Ag和CMC2-D1-Ag的平均粒径尺寸分别为8.11和5.04 nm,这与之前的TEM结果一致。
|
图 5 CMC2-Ag及CMC2-D1-Ag的XRD图谱 Fig. 5 XRD patterns of CMC2-AgNPs and CMC2-D1-AgNPs |
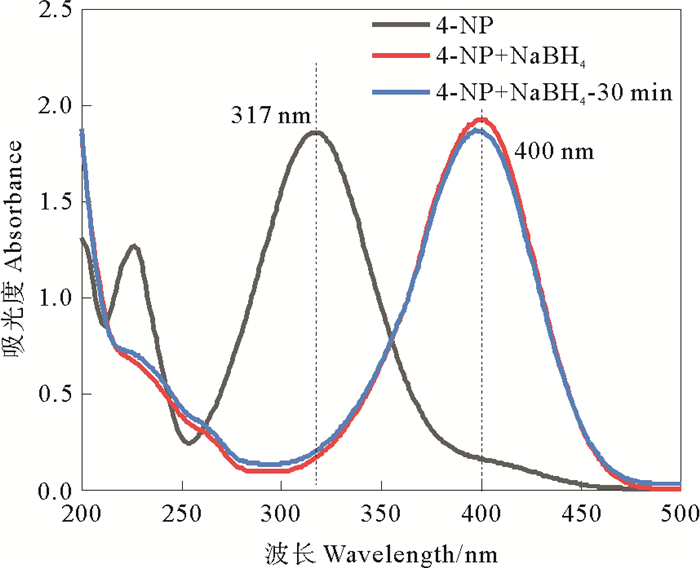
不添加AgNPs催化剂时,4-NP及4-NP和NaBH4混合溶液的UV-vis光谱图如图 6所示。4-NP的最大吸收波长位于317 nm,加入NaBH4后生成了4-NPi,最大吸收波长红移至400 nm。4-NP与NaBH4的混合溶液在30 ℃下振荡30 min后吸收峰强度也没有明显改变,说明没有AgNPs作催化剂时,NaBH4不能还原4-NP。这是因为4-NP/4-AP与H3BO3/BH4-的标准电极电位分为-0.76和-1.33 V,与标准氢电极电位相比,在不添加催化剂时,在动力学上是受限的[42]。此外,BH4-和4-NPi会产生相互排斥,导致两者之间产生了较高的动力学壁垒[43]。
|
图 6 4-NP以及4-NP与NaBH4混合溶液的UV-vis光谱图 Fig. 6 UV-vis spectra of 4-NP and 4-NP mixed with NaBH4 solution |
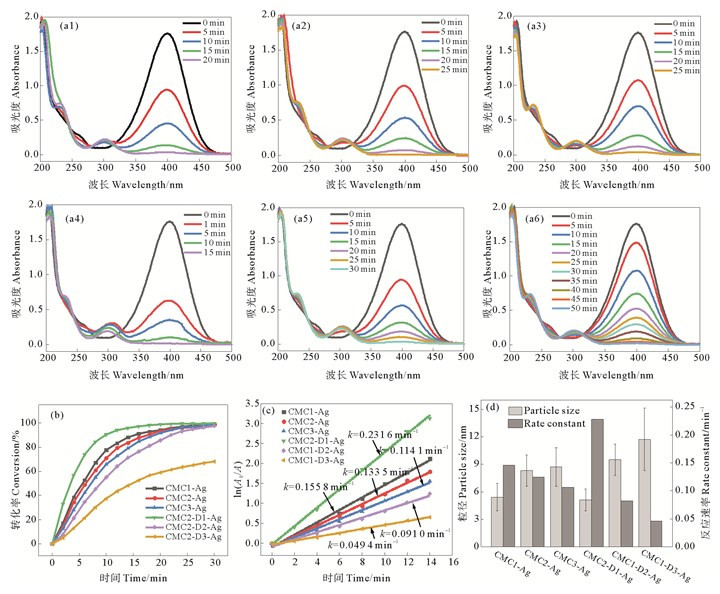
图 7(a)为以不同分子参数CMC同时为还原剂和稳定制备的AgNPs为催化剂催化还原水溶液中4-NP的UV-vis光谱。如图 7(a1)所示,向4-NP和NaBH4的混合溶液中加入AgNPs后,400 nm处4-NPi的吸收峰强度逐渐减弱,并在300 nm处出现了4-AP的吸收峰。如图 7(a1)—(a3)所示,以CMC1-Ag为催化剂时,完成催化还原反应需20 min;以CMC2-Ag和CMC3-Ag为催化剂,完成催化还原反应需25 min,表明以低取代度CMC为还原剂和稳定剂制备的AgNPs具有较高的催化还原活性。如图 7(a4)—(a6)所示,以不同分子量CMC为还原剂和稳定剂制备的AgNPs具有明显不同的4-NP催化活性。以CMC2-D1-Ag为催化剂时,仅在15 min即可将4-NP完全转化为4-AP;而以CMC2-D2-Ag和CMC2-D3-Ag为催化剂时,实现4-NP的完全转化则分别需30和50 min。
|
((a1) CMC1-Ag; (a2) CMC2-Ag; (a3) CMC3-Ag; (a4) CMC2-D1-Ag; (a5) CMC2-D2-Ag; (a6) CMC2-D3-Ag. ) 图 7 不同种类催化剂催化还原4-NP的UV-vis图(a),不同种类催化剂催化4-NP的转化率(b),lnA0/A随时间t的变化图(c)及粒径和转化率的关系图(d) Fig. 7 UV-vis spectra of the catalytic reduction of 4-NP with(a), 4-NP conversion versus time (b), ln(A0/A) versus time for the catalytic reduction of 4-NP with different catalyst species(c) and the relationship diagram between particle size and conversion rate(d) |
图 7(b)为不同分子参数CMC制备的AgNPs催化还原水溶液中4-NP的转化率随时间的变化图。所有AgNPs催化4-NP的转化率均随反应时间的延长而增加。以CMC1-Ag、CMC2-Ag、CMC3-Ag、CMC2-D1-Ag、CMC2-D2-Ag和CMC2-D3-Ag为催化剂时,反应20 min后,4-NP的催化还原转化率分别为94.1%、93.3%、91.7%、98.8%、85.5%和59.1%。延长反应时间至30 min时,CMC2-D3-Ag催化4-NP的转化率增加至68.0%,其他催化剂的反应体系中4-NP的转化率均达97%以上。
图 7(c)为不同分子参数CMC制备的AgNPs催化还原水溶液中4-NP的动力学方程拟合图。如图所示,催化反应符合伪一级反应动力学方程,ln(A0/A)与反应时间t呈现较好的线性关系(R2均大于0.98)。由伪一级反应动力学方程得到的反应速率常数列于图 7(d)中。如图所示,以CMC1-Ag、CMC2-Ag、CMC3-Ag、CMC2-D1-Ag、CMC2-D2-Ag和CMC2-D3-Ag为催化剂时,催化还原4-NP的速率常数分别为0.155 8、0.133 5、0.114 1、0.231 6、0.091 0和0.049 4 min-1。由此可见,CMC2-D1-Ag催化的4-NP还原反应具有最高的反应速率。结合AgNPs的TEM分析结果可以看出,AgNPs的催化活性与其粒径相关,CMC2-D1-Ag可能因其小粒径和大比表面积,表现了最高的4-NP催化还原活性。
将CMC-Ag催化还原4-NP的k值与其他文献进行比较(见表 2),结果表明,本研究获得的k值高于一些已报道的AgNPs催化还原4-NP的k值。
|
|
表 2 CMC-Ag催化还原4-NP的速率常数(k) 与文献报道的催化剂体系的比较 Table 2 Comparison of the rate constant (k) for CMC-Ag catalytic reduction of 4-NP with other reported catalyst systems |
以不同取代度及分子量的羧甲基壳聚糖同时为还原剂和稳定剂成功制备了AgNPs。通过调节反应温度、时间和羧甲基壳聚糖的取代度及分子量可以控制AgNPs的尺寸和产量。由低取代度和低分子量羧甲基壳聚糖可制备分散性良好的小粒径AgNPs。以羧甲基壳聚糖同时为还原剂和稳定剂制备的AgNPs对水溶液中4-NP表现出优异的催化还原性能。AgNPs对4-NP的催化活性与其粒径相关,小粒径的AgNPs对4-NP的催化还原活性较强。本研究提供了一种绿色的AgNPs制备方法,为催化还原水溶液中4-NP的高效催化剂的制备提供了一种新的思路。
| [1] |
Wang Q, Yang Z. Industrial water pollution, water environment treatment, and health risks in China[J]. Environmental Pollution, 2016, 218: 358-365. DOI:10.1016/j.envpol.2016.07.011 (  0) 0) |
| [2] |
Pizarro A H, Molina C B, Casas J A, et al. Catalytic HDC/HDN of 4-chloronitrobenzene in water under ambient-like conditions with Pd supported on pillared clay[J]. Applied Catalysis B: Environmental, 2014, 158-159: 175-181. DOI:10.1016/j.apcatb.2014.04.011 (  0) 0) |
| [3] |
Dai R, Chen J, Lin J, et al. Reduction of nitro phenols using nitroreductase from E. coli in the presence of NADH[J]. Journal of Hazardous Materials, 2009, 170(1): 141-143. DOI:10.1016/j.jhazmat.2009.04.122 (  0) 0) |
| [4] |
Kumar P, Kim K, Lee J, et al. Metal-organic framework for sorptive/catalytic removal and sensing applications against nitroaromatic compounds[J]. Journal of Industrial and Engineering Chemistry, 2020, 84: 87-95. DOI:10.1016/j.jiec.2019.12.024 (  0) 0) |
| [5] |
Schmalz L, Weber A, Trnckner S. Determination of polar nitroaromatic compounds in soils and the impact of the soil properties on the extraction results[J]. Analytica Chimica Acta, 2010, 678: 189-194. DOI:10.1016/j.aca.2010.08.030 (  0) 0) |
| [6] |
Frka S, Sala M, Brodnik H, et al. Seasonal variability of nitroaromatic compounds in ambient aerosols: Mass size distribution, possible sources and contribution to water-soluble brown carbon light absorption[J]. Chemosphere, 2022, 299: 134381. DOI:10.1016/j.chemosphere.2022.134381 (  0) 0) |
| [7] |
周文敏, 傅德黔, 孙宗光. 中国水中优先控制污染物黑名单的确定[J]. 环境科学研究, 1991, 4(6): 9-12. Zhou W M, Fu D Q, Sun Z G. Determination of blacklist of priority pollutants in water in China[J]. Research of Environmental Sciences, 1991, 4(6): 9-12. DOI:10.3321/j.issn:1001-6929.1991.06.003 (  0) 0) |
| [8] |
Atarod M, Nasrollahzadeh M, Sajadi S M. Green synthesis of Pd/RGO/Fe3O4 nanocomposite using Withania coagulans leaf extract and its application as magnetically separable and reusable catalyst for the reduction of 4-nitrophenol[J]. Journal of Colloid and Interface Science, 2016, 465: 249-258. DOI:10.1016/j.jcis.2015.11.060 (  0) 0) |
| [9] |
Khatoon U, Velidandi A, Rao G. Sodium borohydride mediated synthesis of nano-sized silver particles: Their characterization, anti-microbial and cytotoxicity studies[J]. Materials Chemistry and Physics, 2022, 294: 126997. (  0) 0) |
| [10] |
Ping Y, Zhang J, Xing T, et al. Green synthesis of silver nanoparticles using grape seed extract and their application for reductive catalysis of Direct Orange 26[J]. Journal of Industrial and Engineering Chemistry, 2018, 58: 74-79. DOI:10.1016/j.jiec.2017.09.009 (  0) 0) |
| [11] |
Hebeish A, Shaheen T, El-Naggar M. Solid state synthesis of starch-capped silver nanoparticles[J]. International Journal of Biological Macromolecules, 2016, 87: 70-76. DOI:10.1016/j.ijbiomac.2016.02.046 (  0) 0) |
| [12] |
Lou C W, Chen A P, Li T T, et al. Antimicrobial activity of UV-induced chitosan capped silver nanoparticles[J]. Materials Letters, 2014, 128: 248-252. DOI:10.1016/j.matlet.2014.04.145 (  0) 0) |
| [13] |
Yang G, Xie J, Deng Y, et al. Hydrothermal synthesis of bacterial cellulose/AgNPs composite: A "green" route for antibacterial application[J]. Carbohydrate Polymers, 2012, 87: 2482-2487. DOI:10.1016/j.carbpol.2011.11.017 (  0) 0) |
| [14] |
Li Y, Yang D, Li P, et al. Lignin as a multi-functional agent for the synthesis of Ag nanoparticles and its application in antibacterial coatings[J]. Journal of Materials Research and Technology, 2022, 17: 3211-3220. DOI:10.1016/j.jmrt.2022.02.049 (  0) 0) |
| [15] |
Novikov I, Pigaleva M, Abramchuk S, et al. Chitosan composites with Ag nanoparticles formed in carbonic acid solutions[J]. Carbohydrate Polymers, 2018, 190: 103-112. DOI:10.1016/j.carbpol.2018.02.076 (  0) 0) |
| [16] |
Riegger B, Baurer B, Mirzayeva A, et al. A systematic approach of chitosan nanoparticle preparation via emulsion crosslinking as potential adsorbent in wastewater treatment[J]. Carbohydrate Polymers, 2018, 180: 46-54. DOI:10.1016/j.carbpol.2017.10.002 (  0) 0) |
| [17] |
Shariatinia Z. Carboxymethyl chitosan: Properties and biomedical applications[J]. International Journal of Biological Macromolecules, 2018, 120: 1406-1419. DOI:10.1016/j.ijbiomac.2018.09.131 (  0) 0) |
| [18] |
Huo W, Zhang W, Wang W, et al. Physicochemical properties and drug release behavior of biguanidino and O-carboxymethyl chitosan microcapsules[J]. International Journal of Biological Macromolecules, 2014, 70: 257-265. DOI:10.1016/j.ijbiomac.2014.06.049 (  0) 0) |
| [19] |
Chen X, Wang Z, Liu W, et al. The effect of carboxymethyl-chitosan on proliferation and collagen secretion of normal and keloid skin fibroblasts[J]. Biomaterials, 2002, 23: 4609-4614. DOI:10.1016/S0142-9612(02)00207-7 (  0) 0) |
| [20] |
Xu Q, Zheng W, Duan P, et al. One-pot fabrication of durable antibacterial cotton fabric coated with silver nanoparticles via carboxymethyl chitosan as a binder and stabilizer[J]. Carbohydrate Polymers, 2019, 204: 42-49. DOI:10.1016/j.carbpol.2018.09.089 (  0) 0) |
| [21] |
Fouda M G, Aassar M R, Deyab S S. Antimicrobial activity of carboxymethyl chitosan/polyethylene oxide nanofibers embedded silver nanoparticles[J]. Carbohydrate Polymers, 2013, 92(2): 1012-1017. DOI:10.1016/j.carbpol.2012.10.047 (  0) 0) |
| [22] |
Jayakumar R, Prabaharan M, Nair S V, et al. Novel carboxymethyl derivatives of chitin and chitosan materials and their biomedical applications[J]. Progress in Materials Science, 2010, 55(7): 675-709. DOI:10.1016/j.pmatsci.2010.03.001 (  0) 0) |
| [23] |
Lei M, Huang W, Sun J, et al. Synthesis, characterization, and performance of carboxymethyl chitosan with different molecular weight as additive in water-based drilling fluid[J]. Journal of Molecular Liquids, 2020, 310: 113-127. (  0) 0) |
| [24] |
El-Nesr E M, Raafat A I, Nasef S M, et al. Radiation synthesis and characterization of N, O-carboxymethyl chitosan/poly (vinylpyrrolidone) copolymer hydrogel[J]. Arab Journal of Nuclear Science and Applications, 2014, 47(1): 14-27. (  0) 0) |
| [25] |
Li J, Du Y, Liang H. Influence of molecular parameters on the degradation of chitosan by a commercial enzyme[J]. Polymer Degradation and Stability, 2007, 92(3): 515-524. DOI:10.1016/j.polymdegradstab.2006.04.028 (  0) 0) |
| [26] |
Chen L, Du Y, Wu H, et al. Relationship between molecular structure and moisture-retention ability of carboxymethyl chitin and chitosan[J]. Journal of Applied Polymer Science, 2002, 83(6): 1233-1241. DOI:10.1002/app.2290 (  0) 0) |
| [27] |
Lee K S, El-Sayed M A. Gold and silver nanoparticles in sensing and imaging: Sensitivity of plasmon response to size, shape, and metal composition[J]. Journal of Physical Chemistry B, 2006, 110(39): 19220-19225. DOI:10.1021/jp062536y (  0) 0) |
| [28] |
Wu F, Cheng L, Wang W. Surface plasmon resonance of large-size Ag nanobars[J]. Micromachines, 2022, 13: 638-649. DOI:10.3390/mi13040638 (  0) 0) |
| [29] |
Kottappara R, Pillai S C, Vijayan B K. Copper-based nanocatalysts for nitroarene reduction—A review of recent advances[J]. Inorganic Chemistry Communications, 2020, 121: 108181. DOI:10.1016/j.inoche.2020.108181 (  0) 0) |
| [30] |
吴宗山, 李莉. 天然产物绿色合成小尺寸纳米银及抗菌性[J]. 精细化工, 2014, 31(8): 964-968. Wu Z S, Li L. Green synthesis of small size silver nanoparticles from natural products and their antibacterial properties[J]. Fine Chemicals, 2014, 31(8): 964-968. (  0) 0) |
| [31] |
Yuan J, Li C, Yang B, et al. The facile synthesis, crystallization behavior and magnetic property of FeNiP amorphous nanoparticles[J]. Materials Characterization, 2018, 136: 94-99. DOI:10.1016/j.matchar.2017.12.008 (  0) 0) |
| [32] |
Sun L, Pu S, Li J, et al. Size controllable one step synthesis of gold nanoparticles using carboxymethyl chitosan[J]. International Journal of Biological Macromolecules, 2019, 122: 770-783. DOI:10.1016/j.ijbiomac.2018.11.006 (  0) 0) |
| [33] |
Huang S, Yu Z, Zhang Y, et al. In situ green synthesis of antimicrobial carboxymethyl chitosan-nanosilver hybrids with controlled silver release[J]. International Journal of Nanomedicine, 2017, 12: 3181-3191. DOI:10.2147/IJN.S130397 (  0) 0) |
| [34] |
Tian F, Liu Y, Hu K, et al. The depolymerization mechanism of chitosan by hydrogen peroxide[J]. Journal of Materials Science, 2003, 38: 4709-4712. DOI:10.1023/A:1027466716950 (  0) 0) |
| [35] |
Chen L, Du Y, Zeng X. Relationships between the molecular structure and moisture-absorption and moisture-retention abilities of carboxymethyl chitosan: Ⅱ. Effect of degree of deacetylation and carboxymethylation[J]. Carbohydrate Research, 2003, 338(4): 333-340. DOI:10.1016/S0008-6215(02)00462-7 (  0) 0) |
| [36] |
曾春芽, 单慧媚, 赵超然, 等. 纳米铁-氧化石墨烯/壳聚糖复合材料的制备及其力学性能[J]. 复合材料学报, 2022, 39(4): 1739-1747. Zeng C Y, Shan H M, Zhao C R, et al. Preparation and mechanical properties of iron nanoparticles-graphene oxide/chitosan composites[J]. Acta Materiae Compositae Sinica, 2022, 39(4): 1739-1747. (  0) 0) |
| [37] |
Madhusudhan A, Reddy G, Venkatesham M, et al. Efficient pH dependent drug delivery to target cancer cells by gold nanoparticles capped with carboxymethyl chitosan[J]. International Journal of Molecular Sciences, 2014, 15: 8216-8234. DOI:10.3390/ijms15058216 (  0) 0) |
| [38] |
Laudenslager M, Schiffman J, Schauer C. Carboxymethyl chitosan as a matrix material for platinum, gold, and silver nanoparticles[J]. Biomacromolecules, 2008, 9: 2682-2685. DOI:10.1021/bm800835e (  0) 0) |
| [39] |
Youssef A M, El-Aziz M, El-Sayed E, et al. Rational design and electrical study of conducting bionanocomposites hydrogel based on chitosan and silver nanoparticles[J]. International Journal of Biological Macromolecules, 2019, 140: 886-894. DOI:10.1016/j.ijbiomac.2019.08.199 (  0) 0) |
| [40] |
Ramaraghavulu R, Rao V, Devarayapalli K, et al. Green synthesized AgNPs decorated on Ketjen black for enhanced catalytic dye degradation[J]. Research on Chemical Intermediates, 2021, 47(2): 1-12. (  0) 0) |
| [41] |
Sahoo P K, Panigrahy B, Bahadur D. Facile synthesis of reduced graphene oxide/Pt-Ni nanocatalysts: Their magnetic and catalytic properties[J]. RSC Advances, 2014, 4(89): 48563-48571. DOI:10.1039/C4RA07686A (  0) 0) |
| [42] |
Geng Q, Du J. Reduction of 4-nitrophenol catalyzed by silver nanoparticles supported on polymer micelles and vesicles[J]. RSC Advances, 2014, 4(32): 16425-16428. DOI:10.1039/C4RA01866D (  0) 0) |
| [43] |
Rout L, Kumar A, Dhaka R S. Bimetallic Au-Cu alloy nanoparticles on reduced graphene oxide support: Synthesis, catalytic activity and investigation of synergistic effect by DFT analysis[J]. Applied Catalysis A: General, 2017, 538: 107-122. DOI:10.1016/j.apcata.2017.03.017 (  0) 0) |
| [44] |
Shaha Z, Gul T, Khanb S, et al. Synthesis of high surface area AgNPs from Dodonaea viscosa plant for the removal of pathogenic microbes and persistent organic pollutants[J]. Materials Science and Engineering B, 2021, 263: 114770. DOI:10.1016/j.mseb.2020.114770 (  0) 0) |
| [45] |
Muhammad I, Khan M I, Khan S, et al. Catalytic reduction of picric acid, nitrophenols and organic azo dyes via green synthesized plant supported Ag nanoparticles[J]. Journal of Molecular Liquids, 2018, 268: 87-101. DOI:10.1016/j.molliq.2018.07.030 (  0) 0) |
| [46] |
Elged A H, Shaban S M, Eluskkary M M, et al. Impact of hydrophobic tails of new phospho-zwitterionic surfactants on the structure, catalytic, and biological activities of AgNPs[J]. Journal of Industrial and Engineering Chemistry, 2021, 94: 435-447. DOI:10.1016/j.jiec.2020.11.017 (  0) 0) |
| [47] |
Zheng Z, Huang Q, Guan H, et al. In situ synthesis of silver nanoparticles dispersed or wrapped by a Cordyceps sinensis exopolysaccharide in water and their catalytic activity[J]. RSC Advances, 2015, 85: 69790-69799. (  0) 0) |
| [48] |
Narayanan K B, Park H H, Sakthivel N. Extracellular synthesis of mycogenic silver nanoparticles by Cylindrocladium floridanum and its homogeneous catalytic degradation of 4-nitrophenol[J]. Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy, 2013, 116: 485-490. DOI:10.1016/j.saa.2013.07.066 (  0) 0) |
2. Key Laboratory of Marine Environmental and Ecology, Ministry of Education, Ocean University of China, Qingdao 266100, China;
3. College of Chemistry and Chemical Engineering, Ocean University of China, Qingdao 266100, China
 2024, Vol. 54
2024, Vol. 54


