2. 中国海洋大学海洋环境与生态教育部重点试验室,山东 青岛 266100
随着水产养殖业的快速发展,抗生素类药物被广泛使用,但同时带来了抗生素原药或代谢产物在环境中的残留问题。目前,抗生素被认为是新兴的污染物,它们对生态系统存在潜在毒性,对抗生素耐药细菌和耐药基因存在持续选择性压力[1]。在抗生素的种类、数量和检出率方面,养殖区沉积物均远远高于水体,说明养殖区沉积物不仅是抗生素的储存库,也是水体抗生素潜在的释放源[2]。
与其它抗生素相比,喹诺酮类抗生素由于抗菌谱广、杀菌作用强、耐药性和毒副作用小等优点被广泛应用于水产养殖中[3]。其中恩诺沙星属第三代氟喹诺酮类抗生素,目前被我国指定为动物专用药,在水产养殖中防治病害[4]。由于恩诺沙星有较大的疏水性,极易被吸附在沉积物中[3],在养殖沉积物中有很高的残留浓度和检出率[5],因此研究沉积物中恩诺沙星的去除方法对降低海水养殖区抗生素的污染具有重要意义。目前对海水养殖过程抗生素去除的研究主要集中在海水中抗生素的降解,关于沉积物中抗生素去除技术的报道较少,尤其对海水养殖区沉积物中抗生素去除的报道更是匮乏。赵晴[6]构建河湖沉积物微生物燃料电池,运行45 d后发现,沉积物中四环素和土霉素均有一定的降解效果,去除率分别为67.8%和60%。邓经惠[7]应用沉积物微生物燃料电池对沉积物中的磺胺甲噁唑进行降解,运行25 d后去除率高达80% 以上。
已有研究表明,沉积物微生物燃料电池(Sediment microbial fuel cell, SMFC)可以有效降解沉积物中多种持久性污染物,包括多环芳烃[8]、多氯联苯[9]和抗生素[10]等。SMFC是微生物燃料电池(Microbial fuel cell, MFC)的一种,它在降解污染物的同时,可以将有机废物中的化学能转化为电能[11]。生物电化学过程中的电子是通过阳极(埋在厌氧的沉积物中)上的电化学活性细菌氧化有机物产生的,并迁移到阴极(悬浮在有氧的上覆水中),最终与水中的氧气、质子发生反应生成水[12-13]。阳极材料的选择对产电性能至关重要,主要表现在微生物附着和电子传递方面[14]。近年来,聚苯胺(Polyaniline, PANI)和MnO2得到了广泛的研究:PANI是一种导电聚合物,易于经济合成且生物相容性较高[15]; MnO2是过渡金属氧化物,原料廉价易得,化学稳定性好并且对环境友好[16]; 但是它们也分别存在机械强度差[17]、导电性不高[18]等缺点。理想的阳极材料应该满足比表面积大、导电性强和生物相容性高等要求[19],因此通常利用不同材料的优点进行复合以制得良好的阳极。
本研究以海水养殖区沉积物为燃料构建SMFC系统,通过合成PANI、MnO2、PANI/MnO2 3种材料对阳极碳毡(Carbon felt, CF)进行修饰,以提高SMFC的产电性能; 以沉积物中特定污染物恩诺沙星为研究对象,探究SMFC系统对恩诺沙星的去除效果和同步产电性能; 结合恩诺沙星降解过程的生物毒性分析来验证SMFC系统作为新兴的生物修复技术对沉积物中抗生素类污染物去除的可行性。研究结果可为SMFC系统在底泥生物修复的实际应用提供参考。
1 材料与方法 1.1 样品的采集和预处理沉积物采自山东省海洋生物研究院海水养殖基地,用不锈钢筛网过筛去除杂质后再离心弃去上清液,最后搅拌均匀避光保存。在同一地点采集新鲜的养殖海水。沉积物和海水样品均储存在4 ℃的冰箱里备用。
1.2 三种改性阳极的制备采用原位化学聚合法制备三种改性阳极[20]。
对CF进行预处理:在丙酮溶液中浸泡24 h后在乙醇溶液中超声清洗30 min,再将其分别放在10% H2O2和10% 稀HCl中,90 ℃水浴各加热3 h,用蒸馏水冲洗干净后置于60 ℃烘箱中干燥备用。
MnO2/CF:称取0.245 g的MnO2粉末,加入5 mL去离子水,超声分散30 min,再加入3 mL 60% 的聚四氟乙烯(PTFE)乳液,用毛刷均匀地涂抹在预处理后的CF表面,并在40 ℃烘箱中烘干。
PANI/CF:称取2.28 g过硫酸铵(APS),溶于1 mol·L-1 HCl溶液中备用。量取0.91 mL蒸馏提纯后的苯胺单体,溶解到300 mL 1 mol·L-1 HCl溶液中,将预处理后的CF浸没在上述溶液中,并在冰浴和磁力搅拌条件下逐滴加入25 mL APS溶液,反应6 h,取出CF(墨绿色),置于1 mol·L-1 HCl中浸泡直至不褪色,用去离子水冲洗后放在60 ℃烘箱中烘干。
PANI-MnO2/CF:将上述MnO2和PANI溶液在常温下反应5 h,用丙酮和0.2 mol·L-1 HCl溶液洗涤去除反应副产物,然后在1 mol·L-1 HCl溶液中浸泡1.5 h后过滤洗涤多次,所得样品在60℃下干燥研磨即得PANI/MnO2复合材料。称取0.32 g复合材料与PTFE稀释液混合,超声分散30 min,制成浆糊,将其均匀涂覆在预处理后的CF表面,60 ℃下干燥即得PANI-MnO2/CF改性阳极。
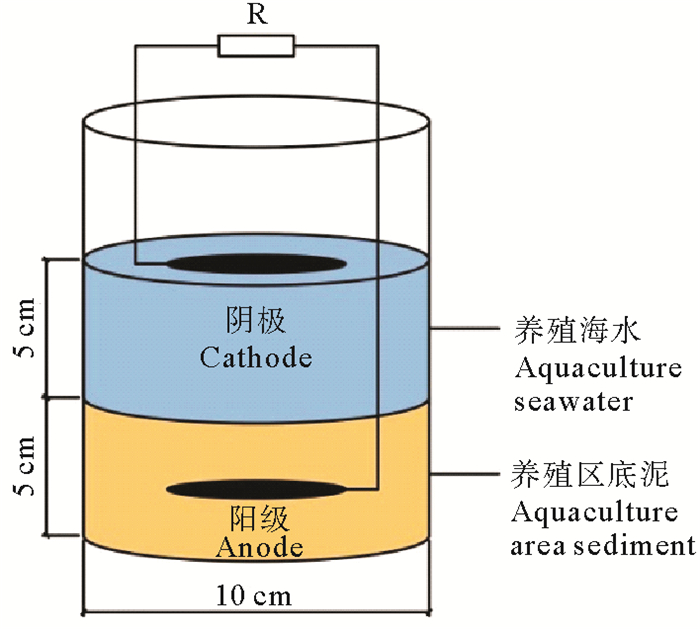
1.3 SMFC系统的构建与运行本实验采用5个SMFC反应器,结构如图 1所示。反应容器为1 L的烧杯,底部沉积物和上覆海水的厚度均为5 cm。阴阳极均选用碳毡,直径为6 cm,厚度为0.5 cm,阳极埋在沉积物中,距离反应器底部2 cm,阴极漂浮在水面上,阴阳极的间距为7.5 cm。选用耐腐蚀的钛丝作为导线,直径0.5 mm,连接阴阳极的外阻为1 500 Ω。装置全程在黑暗条件下运行。
|
图 1 SMFC反应器结构图 Fig. 1 SMFC reactor structure |
表 1为不同反应装置的运行条件。研究不同改性阳极SMFC的产电性能时,将未改性CF、MnO2/CF、PANI/CF、PANI-MnO2/CF修饰的SMFC系统依次命名为SMFC-1、SMFC-2、SMFC-3、SMFC-4。研究沉积物中恩诺沙星的降解情况时,向处理好的沉积物中加入12.81 ng·g-1的恩诺沙星,分别设置实验组和对照组。实验组(有SMFC系统)选用PANI-MnO2/CF复合电极做阳极,对照组(无SMFC系统)模拟自然环境下抗生素的降解情况。
|
|
表 1 不同反应装置的运行条件 Table 1 Operating conditions of different devices |
用万用表采集SMFC的电压。采用稳态放电法测定SMFC的极化曲线,改变电阻箱的阻值,使外电阻阻值在10 000~100 Ω的范围内不断降低。功率密度根据标准方法计算[21]。用扫描电镜(Scanning electron microscope, SEM)表征CF、MnO2/CF、PANI/CF、PANI-MnO2/CF 4种电极的表面形貌,X射线能谱(Energy dispersive X-ray spectrometry, EDX)表征PANI-MnO2/CF的元素组成。用固相萃取(Solid phase extraction, SPE)提取样品中的抗生素、高效液相色谱-质谱(High performance liquid chromatography-mass spectrometry, HPLC-MS)测定恩诺沙星的浓度[22]。恩诺沙星的色谱条件如下:色谱柱:Waters BEH C18(2.1 mm×100 mm,1.7 μm); 柱温:40 ℃; 进样量:5 μL; 流动相:(A) 0.1%甲酸-10 mmol甲酸铵水溶液(B)乙腈; 流速:0.3 mL·min-1; 荧光检测波长: 激发波长280 nm,发射波长452 nm。恩诺沙星的质谱条件如下:离子源模式:ESI; 正离子模式传输毛细管温度:250 ℃; 离子源温度:350 ℃; 雾化器温度:325 ℃; 电压:3.2 kV; 采集模式:一级高分辨母离子模式。称重法测定沉积物的烧失量(Loss of ignition, LOI)。发光细菌法测定抗生素的生物急性毒性[23]。
2 结果与讨论 2.1 阳极表征如图 2所示,a、b、c、d依次是未改性CF、PANI/CF、MnO2/CF、PANI-MnO2/ CF的扫描电镜图像。可以看出,未改性CF碳纤维表面光滑、干净,有少量的浅沟槽,纹路清晰; PANI修饰的CF表面出现絮状沉积聚合物且结构疏松,说明颗粒间存在团聚现象,加大了CF的粗糙程度,有利于微生物的富集; MnO2颗粒饱满且表面比较光滑,一定程度上提高了CF的比表面积,但分散不均匀; PANI-MnO2/CF复合材料修饰的CF表面不仅粗糙而且致密紧凑,大大提高了颗粒的表面积,有利于微生物在颗粒的三维方向上吸附生长,增加微生物的吸附数量,加大反应位点以提高产电性能。

|
图 2 不同阳极的扫描电镜图像 Fig. 2 SEM images of different anodes |
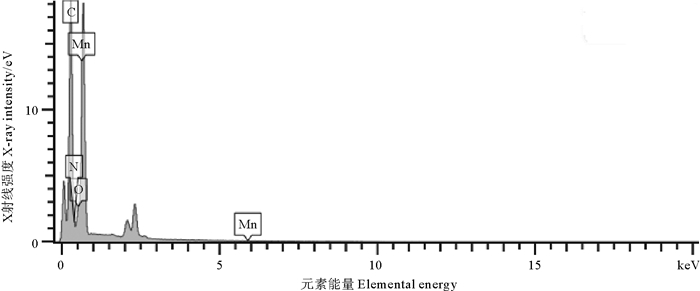
为了鉴定PANI是否被MnO2颗粒包裹,对制备的PANI-MnO2/CF复合材料进行了EDX元素组成分析。如图 3所示,EDX表明复合材料表面含有氮元素、锰元素和氧元素,证明MnO2成功涂覆在PANI的表面。
|
图 3 PANI-MnO2/CF的X射线能谱图 Fig. 3 EDX spectra of PANI-MnO2/CF |
|
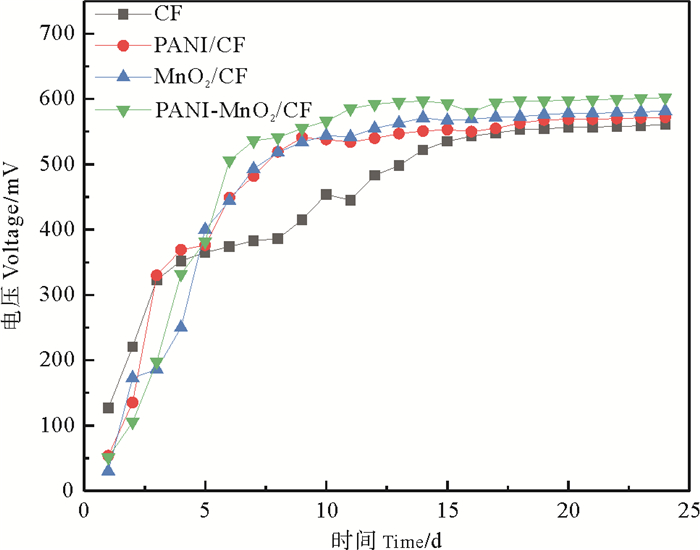
图 4 不同阳极条件下的电压变化 Fig. 4 Voltage changes of different anodes conditions |
分别采用未改性CF、MnO2/CF、PANI/CF、PANI-MnO2/CF为阳极,研究了以海水养殖区沉积物为燃料的SMFC系统的产电性能。
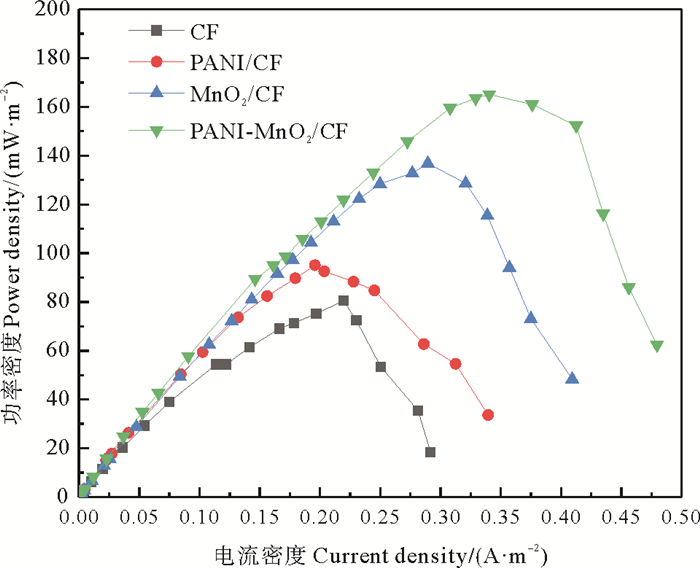
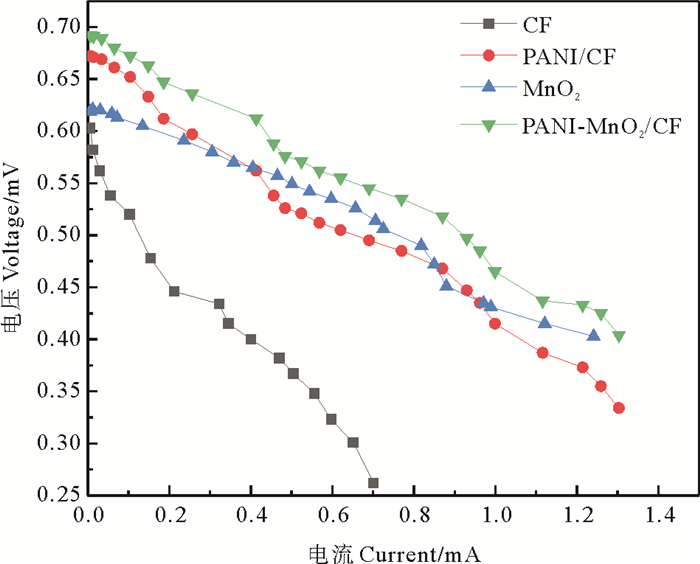
由图 4可知,4种不同阳极修饰的SMFC系统,其电压随时间变化的整体趋势一样,自启动第1天起就开始产生电压,并且一直持续上升最终趋于稳定。其中输出电压最高的是SMFC-4装置,在第10天左右电压趋于稳定,说明此时产电细菌已成功富集在阳极生物膜上,电池启动成功[24],最后电压达到最大值602 mV。而装置SMFC-2和SMFC-3的电压始终低于SMFC-4,最大电压分别为582和572 mV; SMFC-1启动速率是最慢的,输出电压也是最低的,第15天时才达到最大电压561 mV。从图 5可知,装置SMFC-1、SMFC-2、SMFC-3和SMFC-4的最大功率密度分别为80.52、141.83、95.10和165.09 mW·m-2,其中装置SMFC-4的最大功率密度最大,产电性能最佳。阳极改性后的装置SMFC-2、SMFC-3和SMFC-4最大功率密度分别是未改性装置SMFC-1的1.76、1.18和2.05倍。图 6是极化曲线,它的斜率表示电池内阻的大小,内阻越大,电子传递效率越低。可以看出阳极改性后装置SMFC-2、SMFC-3和SMFC-4的斜率均比未改性装置SMFC-1的平缓,说明它们的内阻都小于SMFC-1的内阻。改性后的阳极提高了电池的抗极化能力,进而使SMFC产电稳定性增强。
|
图 5 不同阳极条件下的功率密度曲线 Fig. 5 Power density of different anodes conditions |
|
图 6 不同阳极条件下的极化曲线 Fig. 6 Polarization curves of different anodes conditions |
通过分析输出电压、功率密度和极化曲线,可知4种不同阳极修饰的SMFC系统的产电性能从大到小依次为SMFC-4>SMFC-2>SMFC-3>SMFC-1。因此通过阳极改性可以使电极的比表面积增大,从而增加了产电细菌在电极的附着量,生物相容性增大,使电极得以活化,电子的传递效率大大提高,最终提高了电池的产电性能[25]。
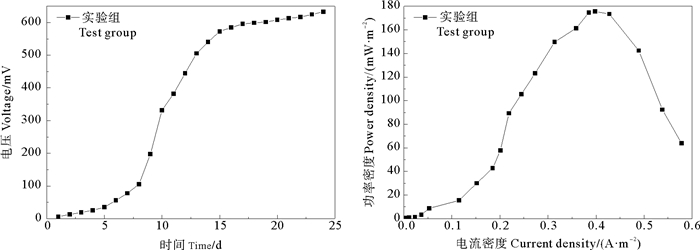
2.3 恩诺沙星对SMFC产电性能的影响由2.2得知,PANI-MnO2/ CF为阳极的SMFC系统产电性能最佳,因此选用PANI-MnO2/ CF进行实验。图 7为实验组的输出电压变化和功率密度曲线。从图中可以看出,输出电压在实验前期(7~8 d内)先缓慢增长,后面急速上升,15 d后趋于稳定,最终达到最大电压633 mV,并且最大功率密度为175 mW·m-2。与装置SMFC-4相比,抗生素的加入只是延长了电池的启动时间,电池的最大输出电压和功率密度不仅没有下降反而有所提高,Zhang等[26]也有类似的研究结果。这说明刚开始恩诺沙星的加入只是暂时抑制了产电细菌的生长,7 d后产电细菌对恩诺沙星有了耐受性[27],并把抗生素作为阳极电子供体加以利用,促进了SMFC系统的电子传递,从而促进了SMFC产电性能的提高,这与Zhou等[28]的结果相一致。抗生素的加入并不都是抑制微生物的生长,SMFC系统对抗生素具有很强的耐受性,在一定范围内低浓度的抗生素可以促进SMFC产电性能的提高。
|
图 7 实验组的输出电压变化和功率密度曲线 Fig. 7 Output voltage variation and power density curve of the test group |
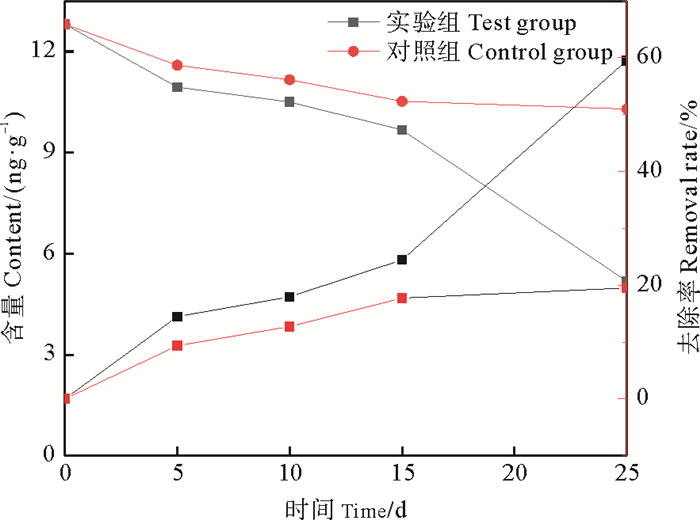
图 8为恩诺沙星在沉积物中的含量变化。随着反应时间增加,沉积物中恩诺沙星含量一直在下降,且实验组的下降速率大于对照组的下降速率。恩诺沙星在沉积物中的初始含量均为12.81 ng·g-1,而实验末期恩诺沙星的含量分别为5.18和10.29 ng·g-1,去除率分别达到了59.52%和19.53%。实验组对沉积物中恩诺沙星的去除率是对照组的3.05倍,说明SMFC系统可以有效去除沉积物中的恩诺沙星,从而减少恩诺沙星向上覆海水中扩散的浓度。这是因为一方面恩诺沙星成为产电细菌的碳源之一[10],继而被产电细菌利用,从而加快了抗生素的去除; 另一方面由于沉积物中加入了SMFC系统,为降解恩诺沙星的微生物提供了更多的活性位点,大大提高了降解该种抗生素菌群的生存空间和成活条件[29]。
|
图 8 沉积物中恩诺沙星的降解情况 Fig. 8 Degradation of enrofloxacin in sediments |
表 2为海水中恩诺沙星的浓度变化和降幅。虽然初期上覆海水中没有恩诺沙星,但在整个运行过程中,沉积物中的恩诺沙星不断向上覆海水中迁移扩散,即沉积物为恩诺沙星的释放源。在实验组和对照组两个装置中,海水里恩诺沙星的浓度都是先升高后下降,但在整个迁移扩散过程中,实验组迁移到上覆海水里恩诺沙星的浓度始终低于对照组。在第5天到第25天内,对照组迁移到上覆海水的恩诺沙星浓度从0.021 ng·mL-1减少到0.018 ng·mL-1,降幅为14.29%。实验组迁移到上覆海水的恩诺沙星浓度从0.019 ng·mL-1减少到0.005 ng·mL-1,降幅为73.68%,是对照组的5.16倍。另外,上覆海水中恩诺沙星的降幅与沉积物中恩诺沙星的降幅正相关。
|
|
表 2 海水中恩诺沙星的浓度变化 Table 2 Concentration changes of enrofloxacin in seawater |
因此,应用SMFC系统既可以有效降解沉积物中的恩诺沙星,减轻对上覆海水的内源污染,也能使迁移到上覆海水中恩诺沙星的浓度大幅度降低,在一定程度上同时减少沉积物和上覆水中抗生素的污染。
2.5 沉积物中有机物含量的变化采用LOI分析各装置沉积物中可氧化有机质含量的变化,结果如表 3所示。初始LOI为4.3%,在实验末期实验组和对照组中沉积物的LOI分别降低到1.7%和3.11%,降幅分别为60.47%和27.67%。实验组对LOI的降幅是对照组的2.19倍。这些结果表明,SMFC系统对有机物的降解效果优于自然情况下的生物厌氧降解。因为SMFC系统中的电极为微生物提供了更多的活性位点,闭路条件又为电子传递提供了便利,从而加快了沉积物中有机物的氧化。另外,沉积物中的有机物在SMFC系统被阳极上的细菌氧化后,在沉积物表面形成氧化层,该氧化层可以防止沉积物中的有毒化合物扩散到上覆海水中,使养殖区的水质更好地适合养殖动物的生长。反过来,利用SMFC系统也能更好地维持养殖区底部沉积物氧化层不受破坏[30]。
|
|
表 3 沉积物烧矢量的变化 Table 3 Changes of LOI in sediment |
用发光细菌法分别检测实验组和对照组反应过程中海水和沉积物中的生物毒性变化。发光抑制率越高,生物急性毒性越强。
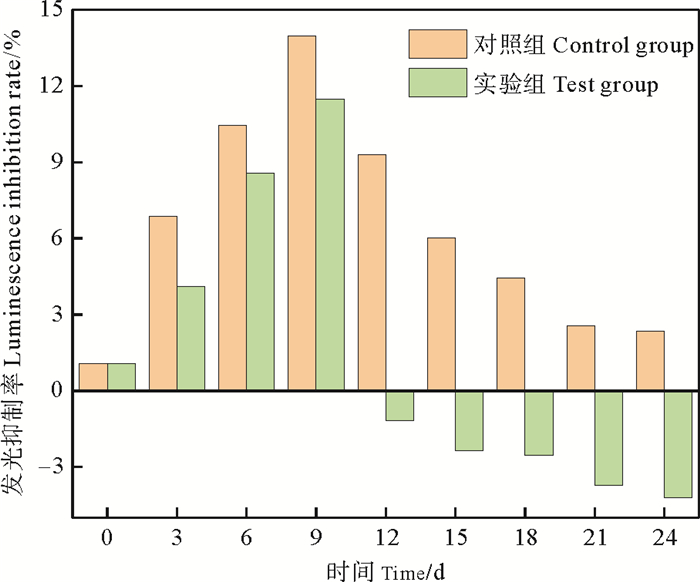
图 9为海水中的生物毒性变化。随着反应的进行,实验组和对照组的发光抑制率均先升高后下降,海水中毒性也是先升高后下降,说明迁移到海水中的目标污染物恩诺沙星的浓度也是先升高后下降,表明实验组和对照组对海水中恩诺沙星的去除均有效果。但是实验组的发光抑制率总是低于对照组,尤其12 d以后,实验组的发光抑制率为负值,最终海水未检测出毒性。这些结果说明,海水经SMFC系统处理后的生物毒性远低于自然降解条件下的生物毒性,与系统中恩诺沙星的去除率高是一致的。Li等[31]在应用CW-MFC装置对磺胺类抗生素的降解过程中也得到类似的结果,最终出水无毒性。
|
图 9 海水中的生物毒性变化 Fig. 9 Changes of biological toxicity in seawater |
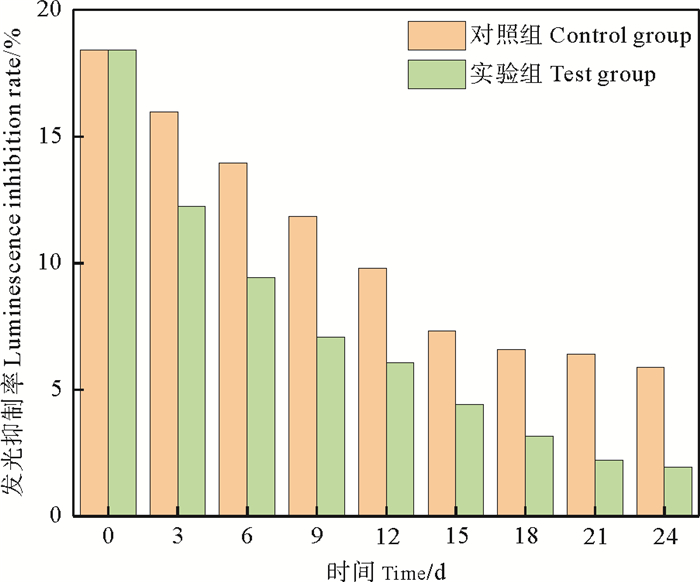
图 10为沉积物中的生物毒性变化。随着反应的进行,实验组和对照组的发光抑制率均一直下降,说明沉积物中目标污染物恩诺沙星的浓度也一直在下降,因此沉积物中的生物毒性在降低。与海水中生物毒性变化趋势一样,实验组的发光抑制率始终低于对照组,最终实验组的发光抑制率低于2%,为低毒。说明SMFC系统对恩诺沙星的去除有显著效果。
|
图 10 沉积物中的生物毒性变化 Fig. 10 Changes of biological toxicity in sediments |
(1) 用原位化学聚合法制备了3种电极材料以改性阳极碳毡(MnO2/CF、PANI/CF、PANI-MnO2/CF)。3种改性碳毡表面积和粗糙程度均比未改性碳毡大,有利于产电细菌的富集,促进阳极电子传递。其中PANI-MnO2/CF改性的SMFC系统产电性能最好,最高输出电压为602 mV,最大功率密度为165.09 mW·m-2。
(2) 低浓度恩诺沙星(12.81 ng·g-1)的存在既可以提高SMFC系统的产电性能,也可以被SMFC系统有效降解,去除率为59.52%;从沉积物迁移到上覆海水的恩诺沙星浓度先升高后下降,降幅为72.73%,是自然条件下的5.16倍。由于阳极微生物对恩诺沙星有很好的耐受性,恩诺沙星可以作为碳源被产电细菌和抗生素类降解细菌利用,从而提高产电性能和抗生素的去除效果。
(3) SMFC系统对沉积物中有机物的降解效果优于自然条件下的生物降解,LOI的降幅分别为60.47%和27.67%。SMFC系统在氧化沉积物中有机物的同时在其表面形成氧化层,该氧化层可以防止沉积物中的有毒化合物扩散到上覆海水中。
(4) SMFC系统运行结束后上覆海水未检测出生物毒性,最终沉积物中的生物毒性远低于自然降解条件下的生物毒性,说明SMFC系统可降低海水和沉积物中恩诺沙星的生态风险。
| [1] |
Stephen B, Nicholas T, François-Xavier W, et al. Genomic insights into the emergence and spread of antimicrobial-resistant bacterial pathogens[J]. Science, 2018, 360(6390): 733-738. DOI:10.1126/science.aar3777 (  0) 0) |
| [2] |
梁惜梅, 施震, 黄小平, 等. 珠江口典型水产养殖区抗生素的污染特征[J]. 生态环境学报, 2013, 22(2): 304-310. Liang X M, Shi Z, Huang X P, et al. Pollution characteristics of antibiotics in a typical aquaculture area of the Pearl River Estuary[J]. Acta Eco-Environmental Sciences, 2013, 22(2): 304-310. DOI:10.3969/j.issn.1674-5906.2013.02.022 (  0) 0) |
| [3] |
Van D X, Dewulf J, Van L H, et al. Fluoroquinolone antibiotics: An emerging class of environmental micropollutants[J]. Science of the Total Environment, 2014(500-501): 250-269. (  0) 0) |
| [4] |
黄铢玉, 方龙香, 宋超, 等. 抗生素恩诺沙星在渔业中的研究进展[J]. 农学学报, 2019, 9(11): 57-62. Huang Z Y, Fang L X, Song C, et al. Research progress of antibiotic enrofloxacin in fishery[J]. Acta Agricultural Sciences, 2019, 9(11): 57-62. DOI:10.11923/j.issn.2095-4050.cjas20190500023 (  0) 0) |
| [5] |
Han Q F, Zhang X R, Xu X Y, et al. Antibiotics in marine aquaculture farms surrounding Laizhou Bay, Bohai Sea: Distribution characteristics considering various culture modes and organism species[J]. Science of the Total Environment, 2021(760): 143863-143875. (  0) 0) |
| [6] |
赵晴. 河湖沉积物微生物燃料电池的运行特性与微生物群落特征[D]. 天津: 天津大学, 2017. Zhao Qin. Operational Characteristics and Microbial Comunity Characteristics of Microbial Fuel Cells in River and Lake Sedments[D]. Tianjin: Tianjin University, 2017. (  0) 0) |
| [7] |
邓经惠. 沉积物微生物燃料电池对磺胺甲噁唑的降解及微生物群落结构变化的影响研究[D]. 天津: 天津大学, 2018. Deng Jinghui. Effects of Sedimiment Microbial Fuel Cells on the Degradation of Sulfamethoxazole and Changes in Microbial Community Structure[D]. Tianjin: Tianjin University, 2017. (  0) 0) |
| [8] |
Sherafatmand M, Ng H Y. Using sediment microbial fuel cells (SMFCs) for bioremediation of polycyclic aromatic hydrocarbons (PAHs)[J]. Bioresource Technology, 2015(195): 122-130. (  0) 0) |
| [9] |
Wu M S, Xu X, Lu K X, et al. Effects of the presence of nanoscale zero-valent iron on the degradation of polychlorinated biphenyls and total organic carbon by sediment microbial fuel cell[J]. Science of the Total Environment, 2019(656): 39-44. (  0) 0) |
| [10] |
Wang Y Z, Zhang H M, Feng Y J, et al. Bio-Electron-Fenton (BEF) process driven by sediment microbial fuel cells (SMFCs) for antibiotics desorption and degradation[J]. Biosensors and Bioelectronics, 2019(136): 8-15. (  0) 0) |
| [11] |
Pant D, Van B G, Diels L, et al. A review of the substrates used in microbial fuel cells (MFCs) for sustainable energy production[J]. Bioresource Technology, 2010, 101(6): 1533-1543. DOI:10.1016/j.biortech.2009.10.017 (  0) 0) |
| [12] |
Logan B E, Hamelers B, Rozendal R, et al. Microbial fuel cells: methodology and technology[J]. Environmental Science & Technology, 2006, 40(17): 5181-5192. (  0) 0) |
| [13] |
Gowthami P, Ho-Young J, Sadhasivam T, et al. A comprehensive review on microbial fuel cell technologies: Processes, utilization, and advanced developments in electrodes and membranes[J]. Journal of Cleaner Production, 2019(221): 598-621. (  0) 0) |
| [14] |
Wang Y Q, Li B, Zeng L Z, et al. Polyaniline/mesoporous tungsten trioxide composite as anode electrocatalyst for high-performance microbial fuel cells[J]. Biosensors and Bioelectronics, 2013(41): 582-588. (  0) 0) |
| [15] |
Li C, Luo M M, Zhou S H, et al. Study on synergistic mechanism of PANDAN modification, current and electroactive biofilms on Congo red decolorization in microbial fuel cells[J]. International Journal of Hydrogen Energy, 2020, 45(53): 29417-29429. DOI:10.1016/j.ijhydene.2020.07.246 (  0) 0) |
| [16] |
Praveena M, Rajeev J. Electrochemical deposition of MWCNT-MnO2/PPy nano-composite application for microbial fuel cells[J]. International Journal of Hydrogen Energy, 2016, 9(20): 22394-22405. (  0) 0) |
| [17] |
Zhai D D, Fang Z, Jin H W, et al. Vertical alignment of polyaniline nanofibers on electrode surface for high-performance microbial fuel cells[J]. Bioresource Technology, 2019(288): 121-127. (  0) 0) |
| [18] |
Fischer A E, Pettigrew K A, Rolison D R, et al. Incorporation of homogeneous, nanoscale MnO2 within ultraporous carbon structures via self-limiting electroless deposition: Implications for electrochemical capacitors[J]. Nano Letters, 2007, 7(2): 281-287. DOI:10.1021/nl062263i (  0) 0) |
| [19] |
Wang Y Y, Zheng H T, Chen Y, et al. Macroporous composite capacitive bioanode applied in microbial fuel cells[J]. Chinese Chemical Letters, 2020, 31(1): 205-209. DOI:10.1016/j.cclet.2019.05.052 (  0) 0) |
| [20] |
Wang Y Y, Wen Q, Chen Y, et al. A novel polyaniline interlayer manganese dioxide composite anode for high-performance microbial fuel cell[J]. Journal of the Taiwan Institute of Chemical Engineers, 2017(75): 112-118. (  0) 0) |
| [21] |
刘志华, 李小明, 方丽, 等. 污泥为燃料的微生物燃料电池运行特性研究[J]. 中国环境科学, 2012, 32(2): 268-273. Liu Z H, Li X M, Fang L, et al. Operating characteristic of microbial fuel cell using sludge[J]. China Environmental Science, 2012, 32(2): 268-273. DOI:10.3969/j.issn.1000-6923.2012.02.013 (  0) 0) |
| [22] |
Han Q F, Zhao S, Zhang X R, et al. Distribution, combined pollution and risk assessment of antibiotics in typical marine aquaculture farms surrounding the Yellow Sea, North China[J]. Environment International, 2020(138): 1051-1055. (  0) 0) |
| [23] |
孙成华, 刘保献, 衡丽娜, 等. 发光细菌急性毒性─费氏弧菌冻干法方法建立及质控[J]. 现代科学仪器, 2014, 12(6): 155-159. Sun C H, Liu B X, Heng L N, et al. Establishment and quality control of freeze-drying method for the acute toxicity of luminescent bacteria-Vibrio fischeri[J]. Modern Scientific Instruments, 2014, 12(6): 155-159. (  0) 0) |
| [24] |
Liang Y X, Zhai H Y, Liu B Y, et al. Carbon nanomaterial-modified graphite felt as an anode enhanced the power production and polycyclic aromatic hydrocarbon removal in sediment microbial fuel cells[J]. Science of the Total Environment, 2020(713): 1364-1383. (  0) 0) |
| [25] |
Liao Z H, Sun J Z, Sun D Z, et al. Enhancement of power production with tartaric acid doped polyaniline nanowire network modified anode in microbial fuel cells[J]. Bioresource Technology, 2015(192): 831-835. (  0) 0) |
| [26] |
Zhang E R, Yu Q L, Zhai W J, et al. High tolerance of and removal of cefazolin sodium in single-chamber microbial fuel cells operation[J]. Bioresource Technology, 2018(249): 76-81. (  0) 0) |
| [27] |
Brim S O, Li S N, Zhou Q X, et al. Simultaneous removal and high tolerance of norfloxacin with electricity generation in microbial fuel cell and its antibiotic resistance genes quantification[J]. Bioresource Technology, 2020(304): 122-129. (  0) 0) |
| [28] |
Zhou Y, Zhu N W, Guo W Y, et al. Simultaneous electricity production and antibiotics removal by microbial fuel cells[J]. Journal of Environmental Management, 2018(217): 565-572. (  0) 0) |
| [29] |
Yan W F, Wang S H, Ding R, et al. Long-term operation of electroactive biofilms for enhanced ciprofloxacin removal capacity and anti-shock capabilities[J]. Bioresource Technology, 2019(275): 192-199. (  0) 0) |
| [30] |
Sajana T K, Ghangrekar M M, Mitra A, et al. Application of sediment microbial fuel cell for in situ reclamation of aquaculture pond water quality[J]. Aquacultural Engineering, 2013(57): 101-107. (  0) 0) |
| [31] |
Li H, Cai Y, Gu Z L, et al. Accumulation of sulfonamide resistance genes and bacterial community function prediction in microbial fuel cell-constructed wetland treating pharmaceutical wastewater[J]. Chemosphere, 2020(248): 126-140. (  0) 0) |
2. The Key Laboratory of Marine Environment and Ecology, Ministry of Education, Ocean University of China, Qingdao 266100, China
 2022, Vol. 52
2022, Vol. 52


