2. 青岛张村河水务有限公司,山东 青岛 266100;
3. 中国海洋大学海洋环境与生态教育部重点实验室,山东 青岛 266100
氯代烃(Chlorinated aliphatic hydrocarbons, CAHs)主要作为电子元器件的清洗剂、多种有机物质的溶剂以及重要的化工原料,自20世纪40年代起被大量应用于现代工业中[1-2]。氯代烃微溶于水,是重质非水相流体,其在包气带中垂直迁移能力强,容易进入地下水并在隔水层中累积形成不断扩散的污染羽,对周边地下水的水质产生极大影响[3]。三氯乙烯(Trichloroethylene, TCE)作为脱脂剂和工业清洗剂,由于意外泄漏和过去的不当处置,已成为地下水中最常见的氯代烃之一。TCE的生物降解性较低,在土壤中的半衰期可达0.5~1.5 a,在地下水中的半衰期可达1.0~4.5 a[4],对人类健康可产生长期威胁。因此,探索经济高效的TCE污染地下水修复技术是对污染场地进行风险控制和管理的必然需求和重要前提。
微米零价铁(Micron zero-valent iron, mZVI)作为一种高效修复材料在发挥其自身还原优势基础上,还能有效激活原位微生物,实现对TCE的耦合修复[5-6],在氯代烃污染地下水修复中具有良好的应用前景[7]。然而,复杂的地下水中存在大量天然电子受体将与氯代烃竞争电子导致ZVI材料浪费,诱导有毒有害副产物产生,在氯代烃的脱氯效率、电子效率和产物构成等方面影响整体修复性能,例如硝酸盐(NO3-)作为地下水中最常见的天然电子受体之一,将与TCE竞争电子并影响耦合技术对目标污染物的还原效果[8],引发负面的经济、环境效应。
目前,人们提出了多种有前景的材料改性手段来解决TCE作为电子供体时ZVI体系对其选择性低下的问题,包括硫化[9-11]、碳改性[12-15]等,主要是通过增加对疏水有机物的高结合能力,形成原电池以加速ZVI的腐蚀,防止ZVI颗粒聚集以减少ZVI在现场应用中的堵塞和浪费,从而提高ZVI的电子选择性和活性。对于ZVI的硫化和碳改性技术,近年来学者研究出一种共同的材料制备方法——球磨法,可以使得某些固-固反应在常温常压条件下完成,操作简单高效,且材料改性效果更佳。但是在实际应用中,球磨法会受到关键参数——改性剂添加量(如S/Fe摩尔比、C/Fe质量比)的影响,进而影响去除目标污染物的活性和选择性[2]。对于硫化技术,一方面,S/Fe摩尔比会影响经硫化后铁(S-ZVI)的性能:较高的S/Fe摩尔比可使S-ZVI产生更多的FeS和更大的比表面积,有利于污染物的还原;另一方面,高S/Fe摩尔比会加剧Fe0向铁氧化物转化,造成ZVI还原能力的浪费[16]。对于碳改性技术,碳含量会影响对目标污染物的吸附能力,随着碳含量的增加,材料的孔隙和比表面积均显著增加,对污染物的吸附能力也随之增加,促进了污染物的去除效果[17]。但值得注意的是,随着碳含量的增加,对污染物吸附能力的增强并不能保证ZVI对污染物发生显著的还原去除,因为碳含量的增加会增加碳层厚度,延长电子迁移距离,使ZVI的活性大大减弱[17]。因此,为了提高硫化及碳改性技术对污染物的去除能力,选择合适的改性剂添加量十分重要。而目前学者对改性剂添加量的研究仅停留在ZVI体系,尚未展开研究改性剂添加量对硫化和碳改性技术应用于耦合体系时的影响,因此亟待寻求改性耦合体系中最佳的改性剂添加量,这对提高耦合体系去除TCE的效率十分必要。
本研究拟以典型氯代烃TCE为目标污染物,以NO3-为代表性共存电子受体,以室内批量实验为依托,对比不同改性剂添加量对硫化、碳改性耦合体系去除TCE和NO3-的动力学特征和产物构成的影响,并阐明不同改性剂添加量对耦合体系微生物群落构成的影响。
1 材料方法 1.1 不同铁基材料的制备本研究采用了文献中常用的球磨方法[16]制备硫化及碳改性后的mZVI(S-mZVIbm、C-mZVIbm,其中上标bm表示球磨法),将铁粉分别与硫粉、活性炭按一定比例(S/Fe摩尔比分别为0、0.01、0.05、0.1,C/Fe质量比分别0、0.2%、0.5%、1%)混合在球磨介质中,以球料比为60∶1加入氧化锆球珠。向球磨罐内冲入N2作为保护气,将其密封后置于行星式球磨机上,设定转速为300 r·min-1,硫化mZVI球磨8 h,碳改性mZVI球磨6 h后,在充满氩气的手套箱中分离出球磨介质内的材料,得到S-mZVIbm和C-mZVIbm。
1.2 厌氧微生物的驯化本研究所使用的活性污泥取自青岛市张村河生活污水处理厂厌氧消化池。将20 mL活性污泥置于180 mL含有TCE(20 mg/L)和NO3-(10 mg/L)的培养基中进行厌氧驯化,以模拟受TCE和NO3-污染的环境,培养基成分见表 1。使用N-2-羟乙基哌嗪-N-2-乙烷磺酸(HEPES)缓冲溶液将培养基的初始pH值调至7.0±0.2。用N2对血清瓶进行除氧,以保持溶解氧(DO)浓度低于0.5 mgO2/L,每隔两天向血清瓶中通入60 mLH2为微生物提供足够的电子供体。将血清瓶置于摇床中,转速设定为160 r·min-1,初始温度设定为30 ℃,而后逐渐冷却直至驯化结束时温度保持在18 ℃,以此来模拟地下水真实环境并保证微生物良好的生长活性。以7 d为一个驯化周期,当第一周期结束时,倒去血清瓶中180 mL上清液并置换新的培养基,加入20 mg/L TCE,10 mg/L NO3-并定期加入H2继续培养,以相同的步骤连续驯化四个周期,监测到TCE和NO3-去除率达到100%说明厌氧驯化完成。
|
|
表 1 培养基的成分组成 Table 1 Composition of the medium |
批量实验在52 mL的厌氧顶空瓶中进行,将驯化结束且具有良好生物活性的厌氧微生物加入到科学配制的模拟地下水中(见表 1),稀释微生物至波长600 nm处吸光度(OD600)在0.10~0.12之间,表示体系中微生物的生物量,得到供使用的模拟地下水及微生物混合液。利用HEPES调节模拟地下水pH至约7.0±0.2,设置厌氧顶空瓶蒸汽(顶空)与液相(模拟地下水)体积约为1∶3,利用N2流对厌氧顶空瓶进行脱氧以保持DO浓度低于0.5 mgO2/L。设置mZVI、TCE和NO3-的浓度分别为5 g/L、20 mg/L和10 mg/L(以N计)。将厌氧顶空瓶放置在18 ℃和140 r·min-1的恒温振荡器中,以模拟真实的地下水条件。实验组别设置如下:(1)硫化改性剂添加量对TCE还原性能的影响:设置一个对照组(mZVI/AB,其中AB表示微生物)和三个处理组(S/Fe摩尔比分别为0.01、0.05、0.1)以比较TCE及NO3-去除的整体性能。(2)碳改性技术改性剂添加量对TCE还原性能的影响:设置一个对照组(mZVI/AB)和三个处理组(C/Fe质量比分别为0.2%、0.5%、1%)以比较TCE及NO3-去除的整体性能(见表 2)。所有体系于0、0.5、1、1.5、2、2.5、3、4、5、7、9、11、15、20、30 d测定NO3-及其还原产物的浓度,C-mZVIbm/AB和mZVI/AB体系于0、3、5、7、13、16、20、25、30、40、65、80 d测量TCE及其降解产物的浓度,S-mZVIbm/AB体系于0.25、0.5、0.75、1、1.5、2、3、5、7 d时测量TCE及其降解产物的浓度。
|
|
表 2 批量实验组别设置 Table 2 Batch experiment group settings |
(1) TCE及其降解产物的测定
厌氧顶空瓶中的TCE及其降解产物(顺式-二氯乙烯(cis-DCE)、反式-二氯乙烯(trans- DCE)、1, 1-二氯乙烯(1, 1- DCE)、氯乙烯(VC)、乙炔(C2H2)、乙烯(C2H4)和乙烷(C2H6))采用配置有氢火焰离子检测器(FID)的Agilent 8890气相色谱仪进行检测。毛细色谱柱型号为GS-Q,长为30 m,直径为0.53 mm。具体参数如下:进样口温度为200 ℃,检测器温度为230 ℃,进样量为100 μL顶空气体,进样口分流比为5∶1,色谱柱初始温度为50 ℃,保持7 min,然后以20 ℃/min上升至230 ℃并保持4 min。
(2) NO 3-及其去除产物的测定
NO3--N采用国家标准HJ/T 346-2007中的NO3--N紫外分光光度法进行测定;NO2--N采用国家标准GB/7493-89中的N-1-萘基-乙二胺光度法进行测定;NH4+-N采用国家标准GB/11894-89中的碱性过硫酸钾消解紫外分光光度法进行测定,经过计算得到总NO3--N的含量,然后通过差减NO 3--N和NO2--N含量计算得出NH4+-N含量(由于调节配制的模拟地下水溶液pH时使用HEPES缓冲溶液会干扰NH4+-N的测试,因此未直接测定NH4+-N含量)。
(3) pH的测定
pH采用携带有pH(HQ 11d Portable pH Meter)探头的手握式便携器进行测定。
(4) 微生物群落分析
以厌氧顶空瓶中TCE和NO3-的去除完成时作为反应终止期(mZVI/AB体系以80 d作为反应终止期),采用离心法并设置转速为3 000 r·min-1分离厌氧瓶中的微生物与模拟地下水,将分离的微生物样品保存在无菌离心管内,置于-20 ℃冰箱中,委托上海美吉生物技术有限公司进行16SrDNA测序。使用高通量测序通用引物338F(5′-ACTCCTACGGGAGGCAGCAG-3′)和806R(5′-GGACTACHVGGGTWTCTAAT-3′)对细菌16S rRNA的V3-V4区进行了聚合酶链反应(PCR)扩增得到最终高通量测序结果。为保证样品结果的准确性,首先对序列质量进行抽平处理,随后对97%相似水平的OUT代表序列进行OUT聚类(Uparse 7.0.1090)和序列分类注释(RDPClassifier 2.11,贝叶斯算法),分别在门、属统计各样本的群落物种组成,并通过Mothur1.30.2计算Alpha多样性指数。
1.5 反应动力学拟合本研究的数据结果利用Excel 2019和Origin 2019软件进行分析和绘制。采用一级动力学模型(1)描述TCE在不同耦合体系中的降解动力学:
| $ \ln \left(\frac{C_{\mathrm{t}}}{C_0}\right)=-K_{\text {obs }} \cdot t。$ | (1) |
式中:C0为目标污染物初始质量浓度(mg/L);Ct为目标污染物瞬时质量浓度(mg/L);Kobs为速率常数,d-1。
1.6 电子效率计算电子效率(EE),指降解TCE所消耗的电子量占Fe0释放电子总量的比例。假设Fe0释放的所有电子都用于还原TCE、NO3-和H2O(析出H2),用Nt和Ne分别表示Fe0释放电子的总数和用于还原TCE的电子数,则电子效率为Ne与Nt的比值。
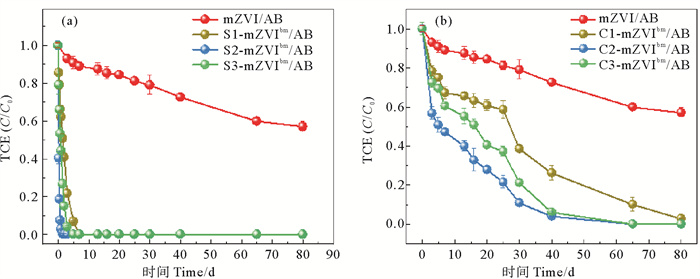
2 结果 2.1 TCE还原特征 2.1.1 TCE降解动力学特征从去除率和一级动力学速率常数(Kobs)的角度比较不同S/Fe摩尔比对TCE降解的影响(见图 1(a)、表 3),结果表明,不同S/Fe摩尔比的S-mZVIbm/AB体系TCE去除效果均显著优于对照组(mZVI/AB),且随着S/Fe摩尔比的增加,TCE去除速率呈现先上升后下降的趋势。S-mZVIbm/AB体系TCE去除率均可在6 d前达到99%,而mZVI/AB体系在反应结束时(80 d)TCE去除率仅为42.96%。本研究中S/Fe摩尔比为0.05时TCE的去除效果最佳,以反应初始阶段1 d为例,S/Fe摩尔比为0.01、0.05、0.1的耦合体系TCE去除率分别是37.86%,97.18%,55.76%;此外,S/Fe摩尔比为0.05时耦合体系中TCE的去除速率也最快,其Kobs为3.51 d-1,分别是S/Fe摩尔比为0.01、0.1的7.25、4.02倍。
|
图 1 mZVI/AB、S-mZVIbm/AB体系(a),mZVI/AB、C-mZVIbm/AB体系(b)TCE降解曲线 Fig. 1 Degradation curves of TCE in mZVI/AB and S-mZVIbm/AB systems(a), mZVI/AB and C-mZVIbm/AB systems(b) |
|
|
表 3 mZVI/AB、S-mZVIbm/AB及C-mZVIbm/AB体系TCE的一级动力学速率常数 Table 3 First order kinetic rates constant of TCE in mZVI/AB, S-mZVIbm/AB and C-mZVIbm/AB systems |
不同C/Fe质量比的耦合体系中TCE去除效果也均显著优于对照组,且与硫化组相似,随着C/Fe质量比的增大,TCE的去除速率呈现先上升后下降的趋势(见图 1(b)、表 3)。C1-mZVIbm/AB、C2-mZVIbm/AB及C3-mZVIbm/AB体系TCE去除率达到90%以上的时间分别为65、40及40 d,而mZVI/AB体系TCE最终去除率(80 d)仅为42.96%,且C1-mZVIbm/AB、C2-mZVIbm/AB及C3-mZVIbm/AB体系TCE的Kobs分别为mZVI/AB体系的3.95、10.68、6.40倍,碳改性技术对耦合体系去除TCE有显著的增强效果。C/Fe质量比为0.5%时TCE去除效果最佳,例如C2-mZVIbm/AB体系的Kobs分别是C3-mZVIbm/AB和C1-mZVIbm/AB体系的2.70、1.67倍。
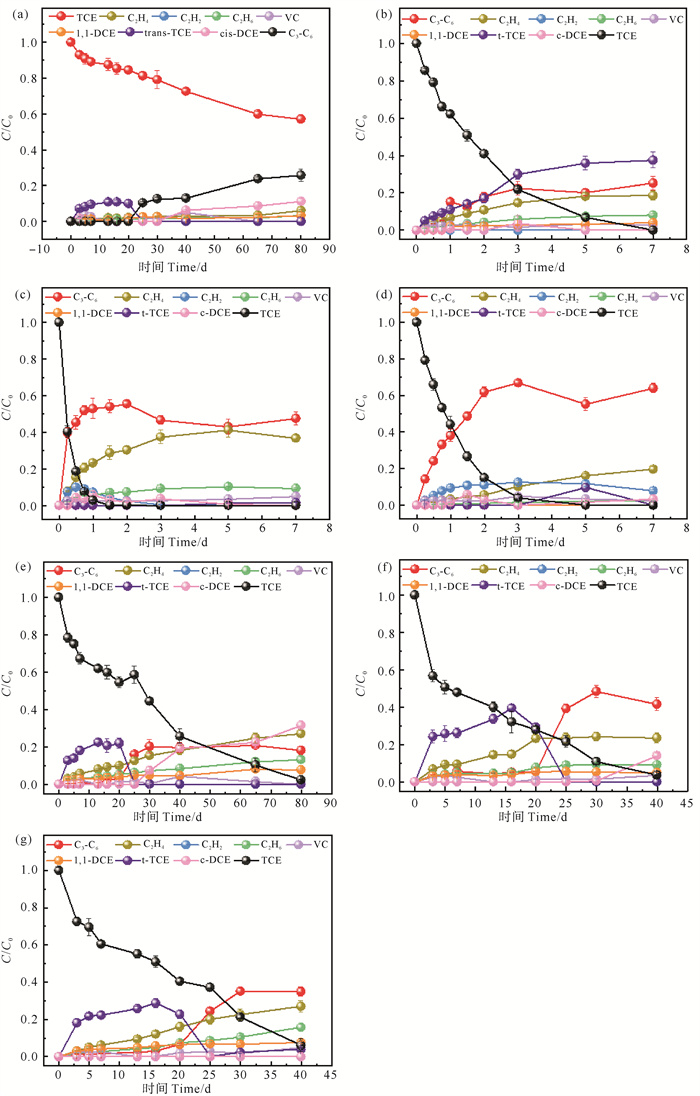
2.1.2 TCE产物构成及还原途径硫化组与对照组相比,TCE产物组成相似,但含量有所差异,主要体现在氯代产物方面:随着S的加入,氯代产物含量逐渐减少,更饱和或更长链的碳氢化合物含量增加(见图 2(a)—(d))。对照组中TCE终产物主要是C3-C6(24.1%)和cis-DCE(10.5%),且整个反应周期中均有氯代产物的积累。S1-mZVIbm/AB体系中trans-DCE、C3-C6、C2H4为主要终产物,其含量分别为:37.46%、25.23%、18.55%。S2-mZVIbm/AB和S3-mZVIbm/AB体系中主要终产物为C3-C6、C2H4,含量分别为47.52%、36.70%(S2-mZVIbm/AB)以及63.96%、19.70%(S3-mZVIbm/AB)。可见随着S/Fe摩尔比的增大,C3-C6含量持续增大,说明高的S/Fe摩尔比不仅加快了TCE的转化率,还促进了TCE转化为更饱和的产物或更长链的碳氢化合物。
|
图 2 mZVI/AB(a),S1-mZVIbm/AB(b),S2-mZVIbm/AB(c),S3-mZVIbm/AB(d),C1-mZVIbm/AB(e),C2-mZVIbm/AB(f),C3-mZVIbm/AB(g)体系TCE产物生成图 Fig. 2 Produces formation diagram of TCE in mZVI/AB(a), S1-mZVIbm/AB(b), S2-mZVIbm/AB(c), S3-mZVIbm/AB(d), C1-mZVIbm/AB(e), C2-mZVIbm/AB(f), C3-mZVIbm/AB(g) systems |
不同改性剂添加量的C-mZVIbm/AB体系将TCE降解还原为C3-C6、C2H4、C2H6、VC、DCEs等(见图 2(e)—(g))。C1-mZVIbm/AB体系主要终产物为cis-DCE和C2H4,含量分别为31.53%、27.10%,C2-mZVIbm/AB体系主要终产物为C3-C6、C2H4,其含量分别为41.49%、23.47%,与C1-mZVIbm/AB体系相比,氯代产物含量显著降低;在C3-mZVIbm/AB体系中,主要终产物与C2-mZVIbm/AB体系相同,为C3-C6(34.90%)和C2H4(27.00%),且次要终产物与C2-mZVIbm/AB体系也类似,说明随着C/Fe质量比的增大,碳改性体系产物组成将不再显著变化,但在一定程度上可促进饱和烃类的生成。
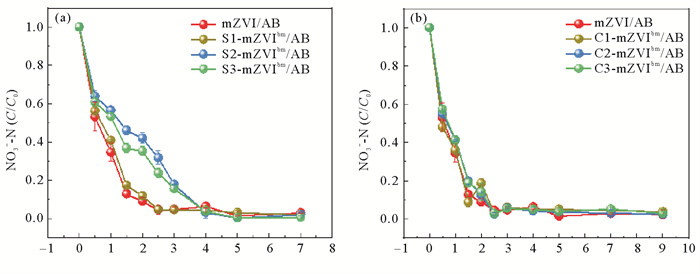
2.2 NO3-还原特征 2.2.1 NO3-去除动力学特征与对照组相比,不同S/Fe摩尔比的耦合体系均对NO3-的去除表现出较显著抑制作用,且当S/Fe摩尔比≥0.05时,NO3-的去除速率显著下降(见表 4);碳改性体系对NO3-去除效果的影响不会随着C/Fe质量比的改变发生明显变化。在mZVI/AB、S1-mZVIbm/AB、S2-mZVIbm/AB、S3-mZVIbm/AB体系中,NO3-去除率达到95%的时间分别为2.5、2.5、4、4 d,Kobs分别为1.18、1.04、0.54、0.63 d-1,S/Fe摩尔比增大显著降低了NO3-的去除效果。mZVI/AB、C1-mZVIbm/AB、C2-mZVIbm/AB、C3-mZVIbm/AB体系NO3-去除率均在2.5 d达到95%,Kobs分别为1.18、1.18、1.02、1.00 d-1,NO3-的去除效果相差不大。
|
图 3 mZVI/AB、S-mZVIbm/AB(a),mZVI/AB、C-mZVIbm/AB(b)体系NO3-去除曲线 Fig. 3 Removal curves of NO3- in mZVI/AB, S-mZVIbm/AB(a), mZVI/AB, C-mZVIbm/AB(b) systems |
|
|
表 4 mZVI/AB、S-mZVIbm/AB、C-mZVIbm/AB耦合体系NO3-的一级动力学速率常数 Table 4 First order kinetic rates constant of NO3- in mZVI/AB, S-mZVIbm/AB, and C-mZVIbm/AB systems |
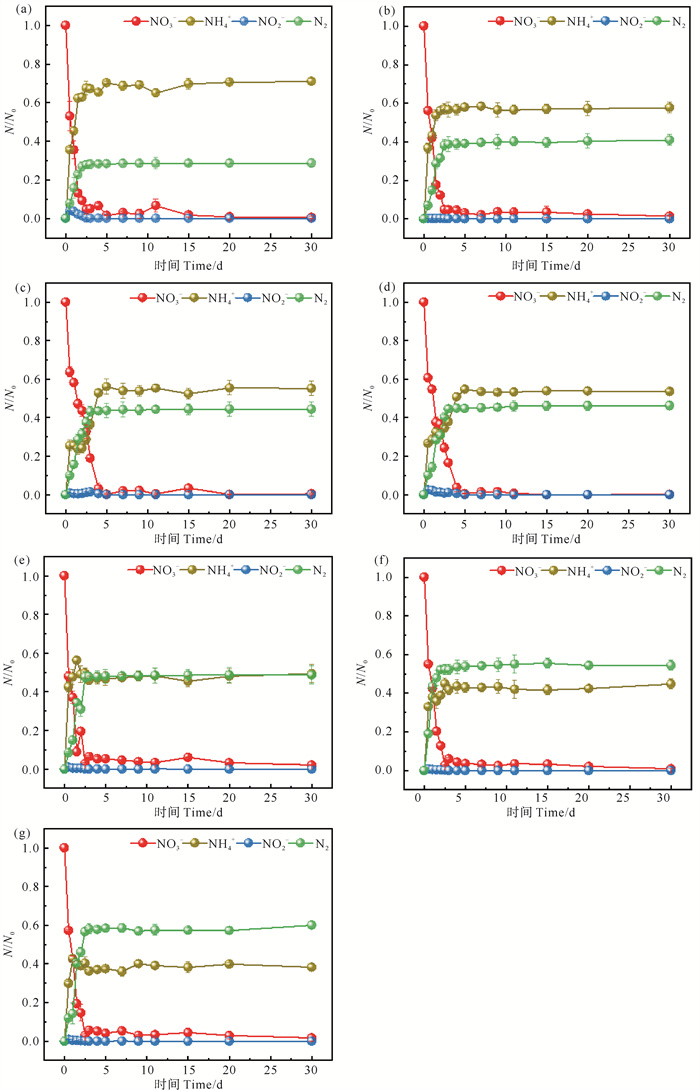
不同S/Fe摩尔比的S-mZVIbm/AB体系NO3-主要还原产物为NH4+和N2,少量NO2-作为中间产物产生(见图 4)。在mZVI/AB、S1-mZVIbm/AB、S2-mZVIbm/AB、S3-mZVIbm/AB体系中,终产物中NH4+-N占总氮含量的百分率分别为70.96%、57.68%、55.19%、53.59%,N2-N占总氮含量的百分率分别为28.59%、40.87%、44.39%、46.25%,与对照组相比,硫化作用会影响耦合体系NO3-的产物分布,尤其是促进了N2的生成,且该促进作用与S/Fe摩尔比的提高程度成正比。C1-mZVIbm/AB、C2-mZVIbm/AB、C3-mZVIbm/AB体系中NO3-终产物中N2-N占总氮含量的百分率分别为:48.59%、54.34%、60.00%,分别是对照组N2-N百分率的1.70、1.90、2.10倍,而NH4+-N占总氮含量的百分率分别为:49.28%、44.72%、38.30%,可见随着C/Fe质量比的增大,N2百分率不断上升,NH4+百分率不断下降。
|
图 4 mZVI/AB(a),S1-mZVIbm/AB(b),S2- mZVIbm/AB(c),S3-mZVIbm/AB(d),C1-mZVIbm/AB(e),C2-mZVIbm/AB(f),C3-mZVIbm/AB(g)体系NO3-产物生成图 Fig. 4 Products formation diagram of NO3- in mZVI/AB(a), S1-mZVIbm/AB(b), S2-mZVIbm/AB(c), S3-mZVIbm/AB(d), C1-mZVIbm/AB(e), C2-mZVIbm/AB(f), C3-mZVIbm/AB(g) systems |
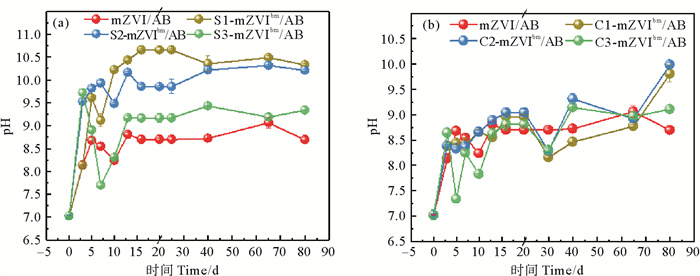
对照组与不同S/Fe摩尔比的S-mZVIbm/AB体系中pH的整体变化均呈现“急剧上升-上下波动-趋于稳定”的趋势(见图 5(a))。与对照组相比,反应初始阶段S-mZVIbm/AB体系pH值一直处于高水平,随着S/Fe摩尔比的增大,S-mZVIbm/AB体系pH在中后期的增长幅度变小,说明S添加量的增多可以减缓pH上升,从而减缓mZVI的钝化程度,这与目前的研究结论一致[2]。不同C/Fe质量比的C-mZVIbm/AB体系中pH的整体变化趋势也均呈现“急剧上升-上下波动-趋于稳定”的趋势(见图 5(b)),且碳改性组对pH的影响程度同C/Fe质量比有关。在反应开始阶段(0~5 d),随着C/Fe质量比的增加,pH逐渐降低,以5 d为例,mZVI/AB、C1-mZVIbm/AB、C2-mZVIbm/AB、C3-mZVIbm/AB体系pH分别为8.68、8.44、8.33、7.34,说明活性炭的加入可以在前期减缓耦合体系钝化。而在反应结束时,mZVI/AB、C1-mZVIbm/AB、C2-mZVIbm/AB、C3-mZVIbm/AB体系pH分别为8.69、9.80、9.98、9.10,可见碳改性措施在反应后期提高了耦合体系的pH,且当C/Fe质量比增大到一定程度时,pH显著降低,在一定程度减缓耦合体系的钝化。
|
图 5 mZVI/AB、S-mZVIbm/AB(a),mZVI/AB、C-mZVIbm/AB(b)体系pH变化趋势图 Fig. 5 pH trend in mZVI/AB, S-mZVIbm/AB(a), mZVI/AB, C-mZVIbm/AB(b) systems |
表 5总结了mZVI/AB、S-mZVIbm/AB和C-mZVIbm/AB体系中微生物群落的丰度和多样性。ACE和Chao指数表征群落的丰度,且值越高表示群落丰度越高[6]。与对照组相比,硫化组群落丰度较高,且随着S/Fe摩尔比的增加,S-mZVIbm/AB体系中微生物群落丰度不断增高。C-mZVIbm/AB体系仅当C/Fe质量比≥0.5%时,群落丰度才会随C/Fe的增大而增大。Shannon和Simpson指数反映了群落的多样性,且Shannon指数越大、Simpson指数越小,群落多样性越高[6]。S-mZVIbm/AB体系的Shannon指数均高于对照组,Simpson指数均小于对照组,说明S的加入会提高体系群落的多样性,且随着S/Fe摩尔比的增大,群落多样性呈现先升高后下降的趋势。C-mZVIbm/AB体系当C/Fe≥0.5%时,群落多样性才会显著升高,C1-mZVIbm/AB的群落多样性与对照组相差不大。
|
|
表 5 耦合体系的群落丰度和多样性指数表 Table 5 Community richness and diversity indices of coupled systems |
各耦合体系中群落相对丰度较高的细菌门类为Proteobacteria、Firmicutes、Actinobacteriota和Chloroflexi(见图 6(a)),其中Firmicutes和Proteobacteria为优势细菌门类。Firmicutes和Proteobacteria为严格厌氧菌,可降解包括CAHs在内的有机物,且Firmicutes也被证明具有反硝化潜力[6, 18-19],在mZVI/AB、S1-mZVIbm/AB、S2-mZVIbm/AB、S3-mZVIbm/AB体系中,Firmicutes和Proteobacteria的总相对丰度分别为80.15%、83.32%、69.63%、74.51%,在C1-mZVIbm/AB,C2-mZVIbm/AB,C3-mZVIbm/AB体系中,其总相对丰度为83.89%、70.61%、72.99%,可见当S/Fe摩尔比、C/Fe质量比增大到一定程度时,Firmicutes和Proteobacteria的总相对丰度有所降低。
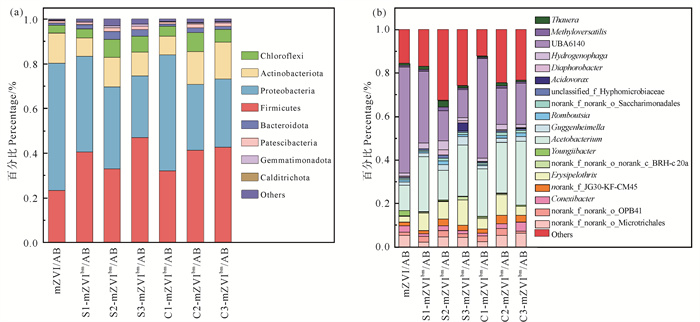
|
图 6 门水平(a),属水平(b)上群落的相对丰度 Fig. 6 The relative abundance of community at the phylum level(a), genus level(b) |
各耦合体系中均发现了具有脱氯功能的菌属(见图 6(b)),如Acetobacterium和norank_f_JG30-KF-CM45。Acetobacterium可参与脱卤呼吸代谢过程,能将四氯甲烷还原为二氯甲烷和二氧化碳[6],norank_f_JG30-KF-CM45的目标污染物多为难降解有机物[6]。与对照组相比,Acetobacterium在不同S/Fe摩尔比的S-mZVIbm/AB体系与不同C/Fe质量比的C-mZVIbm/AB体系中相对丰度较高,表明S与C的添加也可促进脱氯细菌Acetobacterium的富集。此外,C的添加还可促进norank_f_JG30-KF-CM45的富集,但促进作用微弱。在属水平上各耦合体系中也均发现具有反硝化功能的菌属(见图 6(b)),且为优势菌属,如UBA6140、Erysipelothrix、Conexibacter和Hydrogenophaga,为耦合体系中NO3-的去除做出了巨大的贡献[20]。反硝化菌属中UBA6140的相对丰度最高,在mZVI/AB、S1-mZVIbm/AB、S2-mZVIbm/AB、S3-mZVIbm/AB体系中相对丰度分别为48.66%、32.91%、13.81%、12.84%,随着S/Fe摩尔比的增加,其相对丰度逐渐下降。Erysipelothrix、Conexibacter和Hydrogenophaga在上述四个耦合体系中总相对丰度为7.04%、11.85%、13.99%、14.37%,可见不同S/Fe摩尔比的S-mZVIbm/AB体系中参与反硝化的上述三种细菌含量均高于mZVI/AB体系。在C1-mZVIbm/AB、C2-mZVIbm/AB、C3-mZVIbm/AB体系中,UBA6140的相对含量为46.01%、16.87%、18.91%,与S-mZVIbm/AB体系类似,C/Fe质量比的增加不利于UBA6140菌的富集。此外,参与反硝化的菌属Erysipelothrix、Conexibacter和Hydrogenophaga在上述三个耦合体系中总相对丰度分别为7.49%、14.32%、9.87%,均比mZVI/AB体系高。
3 讨论 3.1 改性剂添加量对TCE去除的影响机制 3.1.1 改性剂添加量对TCE降解动力学影响机制分析分析TCE的去除率和Kobs可知,不同S/Fe摩尔比的S-mZVIbm/AB体系TCE去除效果均显著优于对照组,这是由于ZVI硫化过程中表面形成的FeSx会增加表面粗糙度,提供更多反应位点,Gu[16]的研究已证明这一结论,且S-ZVI的电极电势(5.02 eV)高于ZVI的电极电势(4.02 eV),可促进电子从颗粒内部转移到污染物[21]。S-mZVIbm/AB体系的pH在整个反应阶段均高于对照组,这是由于S-mZVIbm与NO3-、TCE的反应均处于活跃的状态,S-mZVIbm被腐蚀的程度高于其他体系,S-mZVIbm与H2O的反应位点增多,OH-不断产生,同时验证了S-mZVIbm/AB体系中电子快速传递的现象。此外,过度硫化将会导致ZVI(主要电子供体)含量降低[2],因此随着S/Fe摩尔比的继续增加,TCE的去除速率反而下降。值得注意的是,随着S/Fe摩尔比的增大,S-mZVIbm/AB体系pH在中后期的增长幅度变小,减缓了mZVI的钝化程度,这是由于Fe表面上覆盖的S原子削弱了H2O分子与Fe表面的相互作用,使得经硫化后的Fe表面对H2O的解离效率变低,因此ZVI材料耐表面钝化[22]。与对照组相比,S-mZVIbm材料不易失活,在实际工程应用中将具有更好长期修复TCE污染地下水的效果。
不同C/Fe质量比的耦合体系中TCE的去除效果也均显著优于对照组,其TCE去除效果改善的原因推测是随着C含量的增加,C-mZVIbm对TCE的吸附能力增加,提高了TCE在ZVI颗粒表面的浓度[17],促进了TCE降解。反应开始阶段随着C/Fe质量比的增加,pH逐渐降低,说明活性炭的加入可以在前期减缓耦合体系钝化,这也是C-mZVIbm/AB体系中TCE去除效果显著优于对照组的原因之一。但是随着C/Fe质量比的增大,TCE去除速率呈现先上升后下降的趋势,这是由于高C/Fe将会导致过量活性炭片覆盖在ZVI反应位点上,阻碍传质过程[23],从而降低了ZVI的反应性。值得注意的是,碳改性措施在反应后期可提高耦合体系的pH,但是随着C/Fe质量比的增大,pH呈现先略微上升后显著下降的趋势,说明当C/Fe质量比增大到一定程度时,可在一定程度减缓耦合体系的钝化程度,有利于减缓C-mZVIbm材料的失活。
3.1.2 改性剂添加量对TCE产物构成及还原途径影响机制分析在ZVI-微生物耦合体系中,TCE主要通过以下途径还原:(1)ZVI通过氢解、α消除、β消除途径主要将TCE还原为不含氯的烯烃、烷烃、炔烃[24-26];(2)微生物主要将TCE还原为cis-DCE和VC[27];(3)ZVI发生析氢腐蚀时产生的H2作为连接ZVI化学和微生物系统的纽带,可作为微生物的电子供体,催化还原TCE[28],并对微生物还原过程产生的主要中间产物cis-DCE具有高反应活性使其快速降解,最终将TCE全部还原为C2H6和C2H4。
S-mZVIbm/AB体系随着S的加入,氯代产物含量减少,饱和或长链的碳氢化合物含量增多,根据产物分布推测随着S/Fe增加,反应不完全易产生氯代产物的生物还原过程[5]逐渐变得微弱,TCE主要通过氢解和β消除产生碳烃化合物。在S1-mZVIbm/AB体系中不完全脱氯产物DCE含量较多,与对照组相比,Firmicutes和Proteobacteria总相对丰度较高,这两种菌已被证明可降解包括CAHs在内的有机物[6, 18],说明适当加入少剂量的S可以促进体系厌氧菌的富集,并推测TCE通过以氢解为主的化学途径以及生物途径被还原降解。S2-mZVIbm/AB和S3-mZVIbm/AB体系TCE产物主要为C3-C6和C2H4,较高的S/Fe摩尔比不仅提高了TCE的去除率,还促进其转化为更饱和或更长链的碳氢化合物。此外,随着S/Fe摩尔比的增大,Firmicutes和Proteobacteria的含量呈现先降低后上升的趋势,与S2-mZVIbm/AB体系TCE降解最快、化学还原最为显著、微生物脱氯作用微乎其微的现象一致。与对照组相比,Acetobacterium作为脱氯菌[18]中的优势菌在不同S/Fe摩尔比的S-mZVIbm/AB体系中相对丰度较高,推测S-mZVIbm/AB体系TCE还原虽以化学途径为主,但硫化作用仍能促进脱氯细菌的富集。此外,与其余体系未监测到C2H2相比,S3-mZVIbm/AB体系有少量C2H2的积累,其原因是C2H2主要是通过β-消除途径产生,且ZVI对C2H2具有较高的降解活性,但是随着S/Fe摩尔比的增加,ZVI减少而FeS增加,C2H2反应位点减少[16],因此S3-mZVIbm/AB体系积累了少量C2H2。
不同改性剂添加量的C-mZVIbm/AB体系TCE主要产物为C3-C6、C2H4、C2H6、VC、DCEs,氯代产物的出现表明部分TCE通过生物脱氯途径被还原,由于产物中未出现C2H2,故推测上述碳烃化合物主要通过氢解途径产生,且在不同C/Fe质量比的C-mZVIbm/AB体系中生物脱氯还原和氢解途径的贡献度不同。在C1-mZVIbm/AB体系中,主要终产物为cis-DCE和C2H4,推测C1-mZVIbm/AB体系TCE还原途径可能为氢解、微生物脱氯还原;在C2-mZVIbm/AB和C3-mZVIbm/AB体系中,主要终产物为C3-C6、C2H4,与C1-mZVIbm/AB体系相比,氯代产物含量显著降低,饱和碳烃化合物含量逐渐上升,化学还原作用显著。Firmicutes和Proteobacteria的总相对丰度随着C/Fe质量比的增加先下降后略微升高,验证了随着C的不断加入,C-mZVIbm/AB体系微生物还原TCE作用逐渐减弱的现象。
3.2 改性剂添加量对NO3-去除的影响机制 3.2.1 改性剂添加量对NO3-去除动力学影响机制分析与对照组相比,不同S/Fe摩尔比的耦合体系均对NO3-去除表现出较显著的抑制作用,这是由于S-mZVIbm材料的高疏水性导致,其更倾向于富集疏水有机污染物[29],故与mZVI相比对NO3-的去除效果不佳。此外,在S-mZVIbm/AB体系中参与反硝化的微生物UBA6140[20]作为优势菌对NO3-的去除做出了巨大贡献,且在S1-mZVIbm/AB体系中UBA6140的相对丰度显著较高,与NO3-去除效果最佳的结论相一致。而不同C/Fe质量比的C-mZVIbm/AB体系中NO3-的去除效果相差不大,说明C的添加不会影响mZVI对NO3-的去除效果。值得注意的是,S-mZVIbm/AB与C-mZVIbm/AB体系中pH前期呈现急剧上升的趋势,其原因是在耦合体系中铁化学还原和微生物反硝化还原NO3-都会消耗质子[30],根据NO3-去除情况可知耦合体系均可在5 d内近似完全去除NO3-,从而增加了体系的pH;而pH呈上下波动趋势是由于微生物进行代谢活动释放的酸性物质中和了ZVI腐蚀过程产生的OH-[30],故而在一定程度减缓了pH的继续上升。
3.2.2 改性剂添加量对NO3-产物构成及还原途径影响机制分析目前,mZVI还原NO3-最广泛接受的机制是mZVI向NO3-的直接电子转移,NO2-在反应初始阶段作为反应中间体形成,后被mZVI还原为NH4+和N2,其中NH4+为主要最终还原产物[23]。对于mZVI支持的自养反硝化系统,mZVI既可以作为还原剂还原NO3-,也可以通过腐蚀产生H2作为微生物代谢的电子供体,利用微生物的生物反硝化过程还原NO3-[5]。在反应的早期阶段,化学还原是主导机制,最终产物几乎全是NH4+,而在反应后期阶段,NO3-逐渐从化学还原演变为生物还原生成干净产物N2[5]。
与对照组相比,S-mZVIbm/AB体系终产物中NH4+-N占总氮含量的百分率下降,N2-N占总氮含量的百分率上升,硫化作用会影响耦合体系NO3-的产物分布,尤其是促进N2的生成,且该促进作用与S/Fe摩尔比的提高程度成正比,推测是由于硫化作用增加了mZVI材料的疏水性,导致mZVI与NO3-的反应位点减少[29],化学还原作用不显著。在S-mZVIbm/AB体系中Chloroflexi门类微生物以及优势菌属UBA6140在反硝化过程中发挥了重要作用[20],推测这是S-mZVIbm/AB体系生物反硝化作用显著的原因之一。此外,参与反硝化的微生物Erysipelothrix、Conexibacter和Hydrogenophaga在不同S/Fe摩尔比的S-mZVIbm/AB体系中含量均高于mZVI/AB体系,且与生成较高百分率N2的规律相一致,进一步验证S-mZVIbm/AB体系中NO3-的微生物还原作用较为显著。
C-mZVIbm/AB体系随着C/Fe质量比的不断增大,N2-N百分率不断上升,NH4+-N百分率不断下降,这是由于随着C/Fe质量比的增加,C-mZVIbm的孔隙结构显著增加,提高了厌氧环境的稳定性,有利于微生物的生存和反硝化作用,促进N2生成[23, 31]。与S-mZVIbm/AB体系类似,UBA6140作为优势反硝化菌为C-mZVIbm/AB体系NO3-的去除做出了巨大贡献。此外,参与反硝化的菌属Erysipelothrix、Conexibacter和Hydrogenophaga[20]的含量均比mZVI/AB体系高,也是C-mZVIbm/AB体系中NO3-的微生物还原作用较为显著的原因之一。值得注意的是,活性炭强大的孔隙结构提高了材料的吸附能力,有害副产物NH4+将被吸附在活性炭上,在计算结果上也将表现出N2含量增加[23]。
3.3 电子效率分析为探究S-mZVIbm/AB、C-mZVIbm/AB体系与对照组在去除TCE和NO3-过程中的电子流向和电子效率(Electronic efficiency, EE),本研究选择反应结束期的样品数据,计算各耦合体系中电子受体所消耗的电子量。
如表 6所示,与对照组相比,S1-mZVIbm/AB与S2-mZVIbm/AB体系中EETCE与EENO3-降低,而EEH2O提高,是由于S-mZVIbm在反应前期快速去除TCE与NO3-,当其反应完毕后,仍具有较高活性的S-mZVIbm与H2O大量反应,导致H2O的电子效率较高。与对照组相比,S3-mZVIbm/AB体系EETCE升高,EEH2O下降,其原因是在S3-mZVIbm/AB体系中,mZVI材料表面存在大量高疏水性的FeS,从而使得mZVI材料疏水性增强并减弱了与H2O的反应[16]。因此,在S-mZVIbm/AB体系中,增大S/Fe摩尔比可显著提高TCE的电子效率,避免材料的浪费,这一结论与目前文献报告的一致[16]。与对照组相比,随着C/Fe质量比的增加,EETCE不断提高,说明增加C含量可提高C-mZVIbm/AB体系对TCE的选择性;与S1-mZVIbm/AB和S2-mZVIbm/AB体系类似,C-mZVIbm/AB体系EEH2O高于对照组,其原因是C-mZVIbm去除完TCE与NO3-后仍具有较高活性继续与H2O反应。总的来说,硫化、碳改性的球磨微米铁不仅可以显著提高TCE去除率及去除速率,且在提高电子效率方面也有明显改善,且改善效果与改性剂添加量成正比。
|
|
表 6 耦合体系电子效率分布表 Table 6 Distribution of electronic efficiency of the coupled system |
本研究以S/Fe摩尔比、C/Fe质量比为关键改性参数,制备了不同性质特征的S-mZVIbm和C-mZVIbm材料,构建了改性mZVI-微生物耦合修复体系,考查关键改性参数对耦合体系去除TCE和NO3-动力学特征、产物构成、微生物群落结构等的影响。结果表明:
(1) 随着S/Fe摩尔比和C/Fe质量比的增加,TCE的去除效果呈现先上升后降低的趋势;随着S的不断加入,氯代产物含量逐渐减少,饱和碳烃化合物含量上升,TCE的还原途径逐渐从氢解转化为β消除,微生物还原脱氯作用不显著;随着C/Fe质量比的增加,C-mZVIbm/AB体系还原途径逐渐由氢解和微生物还原脱氯变为以氢解反应为主导的还原脱氯,C3-C6的含量逐渐上升。
(2) 随着S/Fe摩尔比的增大,NO3-的去除效果呈下降趋势,而C/Fe质量比的变化不会影响耦合体系NO3-的去除效果;S-mZVIbm/AB和C-mZVIbm/AB体系均可显著提高N2选择性,且该促进作用与S/Fe摩尔比、C/Fe质量比成正比。
(3) 在不同改性剂添加量的S-mZVIbm/AB和C-mZVIbm/AB体系中存在大量参与脱氯和反硝化的细菌,反硝化菌的相对丰度高于脱氯菌,是NO3-快速去除和较高浓度N2产生的原因;在S2-mZVIbm/AB和C1-mZVIbm/AB体系中参与反硝化的菌属富集较多,与NO3-还原效果最佳的结论相一致。
(4) S-mZVIbm/AB和C-mZVIbm/AB体系可显著提高TCE的电子效率,且提高效果与改性剂添加量成正比。
本研究结果可为真实场地条件下地下水氯代烃污染的绿色可持续修复提供强有力的理论支持和技术指导。
| [1] |
韩君. 改性微米铁对三氯乙烯的去除效能研究[D]. 青岛: 中国海洋大学, 2015. Han J. Study on the Removal Efficiency of Modified Micron Iron on Trichloroethylene[D]. Qingdao: Ocean University of China, 2015. (  0) 0) |
| [2] |
谷亚威. 球磨法制备硫化微米零价铁及其降解地下水中三氯乙烯的研究[D]. 杭州: 浙江工业大学, 2019. Gu Y W. Preparation of Micron Zero-Valent Iron Sulfide by Ball Milling and Its Degradation of Trichloroethylene in Groundwater[D]. Hangzhou: Zhejiang University of Technology, 2019. (  0) 0) |
| [3] |
陆强, 李辉, 林匡飞, 等. 上海浦东某氯代烃场地地下水污染现状调查[J]. 环境科学学报, 2016, 36(5): 1730-1737. Lu Q, Li F, Lin K F, et al. Investigation of groundwater contamination at a chlorinated hydrocarbon site in Pudong, Shanghai[J]. Journal of Environmental Science, 2016, 36(5): 1730-1737. (  0) 0) |
| [4] |
李岩. 好氧共代谢降解地下水和土壤中三氯乙烯的研究[D]. 天津: 南开大学, 2014. Li Y. Study on Aerobic Co-Metabolic Degradation of Trichloroethylene in Groundwater and Soil[D]. Tianjin: Nankai University, 2014. (  0) 0) |
| [5] |
Wang X H, Xin J, Yuan M J, et al. Coupled microscale zero valent iron-autotrophic hydrogen bacteriadechlorination system is not always superior to its standalone counterparts: A sustainable remediation perspective[J]. Science of the Total Environment, 2023, 857: 159364. DOI:10.1016/j.scitotenv.2022.159364 (  0) 0) |
| [6] |
Yuan M J, Xin J, Wang X H, et al. Coupling microscale zero-valent iron and autotrophic hydrogen-bacteria provides a sustainable remediation solution for trichloroethylene-contaminated groundwater: Mechanisms, regulation, and engineering implications[J]. Water Research, 2022, 216: 118286. DOI:10.1016/j.watres.2022.118286 (  0) 0) |
| [7] |
Wang S Q, Chen S Y, Wang Y, et al. Integration of organohalide-respiring bacteria and nanoscale zero-valent iron(Bio-nZVI-RD): A perfect marriage for the remediation of organohalide pollutants?[J]. Biotechnology Advances, 2016, 34(8): 1384-1395. DOI:10.1016/j.biotechadv.2016.10.004 (  0) 0) |
| [8] |
Xin J, Fan S F, Yuan M J, et al. Effects of co-existing nitrate on TCE removal by mZVI under different pollution load scenarios: Kinetics, electron efficiency and mechanisms[J]. Science of the Total Environment, 2020, 716(C): 137111. (  0) 0) |
| [9] |
Li J X, Zhang X Y, Sun Y K, et al. Advances in sulfidation of zerovalent iron for water decontamination[J]. Environmental Science & Technology, 2017, 51(23): 13533-13544. (  0) 0) |
| [10] |
Xu C H, Zhang B L, Wang Y H, et al. Effects of sulfidation, magnetization, and oxygenation on azo dye reduction by zerovalent iron[J]. Environmental Science & Technology, 2016, 50(21): 11879-11887. (  0) 0) |
| [11] |
Qin H J, Guan X H, Bandstra J Z, et al. Modeling the kinetics of hydrogen formation by zerovalent iron: Effects of sulfidation on micro- and nano-scale particles[J]. Environmental Science & Technology, 2018, 52(23): 13887-13896. (  0) 0) |
| [12] |
Gao J, Wang W, Rondinone A J, et al. Degradation of trichloroethene with a novel ball milled Fe-C nanocomposite[J]. Journal of Hazardous Materials, 2015, 300: 443-450. DOI:10.1016/j.jhazmat.2015.07.038 (  0) 0) |
| [13] |
Ren Y M, Ma J J, Lee Y Y, et al. Reaction of activated carbon zerovalent iron with pentachlorophenol under anaerobic conditions[J]. Journal of Cleaner Production, 2021, 297: 126748. DOI:10.1016/j.jclepro.2021.126748 (  0) 0) |
| [14] |
Vogel M, Kopinke F, Mackenzie K. Acceleration of microiron-based dechlorination in water by contact with fibrous activated carbon[J]. Science of the Total Environment, 2019, 660: 1274-1282. DOI:10.1016/j.scitotenv.2019.01.070 (  0) 0) |
| [15] |
Meng F X, Li Z J, Lei C, et al. Removal of trichloroethene by iron-based biochar from anaerobic water: Key roles of Fe/C ratio and iron carbides[J]. Chemical Engineering Journal, 2021, 413: 127391. DOI:10.1016/j.cej.2020.127391 (  0) 0) |
| [16] |
Gu Y W, Wang B B, He F, et al. Mechanochemically sulfidated microscale zero valent iron: Pathways, kinetics, mechanism, and efficiency of trichloroethylene dechlorination[J]. Environmental Science & Technology, 2017, 51(21): 12653-12662. (  0) 0) |
| [17] |
Guan X H, Du X Y, Liu M C, et al. Enhanced trichloroethylene dechlorination by carbon-modified zero-valent iron: Revisiting the role of carbon additives[J]. Journal of Hazardous Materials, 2020, 394: 122564. DOI:10.1016/j.jhazmat.2020.122564 (  0) 0) |
| [18] |
孙仲平, 吴乃瑾, 杨苏才, 等. 微生物降解污染地下水中三氯乙烯的微宇宙试验研究[J]. 环境工程技术学报, 2021, 11(2): 298-306. Sun Z P, Wu N J, Yang S C, et al. Microcosmic experimental study of microbial degradation of trichloroethylene in contaminated groundwater[J]. Journal of Environmental Engineering Technology, 2021, 11(2): 298-306. (  0) 0) |
| [19] |
高书伟. 不同固相碳源在养殖尾水反硝化过程中的基本特征研究[D]. 上海: 上海海洋大学, 2022. Gao S W. Basic Characteristics of Different Solid-phase Carbon Sources in Denitrification of Cultured Tailwater[D]. Shanghai: Shanghai Ocean University, 2022. (  0) 0) |
| [20] |
陈瑞. 厌氧氨氧化反应器脱氮微生物群落结构研究[D]. 乌鲁木齐: 新疆大学, 2019. Chen R. Study on the Structure of Nitrogen Removal Microbial Community in Anaerobic Ammonia Oxidation Reactor[D]. Wulumuqi: Xinjiang University, 2019. (  0) 0) |
| [21] |
廖兵, 叶秋月, 胥雯. 硫化零价铁及其耦合高级氧化技术在水处理中的研究进展[J]. 环境科学研究, 2022, 35(7): 1636-1646. Liao B, Ye Q Y, Xu W. Research progress of zero-valent iron sulfide and its coupled advanced oxidation technology in water treatment[J]. Environmental Science Research, 2022, 35(7): 1636-1646. (  0) 0) |
| [22] |
Gu Y W, Gong L, Qi J L, et al. Sulfidation mitigates the passivation of zero valent iron at alkaline pHs: Experimental evidences and mechanism[J]. Water Research, 2019, 159: 223-241. DOI:10.1016/j.watres.2019.05.006 (  0) 0) |
| [23] |
Zhao F, Xin J, Yuan M J, et al. A critical review of existing mechanisms and strategies to enhance N2 selectivity in groundwater nitrate reduction[J]. Water Research, 2022, 209: 117889. DOI:10.1016/j.watres.2021.117889 (  0) 0) |
| [24] |
Arnold W, Roberts A. Inter-and intraspecies competitive effects in reactions of chlorinated ethylenes with zero-valent iron in column reactors[J]. Environmental Engineering Science, 2000, 17(5): 291-302. DOI:10.1089/ees.2000.17.291 (  0) 0) |
| [25] |
Roberts A, Totten L, Amold W, et al. Reductive elimination of chlorinated ethylenes by zero-valent metals[J]. Environmental Science & Technology, 1996, 30(8): 2654-2659. (  0) 0) |
| [26] |
Denis O C, Brent S, Magdalena K, et al. Nanoscale zero valent iron and bimetallic particles for contaminated site remediation[J]. Advances in Water Resources, 2013, 51(1): 104-122. (  0) 0) |
| [27] |
Field J, Sierra-Alvarez R. Biodegradability of chlorinated solvents and related chlorinated aliphatic compounds[J]. Reviews in Environmntal Science and Biotechnology, 2004, 3(3): 185-254. DOI:10.1007/s11157-004-4733-8 (  0) 0) |
| [28] |
Yanru Y, Perry L M. Competition for hydrogen within a chlorinated solvent dehalogenating anaerobic mixed culture[J]. Environmental Science & Technology, 1998, 32(22): 3591-3597. (  0) 0) |
| [29] |
齐建龙. 硝酸根对球磨零价铁材料降解三氯乙烯的影响及机理研究[D]. 杭州: 浙江工业大学, 2019. Qi J L. Study on the Effect of Nitrate on the Degradation of Trichloroethylene by Ball-Milled Zero-valent Iron Materials and the Mechanism[D]. Hangzhou: Zhejiang University of Technology, 2019. (  0) 0) |
| [30] |
Karanasios A, Vasiliadou A, Pavlou S, et al. Hydrogenotrophic denitrification of potable water: A review[J]. Journal of Hazardous Materials, 2010, 180(1): 20-37. (  0) 0) |
| [31] |
Wei A L, Ma J, Chen J J, et al. Enhanced nitrate removal and high selectivity towards dinitrogen for groundwater remediation using biochar-supported nano zero-valent iron[J]. Chemical Engineering Journal, 2018, 353: 595-605. (  0) 0) |
2. Qingdao Zhangcun River Water Corporation, Qingdao 266100, China;
3. The Key Laboratory of Marine Environmental Science and Ecology, Ministry of Education, Ocean University of China, Qingdao 266100, China
 2024, Vol. 54
2024, Vol. 54


