随着国家海洋战略的实施,海洋油气开发、海滨电厂及网箱养殖等海洋工程的蓬勃发展,海洋生物污损问题日益受到重视。所谓的海洋生物污损是指海洋中的微生物、藻类、植物和动物在涉海设施(如:海洋油气平台,船舶、浮标等)表面的临时性或永久性的不良沉积[1],这些沉积严重影响水下设施的性能与寿命,不仅会给人类的经济带来损失,甚至会给人类的生产带来安全隐患[2-4]。目前最经济有效和普遍采用的防治海洋生物污损的方法就是涂刷含有毒防污剂的防污涂料[5-7]。然而,有毒防污剂在防污的同时还会造成海洋环境的污染进而危害海洋渔业和养殖业甚至是人类健康[8]。因此,开发环境友好的绿色防污剂就具有重要的经济和社会意义。
目前,国内外学者对绿色防污剂的研究聚焦在具有防污活性的天然产物上,这类物质源于自然界,在有效防污的同时还能在环境中快速降解,绿色环保。然而将天然产物用于防污涂料无论从规模上、技术上还是价格上都具有很大的局限性,而人工合成天然产物则多过程繁琐,成本高[9]。因此,通过化学方法合成性能与环境特性均与天然产物相似的类天然产物成为目前绿色防污剂研究的重要方向之一,而其中,辣椒提取物辣素及其衍生物则因药效高、易降解成为新一代环保防污剂的首选。
辣素(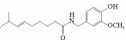
|
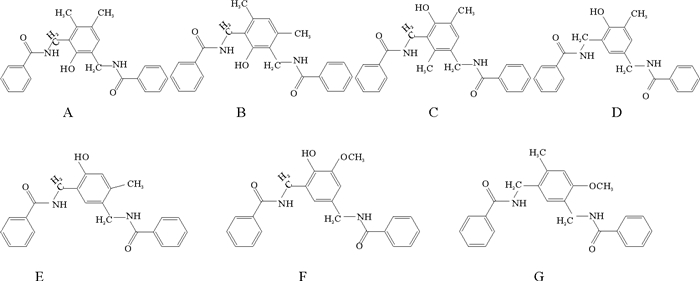
图 1 目标化合物的结构式 Fig. 1 Structural formula of the target compounds |
3, 4-二甲基苯酚、3, 5-二甲基苯酚、2, 5-二甲基苯酚、2-甲基苯酚、3-甲基苯酚、2-甲氧基苯酚、3-甲基苯甲醚, 以上试剂均购自国药集团化学试剂有限公司均为分析纯,无水乙醇、浓硫酸均为工业级。
瑞士BuCHI公司B-545熔点仪;美国NICOLET公司AVATAR-360红外光谱仪;日本电子株式会社(JEOL)JUM-ECP600核磁共振波谱仪;日本Hitachi公司U-2800紫外可见分光光度计。
金黄色葡萄球菌和大肠杆菌均由中国海洋大学海洋生命学院微生物实验室提供。
1.2 合成方法与表征N-(3-苯甲酰胺甲基-2-羟基-4, 5-二甲基苄基)苯甲酰胺(A)的合成与表征:
向配备有温度计、电动搅拌装置和回流冷凝装置的500 mL三口烧瓶中依次加入N-羟甲基苯甲酰胺30.2 g(0.2 mol)、3, 4-二甲基苯酚12.2 g(0.1 mol)、以100 mL无水乙醇作溶剂,加热搅拌,控制反应体系的温度为35~40 ℃之间,滴加催化剂浓硫酸10 mL,用TLC(展开剂: v乙酸乙酯/v石油醚=1:1)监控反应进程,72 h后反应结束,反应体系中有大量白色沉淀,冰浴冷却反应体系至沉淀全部析出,过滤,用冷水洗涤滤饼至中性,即得N-(3-苯甲酰胺甲基-2-羟基-4, 5-二甲基苄基)苯甲酰胺粗产品,用无水乙醇重结晶,得白色粉末,产率:89.0%,m.p.:157.2~158.7 ℃。IR (KBr):696.5,1 301.2,1 547.0,1 626.5,3 320.3 cm-1;1H NMR (CDCl3,600 MHz): 2.19(s,3H,CH3),2.33(s,3H,CH3),4.56 (t,J=6.0,2H,CH2),4.72 (t,J=6.0,2H,CH2), 6.98(s,1H,PhH),7.03(q,J=6.0,1H,NH),7.13(q,J=6.0,1H,NH),7.41 (m,4H,PhH),7.49(m,2H,PhH),7.77 (m,H,PhH), 9.98(s,1H,OH)。
参照上述A的合成方法,合成得到其他6种化合物,其产率、熔点及结构表征如下:
N-(3-苯甲酰胺甲基-2-羟基-4, 6-二甲基苄基)苯甲酰胺(B):产率:78.5%,m.p.:231.1~232.6 ℃。IR (KBr):705.7,1 310.1,1 552.5,1 638.1,3 239.1 cm-1;1H NMR (CDCl3,600 MHz): 2.29(s,3H,CH3),2.35(s,3H,CH3),4.43 (m,4H, CH2),7.50(m,6H,PhH),7.85(m,4H,PhH),8.31(q,J=6.3,1H,NH),8.78 (q,J=5.4,1H, NH),9.71(s,1H,OH)。
N-(4-苯甲酰胺甲基-2-羟基-3, 6-二甲基苄基)苯甲酰胺(C):产率53.5%,m.p.: 201.2~202.1 ℃。IR (KBr): 710.5,1 303.7,1 636.1,3 264.2 cm-1; 1H NMR (DMSO,600 MHz): 2.14(s,3H,CH3),2.37 (s,3H,CH3),4.41(d,J=6.0,2H,CH2),4.48(d,J=5.4,2H,CH2), 7.02 (s,1H,PhH),7.54 (d,J =5.4,4H,PhH),7.57(t,J=7.8,1H,PhH),7.91(t,J=7.8Hz,4H,PhH),8.72(d,J=7.2,1H,PhH),9.40 (t,J=6.0,2H,NH),9.97 (s, 1H,OH)。
N-(3-甲基-5-苯甲酰胺甲基-2-羟基苄基)苯甲酰胺(D):产率:65.7%,m.p.:183.7~184.7 ℃。IR (KBr):692.5,1 308.8,1 541.2,1 650.0,3 338.6 cm-1;1H NMR (DMSO,600 MHz):2.15 (s,3H,CH3),4.34 (d,J=6.1,4H,CH2),6.99 (s,1H,PhH),7.45 (m,4H,PhH),7.47 (m,1H,PhH),7.86 (m,4H,PhH),8.90 (t,J=6.0,2H,NH),9.34 (s,1H,OH)。
N-(4-甲基-5-苯甲酰胺甲基-2-羟基苄基)苯甲酰胺(E):产率:68.2%,m.p.:216.5~217.9 ℃。IR (KBr):696.9,1 310.8,1 543.4,1 624.3,3 314.1 cm-1;1H NMR (DMSO,600 MHz): 2.21 (s,3H,CH3),4.35 (d,J=5.5,4H,CH2),6.63 (s,1H,PhH),7.09 (s,1H,PhH),7.40 (m,4H,PhH),7.50 (m,2H,PhH),7.81 (m,4H,PhH),8.75 (t,J=5.5,1H,NH),8.92 (t,J=5.7, 1H,NH),9.43 (s,1H,OH)。
N-(5-苯甲酰胺甲基-2-羟基-3-甲氧基苄基)苯甲酰胺(F):产率:71.9%,m.p.:207.1~208 ℃。IR (KBr):704.7,1 293.9,1 602.7,1 653.2,3 060.0,3 355.5 cm-1;1H NMR (DMSO,600 MHz): 3.72 (s,3H,OCH3),4.48 (d,J=5.9,4H,CH2),6.78 (s,1H,PhH),6.92 (s,1H,PhH),7.47 (m,4H,PhH),7.53 (m,2H,PhH),7.90 (m,4H,PhH),8.91 (s,1H,OH),8.95 (t,J=5.7,2H,NH)。
N-(5-苯甲酰胺甲基-2-甲氧基-4-甲基苄基)苯甲酰胺(G):产率:50.3%,m.p.: 190.6~191.1 ℃。IR (KBr): 693.0,1 256.3,1 547.7,1 642.0 cm-1; 1H NMR (DMSO,600 MHz): 2.31(s,3H,CH3),3.81(s,3H,OCH3),4.40(d,J=6.0,4H,CH2),6.82(s,1H,PhH),7.15(s,1H,PhH),7.40(t,J=8.4,4H,PhH),7.50(d,J=8.4,2H,PhH),7.78(d,J=7.2,4H,PhH),8.80(t,J=6.0,2H,NH)。
1.3 性能测试海洋中的细菌、单细胞藻类等微生物会在涉水设施的表面上形成一层生物黏膜,这层生物粘膜是其他大型污损生物附着的基础[14]。海上挂板则是最直接有效的反映材料防污性能的实验方法。因此,本文采用最小抑菌浓度实验来测试合成化合物的抑菌活性,进而结合实海挂板实验考察了合成化合物的防生物附着活性。
1.3.1 最小抑菌质量浓度(MIC)实验采用试管二倍稀释法[15],将合成的7种双苯甲酰胺类辣素结构化合物分别配制成2 mg/mL的丙酮溶液,再准确量取2 mL上述配置好的溶液分别加入到含有2 mL的液体培养基的灭菌试管中,以仅接种菌的试管为阳性对照,以仅含液体培养基的试管为阴性对照。合成化合物的初始浓度为1 mg/mL,依次二倍稀释并混合均匀,分别向各试管中加入一定质量浓度的菌悬液200 μL,使最终菌液浓度为104~105 cfu/mL,振荡培养24 h后,以试管中明显无菌生长的最小化合物的浓度为MIC[16-19]。
1.3.2 防污性能实验以合成的7种双苯甲酰胺类辣素结构化合物为辅助防污剂制备海洋防污涂料,配方如下表所示:
参照国家标准GB5370—2007[20]进行试片的处理、涂覆与悬挂。
试片的处理方法:将聚四氟乙烯的样板裁成250 mm×150 mm×3 mm的试片,以120目的砂纸打磨后固定在带槽的木框中,以二甲苯擦拭固定好的试片,放在通风处自然晾干。
将按表 1配方制备好防污涂料涂覆在试片上,自然晾干后,将样板框悬挂在胶州湾青岛港八号码头距离岸边100 m的浮筏上,浸海深度为1 m,浸海时间为120天。
|
|
表 1 防污涂料的配方 Table 1 Basic compositions of antifouling coating |
以化合物A为例进行化合物的结构解析。
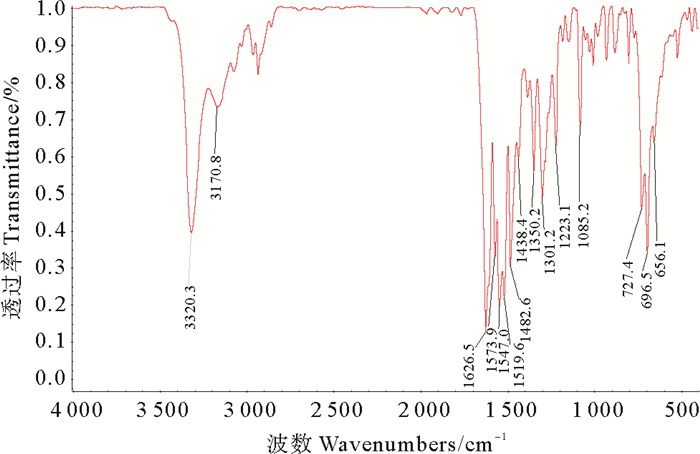
从图 2的红外光谱图中可以看出:产物在3 320 cm-1处出现了OH的伸缩振动吸收峰,在3 170 cm-1处出现了NH的伸缩振动吸收峰,在1 626 cm-1处出现了酰胺中羰基的伸缩振动吸收峰,在1 301 cm-1处出现了酚羟基中碳氧的伸缩振动吸收峰,在1 573、1 519和1 482 cm-1处出现了苯环骨架的伸缩振动吸收峰。
|
图 2 化合物A的红外光谱图 Fig. 2 IR spectra of compound A |
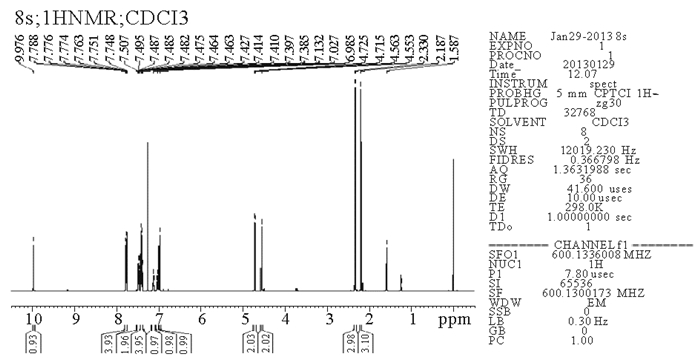
从图 3的核磁氢谱中可以看出:除去CDCl3溶剂峰对积分值的影响,各组峰的化学位移值、质子数目及裂分情况与A化合物结构相符。甲基氢的化学位移是2.19和2.33,亚甲基氢的化学位移是分别为4.56和4.72,母体苯环氢的化学位移为6.98,苯甲酰胺苯环氢的化学位移为7.41,7.49和7.77,酰胺基氢的化学位移为7.03和7.13,羟基的化学位移为9.98,结合红外谱图可以证明所得化合物为设计结构的A化合物。
|
图 3 化合物A的核磁氢谱图 Fig. 3 1H NMR spectra of compound A |
从化合物B~G的红外光谱中可以看出,在3 200~3 400 cm-1之间存在有-NH和-OH的伸缩振动吸收峰,1 624~1 642 cm-1之间有酰胺的羰基的伸缩振动吸收峰,1 250~1 310 cm-1之间有酚羟基中碳氧的伸缩振动吸收峰。而在其核磁氢谱(1H NMR)当中,每个峰的归属也都比较容易确定,如:苯环上取代的甲基氢的δ值在2.14~2.37之间,分别与酰胺基和苯环相连的亚甲基氢的δ值在4.34~4.48之间,羟基氢的δ值在8.91~9.97之间,酰胺基氢的δ值在8.31~9.40之间,苯环上的氢的δ值在6.63~8.72之间,苯环上取代的甲氧基氢的δ值在3.72~3.81之间,且简单峰的裂分均符合N+1规则。结合红外光谱和核磁氢谱的数据可以得出合成的化合物均为预期结构化合物。
2.2 抑菌性能通过最小抑菌浓度(MIC)实验,考察了合成化合物的抑菌活性,并探讨了苯环上不同的取代基对化合物抑菌活性的影响,最小抑菌浓度结果见表 2所示。
|
|
表 2 合成化合物的最小抑菌质量浓度 Table 2 The minimum inhibitory concentration of synthetic compounds |
从上表的实验结果可以看出,合成的7种化合物对两种菌株均具有较好的抑制活性,其中F和G两种化合物的活性最高,而D、E两种化合物的活性最低,这可能与苯环上取代基的电荷密度有关。以化合物D和化合物F为例来进行说明,排除掉化合物所共有的两个苯甲酰胺基团的影响,该2种化合物在苯环上还分别有酚羟基和甲氧基两种取代基,通过量子化学计算可以得到F中甲氧基和羟基的电荷密度分别是-0.272 6和-0.241 8,D中两个羟基的电荷密度分别是-0.271 8和-0.231 7,F的电荷密度大于D的电荷密度,电荷密度越大,抑菌活性越好[21],因此F的抑菌活性要高于D,这与上表实验结果相吻合。其它化合物的量子计算结果也均与实验结果相一致。
2.3 防污性能将制备好的试片框实海挂板120天,每隔30天观察试片上污损生物的附着情况,结果如表 3所示:
|
|
表 3 海上挂板实验结果 Table 3 Results of testing panels in the sea |
从上表实海挂板图片可以看出,在挂板120天后,空白试片已经完全被污损生物所覆盖,仅含氧化亚铜防污剂的空白试片上也已经有近80%以上的面积被藤壶、海鞘等污损生物所覆盖,而添加了合成的A~G辅助防污剂的样板中除了含D的试片有少量藤壶附着生长外,其余试片仅有少量的生物粘膜或污泥附着其上,几乎无污损生物的附着。由此可证明,添加了合成的双苯甲酰胺类辣素结构防污剂的涂料即使在生物生长旺期也能明显抑制海洋污损生物的附着,具有良好的防污效果,防污期效至少120天。总体来看,含F防污剂的样板防污效果最好,含D防污剂的样板防污效果最差,已经开始有小藤壶附着了,这也与两者的抑菌效果一致。
3 结语本文以N-羟甲基苯甲酰胺和7种取代芳烃为起始原料,通过F-C烷基化反应合成了A~G 7种双苯甲酰胺类辣素结构化合物,并通过红外光谱及核磁氢谱对合成化合物的结构进行了表征。探讨了合成化合物对自然界中常见大肠杆菌和金黄色葡萄球菌的抑制活性,实验结果表明该7种双苯甲酰胺类辣素结构化合物对2种菌均具有良好的抑制活性,其中以含有-OCH3基团的化合物F和G的抑制效果最好,对2种菌的MIC均可达0.125 mg/mL。以该7种化合物为辅助防污剂制备的海洋防污涂料,实海挂板120天后,除了含D防污剂的试片上开始有少量藤壶附着外,其它的试片均光洁无明显的生物附着,说明了除D外的A、B、C、E、F和G 6种防污剂均具有优异的防污效果。结合辣素类化合物自身所具有环境友好的特性说明了此6种化合物是一类优良的环境友好型防污剂,具有较好的应用前景。
| [1] |
Callow M E, Callow J A. Marine biofouling: a sticky problem[J]. Biologist, 2002, 49(1): 1-5.
(  0) 0) |
| [2] |
Schultz M P, Bendick J A, Holm E R, et al. Economic impact of biofouling on a naval surface ship[J]. Biofouling, 2011, 27(1): 87-98. DOI:10.1080/08927014.2010.542809
(  0) 0) |
| [3] |
Abarzua S, Jakubowski S. Biotechnological investigation for the prevention of biofouling: Biological and biochemical principles for the preventionof biofouling[J]. Marine Ecology Progress Series, 1995, 123(1): 301-312.
(  0) 0) |
| [4] |
Davis A R, Targett N M, Mcconnell O J, et al. Epibiosis of marine algae and benthic invertebrates: natural products chemistry and other mechanisms inhibiting settlement and overgrowth[J]. Bioorganic Marine Chemistry, 1989, 3: 85-114. DOI:10.1007/978-3-642-74560-7
(  0) 0) |
| [5] |
Finnie A A, Williams D N. Paint and coatings technology for the control of marine fouling[J]. Oxford: Wiley-Blackwell, 2010, 12(12): 185-206.
(  0) 0) |
| [6] |
Guo S F, Lee H P, Chaw K C, et al. Effect of ultrasound on cyprids and juvenile barnacles[J]. Biofouling, 2011, 27(2): 185-192. DOI:10.1080/08927014.2010.551535
(  0) 0) |
| [7] |
Guo S F, Lee H P, Teo S L, et al. Inhibition of barnacle cyprid settlement using low frequency and intensity ultrasound[J]. Biofouling, 2012, 28(2): 131-141. DOI:10.1080/08927014.2012.658511
(  0) 0) |
| [8] |
J Bellas J. Prediction and assessment of mixture toxicity of compounds in antifouling paints using the sea-urchin embryo-larval bioassay[J]. Aquatic Toxicology, 2008, 88(4): 308-315. DOI:10.1016/j.aquatox.2008.05.011
(  0) 0) |
| [9] |
彭必先, 王俊莲, 彭争宏, 等. 辣椒素同系物合成、辣度及海洋生物防污性能研究[J]. 中国科学:化学, 2011, 41(10): 1646-1654. Peng B X, Wang J L, Peng Z H, et al. Studies on the synthesis, pungency and anti-biofouling performance of capsaicin analogues[J]. Scientia Sinica Chimica, 2011, 41(10): 1646-1654. (  0) 0) |
| [10] |
金涌, 李俊, 姚宏伟, 等. 辣椒提取物的抗炎镇痛作用[J]. 安徽医科大学学报, 2001, 36(6): 430-431. Jin Y, Li J, Yao H W, et al. Antiinflammatory and analgesic effects of extract of capsicum[J]. Acta Universitatis Medicinalis Anhui, 2001, 36(6): 430-431. (  0) 0) |
| [11] |
唐胜球, 董小英. 辣椒素的生理功能及应用前景[J]. 粮油食品科技, 2002, 10(6): 25-27. Tang S Q, Dong X Y. Physiological function and application prospect of capsaicin[J]. Science and Technology of Cereals, Oils and Foods, 2002, 10(6): 25-27. (  0) 0) |
| [12] |
汪文龙, 黄燕兰, 胡惟孝, 等. 辣椒素类似物的合成、结构及抗肿瘤活性[J]. 高等学校化学学报, 2010, 31(12): 2400-2406. Wang W L, Huang Y L, Hu W X, et al. Synthesis, structures and anti-tumor properties of capsaicin analogues[J]. Chemical Journal of Chinese Universities, 2010, 31(12): 2400-2406. (  0) 0) |
| [13] |
Wang J L, Peng Z H, Zhou S Z, et al. A study of pungency of capsaicinoid as affected by their molecular structure alteration[J]. Pharmacology & Pharmacy, 2011, 2: 109-115.
(  0) 0) |
| [14] |
Callow M E, Fletcher R L. The influence of low surface energy materials on bioadhesion——a review[J]. International Biodeterioration & Biodegradation, 1994, 34(3-4): 333-348.
(  0) 0) |
| [15] |
Muraina I A, Picard J, Eloff J N. Development of a reproducible method to determine minimum inhibitory concentration (MIC) of plant extract against a slow-growing mycoplasmas organism[J]. Phytomedicine, 2009, 16(2): 262-264.
(  0) 0) |
| [16] |
于良民, 王宝娟, 李霞. 新型吲哚类防污剂抑菌性能评价[J]. 涂料工业, 2007, 37(4): 17-20. Yu L M, Wang B J, Li X. Evaluation of antibacterial activity of indole derivatives as antifouling agent[J]. Paint & Coatings Industry, 2007, 37(4): 17-20. (  0) 0) |
| [17] |
王宝娟. 海洋防污涂料及其主要成分的生物学性能研究[D]. 青岛: 中国海洋大学, 2007. Wang B J. Study on Capability of Marine Antifouling Paints and Its Main Compontent[D]. Qingdao: Ocean University of China, 2007. http://cdmd.cnki.com.cn/Article/CDMD-10423-2008012513.htm (  0) 0) |
| [18] |
董磊. 羧甲基壳聚糖金属盐/壳聚糖包覆氧化亚铜的制备及其海洋防污性能研究[D]. 青岛: 中国海洋大学, 2007. Dong L. The Preparation of Carboxymethyl Chitosan Salt/nano Cu2O Enclosed by Chitosan and the Study of Their Usage in Marine Antifouling Paint[D]. Qingdao: Ocean University of China, 2007. http://cdmd.cnki.com.cn/Article/CDMD-10423-2008010864.htm (  0) 0) |
| [19] |
Pernak J, Skrzypczak A. 3-alkylthiomethyl-1-ethylimidazolium chlorides correlation between critical micelle concentrations and minimum inhibitory concentrations[J]. European Journal of Medicinal Chemistry, 1996, 31(11): 901-903. DOI:10.1016/S0223-5234(97)89853-4
(  0) 0) |
| [20] |
防污漆样板浅海浸泡试验方法[S]. GB/T 5370-2007. Method for testing antifouling panels in shallow submergence[S]. GB/T 5370-2007. (  0) 0) |
| [21] |
袁帅, 刘峥, 赖丽燕, 等. 含羧基席夫碱抑菌活性定量构效关系研究[J]. 化学通报, 2013, 76(12): 1126-1131. Yuan S, Liu Z, Lai L Y. Study on quantitative structure-activity relationship of antibacterial activities of schiff bases containing carboxyl[J]. Chemistry Bulletin, 2013, 76(12): 1126-1131. (  0) 0) |
 2018, Vol. 48
2018, Vol. 48





























