2. 武汉大学中南医院妇瘤科/湖北省肿瘤医学临床研究中心/ 肿瘤生物学行为湖北省重点实验室 湖北 武汉 430071
2. Dept. of Gynecologic Oncology, Zhongnan Hospital of Wuhan University; Hubei Cancer Clinical Study Center; & Hubei Key Laboratory of Tumor Biological Behaviors, Wuhan 430071, China
宫颈癌是发病率最高的女性生殖系统恶性肿瘤,全球平均每年有53万新发宫颈癌病例,宫颈癌总体死亡率达50%,其中发展中国家的宫颈癌死亡率超过85%。宫颈癌的复发及宫颈癌的转移是影响宫颈癌患者预后的重要原因,成为宫颈癌近年治疗研究的重点。肿瘤干细胞学说的提出对宫颈肿瘤的发生、发展和治疗作出了新的诠释[1]。肿瘤干细胞具有自我更新、无限增殖和多向分化潜能特性,这种特性是可能是通过许多发育相关的信号转导及转录活化因子调控实现的[2]。
高迁移率族蛋白B1(HMGB1)是一种DNA结合蛋白,招募多种类型干细胞,参与受损组织修复[3]。但是HMGB1是一个“黏性”很高的分子,细胞外的HMGB1作为信号分子与细胞表面的不同受体结合,可以激活多种信号转导通路而执行各种生物学功能[4]。近年来研究显示HMGB1可通过JAK/信号转导因子(STAT)信号通路对肿瘤的发生、发展产生重要的影响,同时,有研究发现JAK/STAT途径激活可使STAT特别是STAT3过度活化,从而抑制肿瘤细胞凋亡及促进细胞周期进程,导致肿瘤增殖、浸润、转移、血管生成及免疫逃逸,而STAT3可通过结合Oct3/4上调肿瘤干细胞自我更新的增殖关键性基因Naong,进而维持肿瘤干细胞的自我更新[5]。
我们先前已经通过细胞和分子实验研究显示:HMGB1可以通过JAK/ STAT3这一信号传导通路来调控干细胞标志物Nanog蛋白从而调控宫颈肿瘤细胞的干性[6],在本研究中我们通过复习宫颈鳞癌患者临床和病理资料,应用免疫组织化学技术检测HMGB1、Nanog及STAT3的表达水平,探讨HMGB1、STAT3与宫颈癌干细胞标志物Nanog在宫颈癌中的表达及临床意义,从而为探索宫颈肿瘤干细胞与宫颈肿瘤的进展及生存的关系提供理论基础。
1 材料与方法 1.1 组织标本及相关资料收集随访资料完整的2003年6月至2008年12月在武汉大学中南医院妇瘤科接受宫颈癌根治术、经病理学证实的原发性宫颈癌患者石蜡包埋的肿瘤组织标本共78例,详见表 1。所有患者术前无化疗、放疗或其他治疗史,临床分期参照2009年国际妇产科联盟FIGO标准,另外收集正常宫颈鳞状上皮组织标本(因子宫肌瘤行全子宫切除术)91例作为对照研究。所有患者的临床资料完整,病理资料由病理科专业主任医师复习,经医院伦理委员会批准。
| 表 1 患者临床资料 |
鼠抗STAT3抗体、兔抗HMGB1抗体和兔抗Nanog抗体均购自美国abcam生物公司。免疫组织化学检测试剂盒购自基因科技(上海)有限公司。
1.3 免疫组织化学染色标本经10%甲醛固定,石蜡包埋,4 μm厚连续切片,常规SP法免疫组织化学染色。一抗HMGB1、STAT3和Nanog的工作浓度为1:100、1:100和1:20。实验步骤严格按照SP二步法试剂盒说明书进行。已知阳性切片作为阳性对照,PBS缓冲液代替一抗作为阴性对照。
1.4 结果判断免疫组织化学染色结果的判定:临床和病理双盲阅片。HMGB1、STAT3和Nanog主要在细胞核表达,阳性染色呈黄色或棕黄色。综合染色强度和阳性细胞百分率计算染色积分。染色强度:不着色,0分;浅黄色,1分;棕黄色,2分;棕褐色,3分。阳性细胞百分率:0%,0分;1%-25%,1分;26%-50%,2分;51%-75%,3分;76%-100%,4分。两项相加分值即为每个视野的染色积分(0-7分),染色积分0分(-)、1-3分(+)、4-5分(++)和6-7分(+++),200倍高倍镜下随机取5个不同视野求平均染色积分,染色积分>3分为高表达(+),≤3分为低表达(-)。
1.5 随访随访自手术当日起开始计算生存时间,通过门诊电话及信访等方式进行随访,从确诊之日起进行随访,生存期以年为计算单位,随访时间为1-12年,中位随访时间为6年,最后一次随访时间2017年1月31日或失访作为随访结束点。
1.6 统计学方法所有计数资料以例数(%)表示,计量资料以均数±标准差表示,计量资料的组间比较采用独立样本t检验,计数资料的组间比较采用χ2检验或Fishers精确概率法。三种蛋白表达的相关性分析采用Spearman等级相关法。Cox比例风险模型用于分析宫颈癌5年生存率的影响因素。所有的统计分析均通过专业统计分析软件SPSS 22.0完成,P < 0.05为差异具有统计学意义。
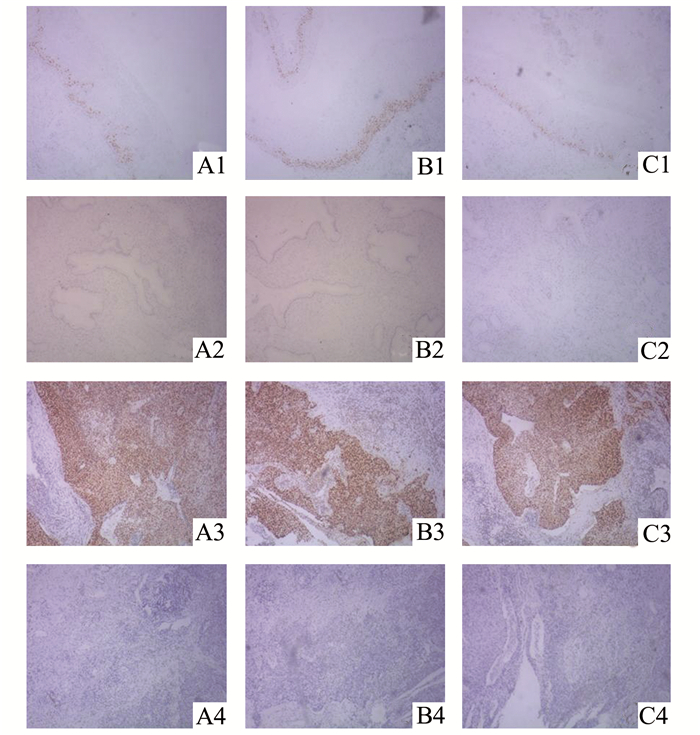
2 结果 2.1 HMGB1、STAT3和Nanog在宫颈癌组织及正常宫颈组织中的表达HMGB1主要表达于宫颈癌细胞胞核,细胞质中少有表达,阳性染色呈棕黄色至棕褐色颗粒状(图 1)。HMGB1在慢性宫颈炎组织和宫颈鳞癌中阳性表达率为13.19% (12/91)和75.64%(59/78),差异具有统计学意义(χ2=67.245,P < 0.001)。STAT3阳性蛋白表达于宫颈鳞癌细胞的胞核中,呈清晰的棕黄色颗粒状至棕褐色颗粒状(图 1)。在宫颈鳞癌组织和慢性宫颈炎组织的阳性表达率分别为61.54%(48/78)和23.08%(21/91),差异具有统计学意义(χ2=25.717 4,P < 0.001);Nanog主要表达于宫颈鳞癌细胞胞核,阳性染色呈棕黄色至棕褐色颗粒状(图 1)。Nanog在慢性宫颈炎组织和宫颈鳞癌组织中的阳性表达率为9.89%(9/91)和71.79%(56/78),差异具有统计学意义(χ2=68.002 4,P < 0.001)。
|
图 1 免疫组化法检测STAT3(A), Nanog(B)和HMGB1(C)在宫颈组织的表达(SP ×200) A1, B1, C1:慢性宫颈炎组织的阳性表达;A2, B2, C2:慢性宫颈炎组织的阴性表达;A3, B3, C3:宫颈癌组织的阳性表达;A4, B4, C4:宫颈癌组织的阴性表达 |
HMGB1及STAT3表达增高,Nanog也增高;HMGB1及STAT3表达降低,Nanog也降低(表 2)。经Spearman等级相关分析,Nanog的表达与HMGB1的表达、STAT3的表达均呈正相关(r1=0.366 8,P < 0.05;r2=0.256 2, P < 0.05)。
| 表 2 HMGB1、STAT3与Nanog蛋白表达的相关性 |
以HMGB1低表达为对照组,发现HMGB1高表达与宫颈浸润深度(χ2=3.863,P=0.049)、盆腔淋巴结状态(χ2=11.759,P < 0.001),5年总生存率(P=0.002)和5年无进展生存率(P=0.010 1)密切相关(表 3),而HMGB1高表达与患者年龄、分化程度、肿瘤的大体形态、肿瘤大小、FIGO分期、病理类型以及阴道切缘之间的关系无统计学意义(P>0.05);以STAT3低表达为对照组,发现STAT3高表达与患者年龄、分化程度、盆腔淋巴结状态、宫颈浸润深度、肿瘤的大体形态、FIGO分期、5年总生存率和5年无进展生存率密切相关(P < 0.05),而STAT3高表达与肿瘤大小、病理类型以及阴道切缘之间的关系无统计学意义(P>0.05);以Nanog低表达为对照组,发现Nanog高表达与患者年龄、宫颈浸润深度、盆腔淋巴结状态、5年总生存率和5年无进展生存率密切相关(P < 0.05),而Nanog高表达与分化程度、肿瘤的大体形态、肿瘤大小、FIGO分期、病理类型以及阴道切缘之间的关系无统计学意义(P>0.05)。
| 表 3 HMGB1、STAT3和Nanog表达与临床病理因素的关系[n(%)] |
以5年生存率为界限对影响宫颈癌预后因素的分析中发现HMGB1高表达(P=0.002),STAT3高表达(P=0.000 9),Nanog高表达(P=0.005 1)、宫颈浸润深度(P=0.028)、分化程度(P= 0.001)、淋巴结状态(P= 0)、临床分期(P=0.002)等因素与宫颈癌的预后相关(表 4)。
| 表 4 宫颈癌患者生存时间的多因素分析[n(%)] |
将上述影响5年生存率的临床病理因素纳入Cox比例风险模型进行多因素分析,发现HMGB1高表达、分化程度、淋巴结状态、宫颈浸润深度、病理类型、FIGO分期、肿瘤直径、阴道切缘等是影响生存的独立预后因素(表 5)。与HMGB1高表达比较,HMGB1低表达更有机会延长生存期[风险比= 17.424,95%CI(1.8123,247.008];Cox回归多因素分析表明STAT3及Nanog高表达不是影响预后的独立因素。
| 表 5 多因素Cox回归分析预后相关因素 |
近些年多项研究证实,HMGB1在多种人类肿瘤组织中过表达,与肝癌[7]和卵巢癌[8]等恶性肿瘤细胞的增殖浸润及侵袭转移能力密切相关,也在一定程度上预示着这些肿瘤的预后。本研究发现HMGB1在正常宫颈鳞状上皮组织中表达明显低于宫颈鳞癌中表达率(P<0.001)。本研究还发现HMGB1高表达与宫颈浸润深度(χ2=3.863,P=0.049)、盆腔淋巴结状态(χ2=11.759,P<0.001)、5年总生存率(P=0.002)、5年无进展生存率密切相关(P=0.000 1),而HMGB1高表达与患者年龄、分化程度、肿瘤的大体形态、肿瘤大小、FIGO分期、病理类型以及阴道切缘之间的关系无统计学意义;HMGB1高表达组的生存时间明显低于低表达组的生存时间,差异有统计学意义(P<0.001),两组间的差异均具有统计学意义(P<0.001),单因素和Cox回归多因素分析表明HMGB1高表达系影响宫颈癌预后的独立因素。
3.2 STAT3的表达及与宫颈肿瘤的关系有研究表明肿瘤干细胞相关信号通路蛋白(如:STAT、Wnt、Notch等)在宫颈癌的发生与发展中被激活,抑制肿瘤自我更新相关信号蛋白则明显改善宫颈癌患者的预后[9]。STAT3作为多种肿瘤的多条信号传导通路的交汇点,STAT3在肺癌、胃癌等多种肿瘤细胞中高表达。我们研究发现:STAT3阳性蛋白在宫颈鳞癌组织和正常宫颈鳞状上皮组织中的阳性表达率有显著性差异(χ2=25.717 4,P<0.001)。STAT3高表达与患者年龄、分化程度、盆腔淋巴结状态、宫颈浸润深度、肿瘤的大体形态、FIGO分期、5年总生存率和5年无进展生存率密切相关(P<0.05),而STAT3高表达与肿瘤大小、病理类型以及阴道切缘之间的关系无统计学意义(P>0.05)。STAT3高表达组的生存时间显著低于低表达组的生存时间,两组间的差异均具有统计学意义(P<0.001),单因素分析表明:STAT3高表达与宫颈癌预后相关,Cox回归多因素分析表明:STAT3高表达不是影响宫颈癌预后的独立因素,故STAT3高表达可能与其他因素共同作用影响宫颈癌的预后。
3.3 Nanog的表达及与宫颈肿瘤的关系Nanog是胚胎干细胞中特异表达的基因, 是维持干细胞自我更新增殖和亚全能性的关键性基因,是全能性或多能性干细胞标志物[10]。我们的实验结果显示:Nanog在正常宫颈鳞状上皮阳性表达率为9.89%(9/91),明显低于宫颈鳞癌组织的阳性表达率71.79%(56/78),差异有统计学意义(χ2=68.002 4,P<0.001)。以Nanog低表达为对照组,发现Nanog高表达与患者年龄、宫颈浸润深度、盆腔淋巴结状态、5年总生存率和5年无进展生存率密切相关(P<0.05),而Nanog高表达与分化程度、肿瘤的大体形态、肿瘤大小、FIGO分期、病理类型以及阴道切缘之间的关系无统计学意义(P>0.05)。单因素分析表明:Nanog高表达与宫颈癌预后相关。Cox回归多因素分析表明:Nanog高表达不是影响宫颈癌预后预后的独立因素,表明Nanog高表达可能与其他因素共同作用影响宫颈癌的预后。
3.4 HMGB1、STAT3和Nanog表达的相关性我们用免疫组化的方法从临床标本中验证HMGB1、STAT3和Nanog表达的相关性,我们的研究结果显示:HMGB1及STAT3表达增高,Nanog也增高;HMGB1及STAT3表达降低,Nanog也降低,经Spearman等级相关分析,Nanog的表达与HMGB1的表达、STAT3的表达均呈正相关。这提示我们HMGB1、STAT3和Nanog联合诊断宫颈癌,提高检测的灵敏度和精确度,为宫颈癌预防提供新的策略,也为宫颈癌的治疗以及后期效果的评估提供新的依据。
| [1] | Guo D, Xu BL, Zhang XH, et al. Cancer stem-like side population cells in the human nasopharyngeal carcinoma cell line cne-2 possess epithelial mesenchymal transition properties in association with metastasis[J]. Oncol Rep, 2012, 28(1): 241-247. |
| [2] | Zhang P, Li H, Yang B, et al. Biological significance and therapeutic implication of resveratrol-inhibited Wnt, Notch and STAT3 signaling in cervical cancer cells[J]. Genes Cancer, 2014, 5(5-6): 154-164. |
| [3] | Zhang QY, Wu LQ, Zhang T, et al. Autophagy-mediated HMGB1 release promotes gastric cancer cell survival via RAGE activation of extracellular signal-regulated kinases 1/2[J]. Oncol Rep, 2015, 33(4): 1630-1638. DOI: 10.3892/or.2015.3782. |
| [4] | Kinjyo I, Ohishi M, Shouda T, et al. Positive and negative roles of IL-6, STAT3, and SOCS3 in inflammatory arthritis[J]. Adv Exp Med Biol, 2007, 602: 113-124. DOI: 10.1007/978-0-387-72009-8. |
| [5] | Do DV, Ueda J, Messerschmidt DM, et al. A genetic and developmental pathway from STAT3 to the OCT4-NANOG circuit is essential for maintenance of ICM lineages in vivo[J]. Genes Dev, 2013, 27(12): 1378-1390. DOI: 10.1101/gad.221176.113. |
| [6] | Wang H, Cai HB, Chen LL, et al. STAT3 Correlates with Stem Cell-related Transcription Factors inCervical Cancer[J]. J Huazhong Univ Sci Technol: Med Sci, 2015, 35(6): 891-897. DOI: 10.1007/s11596-015-1524-0. |
| [7] | Zhang L, Han J, Wu H, et al. The association of hmgb1 expression with clinicopathological significance and prognosis in hepatocellular carcinoma: a meta-analysis and literature review[J]. PLoS One, 2014, 9: e110626. DOI: 10.1371/journal.pone.0110626. |
| [8] | Chen J, Xi B, ZhaoY, et al. High-mobilitygroup protein b1 (HMGB1) is a novel biomarker for human ovarian cancer[J]. Gynecol Oncol, 2012, 126: 109-117. DOI: 10.1016/j.ygyno.2012.03.051. |
| [9] | Mao J, Fan S, Ma W, et al. Roles of Wnt/β-catenin signaling in the gastric cancerstem cells proliferation and salinomycin treatment[J]. Cell Death Dis, 2014, 5: e1039. DOI: 10.1038/cddis.2013.515. |
| [10] | Wang ML, Chiou SH, Wu CW, et al. Targeting cancer stem cells: emerging role ofNanog transcription factor[J]. Onco Targets Ther, 2013, 6: 1207-1220. |
 2018, Vol. 39
2018, Vol. 39


