| SiO2/TiO2复合材料的制备及其光催化性能 |
2. 齐鲁工业大学(山东省科学院)化学与制药工程学院,济南 250353
2. School of Chemistry and Pharmaceutical(Engineering, Qilu University of Technology Shandong Acodemy of Sciences), Jinan 250353, China
介孔二氧化硅自发现以来[1],因具有极高的比表面积,规则有序、大小均一可调的孔径,狭窄的孔径分布等特点,使其在多相催化、分离过程、生物医学系统和主客体化学等方面存在很大的潜在应用[2-4]。
然而介孔二氧化硅表面富含羟基,存在很强的极性,限制了其在多方面的应用。通过对介孔二氧化硅进行有效的改性,制备各种功能化的介孔二氧化硅,可以快速有效地解决该问题[5-6]。电子转移再生催化剂原子转移自由基聚(ARGET ATRP)就是一种“绿色环保”的化学方法,可以保护SiO2的孔道结构,并且对于改性聚合物的分子量、多分散性指数和聚合物结构均是可控的[7]。Cheesman等[8]采用表面引发ARGET ATRP方法在SiO2粒子上接枝了聚甲基丙烯酸二乙基氨基乙酯(PDEA)刷,改性后制得pH敏感的复合材料。Cao等[9]采用简便的ARGET ATRP方法在有序介孔二氧化硅SBA-15孔内接枝聚合物进行孔内改性,以介孔二氧化硅作为支架,孔道约24 nm,接枝的单体是N-异丙基丙烯酰胺和2-甲基丙烯酸甲酯,制得具有响应性的无机物-聚合物复合材料。Liu等[10]首先用水热法制备了多层囊泡状SiO2介孔材料,然后采用ARGET ATRP方法对多层囊泡状SiO2介孔材料进行了接枝改性,选用的单体是pH敏感的甲基丙烯酸二乙氨基乙酯,将制备的改性介孔材料用于对卡托普利药物的控释。测试结果证明,可以通过调节磷酸缓冲溶液的pH,来调控介孔材料对卡托普利药物的释放量,拓展了介孔材料在生物医学领域的应用。
TiO2作为半导体光催化剂,具有化学/光腐蚀稳定性好、成本低、无毒害性以及制备工艺简单等优点[11-12]。然而,TiO2因为吸附性较低,降低了其光催化活性的效果[13]。研究发现,以介孔二氧化硅作为支架,负载TiO2纳米粒子,可以有效地提高TiO2的吸附性,从而提高光催化效果。Zheng等[14]以TiCl3溶液和正硅酸四乙酯(TEOS)作为前驱体,以三嵌段共聚物P123(EO20PO70EO20)为模板,在醋酸锌的弱酸性条件下,通过水热法直接合成了介孔TiO2/SiO2复合材料。该材料在异丙醇的光降解测试中表现出较高的催化活性,这主要是由介孔结构和材料表面的TiO2起的作用。Witte等[15]通过直接合成法成功制备了TiO2/SBA-15,TiO2在合成SBA-15的过程中直接引入,制得的TiO2/SiO2介孔复合材料具有良好的光催化活性和吸附性能。Dong等[16]以钛酸异丙酯和TEOS作为前驱体,三嵌段共聚物P123作为模板,在HCl溶液中经过自组装过程,结合溶剂蒸发方法,成功制得了介孔结构TiO2/SiO2复合材料。然而以上研究也存在缺点:TiO2被均匀地分布到介孔SiO2结构之中,降低了催化活性;TiO2纳米粒子负载在SiO2表面,易形成团聚。
我们采用ARGET ATRP方法对短棒状介孔SiO2进行了接枝亲水性聚合物改性,可以使TiO2纳米粒子均匀地分布在介孔SiO2表面,高温处理后制得短棒状介孔SiO2/TiO2复合材料,并探究了其在可见光条件下对甲基橙的光催化降解活性。
1 实验 1.1 试剂与仪器试剂:嵌段共聚物(P123,EO20PO70EO20),2-溴异丁酰溴(BiB,97%),2-溴异丁酸乙酯(EBiB,>98%),聚乙二醇甲醚甲基丙烯酸甲酯(EGMA,Mn=500 g·mol-1)购于Sigma-Aladdin公司;聚乙二醇(PEG,Mn=6 000)、3-氨丙基三乙氧基硅烷(APTES,99%)、正硅酸四乙酯(TEOS)、抗坏血酸(Vc,>99.7%)、三氯化铁(FeCl3·6H2O,>99%)、三苯基膦(PPh3,>99%)、钛酸四丁酯(TBT)、氨水、无水乙醇、甲基橙,上述试剂均为国药集团化学试剂有限公司生产。所用试剂均为分析纯。
仪器:日本电子株式会社(JEOL)公司JEM-1400型透射电子显微镜(TEM),美国Rheometric公司TGA1500 DSP-SP型热重分析仪(TGA),德国BRUKER公司D8-AVANCE型X-射线衍射仪,美国Micromeritics公司TriStar 3020型全自动比表面和空隙分析仪,日本岛津公司UV-2600型紫外-可见分光光度计(UV-vis)。
1.2 实验过程 1.2.1 催化剂的制备通过模板法[17],以P123和PEG为混合模板,以TEOS为硅源,制备短棒状介孔SiO2。取0.35 g上述制得的SiO2和20 mL甲苯于三口烧瓶中,油浴,搅拌,逐滴加入APTES 0.942 g。在持续通N2保护条件下,75 ℃搅拌反应18 h,离心清洗,然后干燥,得APTES改性后的SiO2,标记为SiO2-NH2。
取0.25 g SiO2-NH2、20 mL甲苯、0.5 mL三乙胺于三口烧瓶中,超声10 min,转移到低温反应浴中,搅拌,0 ℃下通N2保护,然后加入1 mL BiB。反应进行3 h后,将温度调至室温下继续反应;12 h后,离心、洗涤、干燥,得到改性后的SiO2,标记为SiO2-Br。
采用ARGET ATRP法制备短棒状介孔SiO2-PEGMA纳米复合材料。加入各物质的摩尔比如下:n(EGMA):n(FeCl3·6H2O):n(PPh3):n(Vc):n(EBiB)=(790/840/890):1:8:30:3。在三口烧瓶中依次加入:0.05 g引发剂SiO2-Br,10 mL溶剂DMF,0.1 g配体PPh3和0.015 g催化剂FeCl3·6H2O。超声分散均匀后,在通N2保护的条件下,加入EGMA单体20.2 mL和22.5 μL助引发剂EBiB,加入还原剂Vc 0.26 g,然后密封。将三口烧瓶置于90 ℃油浴锅中,反应15 h。离心、洗涤、干燥,得到单体EGMA改性后的SiO2。
上述所得的SiO2-PEGMA样品依次标记为Si-En (Si-E1、Si-E2和Si-E3),其中n代表单体EGMA不同摩尔比例。
将100 mL的三口烧瓶置于油浴锅中,加入50 mL乙醇、0.008 g Si-En,超声20 min。加入0.46 mL氨水,搅拌均匀后,温度升至40 ℃。向该混合溶液中逐滴加入0.5005 g TBT,在磁力搅拌条件下反应24 h。离心、洗涤,干燥后置于管式炉内。450 ℃下煅烧6 h,即得短棒状介孔SiO2/TiO2复合材料。
由不同接枝改性后的样品Si-En (Si-E1,Si-E2和Si-E3),制备得到的SiO2/TiO2复合材料依次标记为SiO2/TiO2-n (SiO2/TiO2-1,SiO2/TiO2-2和SiO2/TiO2-3)。
1.2.2 光催化性能测试紫外照射条件下降解甲基橙,所使用的高压直管汞灯为375 W,石英杯置于双层夹套中,内部流动着循环冷凝水,防止反应局部过热。照射之前,首先取0.05 g样品SiO2/TiO2-n,溶解到100 mL 30 mg·L-1的甲基橙溶液中,在没有紫外灯照射的情况下,搅拌1 h使甲基橙和催化剂达到吸附平衡。然后在高压汞灯的照射条件下,搅拌甲基橙和样品SiO2/TiO2的混合液,并且为该悬浮液提供具有稳定流速的氧气。每隔30 min,取10 mL悬浮液,测试甲基橙的吸光度在紫外灯照射前与照射后的变化。将取出的悬浮液在6000 rpm离心10 min。甲基橙染料水溶液的浓度通过紫外可见分光光度计测试,以蒸馏水作为参比,测试其在最大吸收波长553 nm处的吸光度。根据公式D=[(A0-A)/A0]×100% (D:降解速率,A0:初始吸光度,A:照射后吸光度),计算短棒状介孔SiO2/TiO2-n样品对甲基橙染料的降解率。为了测试准确,每一个样品测试3次,求取平均值。
2 结果与讨论 2.1 催化剂表征结果 2.1.1 TGA结果为了验证对短棒状介孔SiO2是否改性成功,我们对每一步改性后的SiO2进行了热重表征分析。如图 1所示:干燥后的介孔SiO2在800 ℃的热重损失为5.16%(a),主要为少量水分蒸发所致;样品SiO2-NH2和SiO2-Br的热重损失分别为14.31%(b)和16.25%(c),主要是改性后的SiO2表面少量有机成分高温热解的结果。接枝不同量聚合物改性后的样品Si-E1、Si-E2和Si-E3的热重损失分别为23.51%(d)、31.39(e)和21.38(f),主要来源于表面接枝聚合物的高温热解。同时发现样品Si-E2的重量损失明显高于其他样品,说明样品Si-E2表面的聚合物层相对厚一些,接枝效果更好。
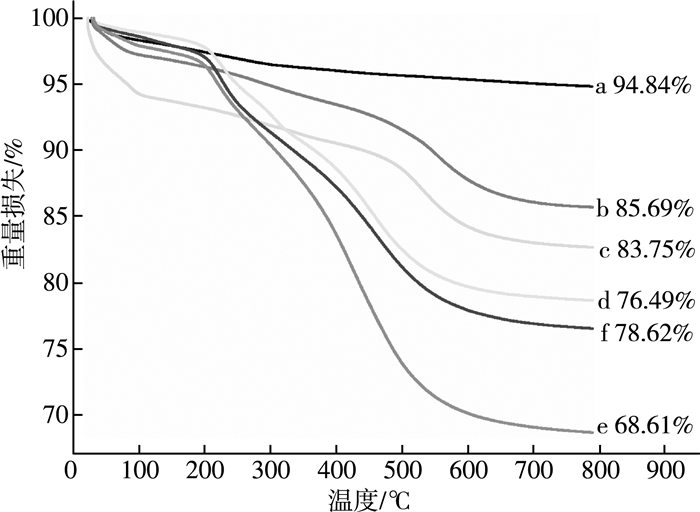 |
| 注:(a)SiO2;(b)SiO2-NH2;(c)SiO2-Br;(d)Si-E1;(e)Si-E2;(f)Si-E3 图 1 不同样品的TGA图 |
2.1.2 TEM结果
图 2是制备的短棒状介孔SiO2的TEM图。从图中可以看出,样品SiO2分散比较均匀,长大约1 μm,具有均一的六方状介孔孔道。
 |
| 图 2 SiO2的TEM图 |
图 3a、图 3c和图 3e是接枝改性后的样品Si-En的TEM图,从图中可以看出,SiO2表面存在聚合物层,且样品Si-E2的表面聚合物层接枝相对均匀、厚实。经过450 ℃高温煅烧后的样品SiO2/TiO2-n的TEM如图 3b、图 3d和图 3f所示,从图中可以看出:介孔SiO2表面变得粗糙,主要由TiO2纳米粒子组成,样品SiO2/TiO2-1和样品SiO2/TiO2-3的表面存在不同程度的TiO2纳米粒子团聚现象,样品SiO2/TiO2-2的表面负载的纳米TiO2粒子相对较均匀一些,这主要与样品Si-E2表面接枝的亲水层聚合物-PEGMA较均匀有关,使得钛源TBT通过氢键作用,在亲水层聚合物链间水解,形成相对较均一的沉淀。
 |
| 注:(a)Si-E1;(b)SiO2/TiO2-1;(c)Si-E2;(d)SiO2/TiO2-2;(e)Si-E3;(f)SiO2/TiO2-3 图 3 不同样品的TEM图 |
2.1.3 XRD结果
图 4显示的是所有样品SiO2/TiO2-n的XRD图。
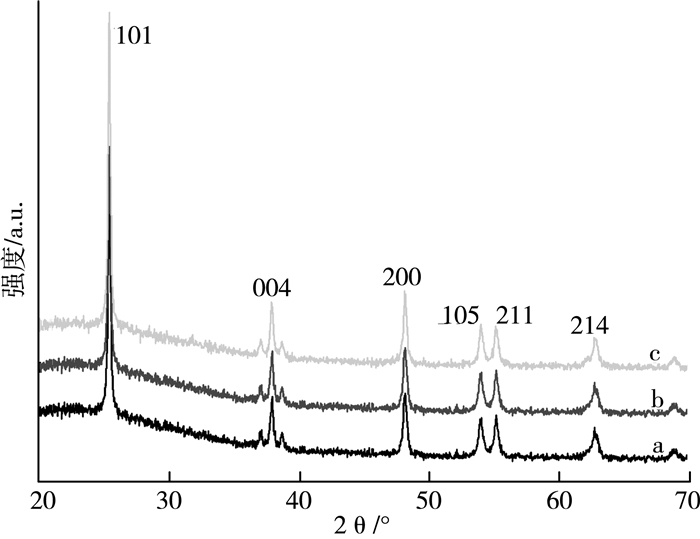 |
| 注:(a)SiO2/TiO2-1;(b)SiO2/TiO2-2;(c)SiO2/TiO2-3 图 4 不同样品的XRD图 |
如图所示:TiO2在25.8°、37.4°、47.9°、53.1°、55.5°和63.4°处存在明显的特征衍射峰,这些特征峰分别归属于TiO2的(101)、(004)、(200)、(105)、(211)和(204)特征峰,表明所有样品SiO2/TiO2-n中的TiO2为锐钛矿相。而且除了以上锐钛特征峰外,没有观察到其他特征峰,说明TiO2纳米粒子只存在锐钛矿相[18]。
2.1.4 N2吸附-脱附结果图 5是所有样品催化剂材料SiO2/TiO2-n的氮气吸附-脱附等温曲线图,插图为样品对应的孔径分布图,测试的相对压力范围为0.0~1.0。根据IUPAC分类,所有样品的氮气吸附-脱附等温曲线类型为Ⅰ和Ⅳ的结合型,具有较窄的孔径分布。而且从图中可以明显看出:所有样品均存在两个滞后环,相对压力较低时为H1型滞后环[19],表明存在长筒状介孔孔道;相对压力较高时为H3型滞后环[20],表明存在狭缝孔。从图 5的插图中可以看出:样品SiO2/TiO2-n的孔主要分布在介孔区域,少量分布在大孔区域;介孔主要来源于SiO2内部的有序孔道,以及高温热解去聚合物层后留下的孔隙;大孔主要是由粒子堆积[21]以及部分粒子间的二次堆积形成的[22-23]。
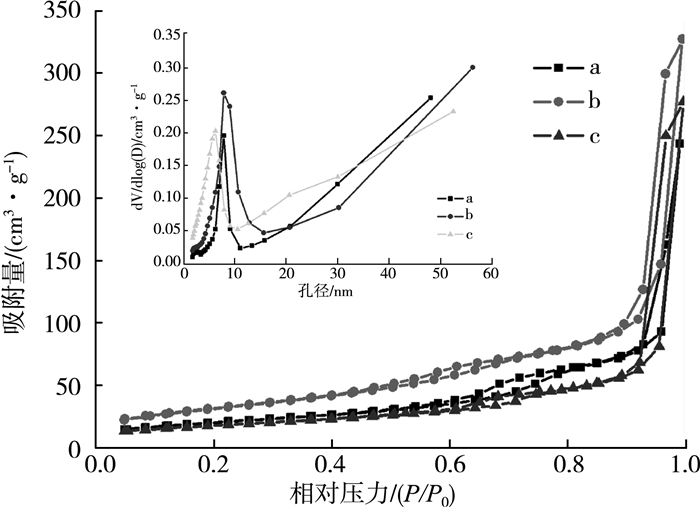 |
| 注:(a)SiO2/TiO2-1;(b)SiO2/TiO2-2;(c)SiO2/TiO2-3 图 5 不同样品的N2吸附-脱附等温线图和相应的孔径分布曲线图 |
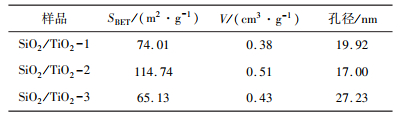
表 1列出的是所有催化剂样品介孔SiO2/TiO2-n的结构性质参数,包括比表面积(SBET)、孔体积(V)和孔径。通过对表中各个样品的结构参数进行比较,可以看出:相对于样品SiO2/TiO2-1和样品SiO2/TiO2-3,样品SiO2/TiO2-2具有较大的比表面积和孔体积,表明该样品具有更好的吸附性能。样品SiO2/TiO2-3的孔径与其他样品比较相对偏大,可能是因为表面的TiO2纳米粒子团聚现象严重、形成较多的堆积大孔所导致的。
| 表 1 催化剂样品介孔SiO2/TiO2-n的结构性质 |
 |
2.2 催化剂光催化降解甲基橙性能
为了测试所制备的催化剂样品SiO2/TiO2-n的催化效果,对染料甲基橙进行了光催化降解测试,所有样品光催化降解甲基橙的结果如图 6所示。在紫外灯照射之前,对所有SiO2/TiO2-n样品进行黑暗静置1 h,达到吸附平衡,此时大约有6%的甲基橙染料分子被吸附到介孔SiO2/TiO2表面。随着紫外灯照射时间的增加,甲基橙被催化降解,浓度降低,所有样品催化降解甲基橙的结果在3.5 h后趋于稳定。样品SiO2/TiO2-1、SiO2/TiO2-2和SiO2/TiO2-3在4.5 h后对甲基橙的最终降解率分别为92.5%、99.5%和82.6%。可以看出,样品SiO2/TiO2-2的催化效果明显优于其他两个样品,这主要与介孔SiO2表面的接枝效果有关。从图 3样品的TEM中可以看出:相对于其他两个样品,样品Si-E2表面接枝的聚合物较均匀、团聚少,所以使得钛源在其表面亲水链间水解,从而形成均一沉淀,减少了TiO2纳米粒子的团聚现象,有效增加了TiO2与染料甲基橙的接触面积,提高了光催化效率。
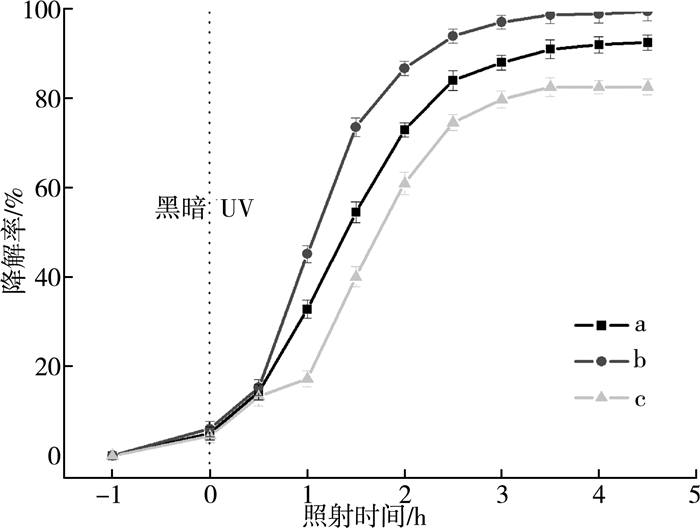 |
| 注:(a)SiO2/TiO2-1;(b)SiO2/TiO2-2;(c)SiO2/TiO2-3 图 6 不同样品对甲基橙降解率的影响 |
3 结论
通过ARGET ATRP方法对短棒状介孔SiO2进行改性,以接枝亲水性聚合物改性后的介孔SiO2为模板,使钛源TBT在亲水层间水解,最后制得介孔SiO2/TiO2复合材料。由于棒状介孔SiO2/TiO2复合材料具有较大的比表面积和良好的吸附性能,在光催化降解甲基橙实验中,可以有效提高光催化效率,从而表现出良好的光催化活性。
| [1] |
KRESGE C T, LEONOWICE M E, ROTH W J, et al. Ordered mesoporous molecular sieves sythesized by a liquid-crystal template mechanism[J]. Nature, 1992, 359(22): 710-712. |
| [2] |
YU F Q, TANG X D, PEI M S. Facile synthesis of PDMAEMA-coated hollow mesoporous silica nanoparticles and their pH-responsive controlled release[J]. Microporous and Mesoporous Materials, 2013, 173: 64-69. DOI:10.1016/j.micromeso.2013.02.012 |
| [3] |
SUN B, ZHOU G W, ZHANG H J. Synthesis, functionalization, and applications of morphology-controllable silica-based nanostructures:A review[J]. Progress in Solid State Chemistry, 2016, 44(1): 1-19. DOI:10.1016/j.progsolidstchem.2016.01.001 |
| [4] |
LEE D W, JIN M H, LEE C B, et al. Facile synthesis of mesoporous silica and titania supraparticles by a meniscus templating route on a superhydrophobic surface and their application to adsorbents[J]. Nanoscale, 2014, 6(7): 3483-3487. DOI:10.1039/c3nr05501a |
| [5] |
LI X, HONG C Y, PAN C Y. Preparation and characterization of hyperbranched polymer grafted mesoporous silica nanoparticles via self-condensing atom transfer radical vinyl polymerization[J]. Polymer, 2010, 51(1): 92-99. |
| [6] |
BHATTACHARYYA S, WANG H, DUCHEYNE P. Polymer-coated mesoporous silica nanoparticles for the controlled release of macromolecules[J]. Acta Biomaterialia, 2012, 8(9): 3429-3435. |
| [7] |
ZHANG Y Z, WANG Y, MATYJASZEWSKI K. ATRP of methyl acrylate with metallic zinc, magnesium, and iron as reducing agents and supplemental activators[J]. Macromolecules, 2011, 44(4): 683-685. DOI:10.1021/ma102492c |
| [8] |
CHEESMAN B T, WILLOTT J D, WEBBER G B, et al. pH-responsive brush-modified silica hybrids synthesized by surface-initiated ARGET ATRP[J]. ACS Macro Letters, 2012, 1(10): 1161-1165. DOI:10.1021/mz3003566 |
| [9] |
CAO L, MAN T, ZHUANG J Q, et al. Poly(N-isopropylacrylamide) and poly[J]. Journal of Materials Chemistry, 2012, 22(14): 6939-6946. DOI:10.1039/c2jm15251g |
| [10] |
LIU F F, ZHANG Y, ZHOU G W. Grafting pH-sensitive poly[J]. Micro & Nano Letters, 2015, 10(4): 187-191. |
| [11] |
JEON H, LEE C S, PATEL R, et al. Well-organized meso-macroporous TiO2/SiO2 film derived from amphiphilic rubbery comb copolymer[J]. ACS Applied Materials and Interfaces, 2015, 7(14): 7767-7775. |
| [12] |
WANG M G, HAN J, XIONG H X, et al. Nanostructured hybrid shells of r-GO/AuNP/m-TiO2 as highly active photocatalysts[J]. ACS Applied Materials & Interfaces, 2015, 7(12): 6909-6918. |
| [13] |
MA J, CHU J, QIANG L S, et al. Synthesis and structural characterization of novel visible photocatalyst Bi-TiO2/SBA-15 and its photocatalytic performance[J]. RSC Advances, 2012, 2(9): 3753-3758. |
| [14] |
ZHENG Y W, YU F T, ZHI L, et al. Hydrothermal synthesis and morphological evolution of mesoporous titania-silica[J]. Journal of Physical Chemistry C, 2009, 113(47): 20335-20348. DOI:10.1021/jp9037842 |
| [15] |
WITTE K D, BUSUIOC A M, MEYNEN V, et al. Influence of the synthesis parameters of TiO2-SBA-15 materials on the adsorption and photodegradation of rhodamine-6G[J]. Microporous and Mesoporous Materials, 2008, 110(1): 100-110. DOI:10.1016/j.micromeso.2007.09.035 |
| [16] |
DONG W Y, SUN Y J, LEE C W, et al. Controllable and repeatable synthesis of thermally stable anatase nanocrystal-silica composites with highly ordered hexagonal mesostructures[J]. Journal of The American Chemical Society, 2007, 129(45): 13894-13904. DOI:10.1021/ja073804o |
| [17] |
WANG C F, ZHOU G W, XU Y Q, et al. Porcine pancreatic lipase immobilized in amino-functionalized short rod-shaped mesoporous silica prepared using poly(ethylene glycol)and triblock copolymer as templates[J]. Journal of Physical Chemistry C, 2011, 115(45): 22191-22199. DOI:10.1021/jp206836v |
| [18] |
MICHAL K, BRUNO D, EWA B, et al. Synthesis of mesoporous carbons using ordered and disordered mesoporous silica templates and polyacrylonitrile as carbon precuror[J]. Jourmal of Physical Chemistry B, 2005, 109(19): 9225-9261. |
| [19] |
ZU G, SHEN J, WANG W, et al. Silica-titania composite aerogel photocatalysts by chemical liquid deposition of titanate onto nanoporous silica scaffolds[J]. ACS Applied Materials & Interfaces, 2015, 7(9): 5400-5409. |
| [20] |
LI X, JOHN V T, ZHAN J, et al. The synthesis of mesoporous TiO2/SiO2/Fe2O3 hybrid particles containing micelle-induced macropores through an aerosol based process[J]. Langmuir, ACS Journal of Surfaces & Colloids, 2011, 27(10): 6252-6259. |
| [21] |
ZHAO M N, ZHOU G W, ZHANG L, et al. Fabrication and photoactivity of a tunable-void SiO2-TiO2 core-shell structure on modified SiO2 nanospheres by grafting an amphiphilic diblock copolymer using ARGET ATRP[J]. Soft Matter, 2014, 10(8): 1110-1120. |
| [22] |
GAO K, ZHANG X M, FANG S, et al. Low-temperature synthesis and photocatalytic activity of TiO2 pillared montmorillonite[J]. Langmuir, ACS Journal of Surfaces & Colloids, 2008, 24(3): 1026-1030. |
| [23] |
LIU J, GU F, LI C Z. Flame synthesis of ball-in-shell structured TiO2 nanospheres[J]. Industrial & Engineering Chemistry Research, 2009, 48(2): 735-739. |
 2018, Vol. 32
2018, Vol. 32

