| 磁共振成像中影响组织弛豫时间的理论分析 |
2. 长治医学院 生物医学工程系, 山西, 长治 046000
2. Department of Biomedicine Engineering, Changzhi Medical College, Changzhi 046000, china
磁共振成像也是一种多参数成像,可形成不同参数下的图像对比度,如组织的纵向弛豫时间T1,横向弛豫时间T2,质子密度,弥散系数D等参数下的加权图像。一般来说,T1和T2反映组织自身特性的参数,是形成组织对比度的原因,但实际成像中,弛豫时间会受到环境因素的影响,如主磁场Bo的大小和均匀性,顺磁性分子的存在,温度T等。这些因素会影响到成像的质量如图像的对比度,分辨率,信噪比等。随着磁共振技术的发展,如超高场(大于3 T)磁共振设备的出现,磁共振成像造影剂研究,以及磁共振温度成像技术的应用等,这些设备和方法的出现,对于正确分析和评价图像质量提出更高的要求。
一般临床磁共振成像的研究中分析和着重讨论的是数据和结果,本文利用BPP弛豫理论,结合临床磁共振研究中的一些结果,对磁共振成像中影响组织驰豫时间的因素进行了讨论和解释,希望对磁共振成像技术的研究和进一步发展提供可参考的理论依据。
1 驰豫时间的物理意义人体中氢元素的含量很丰富,磁共振成像(MRI,Magnetic Resonance Imaging)利用了氢质子群在组织内的物理参数,如质子密度(PD),纵向弛豫时间T1,横向弛豫时间T2,以及弥散系数D等[1],所以磁共振成像是一种多参数成像,可以形成不同参数下的加权图像,如质子密度加权图像(PDWI),T1加权图像(T1WI)等。其中弛豫时间,反映的是经过射频脉冲作用后,组织中氢质子回到平衡状态下的快慢[2]。一般来说,流体有较长的T1(1500~2000 ms),脂肪类组织较短(100~150 ms),含水的组织介于期间。对于某个组织,T2通常比T1要短,流体具有较长的T2(700~1200 ms),含水组织T2比脂肪要长。正是由于不同组织的T1和T2的不同,它们对磁共振信号的贡献也有所不同,从而反映了组织的对比度,T1加权图像下,长的T1组织对应弱的信号,图像表现为暗区,短的T1组织对应强的信号,图像表现为中亮区,对T2加权图像来说正好相反[3]。
纵向弛豫,又称自旋晶格驰豫,当射频脉冲将质子系统从低能态激发到高能态时,系统吸收了能量。纵向驰豫的过程就是质子系统将吸收的能量释放到环境或晶格中的过程。晶格是固体核磁共振研究中的概念,但气体,液体中也有自旋晶格驰豫,所以晶格是个抽象的概念,一般指原子核周围的环境。由于核自旋周围存在原子,分子,离子等的振动以及转动,电子轨道运动和自旋运动,所以核自旋处于一个频率相位不断变化的电磁场中,电磁场的能量会诱发塞曼能级之间的跃迁,且向下(低能级)跃迁占优势,这会导致处于主磁场B0中的大量核自旋会产生一个沿着主磁场方向的宏观磁化强度矢量的出现,也是磁共振信号的来源。生物组织中的水通常归结为相对自由运动的水分子即游离水,以及与大分子紧密接触的结合水两大类。相比于游离水,结合水中水分子运动缓慢,核自旋更容易将能量高效地释放到周围环境中,从而具有较短的T1值[4]。
横向驰豫也称为自旋自旋驰豫,一般将它介绍为自旋核之间的相互作用,本质上说是自旋核处于略有不同的磁场环境中,从而有着不同的旋进频率,使得相位趋于分散,信号减弱。自旋自旋相互作用导致磁场环境不同只是可能的一种原因。常见的T2*加权图像,在梯度回波序列(GRE)中可以得到,反映的是主磁场不均匀以及自旋之间磁场干扰共同作用下的横向弛豫过程。
2 BPP弛豫理论及影响T1和T2的因素及分析驰豫时间是反映生物体组织本身特征的物理量。在磁共振成像中,在相同的主磁场下,不同的组织弛豫时间有所不同,从而形成组织的T1加权和T2加权图像。影响弛豫时间的物理机制是基于1948年(Bloembergen, Purcell and Pound)的BPP驰豫理论[5]。在这个理论中分子运动的概念被引入到驰豫的解释中,即每个原子或者分子都有转动、振动、平动等运动形式,这些运动的方向上是随机的,由于原子或分子的这种随机运动,运动状态在分子间的碰撞下也不断地改变着,而从一种运动状态到改变为另一种运动状态之间的时间间隔,被称为是相关时间。因为固体中分子之间相距很近,移动缓慢,有相对长的相关时间;而气体中相对分散的气体分子运动速度很快,相关时间较短。结合BPP弛豫理论,以下分别从温度,顺磁性造影剂以及主磁场大小这三个主要方面进行讨论。
2.1 温度在磁共振成像中,温度的变化会影响到很多参数,如共振频率,平衡状态下的磁化强度矢量,弛豫时间以及弥散系数等,其中,驰豫时间与温度的关系可以根据BPP驰豫理论中的“相关时间”的概念来解释。
用统计学的方法得到了不同相关时间的材料,或者组织运动频率统计结果[5]。如图 1所示,横坐标表示某个组织中分子原子运动的频率范围,纵坐标表示某个频率下的分子原子的相对数量的多少,即谱密度函数J(ω)。
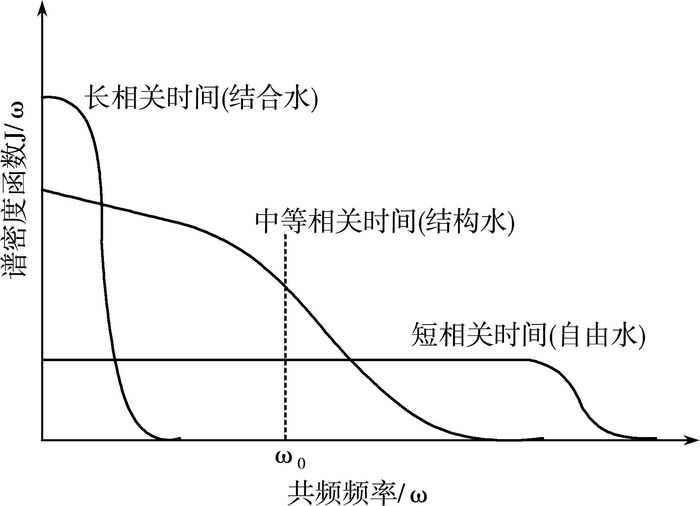 |
| 图 1 不同相关时间的组织的谱密度函数 |
谱密度函数中指出了具有短的相关时间的自由水,长相关时间的结合水以及介于两者之间的结构水这三种不同类型的组织的谱密度分布情况。间接说明了相关时间,分子运动频率与驰豫时间的关系。竖直虚线反映了临床磁共振成像的拉莫尔共振频率ω0下,不同组织中具有拉莫尔频率的分子原子的相对数量的多少。由图 1可知,结构水组织中含有ω0运动的原子分子较多,此时,氢质子容易与周围环境发生能量交换,将多余的能量更快地释放到周围环境中,导致T1减小,如脂肪组织相关时间介于自由水和结合水之间,原因是其中含有更多具有拉莫尔频率运动的分子原子,环境中电磁波频率为拉莫尔频率的成分较多,所以其T1值相对较短。
温度对T1的影响,可以利用BPP理论和谱密度函数进行解释。较高的温度加快了分子原子的运动,会使得相关时间变短,从谱密度函数中可知,此时氢质子周围环境中处于拉莫尔频率运动形式的分子原子相对较少,不利于能量交换,使得T1变长。
同样,影响T2的因素主要是磁场微环境的不均匀程度。由于自旋(磁矩)在不均匀磁场中会受到力的作用[6],即
在磁共振成像中,由于人体组织的温度一般在32°~37°之间,温度对弛豫时间影响不大。但在磁共振温度成像技术[7]如磁共振介入下的消融疗法[8],温度和驰豫时间的关系被更多的讨论。
2.2 顺磁性造影剂对组织驰豫时间的影响磁共振成像中,为了提高组织对比度,会引入造影剂,如超顺磁性氧化铁(SPIO)[9],通过缩短质子自旋-自旋横向驰豫时间(T2)以及有效横向驰豫时间(T2*)来增加病变组织和健康组织的对比度。人为改变组织中氢质子的驰豫时间从而得到更好的对比度图像,常见的对比剂是钆和铁氧化物,一个是顺磁性元素,一个是超顺磁性分子。引入到人体中的顺磁性分子,产生了与主磁场方向相同的磁场,等效于附加了不均匀的磁场,同时,顺磁性分子的运动包含了拉莫尔频率波段的磁场成分,有利于氢质子和顺磁性分子之间的能量交换,从而加快了氢质子向周围环境释放能量的效率,所以,顺磁性造影剂实际上减小了与其紧邻的氢质子的驰豫时间。
顺磁性分子对驰豫时间的影响可以用下面的公式来说明[5],
R1'=R1+r1C,R2'=R2+r2C
其中,R代表弛豫率(驰豫时间的倒数,R1=1/T1,R2=1/T2),R'表示的顺磁性分子对比剂环境下的弛豫率,下指标1和2分别表示纵向弛豫和横向弛豫过程。r1和r2为纵向和横向驰豫过程对应的系数,在钆对比剂下,它们大致相同,r1取4 mmol-1 s-1, r2取5 mmol-1 s-1,C为对比剂在人体内的分布浓度,单位mmol kg-1。不考虑其它影响,造影剂浓度C与驰豫时间的变化趋势如图 2所示。
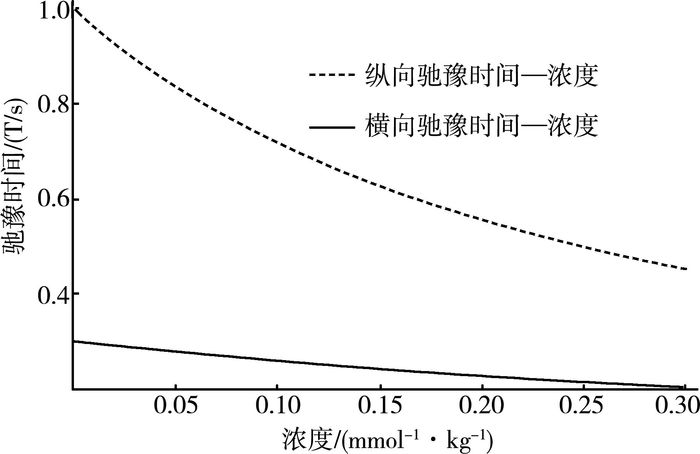 |
| 图 2 驰豫时间随着造影剂浓度的变化规律 |
可知,在造影剂浓度相同的环境中,T1和T2均减小,但相同浓度下T1和T2驰豫时间变化程度的不同,为有针对性地选择不同组织成像的对比度提供了条件。
2.3 主磁场B0对弛豫时间的影响2015年国内引入了当前最前沿的成像设备之一,具有自主屏蔽技术的7T磁共振设备,并在浙江大学正式启用。随着超高场磁共振设备的不断出现,主磁场对驰豫时间影响的讨论越来越广泛。如在3 T和7 T下,大脑皮层和髓质组织驰豫时间分别被测量[10],高场下纵向弛豫时间T1有所增加,T2减小,但这两个组织的驰豫时间变化程度不同。从理论上说,T1会随着主磁场强度的不同而不同,磁场强度增加,T1值也会增加。它们之间存在一个近似的数学关系[5]:
| ${{\rm{T}}_1} \propto {B_0}^{\rm{b}}$ |
其中B0为主磁场强度,b取0.3 ~ 0.4.而T2值一般随着B0的变化不明显,如纯水的T2值在高场和低场下相同。从BPP理论来讨论,从谱密度(图 1)中可以看到,当主磁场增加时,根据磁共振拉莫尔频率公式ω0=γB0可知,当提高主磁场B0时,对结构水来说,拉莫尔频率对应的谱密度减小,这意味着氢质子与周围环境能量交换过程效率降低,从而导致T1值增加,与实验中高场下T1的变化情况相符,而关于T2的变化,超高场(7.0 T)磁共振设备,相较于1.5 T和3 T设备,由于射频场的均匀性和主磁场的均匀性将会有所降低[11-12],客观上将导致横向弛豫过程加快,从而使T2值有所减小。
2.4 小结驰豫时间加权图像会随着不同的成像条件而有不同的效果,以上讨论是对单独考虑某个独立参数下驰豫时间变化的物理机制。除了以上考虑的环境温度,造影剂,主磁场之外,成像组织环境中弥散程度,扩散情况,流动质子,以及序列中的梯度场编码等会对磁共振成像的结果带来较大影响。
3 结论T1和T2作为反映生物体组织特性的两个参数,也是磁共振成像中最主要的两种加权图像。影响组织T1和T2的因素比较复杂,它们也将对磁共振信号和磁共振图像对比度,信噪比等带来较大影响。驰豫时间的大小首先与组织本身的物质组成有关,同时周围环境也会对其产生较大影响。如果从基本理论出发,可以部分合理地分析和解释驰豫时间的变化原因。本文结合已有的实验和临床数据,利用BPP理论和定量分析公式,从分子运动的观点部分解释了温度,对比剂和主磁场等外部因素对驰豫时间的影响,为不同环境和成像条件下的变化提供了理论依据。同时,正确理解人体组织弛豫现象的物理机制,对于分析和解释复杂情况下的磁共振成像有重要意义。
| [1] |
俎栋林. 核磁共振成像学[M]. 北京: 高等教育出版社, 2004.
|
| [2] |
BARBER D C. Webb's Physics of Medical Imaging(Second Edition), edited by M[J]. Flower.Contemporary Physics, 2014, 55: 142-143. DOI:10.1080/00107514.2014.885567 |
| [3] |
邱小红, 苏春秋, 马蔚吟, 等. 磁共振成像数据种类及其临床应用[J]. 实用医学影像杂志, 2014(6): 448-450. |
| [4] |
吉强. 医学影像物理学[M]. 北京: 人民卫生出版社, 2010, 86.
|
| [5] |
MEROBBIE D W, MOORE E A, GRAVES M J, et al. MRI, from Ricture to Proton[M]. Cambridge university Press, 2007.
|
| [6] |
佚名. 原子物理学[M]. 合肥: 中国科学技术大学出版社, 2015.
|
| [7] |
CLINE HE, HYNYNCN K, Hardy CJ, et al. MR temperature mapping of focused ultrasound surgery[J]. Magnetic Resonance in Medicine Official Journal of the Society of Magnetic Resonance in Medicine, 1994, 31(6): 628-636. DOI:10.1002/(ISSN)1522-2594 |
| [8] |
辜石勇. 超高场磁共振引导超声聚焦热消融的SAR安全研究[J]. 广州:南方医科大学, 2014, 1-3. |
| [9] |
殷敏. 磁性多壁碳纳米管的功能化修饰及在磁共振成像中的应用[J]. 上海:上海师范大学, 2010, 6-7. |
| [10] |
XIUFENG L, BOLAN P J, KAMIL U, et al. Measuring renal tissue relaxation times at 7 T[J]. Nmr in Biomedicine, 2015, 28(1): 63-69. |
| [11] |
杨保联. 超高场磁共振人体成像应用研究和医学前景[J]. 波谱学杂志, 2015(4): 707-714. DOI:10.11938/cjmr20150416 |
| [12] |
MCGOWAN J C. Basic Principles of Magnetic Resonance Imaging[J]. Neuroimaging Clinics of North America, 2008, 18(4): 623-636. DOI:10.1016/j.nic.2008.06.004 |
 2016, Vol. 30
2016, Vol. 30

