| 高铼酸铵热分解及其在银催化剂中的应用研究 |
金属铼因具有多种价态和复杂的配位方式,使其氧化物呈现出独特的物理化学性质。尤其是铼氧化物作为催化剂、催化助剂及催化载体,在有机合成、石油化工等方面有着广泛的应用[1-4]。环氧乙烷是乙烯工业衍生物中仅次于聚乙烯的大宗石油化工产品,除了用于乙二醇生产,还用于表面活性剂和医药等精细化工产品的制备。目前工业上环氧乙烷主要通过乙烯与氧气直接环氧化反应制得,银催化剂是唯一有效的催化剂,而其中铼助剂对提高催化剂的选择性至关重要。Dellamorte等[5-6]认为,铼能改变银颗粒的分布;采用先负载铼再负载银的分步浸渍方法,所得催化剂性能要优于共浸渍法。Yang等[7-10]认为,铼可使催化剂表面吸附氧的电子密度降低,进而提高EO的选择性。
Re的抗氧化能力较差,在空气中600 ℃即开始氧化并形成极易挥发的白烟状Re2O7;随着温度的上升,Re的氧化失重迅速增加。可能存在的Re氧化物大约有8种,但最为常见的氧化物有4种,即ReO4、Re2O7、ReO3和ReO2。铼是一种极其稀缺及分散的金属元素,其在地壳中的含量比所有的稀土元素都小,平均含量约为1 ppb。高铼酸铵是铼元素形成众多盐类化合物中的一种,也是工业应用最为广泛的铼化合物。
本工作以高铼酸铵为研究对象,考察其分解产物及形成温度,为银催化剂性能调控提供合适的铼助剂。采用TG-DSC、变温XRD对高铼酸铵的分解过程进行分析,在不同温度和气氛下对高铼酸铵进行热处理,并用XRF、XPS等方法表征焙烧产物。研究了热处理温度及气氛等条件对高铼酸铵分解过程的影响,提出了制备银催化剂中铼助剂的优化条件。
1 实验方法 1.1 实验材料高铼酸铵(NH4ReO4):纯度高于99.99%,购于国药集团化学试剂有限公司。
1.2 实验方法高铼酸铵焙烧实验1步骤如下:称量5 g NH4ReO4,将其放在坩埚中,放入气氛炉中通空气,控制升温速率为5 ℃/min,200 ℃下停留10 min。
高铼酸铵焙烧实验2步骤如下:称量5 g NH4ReO4,将其放在坩埚中,放入气氛炉中通空气,控制升温速率为5 ℃/min,400 ℃下停留10 min。
高铼酸铵焙烧实验3步骤如下:称量5 g NH4ReO4,将其放在坩埚中,放入气氛炉中通空气,控制升温速率为5 ℃/min,500 ℃下停留10 min。
高铼酸铵焙烧实验4步骤如下:称量5 g NH4ReO4,将其放在坩埚中,放入气氛炉中通氮气,控制升温速率为5 ℃/min,550 ℃下停留10 min。
1.3 测试仪器 1.3.1 TGA-DSC采用Mettler Toledo公司的TGA/DSC 1型同步热分析仪对试样进行TG和DSC表征,室温至700 ℃,空气气氛,升温速率为10 ℃ /min。
1.3.2 XPS采用Thermo Scientific公司的Escalab 250型X射线光电子能谱仪进行XPS表征,Al Kα射线,功率150 W。
1.3.3 XRD采用帕纳科公司的Empyrean型X射线衍射仪进行变温XRD表征,阳极靶为Cu靶,Pixcel 3D探测器,管压40 kV,管流40 mA。测试温度分别为:室温、30 ℃、210 ℃、240 ℃、270 ℃、300 ℃、330 ℃、360 ℃、400 ℃、30 ℃ (降温),升温速率5 ℃/min,每个温度停留1 min。
1.3.4 XRF采用荷兰帕纳科公司的PW4400/40型X射线荧光光谱仪进行XRF表征,75 μ超薄铍窗,超尖锐端窗铑靶X光管,功率4.0 kW,最大管流可达160 mA,最大管压60 kV。
2 结果与讨论 2.1 热分解铼是一种多价态的金属,其氧化物有8种,最常见的4种包括:ReO4、Re2O7、ReO3、ReO2。根据文献报道[11],高铼酸铵在360 ℃下发生热分解首先生成气态的Re2O7,更高温度下Re2O7可以继续氧化生成ReO4或者脱氧生成ReO3、ReO2甚至Re。ReO4、Re2O7、ReO3、ReO2的沸点分别为220 ℃、362 ℃、614 ℃、1363 ℃,可以看出高价铼氧化物相较于低价氧化物来说更容易挥发。控制反应体系中的氧浓度可以阻止反应(3) ~(6)的发生,从而在适宜的温度下得到所需的铼氧化物。
| $ 2{\rm{N}}{{\rm{H}}_4}{\rm{Re}}{{\rm{O}}_4} + \left( {3/2} \right){{\rm{O}}_2} = {\rm{R}}{{\rm{e}}_2}{{\rm{O}}_7}\left( {\rm{g}} \right) + 4{{\rm{H}}_2}{\rm{O}}\left( {\rm{g}} \right) + {{\rm{N}}_2}\left( {\rm{g}} \right) $ | (1) |
| $ {\rm{R}}{{\rm{e}}_2}{{\rm{O}}_7} + \left( {1/2} \right){{\rm{O}}_2}\left( {\rm{g}} \right) = 2{\rm{Re}}{{\rm{O}}_4} $ | (2) |
| $ {\rm{R}}{{\rm{e}}_2}{{\rm{O}}_7} = 2{\rm{Re}}{{\rm{O}}_3} + \left( {1/2} \right){{\rm{O}}_2}\left( {\rm{g}} \right)\left( {低于527^\circ {\rm{C}}} \right) $ | (3) |
| $ {\rm{R}}{{\rm{e}}_2}{{\rm{O}}_7} = 2{\rm{Re}}{{\rm{O}}_3} + \left( {2/3} \right){{\rm{O}}_2}\left( {\rm{g}} \right)\left( {高于527^\circ {\rm{C}}} \right) $ | (4) |
| $ {\rm{Re}}{{\rm{O}}_3} = 2{\rm{Re}}{{\rm{O}}_2} + \left( {1/2} \right){{\rm{O}}_2}\left( {\rm{g}} \right) $ | (5) |
| $ 2{\rm{Re}}{{\rm{O}}_2}{\rm{ = }}2{\rm{Re}} + 2{{\rm{O}}_2} $ | (6) |
高铼酸铵在空气下的DSC-TGA曲线分别如图 1所示。从图中可以看出:在空气中,NH4ReO4在360 ℃左右开始分解产生Re2O7,400 ℃时完全热解生成Re2O7气体,在350 ℃~500 ℃之间NH4ReO4有98%的重量损失,这与DSC曲线中400 ℃~500 ℃之间的放热峰一致,代表高铼酸铵分解产物的热失重。称重发现经过400 ℃热处理后高铼酸铵开始有部分重量损失,失重率为18.9%,经过500 ℃处理后所有物质都挥发了,失重率为100%,与热重分析结果吻合。
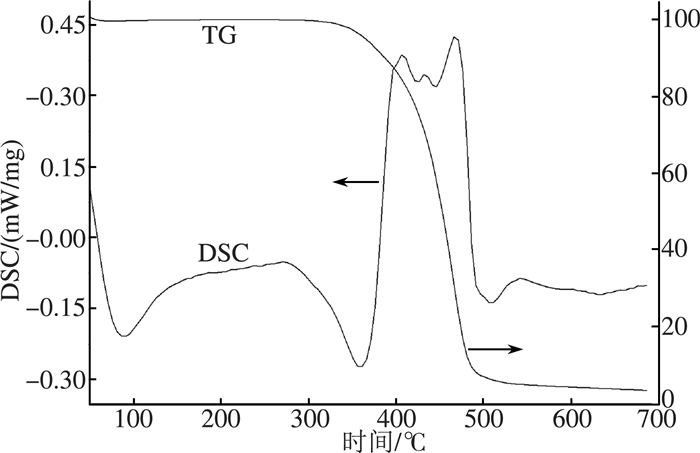 |
| 图 1 NH4ReO4的DSC-TG曲线 |
2.3 高铼酸铵变温XRD分析
在空气气氛下对高铼酸铵进行变温XRD分析(图 2)。从图中可以看出:温度达到210 ℃时开始有新物质生成;温度控制在300 ℃以内时,高铼酸铵还可以稳定存在,而当温度达到330 ℃时,已经没有高铼酸铵存在,而是形成了易挥发的Re2O7。由于变温XRD分析中样品很少,表现出的分解温度比DSC测试结果稍低。
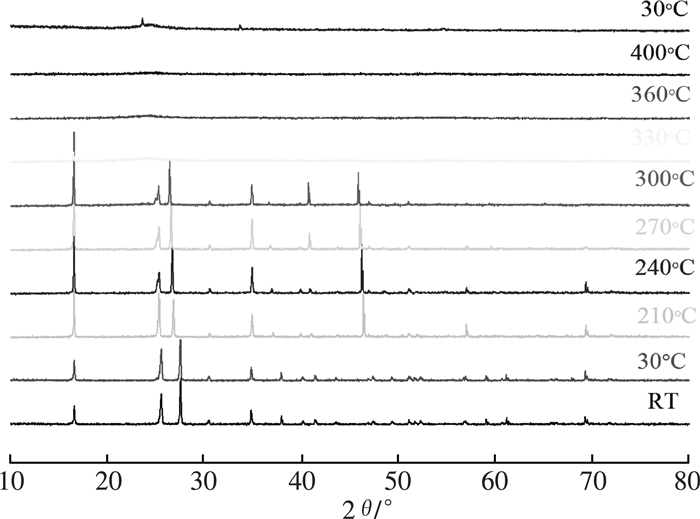 |
| 图 2 NH4ReO4的变温XRD图谱 |
2.4 焙烧实验 2.4.1 空气中焙烧
焙烧实验表明,空气中在较低温度下对高铼酸铵进行热处理时,样品表面变为灰白色,比较干燥;而当升高温度时,高铼酸铵样品变黑,变潮湿。说明焙烧过程中高铼酸铵发生了分解,生成了Re2O7和水等,与DSC-TG及变温XRD的结果一致。为了进一步验证分析结果,将焙烧产物进行了XRF分析,发现高铼酸铵焙烧产物中铼的含量增大,这是因为焙烧过程中部分产品分解挥发出水等小分子物质。
2.4.2 惰性气氛中焙烧采用XPS对NH4ReO4及其在惰性气氛中550 ℃焙烧1 h的产物进行了表征(图 3、图 4)。对比原料的XPS图谱,焙烧后多了一个峰,将45.75 eV位置的Re 4f7峰归于Re2O7,42.86 eV位置的Re 4f7峰归于ReO2。
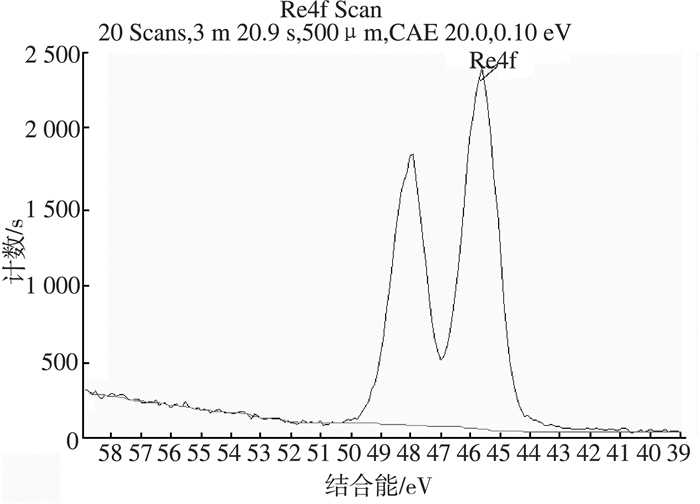 |
| 图 3 NH4ReO4的XPS图谱 |
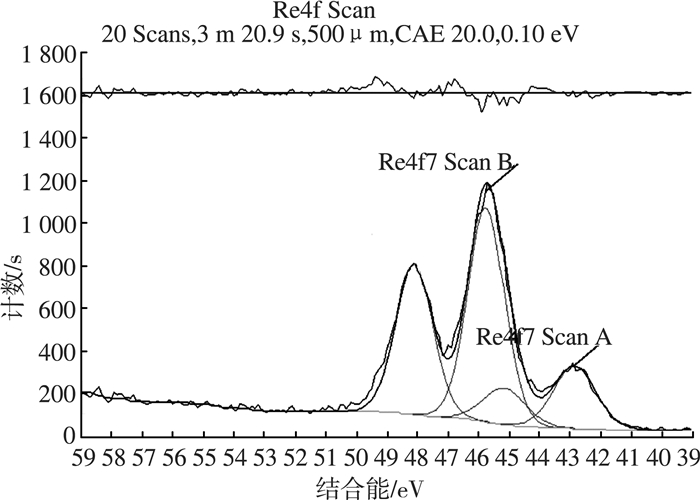 |
| 图 4 NH4ReO4焙烧产物的XPS图谱 |
2.5 高铼酸铵热分解在银催化剂制备中的应用
助剂铼对提高银催化剂的选择性至关重要。有文献报道七价的铼化合物能提高银的化合价,使活性银化合价升高,氧吸附在缺电子的银位点上将增加其亲电性能,更有利于与富含电子的碳碳双键作用生成环氧乙烷。
高铼酸铵活化产物主要受温度和气氛两种因素的影响。为了保留更多的高价铼化合物,活化温度宜选择330 ℃以下,以减少高价铼氧化物的分解及挥发损失。有文献计算了RexOy的氧势图,发现在400 ℃~1 000 ℃范围内,控制氧压超过1 013.25 Pa可以有效阻止Re2O7脱氧生成ReO3或ReO2。
3 结论在不同的气氛及温度下,高铼酸铵热分解可以生成ReO4、Re2O7、ReO3、ReO2和Re等产物。银催化剂中高价铼氧化物能够大大提高催化剂的选择性,可以通过控制温度和气氛的方法获得高价铼氧化物,活化温度宜选择330 ℃以下,活化气氛中氧压超过1 013.25 Pa。
| [1] |
AZZAMK G, BABICH I V, LEFFERTS L. Stable and efficient Pt-Re/TiO2 catalysts for water-gas-shift:On the effect of rhenium[J]. Chemcatchem, 2013, 5(2): 557-564. DOI:10.1002/cctc.201200492 |
| [2] |
SINGHB, SAIN B. Silica-immobilized highly dispersed oxo-rhenium and its catalytic activity for the direct synthesis of nitrones[J]. Chemcatchem, 2010, 2(10): 1260-1264. DOI:10.1002/cctc.201000121 |
| [3] |
KESSLER V G, SEISENBAEVA G A. Rhenium nanochemistry for catalyst preparation[J]. Minerals, 2012, 2(3): 244-257. DOI:10.3390/min2030244 |
| [4] |
GURYEV Y V, IVANOVA I I, LUNIN V V, et al. Characterization of metal segregation in Pt-Re/Al2O3 reforming catalysts[J]. Appl.Catal.A-Gen., 2007, 329: 16-21. DOI:10.1016/j.apcata.2007.06.015 |
| [5] |
DELLAMORTE J C, LAUTERBACH J, BARTEAU M A. Promoter-induced morphological changes of Ag catalysts for ethylene epoxidation[J]. Ind.Eng.Chem.Res., 2009, 48(12): 5943-5953. |
| [6] |
DELLAMORTE J C, LAUTERBACH J, BARTEAU M A. Effect of preparation conditions on Ag catalysts for ethylene epoxidation[J]. Top.Catal., 2010, 53(1-2): 13-18. DOI:10.1007/s11244-009-9440-9 |
| [7] |
任冬梅, 李建伟, 李金兵, 等. 铼前体对乙烯环氧化银催化剂性能的影响[J]. 石油化工, 2018, 47(2): 115-119. |
| [8] |
YANG JUN, DENG J F, YUAN X H. Rhenium as a promoter for ethylene epoxidation[J]. Appl.Catal.A, 1992, 92(2): 73-80. |
| [9] |
袁晓红, 张式, 杨军, 等. 乙烯环氧化反应中铼的助催化机理[J]. 石油化工, 1993(5): 293-298. |
| [10] |
DIAOW J, DIGIULIO C D. An investigation on the role of Re as a promoter in Ag-Cs-Re/a-Al2O3 high-selectivity ethylene epoxidation catalysts[J]. Journal of Catalysis, 2015, 322: 14-23. DOI:10.1016/j.jcat.2014.11.007 |
| [11] |
BAI M, ZHOU L J. Preparation of ultrafine rhenium powders by CVD hydrogen reduction of volatile rhenium oxides[J]. Trans.Nonferrous Met.Soc.China, 2013, 23(2): 538-542. DOI:10.1016/S1003-6326(13)62496-6 |
 2019, Vol. 33
2019, Vol. 33

