——
2. 中国农业科学院农业信息研究所;
3. 天津大学生物安全战略研究中心;
4. 天津大学化工学院
作为21世纪最受瞩目的新兴融合学科之一,合成生物学的相关理论、研发、应用引起了科学界和企业界的广泛关注。合成生物学在通过人为设计和建造新的基因组和生物体来解决医学、能源、环境、农业等问题方面展现出了巨大的发展潜力,为诸多瓶颈问题提供了全新的解决思路。此外,其他生物科学和工程技术的进步也加速了该领域的迅猛发展,比如第三代基因组测序和基因编辑等技术的突破性进展。合成生物学被广泛认为是21世纪的重要“颠覆性”技术,开启了第三次生物技术革命的序幕。近年来,合成生物学逐渐成为世界各国重点发展的新兴科学技术领域,甚至是综合国力的较量之处。
合成生物学作为典型的两用生物技术,风险与福祉同时存在。随着研究的不断深入,人们逐渐意识到了人工设计合成细胞和生物系统的复杂性与风险性。例如,基因驱动释放到自然界中会导致生物特定性状的消失,合成生物实验室中的微生物泄露到外部生态环境中会造成自然界的紊乱等。[1]针对上述合成生物学的生物安全风险,世界各国也相继设立了监管机构,出台了各种相关的政策与法规。中国一直以来十分重视生物风险与安全问题。2015年12月,在《禁止生物武器公约》缔约国会议基础上,中国提出了生物科学家行为准则范本。[2]2020年,中国出台了《中华人民共和国生物安全法》,为生物技术研发和应用监管提供了重要的法律依据,为合成生物学的健康安全发展制定了合理的法律框架。然而由于技术的快速发展,当前仍存在合成生物技术逃脱监管框架的情况。[3]已有文献对于合成生物技术快速发展过程中相关风险的研究尚显薄弱,为了保障合成生物学理论与技术应用持续、快速、科学地发展,亟需对风险类型开展系统性的研究梳理。
二、合成生物学发展现状在合成生物学前沿学术领域,基础研究成果大部分发表于国际著名学术期刊,本章基于Web of Science核心集,借助文献计量方法,依托SCI-E、SSCI、AHCI三大数据库,检索式请见附录,共检索出16831篇文献,时间跨度为1900年-2021年①。这一部分利用CiteSpace文献计量软件对合成生物学领域学科发展规模、脉络、研究热点等进行了定量化分析,为后续风险类型识别与分析奠定了基础。
对合成生物学研究主题以及相关学科领域进行聚类分析,我们得到了图1所示结果。合成生物学的相关研究主要分布在生物化学、分子生物学、生物技术与应用微生物学等领域。此外,合成生物学还与化学、细胞生物学、材料科学、遗传学、生物物理学等领域相互融合,呈现出了交叉学科的明显特点。

|
图 1 合成生物学研究相关学科领域知识图谱 |
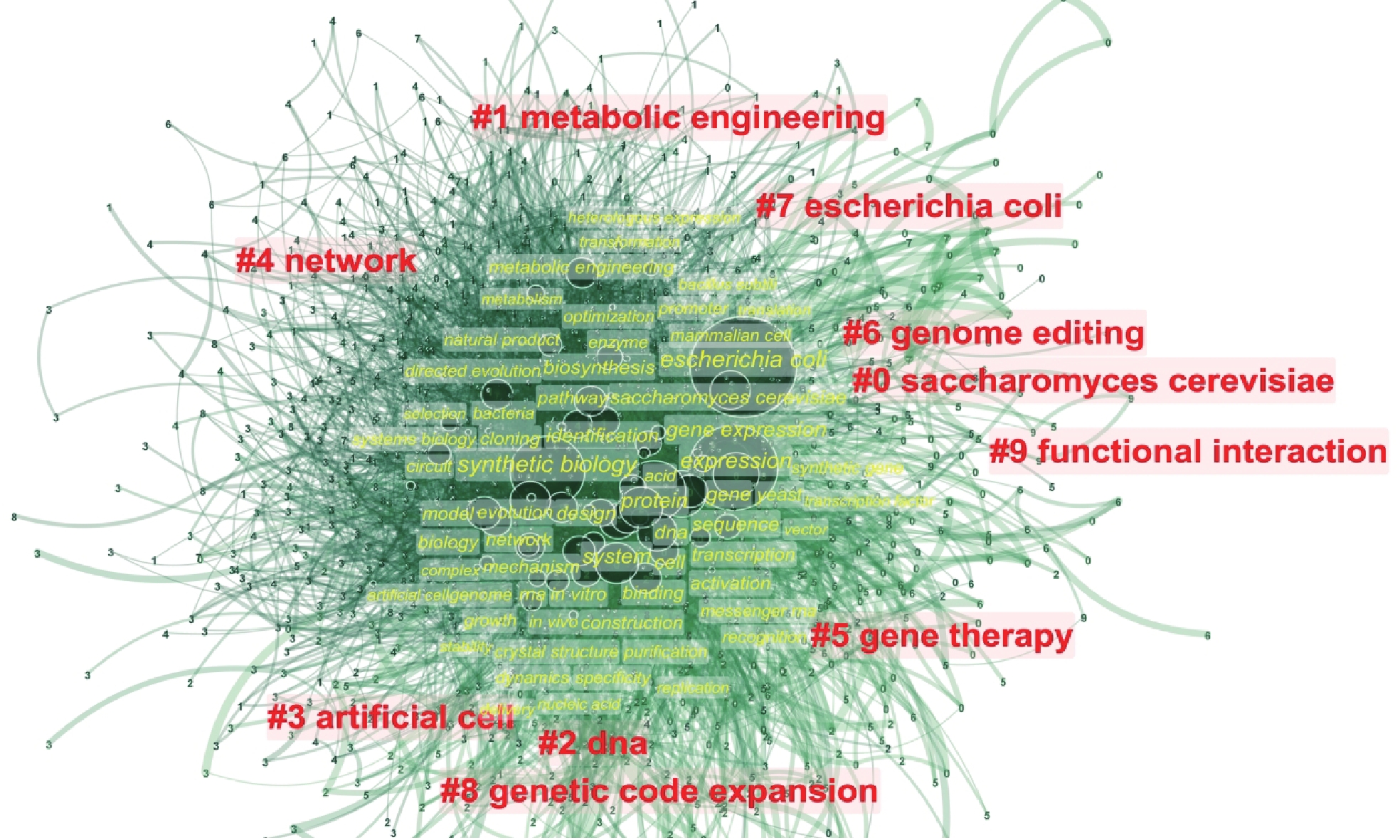
通过构建关键词共现图谱,我们发现大肠杆菌、蛋白质工程、基因表达、系统、酿酒酵母、设计等关键词的出现频率在100次以上。进一步将关联密切的关键字按照相关算法进行聚类整合,结果如图2所示。基于CiteSpace,本文所研究的文献数据关键词聚类分析的模块值(Q值)为0.4047(大于0.3),平均轮廓值(S值)为0.7034(达到0.7),表明聚类结构显著,且结果可信。[4]
|
图 2 合成生物学研究关键词聚类分析图谱 |
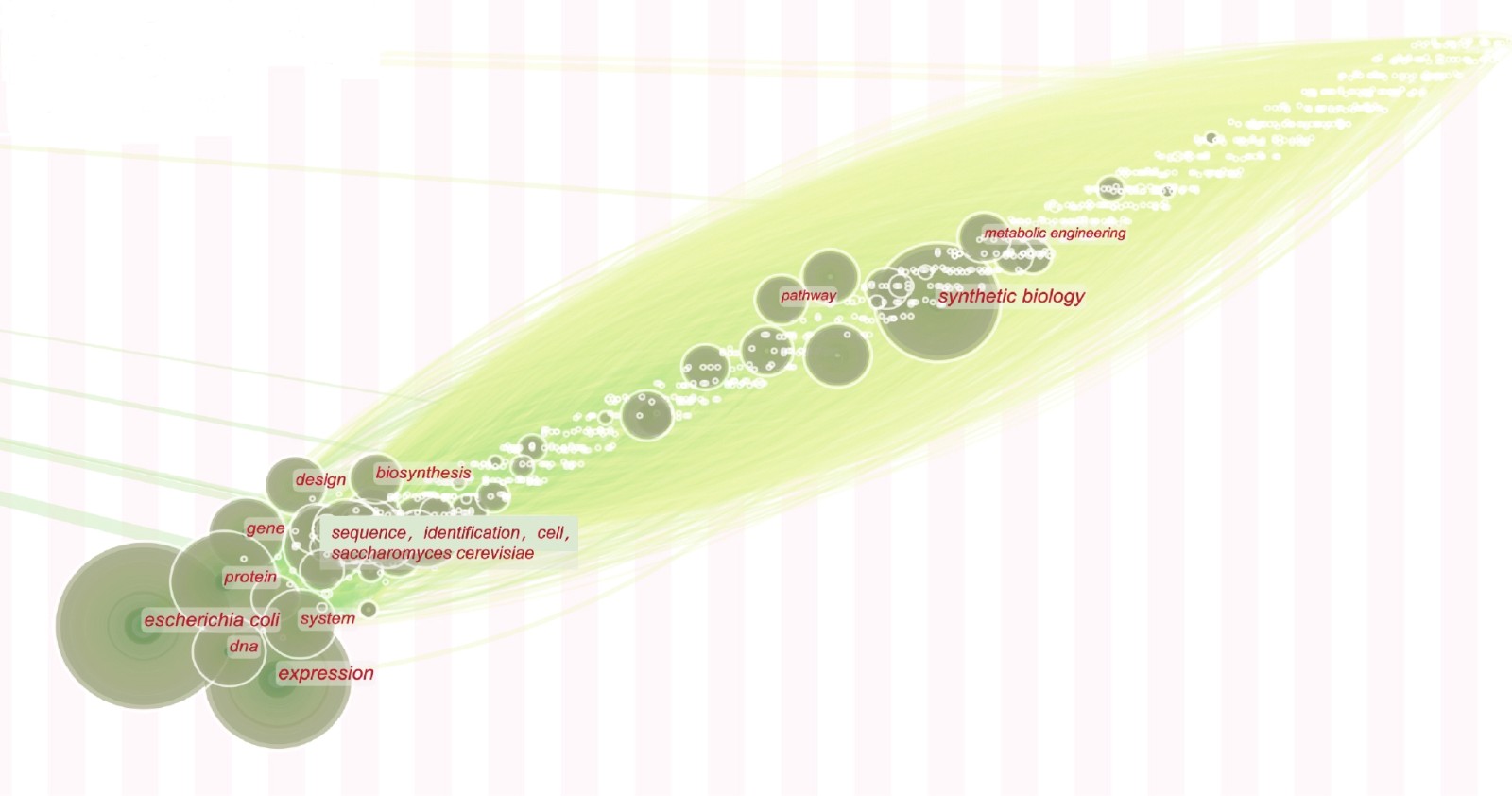
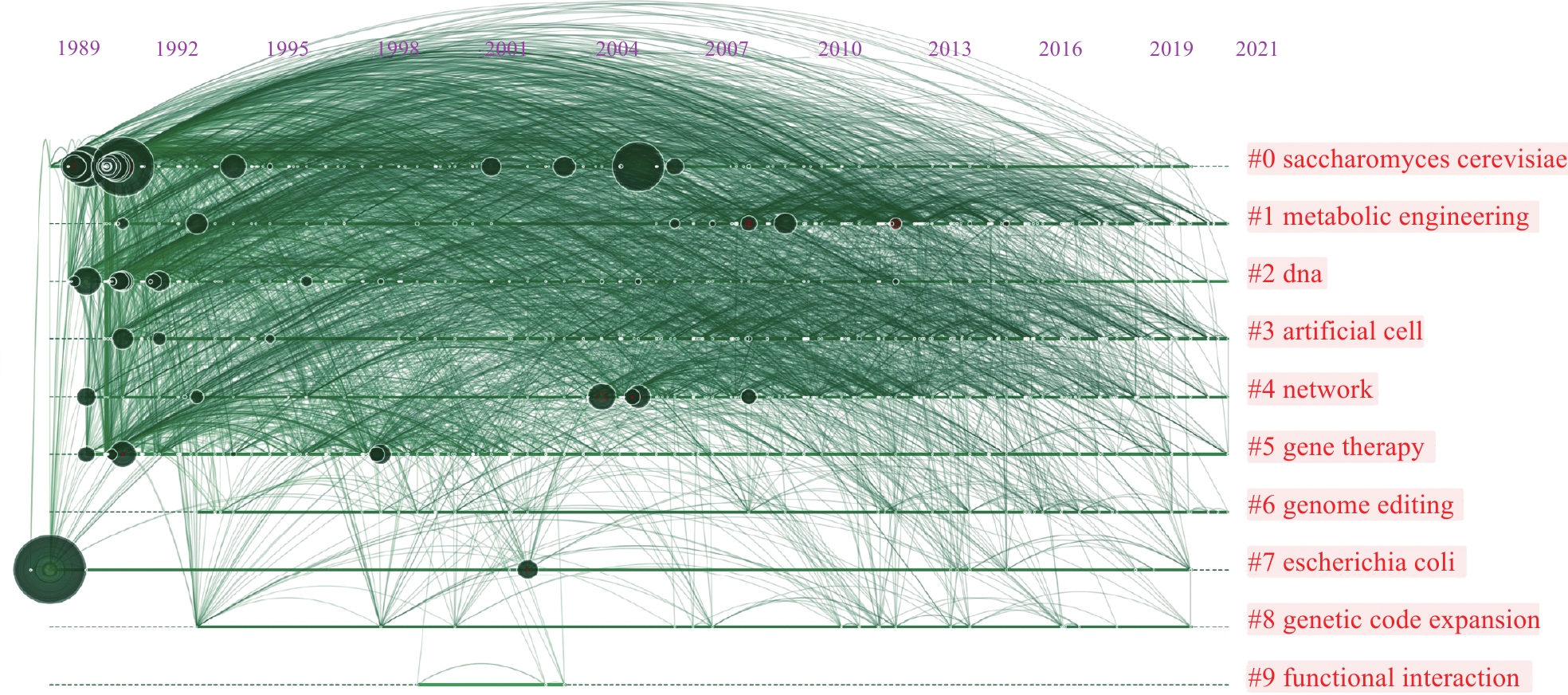
关键词时区视图展示了1928年—2021年不同阶段合成生物学领域的研究热点(图3)。之所以选择这一时段,是由于合成生物使能技术相关关键词可追溯至1928年。时间序列可视化图谱(图4)表明合成生物学发展初期(20世纪80年代末期至2005年)的相关研究主要集中在理论层面。图5展示了合成生物学领域引用次数最多的前25个突发词探测结果,即短时间内突然成为相应领域研究热点的关键词,突发词探测结果能够进一步揭示该领域的研究前沿。从图5可知,研究前沿主要包括聚合酶链反应、合成基因、净化、基因等。
|
图 3 合成生物学研究关键词时区图谱 |
|
图 4 合成生物学关键词聚类时间序列可视化图谱 |

|
图 5 合成生物学突发词检测结果 |
Meta分析是一种针对某个特定的科学问题或研究领域已有的同类研究成果、文献数据等进行系统汇总整合、类比分析、定量化评价的统计学方法,[5]常被用于系统性综述的定量分析。在16831篇文献的基础上,这部分增加了“risk”作为检索词,运用Meta分析和CiteSpace的方法,共筛选出了771篇与合成生物学风险相关的文章。同时,在中国知网检索并阅读部分相关文献后,研究人员另选择了3篇文献纳入本次研究。更进一步地,在审查了文章来源期刊级别,阅读了标题和摘要之后,剔除了与主题无关的论文,最终选择了来自Q2及以上期刊的88篇英文文献与3篇中文文献作为研究对象。
为了确保Meta分析的结果更加真实可靠,避免文献分析过程中出现真实情况与研究结果之间的误差。在数据分析前,研究人员从纳入Meta分析的文献中随机抽取了30篇,利用Cochrane风险评价软件对文献的选择性、实施、随访、测量、报告偏倚等进行了合理评估。文献综述类研究的选择偏倚与数据完整性主要是根据该研究综述中选择文献的方法、所涉及文献的主题、范围、数量等进行评估。结果评估偏倚的研究方法是判断其在文献筛选评估阶段是否由2名及以上研究人员进行初筛和复筛并确保意见一致。对于访谈和问卷类研究,选择偏倚和表现偏倚主要是通过评估研究对象的抽取随机性、类别全面性的方式判断的。此外,检测偏倚是评估数据的收集匿名性,磨损偏倚是评估数据统计的完整性。
按照表1的各项偏倚变量,本研究在Cochrane软件中对每篇文献各项可能的偏倚风险(risk of bias)进行了评级。
| 表 1 Cochrane文献偏倚评估变量[6] |
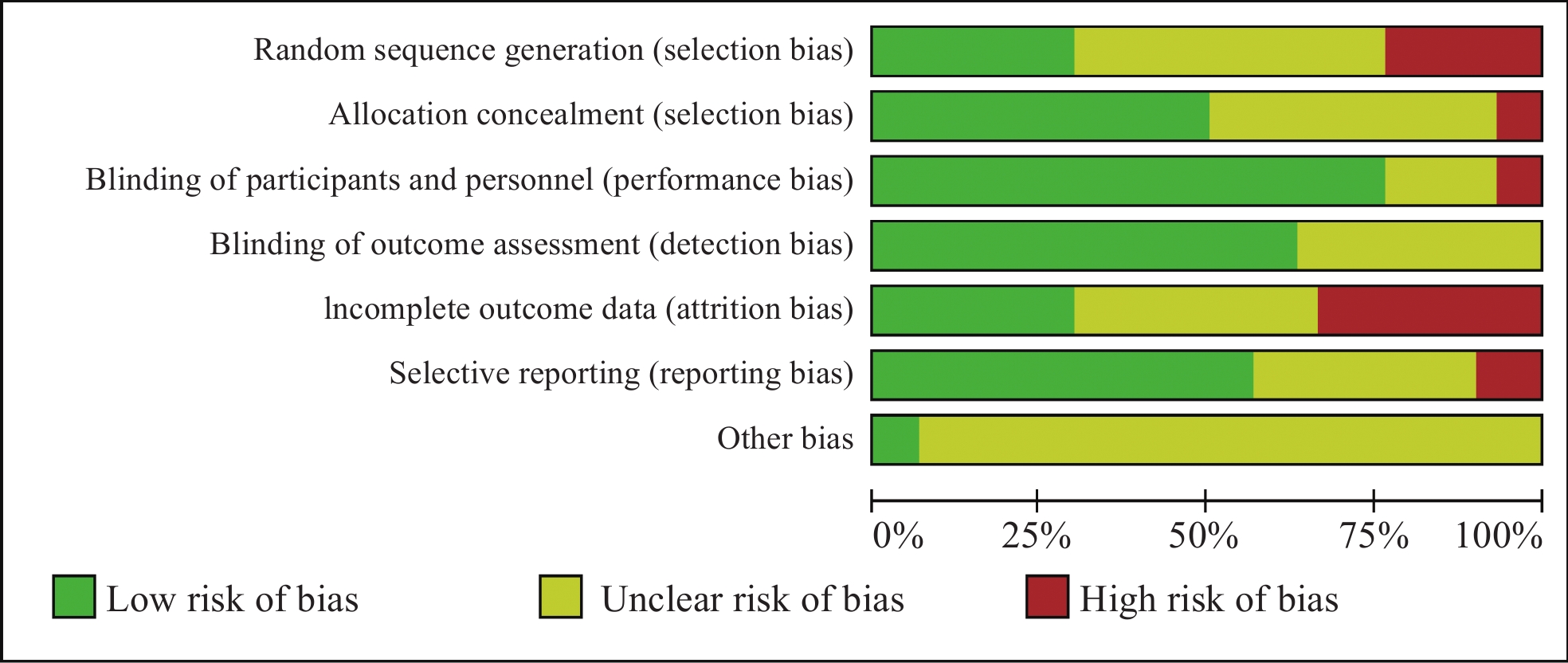
其中6项访谈类、问卷类、实验类研究均设置了随机分组与分配隐藏。另外3项文献综述类研究对文献数据选择的随机性或全面性进行了说明,因此在选择偏倚中属于低风险等级。同时,有7项研究因为倾向性的结论表现出了高选择偏倚风险。例如,一项关于老年人对合成生物技术态度的问卷调查类研究所选择的调查对象是来自瑞士苏黎世老年大学的86名老年人,他们是具有较高教育背景且对科学发展感兴趣的人群,因此在探索普通公众对于合成生物学的态度时存在选择偏倚。[7]已有文献数据的表现偏倚风险较低,24项研究均为低风险。本文选择的文献数据在实验结果评估盲化方面表现良好,有11项研究风险不明,其余均为低风险。但这些数据在数据完整性即磨损偏倚方面表现一般,主要原因是所选样本中文献综述类研究偏多,且定量分析型综述研究很少,难以保障其代表性。在选择性报道/报道偏倚方面,17项研究均强调了其研究内容和结论的真实性。通过上述分析,本文最终得到了文献偏倚风险图(图6)。结果显示,绝大多数文献属于低风险和不确定风险,高风险占比不高,本文选择样本的整体偏倚风险是可以接受的。
|
图 6 Meta分析文献偏倚风险图 |
在Meta分析中(如循证医学),研究问题的构建通常以PICOS原则为指导,PICOS原则由以下5个用于系统评价临床证据的指标组成:研究对象(Participants)、干预措施(Intervention)、比较措施(Comparison)、结局指标(Outcome)、研究类型(Study)。[8]对于一个明确的研究问题,通常会设计搜索策略来获取相关研究中的“P”、“I”和“S”,而“C”和“O”需要在筛选文献时整理。在本文的Meta分析中,结合合成生物学生物安全风险的实际研究问题,本研究将“PICOS原则”设定为:参考文献、风险类型关键词、风险类型详细解释、判断标准、研究类型/分析方法。根据此原则,本研究对最终样本的上述5部分内容进行了整理汇总,得到了相应的Meta分析数据来源表格。
四、Meta分析的结果在对从91篇文献中整理出来的合成生物学风险类型相关数据进行分析后,本文总结出了8类合成生物学生物安全相关风险点。基于风险主体,合成生物学生物安全相关风险可以从研究者、技术、管理者三个层面进行分类,如图7所示。涉及研究者的风险点主要可以归纳为“滥用风险”、“伦理问题”、“利益分配”三个部分,这一部分的风险主要是由于人的主观观念导致的。技术层面的风险点包括“合成生物学自身技术安全”、“人体伤害”、“意外泄漏/基因污染”,探讨的主要是合成生物技术本身特点所导致的风险。管理者层面的风险包括“缺乏监管”和“实验室生物安全”两个部分。

|
图 7 合成生物学风险类型 |
在总结出合成生物学相关风险类型的基础上,本研究对提取出来的具体风险点进行了分析。生物安全最早的定义来自于对微生物生物污染带来的安全问题的讨论。[9][10]随着合成生物学的不断发展,其定义逐渐演变为由于有害的合成生物制剂与生物体或环境之间发生的交互反应,而可能会给人体健康和生态环境等带来的风险(见表2)。[11]下文将对提取出来的风险点进行具体阐述。
| 表 2 合成生物学风险点类别总结 |
合成生物学的滥用/恶意使用的例子主要包括生物恐怖主义、生物武器、生物攻击以及非法生产毒品等,相关研究如表3所示。
| 表 3 合成生物学滥用风险相关研究梳理 |
在合成生物学的发展中,滥用被认为是一个日益增长的威胁。合成生物学的不断发展让人类对生命本质、致病性毒素的合成和传播等有了深入了解。相应的技术进步也使得人们可以更加容易地获得这些技术。这种潜在的恶意使用造成了“两用性困境”,可能给生态环境、公众生命健康,甚至国家安全带来严重后果。
合成生物学的滥用通常被定义为应受法律惩罚的非法活动,[14]可能会对个人或公众的健康产生直接的负面影响。随着合成生物学与各类信息技术的融合,我们可能无法快速地对可能产生的不良后果做出反应。DIY合成生物学的开源式知识共享使得任何人都能对病毒或细菌的基因组进行测序,甚至是使用廉价易用的设备来进行编辑和合成。技术的进步也可能会让人们找到跨越当前治理障碍的方法。[12]危险毒素和恶意使用制剂的可访问性也会越来越高。这对于环境和人类健康来说将是一个不可忽视的风险挑战。
合成生物学滥用的一个突出例子是生物恐怖主义。生物恐怖主义指的是将传播性强的病毒、病原体等制成生物制剂并进行散播,从而造成较大的公共卫生事故、生命财产损失或引起社会恐慌等。[16]生物恐怖主义和生物战的威胁并非空谈,基因编辑和合成生物学提高了出现生物恐怖分子的总体风险,合成生物学可能在无意中创造了生物武器,或为制造生物武器提供了新工具。[9]例如,利用合成生物学的理论和方法,军事和恐怖组织只需一种恶意病毒和一台过时的合成机器就能合成足够多的具有疫苗抵抗力的天花病毒来摧毁人类。此外,还有一些恐怖组织可能为了开展恐怖袭击而重新设计微生物或生命系统。[17]随着互联网的发展,信息的获取也变得更加容易。生物恐怖分子可能会利用互联网上的信息和生物黑客工具来制造合成病原体或产生毒素的有机体。[18]即使是普通人也可以通过互联网获取复杂的化学和生物材料。因此网络生物安全也是我们需要提防的一大威胁。
2. 合成生物学伦理争论风险合成生物学由“格物致知”向“造物致知”的跨越性转变引发了许多伦理方面的争论,相关研究如表4所示。人们对合成生物学的伦理担忧主要体现在人类会“篡夺上帝的角色”,[11]但又没有足够的能力来控制改造后的自然环境和生命。[15]此外,合成生物产品的市场化还应该考虑与现有物种重新设计相关的伦理问题,[17]这种担忧类似于转基因作物相关的生物安全担忧,如何在保证知情权的前提下促进产业化发展是亟需解决的问题。在应用领域,尊重患者和研究参与者的自主性是现代生命伦理学的核心。[19]如果没有向参与者提供有关临床试验和治疗手段的完整透明的信息,就违反了患者自主决策的伦理原则。临床试验参与者应充分了解实验的各种情况,然后自主决定是否参与合成生物学相关的药物或设备的人体实验研究。综上所述,与合成生物学相关的伦理风险主要体现在如何在实验、应用、产业化过程中保护人的自主性、尊严、公正。
| 表 4 合成生物学伦理争论风险相关研究梳理 |
随着合成生物学的不断发展,出现了利益分配的风险,比如,合成生物学领域的某些产品或应用的专利申请和潜在垄断会引起人们对相关知识和应用的获取可能会受到不公平待遇的担忧,[23]这些问题被归为正义和公平的主题,与社会和全球的利益和责任分配有关。除了分配本身,还有关于分配主体的问题探讨,相关研究如表5所示。
| 表 5 合成生物学利益分配风险相关研究梳理 |
公众会担忧合成生物学的使用是否会导致社会上的不公平分配,[26]是否以牺牲多数人的一般医疗保健为代价,只为享有特权的少数人提供昂贵的治疗?此外,这类专利和商业垄断也可能会对合成生物学的发展产生不利影响,阻碍其科学研究与创新。
与合成生物学有关的社会经济风险也可能发生。新的应用可能会对现有的供应链产生负面影响,原本的利益相关者可能会遭受打击,如利用合成酵母生产抗疟药物青蒿素可能有助于稳定药物供应并降低成本,但相关生产商如果不及时转型,就可能会因此而停产。[27]
4. 合成生物学自身技术安全性风险合成生物学作为一门新兴技术,近年来虽然取得了很大的突破,但是很多研究仍处在发展初期,难免存在技术不成熟和不确定等问题,相关研究如表6所示。
| 表 6 合成生物学自身安全性风险相关研究梳理 |
虽然合成生物学研究在动物实验方面进行得比较顺利,但在人体临床试验阶段(尤其是临床II、III期)仍比较少见,[32]正如公众对各类新兴技术的反应一样,他们对合成生物学等前沿生物技术的安全性和可靠性仍存在担忧。
一些运用生物信息学中保守性分析的基因型疾病治疗方法,尽管研究结果较好,但不同地区基因型患病率差异等问题仍待分析解决。[28]现阶段,从实验室和动物实验到人类的临床前数据的推进仍然十分有限,首次人体实验参与者可能有各种不良反应。[33]因此,很多法规和学术研究都使用“风险”和“风险因素”来描述临床研究中对人类受试者的潜在伤害。此外,基因改造也带来了新的不确定性和风险,如水平基因转移问题。[30]因为哺乳动物系统的复杂性,对其进行基因编辑可能会带来插入性诱变的风险。尤其在农业领域,公众对来自合成生物体的新型食品或成分对人类健康长期影响的不确定性表示担忧,例如担心过敏性的增加。[34]
作为合成生物学风险评估的一部分,学术界也会对异种生物学的生物安全进行审查,如异种生物产生的新分子的毒性、过敏性、致病性,以及对环境的潜在影响,包括生态环境的竞争力和水平基因转移的程度等。[35]
5. 合成生物学可能造成人体伤害风险研究合成生物学中基因编辑技术的初衷主要是为了解决人类遗传疾病的问题,但在没有适当的伦理和生物安全评估的情况下对人类胚胎进行基因编辑会引起严重的生物安全问题。合成生物学还可能会给从事相关研究工作的实验人员带来安全性风险,[36]给利用合成生物学技术进行治疗的患者带来不良反应的风险,以及因逃逸或意外释放到环境中的合成生物体而给公共卫生带来的风险等,[25]相关研究如表7所示。
| 表 7 合成生物学可能造成人体伤害风险相关研究梳理 |
对于基于合成生物学进行设计改造合成的微生物,我们目前仍不清楚它们的环境入侵能力和进化潜力。它们在自然进化和环境压力下,出现反向突变或其他意想不到的不良后果可能是不可避免的,相关研究如表8所示。自20世纪70年代以来,科学家和公众一直对意外释放的转基因生物可能会对环境造成的不良影响表示担忧。具有大量基因修饰的生物体一旦被释放,可能会造成基因污染,[39]对人类、动物、环境造成间接和不可逆转的影响,如对生物多样性的威胁和水平基因转移问题等。
| 表 8 合成生物学意外泄漏风险相关研究梳理 |
转基因生物的有意或无意释放存在很多潜在的负面后果,造成的非法入侵将改变现有的生态系统。如果它们与野生近亲生物交换遗传物质,[41]可能会改变现有的生物多样性,可能会降低自然界现有生物的生存能力,可能会超越甚至取代现有物种,进而减少种群规模,给生物多样性带来负面后果。合成微生物或植物的释放可能会通过影响其他自然物种的方式对环境产生不利影响,并在进入食品系统后对人体健康造成负面影响。[42]
合成生物学产品的许多环境风险已被确认,并在讨论合成生物学风险的文献中被提及,包括增加自身毒性和目标宿主范围,通过合成基因改变性别比降低繁殖能力或与本地生物形成竞争而影响生物多样性,[43]作为病原体的宿主帮助有害生物生产有毒化合物,以及破坏地球化学循环、基本营养源或食物网等。[44]这些风险值得我们加以注意与防护。
7. 合成生物学监管风险对于合成生物学的基因编辑、代谢工程等新技术会给人类健康或生态环境带来伤害的可能性,现阶段仍然缺乏充分的风险评估与监管措施。像很多前沿领域一样,合成生物学的发展与相应法律、伦理、风险监管之间的差距越来越大,学术界将这种差距称为“步调问题”,[45]相关研究如表9所示。
| 表 9 合成生物学监管风险相关研究梳理 |
传统的监督治理机制不足以应对新兴研究领域带来的新问题。新兴生物和化学技术公司的数量正在经历爆炸式增长,即使是在发达国家,监管机构也很难做到完全跟踪和控制两用合成生物学材料和技术交易的泛滥,[47]很多新技术已经超出了政府的监管能力范围。如果想要达成具有多国或全球共识的有关合成生物学相关监管控制的多边条约,可能需要许多国家进行数年的谈判。此外,政策本身也可能存在局限性。[48]这些监管漏洞可能导致双重用途困境或对人类健康或环境造成意外损害。
8. 合成生物学实验室生物安全风险“实验室生物安全”一词通常是指与病原体、转基因生物或病原体生物实验室相关的安全问题,相关研究如表10所示。例如,对病原体的研究会给研究人员、实验室附近的居民以及环境带来一些难以预料的意外风险,如有关高风险病毒和病原体的实验操作处理不当或意外泄漏,可能会带来接触风险。[49]合成生物学研究复杂性和规模的不断增加,为传统的实验设备风险防护带来了新的挑战和风险。[50]
| 表 10 合成生物学实验室生物安全风险相关研究梳理 |
合成生物学以其独特的融合学科优势与发展潜力,在生物医疗、化合物合成、环境检测与修复、新能源等众多应用领域取得了突破性进展,能够为许多处在瓶颈期的传统行业提供难得的快速转型解决方案,有着良好的发展前景。合成生物学作为典型的两用生物技术,需要面对因为滥用困境和早期技术发展不成熟所带来的一系列风险。但是,合成生物学工程化和快速产业化的特点,带来了动态监管机制不匹配、利益分配不公平等新型风险问题。并且,合成生物学本身在深入探索生命本质和设计合成新生命系统方面具有的较大潜力,使得合成生物学在合成有毒病原体、制造生物武器、生产非法毒品、非法改造生命等方面具有“先天优势”,以至于出现病原体意外泄露、生物恐怖主义等重大生物事故风险的概率较大。因此,本研究针对上述可能的风险,从研究者、技术本身、管理者三个角度提出了相应的对策。
首先,针对研究者,由于其可能导致滥用风险和伦理问题,因此需要从学术共同体的角度设计统一的道德伦理与专业素养标准,形成统一的规范与共识,如在研究与应用中进行全面的风险类型识别与评估,进一步完善操作和应用的规范化文件、制度,确保行动和责任落实到位。当前国际学术界正在积极开展相关道德伦理文件的制定,我国科学家也积极参与了生物安全治理,比如从2021年开始,天津大学与美国约翰·霍普金斯大学、国际科学院组织(IAP)共同撰写《生物安全科学家行为准则天津指南》,作为首个由我国发起,以我国地名命名的生物类国际倡议,它受到了广泛的国际关注。2022年9月《生物安全科学家行为准则天津指南》被世界卫生组织列为全球生物安全道德准则和高级别原则,为合成生物学全球治理提供方案。
其次,针对合成生物学技术,建议提高对新分子毒性、过敏性、致病性的识别能力,开展针对具体问题(如逃逸到环境中的合成生物体)的研究。同时还可以研发科研管理系统实现科研精准化管理,确保各实验流程安全有序进行,及时发现失误,减少损害。优化完善新兴科技研究的落地标准,以减少新方案、新产物等在使用过程中可能出现的不确定性风险。对于合成生物学技术需要制定如《生物安全法》对于重要生物资源数据统计的相关风险监管对象清单。
最后,针对管理者,监管政策与法规的制定应该跟上科技发展的脚步。从治理的角度来看,针对本文分析的不同类型的风险应制定不同的制度,针对恶意滥用、伦理、意外泄漏、网络生物信息安全等风险类型应制定对应的监管措施。如对于政府监管机构和相关管理者应开展定期的两用生物技术培训与再教育,加强管理者和科研人员之间的联系,做到知识共享,从而大幅度降低合成生物学相关风险。鼓励使用数字化技术,构建数字化管理平台,加强管理者与科研人员之间的互动,做到跨专业、跨行业的交流。
| 附录 |
① 考虑到研究的严谨性,纳入了合成生物早期观点和思想脉络。
| [1] |
Wang F., Zhang W. Synthetic Biology:Recent Progress, Biosafety and Biosecurity Concerns, and Possible Solutions.
Journal of Biosafety and Biosecurity, 2019, 1(1): 22-30.
DOI: 10.1016/j.jobb.2018.12.003. |
| [2] |
Sun T., Song J., Wang M., Zhao C., Zhang W. Challenges and Recent Progress in the Governance of Biosecurity Risks in the Era of Synthetic Biology.
Journal of Biosafety and Biosecurity, 2022, 4(1): 59-67.
DOI: 10.1016/j.jobb.2022.02.002. |
| [3] |
马诗雯, 王国豫. 如何应对合成生物学的不确定性——《合成生物学的监管: 生物砖, 生物朋克与生物企业》评介.
科学与社会, 2019, 9(3): 124-136.
|
| [4] |
李杰, 陈超美. citespace科技文本挖掘及可视化. 北京: 首都经济贸易大学出版社, 2016.
|
| [5] |
Gurevitch H. Design and Analysis of Ecological Experiment. Meta-analysis: Combining the Results of Independent Experiments. New York: Chapman and Hall, 1993 : 1–21.
|
| [6] |
谷鸿秋, 王杨, 李卫. Cochrane偏倚风险评估工具在随机对照研究Meta分析中的应用.
中国循环杂志, 2014, 29(2): 147-148.
DOI: 10.3969/j.issn.1000-3614.2014.02.017. |
| [7] |
Ineichen C., Biller-Andorno N., Deplazes-Zemp A. Between Fascination and Concern: An Exploratory Study of Senior Citizens’ Attitudes towards Synthetic Biology and Agricultural Biotechnology.
Universal Access in the Information Society, 2021, (20): 391-404.
|
| [8] |
胡良平. 科研设计与统计分析. 北京: 军事医学科学出版社, 2012.
|
| [9] |
Gregorowius D., Deplazes-Zemp A. Societal Impact of Synthetic Biology: Responsible Research and Innovation (RRI).
Essays In Biochemistry, 2016, 60(4): 371-379.
DOI: 10.1042/EBC20160039. |
| [10] |
Ahteensuu Marko. Synthetic Biology, Genome Editing, and the Risk of Bioterrorism.
Science and Engineering Ethics, 2017, 23(6): 1541-1561.
DOI: 10.1007/s11948-016-9868-9. |
| [11] |
Douglas T., Savulescu J. Synthetic Biology and the Ethics of Knowledge.
Journal of Medical Ethics, 2010, 36(11): 687-693.
DOI: 10.1136/jme.2010.038232. |
| [12] |
Howard J., Murashov V., Schulte P. Synthetic Biology and Occupational Risk.
Journal of Occupational & Environmental Hygiene, 2017, 14(3): 224-236.
|
| [13] |
Elgabry M., Nesbeth D., Johnson S. D. A Systematic Review of the Criminogenic Potential of Synthetic Biology and Routes to Future Crime Prevention.
Frontiers in Bioengineering and Biotechnology, 2020, (8): 571672.
|
| [14] |
Gómez-Tatay L., Hernández-Andreu J. M. Biosafety and Biosecurity in Synthetic Biology: A Review.
Critical Reviews in Environmental Science and Technology, 2019, 49(17): 1587-1621.
DOI: 10.1080/10643389.2019.1579628. |
| [15] |
李真真, 董永亮, 高旖蔚. 设计生命: 合成生物学的安全风险与伦理挑战.
中国科学院院刊, 2018, 33(11): 1269-1276.
|
| [16] |
Dieuliis D., Giordano J. Why Gene Editors Like CRISPR/Cas May Be a Game-Changer for Neuroweapons.
Health Security, 2017, 15(3): 296-302: 296.
DOI: 10.1089/hs.2016.0120. |
| [17] |
Serrano L. Synthetic Biology: Promises and Challenges.
Molecular Systems Biology, 2014, (3): 158.
|
| [18] |
Blockus H., Ahteensuu, M. Biohacking and Citizen Engagement with Science and Technology.
Finland:Turun Yliopisto, 2016, : 1-277.
|
| [19] |
Rakic M. , Wienand I., Shaw, D. , et al. Autonomy and Fear of Synthetic Biology: How Can Patients' Autonomy Be Enhanced in the Field of Synthetic Biology? A Qualitative Study with Stable Patients.
Science & Engineering Ethics, 2017, 23(2): 375-388.
|
| [20] |
Thiel V. Synthetic Viruses—Anything New?.
PLoS Pathogens, 2018, 14(10): e1007019.
|
| [21] |
Trump B. D., Cegan J. C., Wells, E., Keisler, J., Linkov, I. A Critical Juncture for Synthetic Biology.
EMBO Reports, 2018, 19(7): e46153.
|
| [22] |
梁慧刚, 黄翠, 宋冬林等. 合成生物学研究和应用的生物安全问题.
科技导报, 2016, 34(2): 307-312.
|
| [23] |
Bubela T., Hagen G., Einsiedel E. Synthetic Biology Confronts Publics and Policy Makers:Challenges for Communication, Regulation and Commercialization.
Trends in Biotechnology, 2012, 30(3): 132-137.
DOI: 10.1016/j.tibtech.2011.10.003. |
| [24] |
Schmidt M., Ganguli-Mitra A., Torgersen, H., Kelle, A., Deplazes, A., Biller- Andorno, N. A Priority Paper for the Societal and Ethical Aspects of Synthetic Biology.
Systems and synthetic biology, 2009, 3(1): 3-7.
|
| [25] |
Kaebnick G. E., Gusmano M. K., Murray T.H. The Ethics of Synthetic Biology:Next Steps and Prior Questions.
Hastings Center Report, 2014, 44(S5): S4.
DOI: 10.1002/hast.392. |
| [26] |
Smith K. Synthetic Biology: A Utilitarian Perspective.
Bioethics, 2013, 27(8): 453-463.
DOI: 10.1111/bioe.12050. |
| [27] |
Shan J. A., Bc,A., Sk, A., et al. Synthetic Biology Applied in the Agrifood Sector: Public Perceptions, Attitudes and Implications for Future Studies.
Trends in Food Science & Technology, 2019, (91): 454-466.
|
| [28] |
Hancock G., Blight J., Lopez-Camacho C., et al. A Multi-genotype Therapeutic Human Papillomavirus Vaccine Elicits Potent T Cell Responses to Conserved Regions of Early Proteins.
Scientific Reports, 2019, 9(1): 18713.
DOI: 10.1038/s41598-019-55014-z. |
| [29] |
George A. M. The National Security Implications of Cyberbiosecurity.
Frontiers in Bioengineering and Biotechnology, 2019, (7): 51.
|
| [30] |
Vallero D. A., Gunsch C. K. Applications and Implications of Emerging Biotechnologies in Environmental Engineering.
Journal of Environmental Engineering, 2020, 146(6): 03120005.
DOI: 10.1061/(ASCE)EE.1943-7870.0001676. |
| [31] |
Schmidt M., Pei L., Budisa N.. Xenobiology: State-of-the-art, Ethics, and Philosophy of New-to-nature Organisms.
Advances in Biochemical Engineering/Biotechnology, 2020, (162): 301-315.
|
| [32] |
Ruder W. C., Lu T., Collins J. J. Synthetic Biology Moving into the Clinic.
Science, 2011, 333(6047): 1248.
DOI: 10.1126/science.1206843. |
| [33] |
Genske A., Engel-Glatter S. Rethinking Risk Assessment for Emerging Technology First-in-human Trials.
Medicine, Health Care and Philosophy, 2016, 19(1): 125-139.
DOI: 10.1007/s11019-015-9660-7. |
| [34] |
Putten M., Frewer L. J. , Gilissen L. , et al. Novel Foods and Food Allergies:A Review of the Issues.
Trends in Food Science & Technology, 2006, 17(6): 289-299.
|
| [35] |
König H., Dorado-Morales P., Porcar M. Responsibility and Intellectual Property in Synthetic Biology.
EMBO Reports, 2015, (16): 1055-1059.
|
| [36] |
欧亚昆, 雷瑞鹏. 伦理视域中合成生物学的利益与风险评价.
伦理学研究, 2016(2): 95-102.
DOI: 10.15995/j.cnki.llxyj.2016.02.017. |
| [37] |
Pacheco-Soares T., de Oliveira Carvalho, A., da Silva Araújo, J., de Souza, G., Machado, O. A Modified, Hypoallergenic Variant of the Ricinus Communis Ric c1 Protein Retains Biological Activity.
Bioscience Reports, 2018, 38(2): BSR20171245.
|
| [38] |
Hayes K. R., Hosack G. R., Dana G. V., Foster S. D., Ford, J. H., Thresher, R., et al. Identifying and Detecting Potentially Adverse Ecological Outcomes Associated with the Release of Gene-drive Modified Organisms.
Journal of Responsible Innovation, 2018, 5(sup1): S139-S158.
|
| [39] |
Herdewijn P., Marlière P. Toward Safe Genetically Modified Organisms through the Chemical Diversification of Nucleic Acids.
Chemistry & Biodiversity, 2010, 6(6): 791-808.
|
| [40] |
Romeis J., Collatz J., Glandorf D., Bonsall M. B. The Value of Existing Regulatory Frameworks for the Environmental Risk Assessment of Agricultural Pest Control Using Gene Drives.
Environmental Science & Policy, 2020, 108(Suppl. 1): 19-36.
|
| [41] |
Redford K. H., Adams W., Carlson R., et al. Synthetic Biology and the Conservation of Biodiversity.
Oryx, 2014, 48(3): 330-336.
DOI: 10.1017/S0030605314000040. |
| [42] |
Bauer-Panskus A., Miyazaki J., Kawall K. , et al. Risk Assessment of Genetically Engineered Plants that can Persist and Propagate in the Environment.
Environmental Sciences Europe, 2020, 32(1): 1-15.
DOI: 10.1186/s12302-019-0282-1. |
| [43] |
Oye K. A., Esvelt K., Appleton E., et al. Regulating Gene Drives.
Science, 2014, 345(6197): 626-628.
DOI: 10.1126/science.1254287. |
| [44] |
Rycroft T., Hamilton K., Haas C. N., et al. A Quantitative Risk Assessment Method for Synthetic Biology Products in the Environment.
The Science of the Total Environment, 2019, (696): 133940.
|
| [45] |
Wallach W., Saner M., Marchant G. Beyond Cost‐Benefit Analysis in the Governance of Synthetic Biology.
Hastings Center Report, 2018, 48(Suppl1): S70-S77.
|
| [46] |
Keiper F., Atanassova A. Regulation of Synthetic Biology: Developments under the Convention on Biological Diversity and Its Protocols.
Frontiers in Bioengineering and Biotechnology, 2020, (8): 310.
|
| [47] |
Engelhardt M. S. V. Industry Self-governance: A New Way to Manage Dangerous Technologies.
Bulletin of Atomic Scientists, 2013, 69(3): 53-62.
DOI: 10.1177/0096340213486126. |
| [48] |
Cummings C. L., Kuzma J. Societal Risk Evaluation Scheme (SRES): Scenario-Based Multi-Criteria Evaluation of Synthetic Biology Applications.
Plos One, 2017, 12(1): e0168564.
DOI: 10.1371/journal.pone.0168564. |
| [49] |
Weiss S., Yitzhaki S., Shapira S. C. Lessons to be Learned from Recent Biosafety Incidents in the United States.
Israel Medical Association Journal Imaj, 2015, 17(5): 269-273.
|
| [50] |
Ortiz L., Pavan M., Mccarthy L., et al. Automated Robotic Liquid Handling Assembly of Modular DNA Devices.
Journal of Visualized Experiments: Journal of Visualized Experiments, 2017, (130): 54703.
|
| [51] |
Wilson C. C., Wozney K. M., Smith C. M. Recognizing False Positives: Synthetic Oligonucleotide Controls for Environmental DNA Surveillance.
Methods in Ecology and Evolution, 2016, (7): 23-29.
|
| [52] |
Knudsen S. M., Karlstrm O. H. Development of Efficient Suicide Mechanisms for Biological Containment of Bacteria.
Applied and Environmental Microbiology, 1991, 57(1): 85-92.
|
2. National Agriculture Science Data Center, Agricultural Information Institute of CAAS;
3. Center for Biosafety Research and Strategy, TianJin University;
4. School of Chemical Engineering and Technology, TianJin University
 2022, Vol. 12
2022, Vol. 12


