| 溶解态钼钒深度分离技术研究现状与展望 |
钼、钒作为重要的战略金属,具有熔点高、硬度大、耐磨耐腐蚀等独特性能[1-2],广泛用于电子工业、航空航天和国防军工等领域,素有“战争金属”和“工业味精”之称[3-4]。钼、钒作为我国储量丰富的优势矿产资源[5-6],普遍存在资源禀赋差、选冶难度大等特征。2020年全球钼资源储量及我国钼资源品位分布如图 1(a)、1(b)所示[7],我国已探明钼矿储量830万t,居世界首位。然而,我国钼矿资源中品位小于0.1%的钼矿约占钼矿储量的65%以上,且大量钨、铅、铜等元素以伴生或类质同象形式存在于辉钼矿中[8],需要经过复杂的选冶过程才能得到钼产品[9]。2020年全球钒资源储量及我国钒资源品位分布如图 1(c)、1(d)所示[7],我国已探明钒资源储量950万t,居世界首位,主要有钒钛磁铁矿、钒铀矿和含钒石煤等。其中钒钛磁铁矿主要分布在四川攀西地区,少量分布在陕西汉中、河北承德等地[10];含钒石煤主要分布在甘肃、陕西、湖南等地,约占全国钒储量的47.4%[11]。然而,我国钒矿资源中钒钛磁铁矿的品位为0.22%~0.93%,钒铀矿的品位为0.8%~1.35%,石煤资源品位为0.13%~1.2%[12]。以目前的工艺水平,当V2O5品位达到0.8%以上才具有工业开采价值。综上,我国钼、钒矿物品位低、资源禀赋差、伴生元素复杂的现状导致钼、钒选冶极其困难。
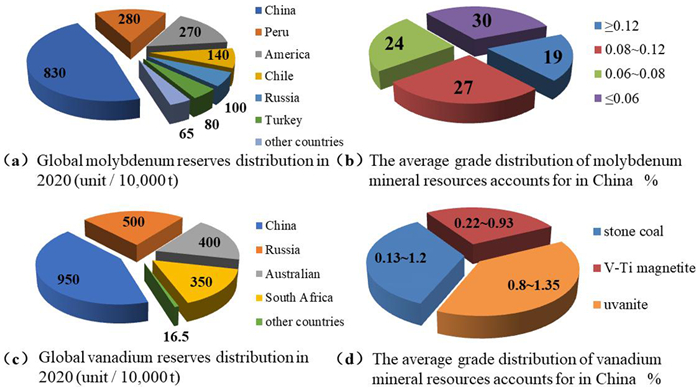 |
| 图 1 2020年全球钼、钒储量及中国钼、钒矿品位分布 Fig.1 Global molybdenum and vanadium reserves and molybdenum and vanadium mine grade distribution in China in 2020 |
我国钼、钒等战略金属的储量保障年限低于世界平均水平。随着经济社会的快速发展,优质钼矿、钒矿资源逐渐枯竭,从富含钼、钒的二次资源中回收钼、钒势在必行。钼、钒二次资源主要包括钼尾矿、钒渣及含钼、钒废催化剂等[1, 13]。加氢脱硫(HDS)催化剂是典型的含钼、钒催化剂,每年报废量约10万t,且仍有不断增加的趋势[14-16]。HDS催化剂主要以氧化铝为载体,钒、钴、镍和钼等作为活性组成,具有有价金属含量高、经济价值大等显著特征,其化学组成及酸浸液离子浓度如图 2所示[17-19]。目前,废催化剂资源化利用过程中首先采用酸浸将有价金属转移至溶液中,再通过传统的化学沉淀、离子交换和溶剂萃取进行分离纯化。实现二次资源中钼、钒的选择性深度分离是其资源化利用的技术瓶颈。一方面,酸浸过程中铝、钴和镍等元素进入浸出液中,造成溶液净化难度大[20];另一方面,钼、钒的化学性质相似,导致分离难度大。
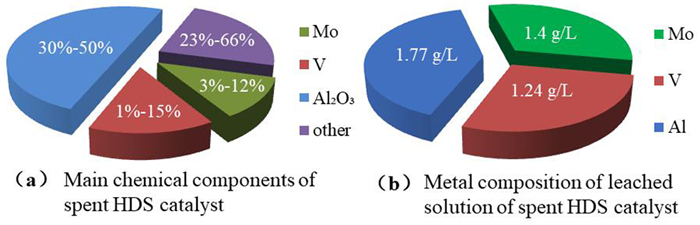 |
| 图 2 废HDS催化剂化学成分及浸出液金属离子浓度 Fig.2 Chemical composition of spent HDS catalyst and concentration of metal ions in leaching solution |
富含战略金属废催化剂的资源化回收与高效利用成为全世界亟待解决的难题,实现废HDS催化剂中钼钒的资源化利用对于缓解环保压力、保障资源安全意义重大[21]。国内外学者围绕浸出液中钼、钒分离纯化进行大量研究,开发了化学沉淀、离子交换和溶剂萃取等多种方法[22-24]。溶剂萃取作为常见的钼、钒分离方法,主要通过共萃取钼钒,再选择性反萃Mo或V达到分离钼、钒的目的,而对于选择性萃取Mo/V的研究报道较少。本文围绕钼、钒分离,综述了钼钒分离的理论基础以及常见钼钒分离技术的方法原理、过程特点及技术局限性。根据钼、钒在不同溶液pH条件下的离子形态特征,并结合钼、钒与药剂结合能力的差异,提出利用浮游萃取强化从钼、钒溶液中选择性分离钼的思路,并对未来钼、钒分离的研究方向进行展望。
2 钼钒分离理论基础相似元素分离的基础是根据元素及相应化合物间某些性质差异而实现。钼、钒选择性分离的关键是找到其元素间物理化学性质差异,并根据其性质差异探索合适的钼、钒分离方法。钼、钒分离效果很大程度上取决于其在水溶液中的存在形态,因此探究钼、钒的水溶液化学意义重大。钼、钒离子形态与溶液pH、离子浓度密切相关[25]。基于Mo(Ⅵ)-V(Ⅴ)-H2O体系化学反应平衡常数和物料守恒[26, 27],可得表 1中式(1)-式(11),若已知体系钼、钒浓度(1 g/L)和溶液pH,求解上述方程可得Mo/V离子形态随溶液pH变化规律,结果如图 3所示。
| 表 1 Mo(Ⅵ)-V(Ⅴ)-H2O体系中的化学反应常数 Table 1 Chemical reaction constants in Mo(Ⅵ)-V(Ⅴ)-H2O system |

|
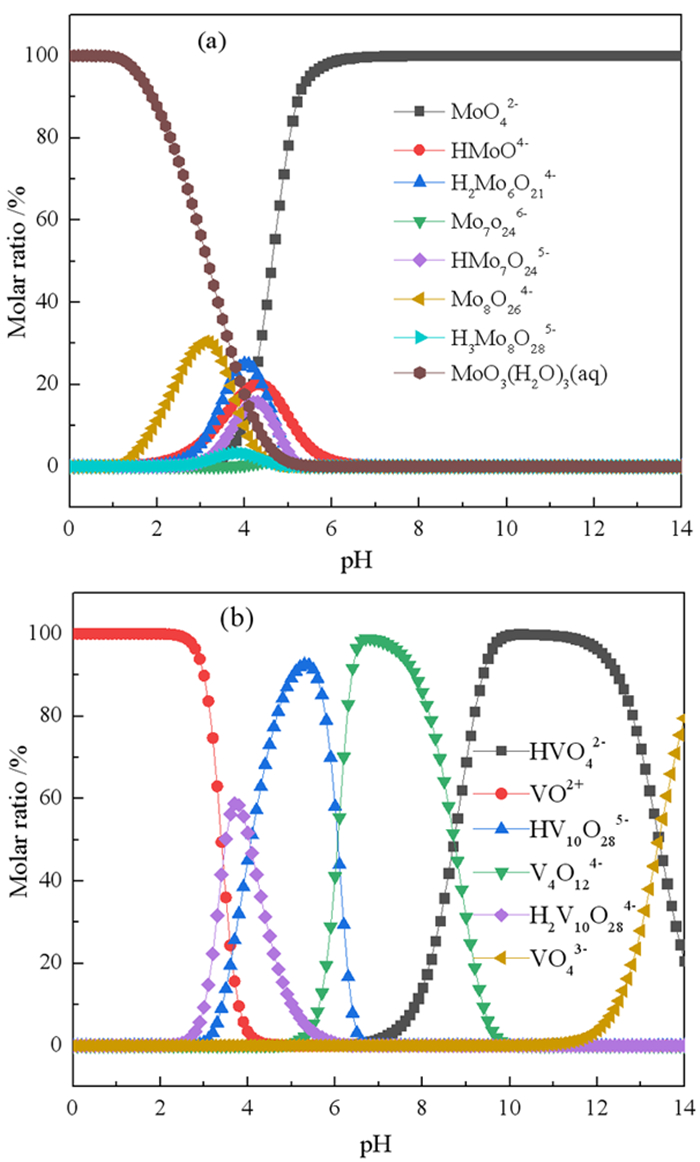 |
| 图 3 MoO42-和VO42-(1 g/L)在不同pH条件下离子形态特征 Fig.3 MoO42- and VO42-(1 g/L) ion form characteristics under different pH conditions |
从图 3可以看出,钼钒的离子存在形态随溶液pH变化较大。当溶液pH < 2时,钼主要以MoO3(H2O)3(aq)的形式存在,溶液2 < pH < 6时,钼以聚合形态存在,当溶液pH>6时,钼以MoO42-的形式存在;而当溶液pH < 2时,钒以VO2+的形式存在,溶液9 < pH < 12时,钒以HVO43-的形式存在,当溶液pH>14时,钒以VO43-的形式存在。综上,强碱性条件下,钼、钒在水溶液中分别以MoO42-和VO43-形式存在,酸化过程中钼、钒逐渐聚合,随溶液pH变化经历了一个从钼、钒酸根到聚多酸根/杂多酸根,最终形成钼、钒过氧阳离子的过程[28]。因此,根据钼、钒离子形态差异,可以确定合适的钼、钒分离条件。
3 钼、钒分离技术研究现状近年来,国内外学者围绕钼、钒分离进行了大量研究,开发了诸如化学沉淀、离子交换、溶剂萃取等多种分离方法[29-32]。
3.1 化学沉淀法化学沉淀法是利用沉淀剂与钼或钒选择性形成沉淀,再通过固液分离实现钼、钒分离。化学沉淀法主要分为硫化沉淀、铵盐沉淀等[33-35]。
硫化沉淀是钼以MoS3形式沉淀,钒留在溶液中,适用于酸性体系。Sebenik和Ference等[23]在适宜的温度与溶液pH条件下,向含钼、钒的废催化剂碱浸液通入H2S得到MoS3沉淀。结果表明,超过99%的钼发生沉淀。向除钼液中加入碱性试剂,钒以水和氧化物(V(OH)4·1.5H2O)形式沉淀;或加入NaClO3溶液,钒以红色饼状物(Na2H2V6O17)形式沉淀,沉淀过程如图 4所示。
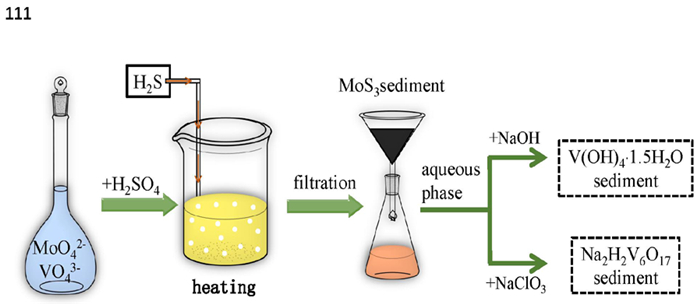 |
| 图 4 硫化沉淀法原理示意图 Fig.4 Schematic diagram of sulfide precipitation method |
铵盐沉淀是向溶液中加入铵盐,使钒以NH4VO3形式沉淀,适用于碱性或盐类体系。Park等[36]将浸出液中的钼以钼酸铵的形式沉淀,经煅烧后得到纯度为97.3%的MoO3产物。主要步骤是首先用HCl处理浸出液,将pH值调至2,使钼酸钠转化为氯化钼,反应过程如式(12)所示:
| $ {{\rm{N}}{{\rm{a}}_2}{\rm{Mo}}{{\rm{O}}_4} + 8{\rm{HCl}} = {\rm{MoC}}{{\rm{l}}_6} + 2{\rm{NaCl}} + 4{{\rm{H}}_2}{\rm{O}}} $ | (12) |
然后用氨水调节氯化钼溶液的pH至11,使其转化为钼酸铵,再向溶液中加入酸,加热至90 ℃,形成钼酸铵沉淀,反应过程如式(13)所示:
| $ {{\rm{MoC}}{{\rm{l}}_6} + 8{\rm{N}}{{\rm{H}}_4}{\rm{OH}} = {{\left( {{\rm{N}}{{\rm{H}}_{\rm{4}}}} \right)}_2}{\rm{Mo}}{{\rm{O}}_{\rm{4}}} \downarrow + 6{\rm{N}}{{\rm{H}}_4}{\rm{Cl}} + 4{{\rm{H}}_2}{\rm{O}}} $ | (13) |
此外,Chen等[37]利用钒酸钡和钼酸钡在水溶液中的溶解度都较低的性质,通过分别向钼、钒溶液中添加氢氧化钡和铝酸钡,从废催化剂碱浸液中选择性沉淀钼和钒[38-39]。研究表明,温度为40 ℃时,加入氢氧化钡反应15 min,钒的沉淀率达94.8%;温度为80 ℃时,加入铝酸钡反应40 min,钼的沉淀率达92.6%。
化学沉淀法具有操作简单、成本较低等优势,但在提高钼、钒分离效率,开发相关深度分离沉淀药剂方面存在较大发展空间。
3.2 离子交换法离子交换法是利用离子交换树脂对钼、钒离子亲和力的差异实现钼、钒的选择性分离。Thi Hong Nguyen等[40]使用离子交换法从含钼、钒的硫酸溶液中分离钼和钒,分离过程如图 5所示。在溶液pH为1.2时,采用阴离子树脂(AG1-x8)选择性吸附钼,吸附反应如式(14)~(16)所示,负钼树脂采用NaOH溶液解吸,实现树脂的循环利用。
| $ {3{\rm{RCl}} + {\rm{M}}{{\rm{o}}_7}{{\rm{O}}_{21}}{{\left( {{\rm{OH}}} \right)}_3}^{3 - } = {{\rm{R}}_3}{\rm{M}}{{\rm{o}}_7}{{\rm{O}}_{21}}{{\left( {{\rm{OH}}} \right)}_3} + 3{\rm{C}}{{\rm{l}}^ - }} $ | (14) |
| $ {5{\rm{RCl}} + {\rm{M}}{{\rm{o}}_7}{{\rm{O}}_{23}}{{\left( {{\rm{OH}}} \right)}^{5 - }} = {{\rm{R}}_5}{\rm{M}}{{\rm{o}}_7}{{\rm{O}}_{23}}\left( {{\rm{OH}}} \right) + 5{\rm{C}}{{\rm{l}}^ - }\;} $ | (15) |
| $ {5{\rm{RCl}} + {\rm{M}}{{\rm{o}}_7}{{\rm{O}}_{23}}{{\left( {{\rm{OH}}} \right)}^{5 - }} = {{\rm{R}}_5}{\rm{M}}{{\rm{o}}_7}{{\rm{O}}_{23}}\left( {{\rm{OH}}} \right) + 5{\rm{C}}{{\rm{l}}^ - }\;} $ | (16) |
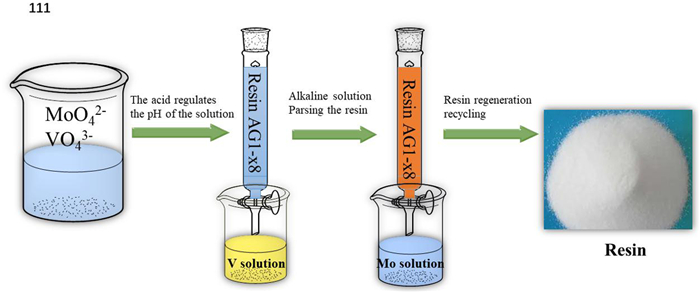 |
| 图 5 离子交换法分离钼、钒示意图 Fig.5 Schematic diagram of separation of molybdenum and vanadium by ion exchange method |
曾理等[22]采用离子交换树脂DP-1从浸出液中分离钒。在溶液pH=7.18、接触时间30 min、料液体积为树脂体积10倍的条件下,钒的去除率达99.84%。负载钒树脂用NaOH溶液解吸,树脂经盐酸洗涤再生后循环利用。
Xian-zheng ZHU等[41]利用多羟基螯合树脂D403从含钼溶液中选择性去除钨和钒,由于D403树脂对于钨和钒的亲和力比钼强,溶液中的钨和钒可优先被D403树脂吸附,钒的去除率高达95%以上。负载树脂用NaOH溶液洗涤,即可实现树脂的再生。
离子交换法具有操作简单、选择性高等优势,今后需在提高树脂饱和容量、循环利用率等研究方面取得突破,并开发适用于低离子浓度的分离体系[42]。
3.3 溶剂萃取法溶剂萃取法是基于钼、钒离子在有机相和水相间分配系数的差异实现选择性分离。溶剂萃取与离子交换具有异曲同工之处,是湿法冶金中较为成熟的单元操作之一。已报道的钼钒萃取体系中,萃取剂主要有胺类萃取剂、有机膦酸类萃取剂及羟肟类萃取剂等。胺类萃取剂主要包括伯胺、仲胺、叔胺和季铵盐[43-44],相较于有机膦酸类[45]或其他类型的萃取剂,合适的胺类萃取剂能够提供更宽的pH范围,尤其对于水溶液性质接近、离子形态多变的体系[42]。
丁扬力等[46]使用甲基三辛基氯化铵(N263)从高浓度含钼溶液中选择性萃取钒。在溶液pH=8.5、15%N263、油水比为1:2时,钒的萃取率达99.6%,而钼的萃取率低于0.5%,萃取及反应过程如图 6、图 7所示。
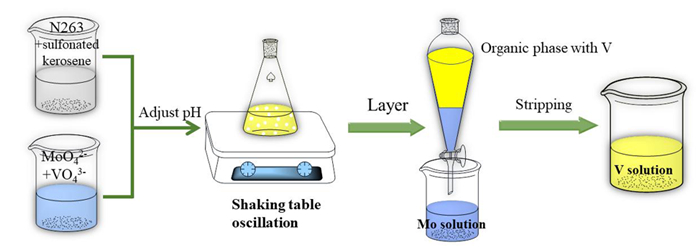 |
| 图 6 N263萃取钼、钒示意图 Fig.6 Schematic diagram of extracting molybdenum and vanadiumby N263 |
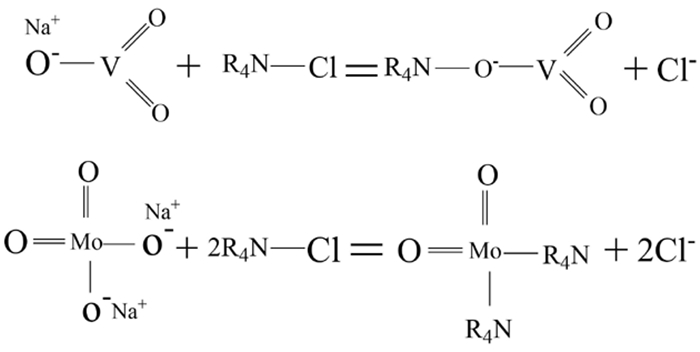 |
| 图 7 N263萃取钼、钒原理 Fig.7 Schematic diagram of extracting molybdenum and vanadium by N263 |
沈明伟等[47]采用P507共萃取钼钒,钼、钒的萃取率均达98%以上,然后采用硫酸选择性反萃钒;钼用10%的氨水-氯化铵溶液反萃,反萃率高达99%。Hailong Li等[48]在此研究的基础上采用P507+N235共萃取浸出液中的钼钒,当溶液pH < 3、O/A=2时,钼和钒萃取率超过99%,然后分别用氨水和硫酸反萃钼和钒,最后通过沉淀、煅烧获得MoO3和V2O5产物。
Yajing Pan等[49-50]利用PEG2000-硫酸钠-水形成的两相体系共萃取钼钒,PEG2000可以选择性萃取钼和钒。当溶液pH=2时,钼钒的萃取率都达到95%以上。Yajing Pan等接着探究了向偏钒酸钠、钼酸钠和硫酸钠的混合溶液中加入硫酸,调节溶液pH值后,加入蒸馏水和表面活性剂(由L35(三嵌段共聚物)、Triton X-100(八苯基聚氧乙烯)、PEG2000(聚乙二醇)和硫酸钠混合而成)萃取钼,在溶液的pH为0.7~0.75,L35为20%,硫酸钠为10%,温度70 ℃的条件下,钼以HMo8O263-的形式被萃取到含表面活性剂的有机相中去,而钒以VO2+的形式留在水相中,钼和钒的单级萃取率分别大于90%和小于20%。
溶剂萃取法是相对较为成熟的方法,具有选择性好、分离效率高等优点[51],广泛应用于钼钒的萃取分离过程中,应在开发新型萃取剂、提高分离效率、简化萃取工艺、调控第三相生成等方面深入研究。
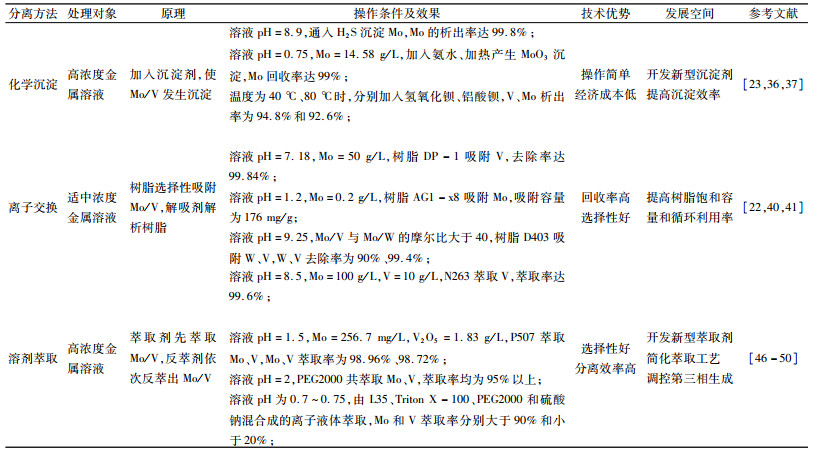
化学沉淀法、离子交换法和溶剂萃取法是溶解态钼、钒分离的主要技术。表 2系统总结了化学沉淀、离子交换和溶剂萃取的原理,技术特征及发展空间等。上述三种方法均存在一定的发展空间,如化学沉淀开发新型沉淀剂、提高沉淀效率,离子交换提高树脂饱和容量和循环利用率,溶剂萃取开发新型药剂、简化萃取工艺、调控第三相生成。此外,对于复杂的分离体系,需要不断开发新型钼、钒分离技术。
| 表 2 常见钼、钒分离方法比较 Table 2 Comparison of several methods for separation ofmolybdenum and vanadium |
|
4 浮游萃取强化钼、钒分离
浮选源于矿物加工,是一种以气泡为载体的界面分离方法[52]。1959年,Sebba根据离子物化性质的差异实现溶液中离子选择性分离,提出“离子浮选”的概念[53]。1962年,Sebba改进离子浮选技术,在浮选溶液上层加入有机溶剂来富集目标物[54],由此提出了溶剂浮选。相比溶剂萃取,溶剂浮选由于强烈的气泡传质作用而使分离过程被显著强化。据此我们提出利用浮游萃取(药剂矿化、气泡矿化强化)深度分离钼、钒的方法,试验过程如图 8所示,主要包括药剂矿化、浮游萃取、反萃解吸等过程[55]。其实质是向含钼钒溶液中加入选择性浮萃剂,使溶液中Mo与浮萃剂形成疏水性缔合物,通入气泡后气泡矿化形成Mo-浮萃剂-气泡微液滴,最后通过浮游萃取富集分离Mo,有机相反萃得到钼产品。
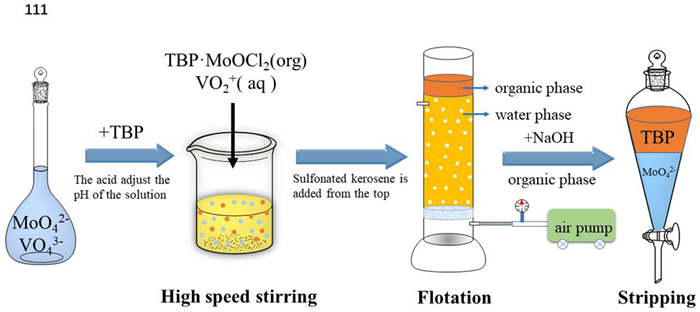 |
| 图 8 浮游萃取分离钼、钒过程示意图 Fig.8 Schematic diagram of separation of molybdenum and vanadium by floating-extraction |
基于浮游萃取技术,探索了模拟废催化剂浸出液(Mo/V均为1 g/L)中钼、钒的选择性分离行为。首先采用盐酸调节溶液pH,然后向溶液中加入磷酸三丁酯(TBP),通过高速搅拌使水相与有机相混合均匀,TBP与溶液中Mo反应形成疏水性络合物TBP·MoCl2[56]。将上述溶液转移至浮选柱中并通入气泡,待气速稳定后,在溶液上层加入有机相开始浮选,溶液中的疏水性络合物TBP·MoCl2经气泡矿化吸附在气泡表面,随气泡上升富集在上层有机相中。结果表明,在盐酸质量浓度为2 mol/L,TBP质量浓度为40%、O/A=1:2的条件下,钼的去除率达95%以上,而V基本不与TBP发生反应,有机相中的钼可以通过氢氧化钠溶液反萃,反应过程如式(17)-式(18)所示。
| $ {{\rm{MoOC}}{{\rm{l}}_{2({\rm{aq}})}} + 2{\rm{TB}}{{\rm{P}}_{{\rm{(org)}}}} = 2{\rm{TBP}} \cdot {\rm{MoOC}}{{\rm{l}}_{{\rm{2(org)}}}}\;} $ | (17) |
| $ \begin{array}{l} {\rm{TBP}} \cdot {\rm{Mo}}{{\rm{O}}_2}{\rm{C}}{{\rm{l}}_{{\rm{2(org)}}}} + 2{\rm{NaO}}{{\rm{H}}_{{\rm{(aq)}}}} = \\ {\rm{N}}{{\rm{a}}_2}{\rm{Mo}}{{\rm{O}}_{4(aq)}} + {\rm{TB}}{{\rm{P}}_{{\rm{(org)}}}} + 2{\rm{HC}}{{\rm{l}}_{{\rm{(aq)}}}} \end{array} $ | (18) |
浮游萃取克服了溶剂萃取过程存在串级萃取流程冗长的缺点,以及化学沉淀法和离子交换法对溶液浓度的限制,具有高分离富集效率、低溶剂消耗、大相比操作等优势,在钼钒的资源化利用过程中,目前浮游萃取技术在钼钒分离领域几乎没有相关报道[57],具有很好的应用前景。然而,浮萃药剂与待分离组分结合能力、形成的配合物疏水矿化程度对于钼钒分离效率影响较大。因此,开发合适的浮萃药剂是实现其选择性分离钼、钒的关键,未来应深入研究与金属离子选择性强、结合能力强、疏水性适中的新型绿色浮萃药剂。
5 结论与展望近年来,溶解态钼钒分离取得显著进步,但仍存在深度分离难题。随着高精尖技术领域对高纯钼、钒产品需求增加,需在现有钼钒分离方法的基础上,进一步探索钼、钒物化性质差异,开发钼、钒分离回收新技术、新工艺,最终实现废催化剂的资源化高效利用。未来钼、钒选择性深度分离技术需重点考虑以下几个方面:
(1) 查明溶解态钼、钒离子形态随溶液pH、离子浓度间的变化规律,开发高选择性的新型沉淀剂、离子交换树脂、溶剂萃取剂,探究药剂与目标组分结合能力,扩大钼、钒物化性质差异,为实现钼、钒的选择性深度分离奠定理论基础。
(2) 借鉴化学沉淀、离子交换、溶剂萃取等方法的技术优势,针对不同研究体系,采用多种分离方法耦合的技术思路,建立沉淀-离子交换、沉淀-溶剂萃取等技术联新工艺,实现溶解态钼、钒的选择性深度分离。
(3) 开发适用于钼、钒选择性深度分离的浮萃药剂(选择性强、疏水性适中),优化浮游萃取工艺,探究浮游萃取过程离子-药剂-气泡间的微观作用行为,深入揭示浮游萃取过程药剂矿化、气泡矿化的作用机制。
致谢
本研究工作得到国家自然科学基金(U2004215,51974280,51774252)和河南省高校科技创新人才项目(20HASTIT012)资助。
| [1] |
张汉鑫, 李慧, 梁精龙, 等. 稀有金属钼资源回收现状及进展[J]. 矿产综合利用, 2020, 221(1): 52-54. |
| [2] |
王秋霞, 马化龙. 我国钒资源和V2O5研究、生产的现状及前景[J]. 矿产保护与利用, 2009(5): 47-50. DOI:10.3969/j.issn.1001-0076.2009.05.013 |
| [3] |
陈桃, 简胜, 谢贤, 等. 钒钛磁铁矿尾矿综合利用研究进展[J]. 矿产保护与利用, 2021, 41(2): 174-178. |
| [4] |
于恒渊. 冰晶石熔盐体系电解制备金属钒的研究[D]. 沈阳: 东北大学, 2014.
|
| [5] |
夏青, 梁治安, 杨秀丽, 等. 某选铁尾矿中低品位钼, 锌分选回收试验研究[J]. 有色金属工程, 2020, 10(5): 81-88. DOI:10.3969/j.issn.2095-1744.2020.05.015 |
| [6] |
朱欣然. 国内外钼资源供需形势分析[J]. 矿产保护与利用, 2020, 40(1): 172-178. |
| [7] |
USGS U S. Geological survey mineral commodity summaries[EB/OL]. [2021-06-14]. https://www.usgs.gov/.
|
| [8] |
李琳, 吕宪俊, 栗鹏. 钼矿选矿工艺发展现状[J]. 中国矿业, 2012(2): 99-103. DOI:10.3969/j.issn.1004-4051.2012.02.028 |
| [9] |
谢铿, 王海北, 张邦胜. 辉钼精矿加压湿法冶金技术研究进展[J]. 金属矿山, 2014(1): 74-79. |
| [10] |
张建廷, 陈碧. 攀西钒钛磁铁矿主要元素赋存状态及回收利用[J]. 矿产保护与利用, 2008(5): 38-41. DOI:10.3969/j.issn.1001-0076.2008.05.010 |
| [11] |
刘景槐, 谭爱华. 我国石煤钒矿提钒现状综述[J]. 湖南有色金属, 2010, 26(5): 11-14. DOI:10.3969/j.issn.1003-5540.2010.05.004 |
| [12] |
李昌林, 周云峰, 费海霞, 等. 石煤提钒工艺研究及应用现状[J]. 稀有金属与硬质合金, 2012, 40(6): 9-14. |
| [13] |
徐正震, 梁精龙, 李慧, 等. 含钒废弃物中钒的回收研究现状及展望[J]. 矿产综合利用, 2020(3): 8-13. DOI:10.3969/j.issn.1000-6532.2020.03.002 |
| [14] |
梁海宁, 刘欣梅, 昌兴文, 等. 炼油废催化剂的处理和利用[J]. 炼油技术与工程, 2010, 40(1): 1-5. DOI:10.3969/j.issn.1002-106X.2010.01.001 |
| [15] |
李富荣, 唐晓. 废钼镍催化剂回收技术现状与分析[J]. 中国资源综合利用, 2011, 29(11): 17-19. DOI:10.3969/j.issn.1008-9500.2011.11.003 |
| [16] |
YANG C, ZHANG J, CHEN Y, et al. Efficient removal of oil from spent hydrodesulphurization catalysts using microwave pyrolysis method[J]. Journal of Analytical and Applied Pyrolysis, 2018, 135(8): 169-175. |
| [17] |
KIM H I, LEE K W, D MISHRA, et al. Separation and recovery of vanadium from leached solution of spent residuehydrodesulfurization (RHDS) catalyst using solvent extraction[J]. Journal of Industrial & amp; Engineering Chemistry, 2014, 20(6): 4457-4462. |
| [18] |
刘公召, 隋智通. 从HDS废催化剂中提取钒和钼的研究[J]. 矿产综合利用, 2002(2): 40-42. |
| [19] |
高崇, 王为振, 常耀超, 等. HDS渣综合回收利用钒钼的研究[J]. 有色金属(冶炼部分), 2021, 4(7): 92-97. |
| [20] |
张梅英, 季登会. 废催化剂中钼、钒回收工艺的研究[J]. 矿冶, 2011, 20(4): 109-112. |
| [21] |
胡佩伟, 谢志诚, 胡兵, 等. 含钒固废综合利用现状及发展[J]. 矿产保护与利用, 2020, 40(5): 148-156. |
| [22] |
曾理, 肖连生, 李青刚, 等. 离子交换法从钼酸铵溶液中分离钼钒的研究[J]. 稀有金属与硬质合金, 2006, 34(2): 1-4. DOI:10.3969/j.issn.1004-0536.2006.02.001 |
| [23] |
施友富, 王海北. 废催化剂中钼和钒的分离[J]. 中国钼业, 2004(2): 39-41. DOI:10.3969/j.issn.1006-2602.2004.02.010 |
| [24] |
ZENG L, CHU Y C. A literature review of the recovery of molybdenum and vanadium from spent hydrodesulphurisation catalysts: Part Ⅱ: Separation and purification[J]. Hydrometallurgy, 2009, 98(1/2): 10-20. |
| [25] |
THI HONG NGUYEN, MAN SEUNG LEE. A review on the separation of molybdenum, tungsten, and vanadium from leach liquors of diverse resources by solvent extraction[J]. Geosystem Engineering, 2016, 19(5): 247-259. DOI:10.1080/12269328.2016.1186577 |
| [26] |
张家靓, 张立峰. Mo(Ⅵ)-V(Ⅴ)-H2O系的热力学平衡与钼酸盐深度除钒工艺的理论分析[J]. 稀有金属, 2016, 40(7): 701-707. |
| [27] |
廖宇龙, 李江涛. Mo(Ⅵ)-V(Ⅴ)-H2O体系的热力学分析[J]. 粉末冶金材料科学与工程, 2016, 21(5): 678-684. DOI:10.3969/j.issn.1673-0224.2016.05.003 |
| [28] |
Cruywagen J J. Protonation, oligomerization, and condensation reactions of vanadate(Ⅴ), molybdate(Ⅵ), and tungstate(Ⅵ)[J]. Advances in Inorganic Chemistry, 1999, 49: 127-182. |
| [29] |
陈亮. 从钒浸出液中沉淀结晶型钒酸铁试验研究[J]. 湿法冶金, 2010, 29(3): 171-175. DOI:10.3969/j.issn.1009-2617.2010.03.009 |
| [30] |
巢亚军, 熊长芳, 朱超. 废工业催化剂回收技术进展[J]. 工业催化, 2006, 14(2): 64-67. DOI:10.3969/j.issn.1008-1143.2006.02.018 |
| [31] |
邓攀, 曾颜亮, 王坤, 等. 钼资源的回收技术现状及发展[J]. 山西冶金, 2012, 35(5): 1-3. DOI:10.3969/j.issn.1672-1152.2012.05.001 |
| [32] |
刘艳. 用离子交换法从加氢脱硫废催化剂的硫酸浸出液中回收高纯钼和钒[J]. 湿法冶金, 2014, 33(4): 288. |
| [33] |
ZHANG P, INOUE K, YOSHIZUKA K, et al. Extraction and selective stripping of molybdenum(Ⅵ) and vanadium(Ⅳ) from sulfuric acid solution containing aluminum(Ⅲ), cobalt(Ⅱ), nickel(Ⅱ) and iron(Ⅲ) by LIX 63 in Exxsol D80[J]. Hydrometallurgy, 1996, 41(1): 45-53. DOI:10.1016/0304-386X(95)00015-9 |
| [34] |
JDA B, JIA L, DHA B, et al. Green separation and recovery of molybdenum from tungstate solution achieved by using a recyclable vulcanizing agent[J]. Journal of Cleaner Production, 2020, 278: 123930. |
| [35] |
ROKUKAWA N. Recovery of Vanadium and Nickel from Heavy Oil Ash[J]. Journal of the Japan Society of Waste Management Experts, 2002, 13(6): 387-393. DOI:10.3985/jswme.13.387 |
| [36] |
PARK K H, MOHAPATRA D, REDDY B R. Selective recovery of molybdenum from spent HDS catalyst using oxidative soda ash leach/carbon adsorption method[J]. Journal of Hazardous Materials, 2006, 138(2): 311-316. DOI:10.1016/j.jhazmat.2006.05.115 |
| [37] |
CHEN Y, FENG Q, ZHANG G, et al. Study on the recycling of valuable metals in spent Al2O3-based catalyst[J]. Minerals and Metallurgical Processing, 2007, 24(1): 30-34. |
| [38] |
FUENZALIDA C. Room temperature electrochemical growth of polycrystalline BaMoO4 films[J]. Journal of the European Ceramic Society, 2003, 23(3): 519-525. DOI:10.1016/S0955-2219(02)00149-8 |
| [39] |
OKA Y, TAMADA O, YAO T, et al. Hydrothermal Synthesis and Crystal Structure of a Novel Barium Vanadium Oxide: Ba0. 4V3O8(VO)0. 4·nH2O[J]. Journal of Solid State Chemistry, 1995, 114(2): 359-363. DOI:10.1006/jssc.1995.1055 |
| [40] |
NGUYEN T H, MAN S L. Separation of molybdenum and vanadium from acid solutions by ion exchange[J]. Hydrometallurgy, 2013, 136(4): 65-70. |
| [41] |
ZHU X, HUO G, NI J, et al. Removal of tungsten and vanadium from molybdate solutions using ion exchange resin[J]. Transactions of Nonferrous Metals Society of China, 2017, 27(12): 2727-2732. DOI:10.1016/S1003-6326(17)60301-7 |
| [42] |
林晓. 伯胺溶剂化萃取在含钒铬钨钼废物资源化处理的应用基础研究[D]. 北京: 中国科学院研究生院(过程工程研究所), 2015.
|
| [43] |
BISHNOI A K, DASS R, SHARMA R G. Extraction of molybdenum(Ⅴ) as its ferron complex with trioctylamine in chloroform from a sulphuric acid medium[J]. Journal of Analytical Chemistry, 2008, 63(3): 214-218. DOI:10.1134/S1061934808030039 |
| [44] |
SOLA B C, KUMARPARHI P, JIN-YOUNGLEE, et al. Environmentally friendly approach to recover vanadium and tungsten from spent SCR catalyst leach liquors using Aliquat 336[J]. RSC Advances, 2020, 10(34): 19736-19746. DOI:10.1039/D0RA02229B |
| [45] |
WANG H, FENG Y, LI H, et al. Recovery of vanadium from acid leaching solutions of spent oil hydrotreating catalyst using solvent extraction with D2EHPA (P204)[J]. Hydrometallurgy, 2020, 195: 105404. DOI:10.1016/j.hydromet.2020.105404 |
| [46] |
丁扬力, 肖连生, 曹佐英, 等. N263从钼酸钠溶液中萃取分离钼钒[J]. 有色金属科学与工程, 2017, 8(1): 15-20. |
| [47] |
沈明伟, 朱昌洛, 李华伦. P507-煤油体系在钒钼萃取分离中的试验研究[J]. 矿产综合利用, 2007(4): 14-19. DOI:10.3969/j.issn.1000-6532.2007.04.004 |
| [48] |
LI H, FENG Y, WANG H, et al. Separation of V (Ⅴ) and Mo (Ⅵ) in roasting-water leaching solution of spent hydrodesulfurization catalyst by co-extraction using P507-N235 extractant[J]. Separation and Purification Technology, 2020, 248: 117135. DOI:10.1016/j.seppur.2020.117135 |
| [49] |
PAN Y, SUN X, QI M, et al. A clean and efficient method for separation of vanadium and molybdenum by aqueous two-phase systems[J]. Journal of Molecular Liquids, 2020, 313: 113540. DOI:10.1016/j.molliq.2020.113540 |
| [50] |
PAN Y, SUN X, ZHANG Y. Separation of vanadium and molybdenum from aqueous solution using PEG2000+sodium sulfate+water aqueous two-phase system[J]. SN Applied Sciences, 2019, 1(11): 1461. DOI:10.1007/s42452-019-1507-z |
| [51] |
NGUYEN T H, LEE M S. Separation of Vanadium and Tungsten from Sodium Molybdate Solution by Solvent Extraction[J]. Industrial & amp; Engineering Chemistry Research, 2014, 53(20): 8608. |
| [52] |
DELIYANNI E A, KYZAS G Z, MATIS K A. Various flotation techniques for metal ions removal[J]. Journal of Molecular Liquids, 2017, 225: 260-264. DOI:10.1016/j.molliq.2016.11.069 |
| [53] |
韩桂洪, 武宏阳, 黄艳芳, 等. 离子浮选法处理有色金属工业废水研究进展[J]. 贵州大学学报: 自然科学版, 2020(4): 1-9. |
| [54] |
SEBBA F. Ion flotation[M]. New York: American Elsevier, 1962.
|
| [55] |
韩桂洪, 刘兵兵, 黄艳芳, 等. 一种用于提取稀贵金属的浮游萃取系统: ZL202022863914.4 [P]. 2021-07-09.
|
| [56] |
TRUONG H T, LEE M S. Separation of rhenium (Ⅶ), molybdenum(Ⅵ), and vanadium(Ⅴ) from hydrochloric acid solution by solvent extraction with TBP[J]. Geosystem Engineering, 2017, 20(4): 1-7. |
| [57] |
韩桂洪, 刘兵兵, 黄艳芳, 等. 一种基于浮游萃取的溶解态高相似稀贵金属富集分离方法: ZL202010167443.5 [P]. 2020-05-29.
|
 2021
2021



