| 废铝基/钯催化剂碱性浸出废液制备拟薄水铝石的研究 |
氢氧化铝又称为水合氧化铝, 化学式为Al2O3·nH2O, 当n=1时Al2O3·H2O被称为一水氧化铝, 分为硬水铝石、薄水铝石和拟薄水铝石3种[1]。薄水铝石与拟薄水铝石之间的主要差别是晶粒大小的不同[2]。
氧化铝具有多种晶型, 在不同的条件下对氢氧化铝进行焙烧, 制备出的氧化铝的晶型各不相同, 其中, γ-Al2O3是工业中应用最广泛的过渡态氧化铝, 它也被称为活性氧化铝。γ-Al2O3具有较大的比表面积, 可以作为载体负载较多的金属或金属氧化物, 而且其孔径可调, 热稳定性较好, 因此, 经常在加氢、重整、甲醇合成等反应中用作催化剂的载体[3]。目前, 工业上使用的活性氧化铝大多是通过焙烧拟薄水铝石得到的, 在炼油和汽车工业中都有着广泛的应用。
要制备大比表面积大孔径的氧化铝, 需要先制备具有大比表面积的薄水铝石或拟薄水铝石前体, 拟薄水铝石的形貌和粒径决定了氧化铝的形貌、比表面积[4]。目前制备拟薄水铝石的方法主要有酸沉淀法、碱沉淀法、醇铝法和偏铝酸钠CO2中和法制备拟薄水铝石。
酸沉淀法是向铝酸钠溶液中加入强酸, 主要的方法就是硝酸法, 也就是利用偏铝酸钠和HNO3的中和反应得到拟薄水铝石, 便于控制反应条件, 且得到的产品孔径分布较为集中, 但是得到产品成分不稳定[5-6], 纯度不高, 质量波动较大, 同时, 硝酸的价格也较为昂贵, 难以在工业上大规模的使用。碱沉淀法制备拟薄水铝石是向酸性的铝盐溶液中加入沉淀剂(氨水、铝酸钠或氢氧化钠), 经沉淀、过滤、洗涤、干燥制得拟薄水铝石。碱沉淀法获得的产品质量稳定, 杂质脱出容易, 不易生成三水氧化铝[7], 但是对原料的纯度要求高, 而且阴离子的脱除也较为困难。无论是酸沉淀法还是碱沉淀法都会存在酸碱中和反应, 酸碱分解时会有有害气体生成, 对人体和环境都会产生污染[8]。醇铝水解法是用铝在催化剂存在的条件下与醇反应生成醇铝, 得到的产品纯度高, 但是有机醇的成本高, 且不易于回收利用, 造成拟薄水铝石的价格过高, 而有机醇的毒性也较高, 同时, 反应会有大量的废水生成, 会对环境造成较大的污染。
偏铝酸钠CO2中和法制备拟薄水铝石依托烧结法生产氧化铝工艺流程, 利用工业生产的中间产物NaAlO2溶液和CO2作为反应原料, 以其工艺操作简单、无污染、成本低的优点成为了目前国内使用最多的一种方法[9]。杨清河、李大东等[10]对偏铝酸钠CO2法制备拟薄水铝石的基本工艺参数进行了研究, 从宏观方面研究了不同工艺条件下拟薄水铝石的质量, 控制合适的参数, 可制得结晶度较高、无三水氧化铝杂晶且Na+含量较低的拟薄水铝石。魏先全、李庆等[11]研究发现生成拟薄水铝石的影响因素大小为:碳化温度>碳化液浓度>终点pH>气体配比, 并且确定了最优碳化方案, 当碳化液初温10~15 ℃, 碳化液浓度≤15 g/L(氧化铝记), 碳化过程碳空比0.5, 终点pH=10.5时, 可制得比表面积达到234 m2/g, 晶型较好, 纯度较高的产品。以上两种方法都是在溶液中进行陈化, 在陈化过程中需要对整个浆液体系进行提温保温, 因而耗费热能较多且提温时间较长, 沉淀过程中会有固体挂壁现象。孟令利、张丽等[13]发明了一种新的陈化方式, 通入CO2制备出沉淀后进行固液分离, 将附着母液的滤饼装入密闭容器中加热陈化, 可以降低陈化时间, 获得结晶度好、胶溶性好的产品。
由于拟薄水铝石的结构对其性能有重要影响, 虽然以上研究制得的拟薄水铝石产品的比表面积和胶溶指数都达到了工业标准, 但是这些研究均未对工艺参数与产品的结构、形态之间的关系进行探究, 工艺参数和结构、形态之间的关系的构建更能指导实际生产。本文拟采用由废铝基/钯石油催化剂经钠化焙烧—碱性浸出的废液为研究对象, 研究CO2中和法制备拟薄水铝在不同的反应条件下得到产品的微观结构, 建立工艺参数与结构之间的关系, 为实现废铝基/钯石油催化剂的高效增值利用提供技术依据, 并为类似的催化剂载体的制备提供思路。
1 试验 1.1 试验原料由废铝基/钯石油催化剂经碱性浸出得到的含铝、钠的废液, 其成分如表 1所示。
| 表 1 废浸出液含量成分 /(mg·L-1) Table 1 Components of waste leaching liquor |
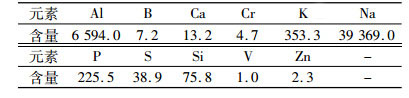 |
从表 1中可以看出, 浸出液的主要成分是铝和钠, 铝的含量高达6 594 mg/L, 钠含量达到39 369 mg/L。该溶液的pH为14, 属于强碱性含铝溶液, 适宜于使用铝酸钠CO2法进行铝的利用, 溶液中大量的钠可以在试验过程中通过洗涤去除。相对铝、钠, 钾和磷含量相对较少, 对该反应无影响, 其他元素含量可以忽略不计。
1.2 试验方法向碱性浸出废液中通入CO2, 废液初始温度为常温(20 ℃左右)[10, 11], 同时使用搅拌器对溶液进行搅拌, 当溶液的pH达到一定值时停止通气, 过滤, 得到滤饼。将滤饼置于一定温度的烘箱中, 陈化一段时间, 得到拟薄水铝石。将得到的拟薄水铝石置于90 ℃的超纯水中, 溶解, 搅拌和过滤, 洗去产品的附着碱, 得到纯净的无杂晶的拟薄水铝石[12]。
1.3 检测方法比表面积:使用BET比表面积检测法。
胶溶指数:称取10 g小于200目的拟薄水铝石(分析其氧化铝质量百分含量X1)于250 mL锥形瓶中, 加入适量蒸馏水, 开动搅拌, 加入适量硝酸, 继续搅拌10 min后, 离心分离, 倒出上层悬浊液, 称取质量(G), 分析其氧化铝质量百分含量(X2)然后计算胶溶指数:DI=GX2/10X1[13]。
沉淀率:量取200 mL溶液, 使用EDTA返滴定法测得原溶液中铝的含量C1, 在反应后, 使用EDTA返滴定发测得原溶液中铝的含量C2, 剩余溶液体积V2, 沉淀率为(200×C1-C2V2)/200×C1。
2 结果与讨论不同反应条件会对产品产生不同影响, 得到不同性能的产品, 而其中主要可控制的反应条件为反应终点pH、陈化时间和陈化温度这三方面。在拟薄水铝石的应用中, 胶溶指数和比表面积是体现产品质量的重要指标。催化剂载体的比表面积大, 有效负载的催化剂的量就大, 而胶溶指数大则产品的纯净度、结晶状况和结构更好。而微观结构可以反映产品的比表面积, 一般来说结晶效果越好, 颗粒粒径越大, 其比表面积越小, 比表面积又对胶溶指数的高低有着直接的影响, 比表面积越小则胶溶指数越低。本节通过比表面积和胶溶指数的测定以及微观结构的表征, 揭示上述三种反应条件对产品性能与结构的影响规律。
2.1 反应终点pH的影响在不同反应终点pH值下, 控制陈化时间4 h, 陈化温度100 ℃, 得到不同的产品。其沉淀率和产品性能如表 2所示。
| 表 2 反应终点pH对沉淀率和产品性能的影响 Table 2 The effect of reaction terminal pH on the rate of deposition and product property |
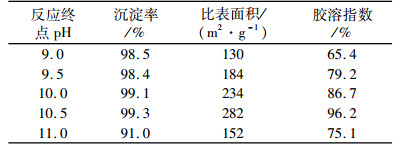 |
从表 2可以看出, 拟薄水铝石的沉淀率很高, 大部分条件下都超过98%, 溶液中的铝可以得到有效利用。当pH在11的时候沉淀率较低, 只有91%, 其原因是pH为11时, 溶液的碱性依然较强, 沉淀尚未完全。通过比表面积和胶溶指数的结果可以看出, 随着反应终点pH的增加, 比表面积和胶溶指数先增大后减小, 反应终点pH为10.5时为最佳反应条件, 产品的比表面积达到282 m2/g, 胶溶指数达到96.2%。
图 1是不同反应终点pH时得到的产品的扫描电镜图, 从图 1中可知, 在反应终点pH小于10.5的时候有针状物质生成, pH达到10.5后针状物质消失, 随着pH的进一步增大, 产品的粒度也进一步增加。由于在NaAlO2基本反应完全后继续通入CO2时, CO2和溶液中的CO32-会反应生成HCO3-, 当HCO32-/Al3+≥1时会有丝钠铝石的生成[14], 而丝钠铝石的微观结构是结晶完善的针状物质, 同时从表 2中的沉淀率数据可以看出, 当反应终点pH达到10.5时沉淀率最高, 反应已经完全进行, 因此, 可以推断出pH小于10.5时生成的针状物质是丝钠铝石。对图 1a和1c中的产物进行XRD检测, 得到的结果如图 2、图 3所示, 根据XRD结果, 可以确定图 1a中的针状物质是丝钠铝石, 图 1c中产品为拟薄水铝石或薄水铝石, 对图 1c中的产物进行热重分析, 如图 4所示, 通过热重分析可以看出, 100 ℃前, 200~250 ℃以及350~400 ℃时产品质量呈大幅度下降, 100 ℃之前是游离水被蒸发, 200~250 ℃是结晶水脱除, 350~450 ℃是γ氧化铝开始形成, 结合XRD和热重结果可以确定该物质是拟薄水铝石。随着pH的增大, 针状结构的生成量越来越少(图 1a, 1b, 1c), 意味着丝钠铝石在pH增大的情况下生成量越来越少, 当pH达到10.5后, 不再有针状结构生成(图 1c), 产品呈多颗粒聚集状。从图 1中可以看出, 在pH为10.5时产品的球状结构最多, 无针状结构, 性能最好, 与表 2中检测得到的数据一致。
 |
|
图 1 反应终点pH不同得到产品的微观结构图 Fig.1 Microstructure diagram of product in different pH at reaction end point 图 1a 反应终点 pH=9;图 1b 反应终点 pH=10; 图 1c 反应终点 pH=10. 5;图 1d 反应终点 pH=11 |
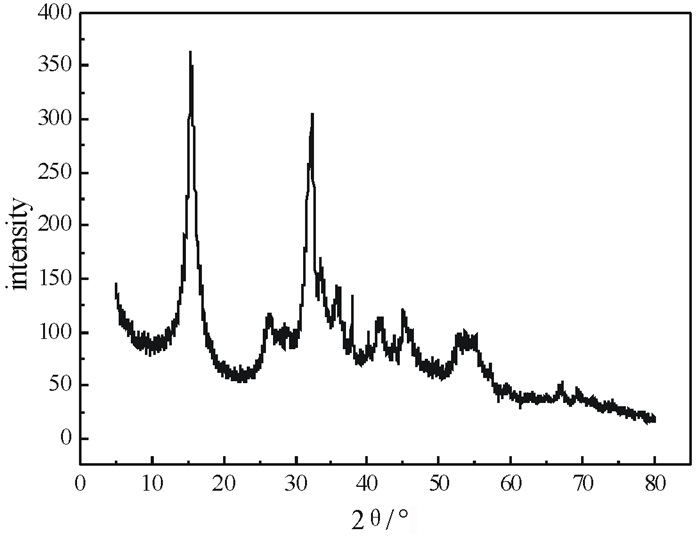 |
| 图 2 反应pH为9时得到的产品的XRD图 Fig.2 XRD patterns of products at pH=9 |
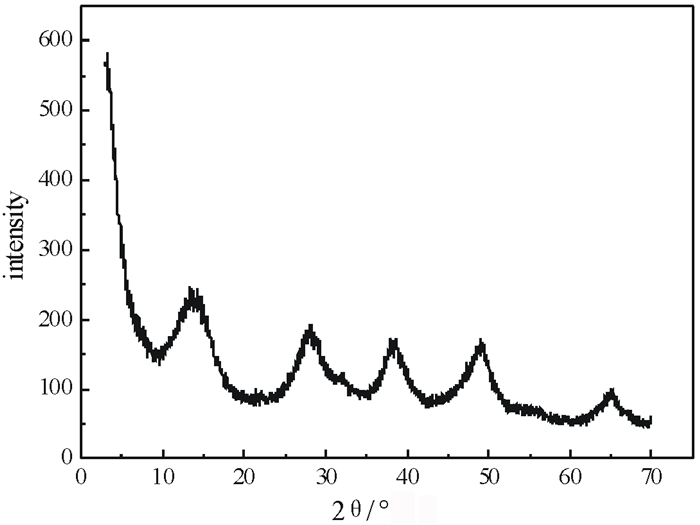 |
| 图 3 反应pH为10.5时得到的产品的XRD图 Fig.3 XRD patterns of products at pH=10.5 |
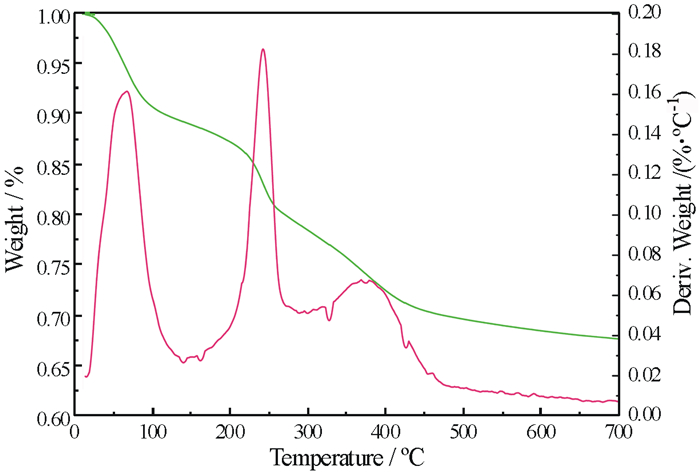 |
| 图 4 反应pH为10.5时产品的TG和DTG曲线 Fig.4 TG and DTG curves of products in pH=10.5 |
2.2 陈化时间的影响
控制反应终点pH为10.5, 制备出产品经过滤后将滤饼置于90 ℃烘箱中, 每隔1 h取一次样, 得到不同的陈化产品, 其产品性能如表 3所示。
| 表 3 陈化时间对产品性能的影响 Table 3 The effect of ageing time to product property |
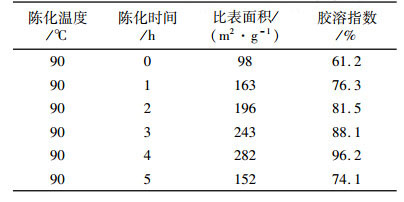 |
从表 3中的比表面积和胶溶指数的检测结果可以看出, 随着陈化时间的增加, 比表面积和胶溶指数先增大后减小, 当陈化时间为4 h时, 得到的产品的性能最好, 比表面积达到282 m2/g, 胶溶指数达到96.2%。
图 5是在陈化时间不同时得到的产品的微观结构图。从图 5中可以看出, 在未进行陈化时产品为片状结构, 如图 5a所示, 随着时间的变化, 产品表面由一个平面逐渐变为一个个多颗粒聚集状结构(图 5b, 5c), 开始时颗粒的直径较大(图 5b), 随着陈化时间的增加, 颗粒的直径逐渐减小, 但是, 在陈化时间超过4 h后, 颗粒的直径随着时间的增加又有所上升(图 5d)。从图 5中可以看出, 陈化时间4 h时产品的颗粒结构最多, 性能最好, 与表 3中检测得到的数据一致。
 |
|
图 5 陈化时间不同得到产品的微观结构图 Fig.5 Microstructure diagram of product in different ageing time 图 5a 陈化时间 0 h;图 5b 陈化时间 3 h; 图 5c 陈化时间 4 h;图 5d 陈化时间 5 h |
2.3 陈化温度的影响
控制反应终点pH为10.5, 制备出产品, 过滤后将滤饼置于不同温度的烘箱中, 陈化4 h, 得到不同的产品, 其产品性能如表 4所示。
| 表 4 陈化温度对产品性能的影响 Table 4 The effect of ageing temperature to product property |
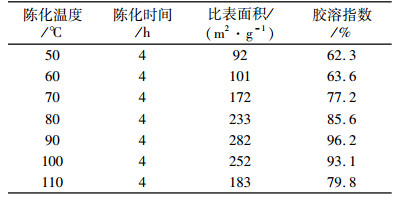 |
从表 4中的比表面积和胶溶指数的检测结果可以看出, 随着陈化温度的增加, 比表面积和胶溶指数先增大后减小, 陈化温度为90 ℃时得到的产品的性能最好, 比表面积可以达到282 m2/g, 胶溶指数达到96.2%。
图 6是在陈化温度不同时得到的产品的微观结构图, 从图 6中可以看出, 当温度较低时(图 6a)与原样(图 5a)相比几乎没有结构的变化, 可以认为在50 ℃时试样并未发生晶体的转变, 随着温度的提高, 80 ℃(图 6b)之后颗粒结构开始生成, 陈化已经发生, 随着温度增加, 颗粒结构的直径越来越小, 当温度达到100 ℃时有大量晶须状物质生成(图 6d)。而将其与陈化时间得到的结果进行对比, 在小于90 ℃的情况下(图 6a, 6b, 6c)可以发现随着陈化温度的提高, 产品结构(图 6a, 6b, 6c)分别达到相同温度陈化时间不同的产品结构(图 5a, 5b, 5c), 说明反应速度随着反应温度的增加而增加。当陈化温度达到100 ℃时有针状结构生成(图 6d), 但是反应时间的增加不会导致针状结构的生成, 同时, 与图 2进行对比, 虽然都是针状物质, 但是此时的反应终点pH较高, 不会有丝钠铝石的生成, 因此, 该现象的原因并不是生成了丝钠铝石而可能是温度高反应速度过快, 各个方向晶体长大速度不均衡导致了针状结构的产生, 陈化温度90 ℃时得到的产品的颗粒结构最多, 性能最好, 与表 4中的检测结果一致。
 |
|
图 6 不同陈化温度下产品的微观结构图 Fig.6 Microstructure diagram of product in different ageing temperature 图 6a陈化温度50 ℃;图 6b陈化温度80 ℃; 图 6c陈化温度90 ℃;图 6d陈化温度100 ℃ |
3 结论
(1) 当反应终点pH超过10.5时, 晶体结构为多颗粒聚集状结构, 随着反应终点pH的降低, 产品的粒径逐渐变小, 当反应终点pH低于10.5时, 有针状结构生成, 为丝钠铝石, 且随着反应终点pH的降低针状结构逐渐增多。
(2) 随着陈化温度的升高, 陈化的速度加快, 产品粒径由大变小, 当陈化温度超过90 ℃时, 反应表面有针状物质生成, 其原因是随着温度的增大反应速度增加, 晶体各个方向的长大速度差异过大, 导致针状物质的生成。
(3) 当反应终点pH为10.5、陈化时间4 h、陈化温度90 ℃时, 产品的比表面积可达到282 m2/g, 胶溶指数可达到96.2%, 溶液的沉淀率达到99.3%。
| [1] |
朱洪法. 催化剂载体制备及应用技术[M]. 北京: 石油工业出版社, 2014.
|
| [2] |
Tettenhorst R. Crystal chemistry of boehmite[J]. Clays & Clay Minerals, 1980, 28(5): 373-380. |
| [3] |
Cejka J. Organized mesoporous alumina:synthesis, structure and potential in catalysis[J]. Applied Catalysis A General, 2003, 254(2): 327-338. DOI:10.1016/S0926-860X(03)00478-2 |
| [4] |
徐向宇, 易淼, 孙建川, 等. 大比表面积大孔体积氧化铝的制备进展[J]. 石油化工, 2016, 45(3): 264-268. |
| [5] |
潘成强, 钱君律, 伍艳辉, 等. 硝酸法制备拟薄水铝石中温度影响研究[J]. 炼油与化工, 2004, 15(1): 21-22. |
| [6] |
伍艳辉, 方学兵, 钱君律, 等. 硝酸法制备拟薄水铝石过程中老化和洗涤条件的影响[J]. 现代化工, 2003, 23(s1): 176-178. |
| [7] |
彭绍忠, 王继锋. γ-氧化铝载体合成的研究[J]. 辽宁化工, 2003, 32(6): 241-243. |
| [8] |
张李锋, 石悠, 赵斌元, 等. γ-Al2O3载体研究进展[J]. 材料导报, 2007, 21(2): 67-71. |
| [9] |
唐国旗, 张春富, 孙长山, 等. 碳化法制备拟薄水铝石技术的研究进展[J]. 工业催化, 2011, 19(4): 21-25. |
| [10] |
杨清河, 李大东, 庄福成, 等. NaAlO2-CO2法制备拟薄水铝石规律的研究[J]. 石油炼制与化工, 1999(4): 59-63. |
| [11] |
魏先全, 李庆, 蔡雅娟, 等. 碳化法制备拟薄水铝石的正交实验研究[J]. 泸天化科技, 2008(3): 277-279. |
| [12] |
孟令利, 张丽, 李广战, 等. 碳酸化法制备拟薄水铝石的老化方法: CN105645446A[P]. 2016-06-08.
|
| [13] |
杨玉旺, 戴清, 高旭东. 制备条件对拟薄水铝石胶溶性的影响[J]. 广州化工, 2014(15): 122-124. DOI:10.3969/j.issn.1001-9677.2014.15.044 |
| [14] |
杨清河, 李大东, 庄福成, 等. NaAlO2-CO2法制备拟薄水铝石过程中的转化机理[J]. 催化学报, 1997, 18(6): 478-482. |
 2018
2018 


