| 铜冶炼渣湿法处理技术研究进展 |
2. 省部共建复杂有色金属资源清洁利用国家重点实验室,云南 昆明 650093
2. State Key Laboratory of Complex Nonferrous Metal Resources Clean Utilization, Kunming 650093, China
我国的年均铜消耗量一直处于快速增长之势,铜产量也随之不断增长,产生的含铜炉渣数量不容小觑。一方面,多数铜渣中仍含有铁、锌及少量铜等有价元素,甚至含有金、银、铅和镍等贵金属,不加以利用会造成资源的巨大浪费;另一方面,国内对这些铜炉渣主要是进行露天堆放处理,大量铜渣的堆存,既占用土地又污染环境[1]。在铜资源逐渐减少和环保压力不断增大等问题日益突出的形势下,如何做到以节约金属资源、保护环境、增加经济效益为前提,对铜渣中的有价金属元素进行回收利用就显得尤为重要。
本文中所指的铜渣一律为火法铜冶炼渣,按照火法冶炼工艺可将铜渣分为熔炼渣、精炼渣、吹炼渣和贫化渣。针对铜渣中主要有价金属的综合利用,目前国内外已开发出的较有效的处理方法主要分为以下几种:火法冶炼、选矿法和湿法浸出。火法冶炼多数情况下耗能大、成本高,弃渣的铜品位仍高于当前开采出的矿石平均铜品位[2];选矿法因回收率高、生产稳定、尾渣含铜可控制在0.30%以内等优点已得到广泛应用[3],但往往存在着所获精矿含硅量偏高、质量差等问题;随着铜渣处理技术的不断进步,湿法浸出无论在实验室规模上还是在实际生产中都取得了快速发展,与其他工艺相比,具有能耗低、污染小、可回收多种金属等优点[4],用来处理低品位铜渣更为适当。因此,本文对湿法浸出铜冶炼渣的技术现状进行了综述。
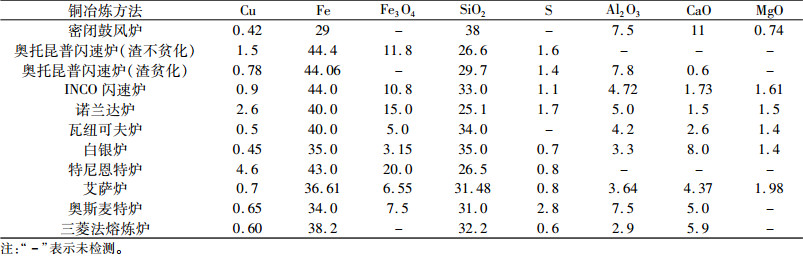
1 铜渣物相组成铜冶炼渣一般呈黑色或黑绿色,大部分致密而坚硬,渣中铁的物相主要表现为铁橄榄石和磁铁矿及少量的磁黄铁矿;铜的物相主要表现为硫化物、金属铜和少量的氧化铜。铁橄榄石和磁铁矿常与铜嵌布在一起,或铜呈球状被磁铁矿所包裹,这是导致铜渣中铜与铁分离困难的主要原因。铜冶炼渣的典型成分为Fe 29%~40%、SiO2 30%~40%、Al2O3≤10%、CaO≤11%、Cu 0.42%~4.6%[5]。通过不同熔炼方法产生的铜渣化学组成见表 1[6]。
| 表 1 各种典型冶炼方法产生铜渣的化学组成[6] /% Table 1 Chemical compositions of copper slag produced by various typical smelting methods |
 |
2 国内外湿法浸出处理铜渣的研究现状
湿法浸出是指浸出剂与铜渣中的有价金属元素发生化学效应,再进行萃取、分杂、提取出金属及其化合物,将铜渣中有价金属加以回收利用[7]。湿法浸出主要可分为直接浸出、间接浸出和微生物浸出。直接浸出包括酸浸出、氧压酸浸出、碱浸、氨浸以及氯浸等工艺;间接浸出是指用适当的预处理方式,将铜渣中的金属赋存相进行相应的改性,使得铜冶炼炉渣更便于回收及分离,预处理方法主要包括还原焙烧、硫酸化焙烧和氯化焙烧。浸出剂种类有酸性浸出剂、碱性浸出剂、氨水以及氯气等[8]。硫酸和盐酸是常用的酸性浸出剂;而微生物浸出指通过向铜渣中添加选择性较强的某一类细菌或真菌对铜渣中的有价金属进行一系列的浸出反应,从而使目的金属溶解的过程。
2.1 直接浸出 2.1.1 酸浸出采用酸浸出剂直接将铜渣中的有价金属浸出回收,常用的酸浸出剂包括硫酸、盐酸和硝酸。此工艺是较传统的浸出方式之一,存在着反应时间长、浸出率低等问题。
陈茂生[9]等对-0.074 mm的水淬渣进行了酸浸试验,在浸出温度70 ℃、硫酸浓度2.5 mol/L、液固比4:1的条件下,浸出120 min后,铜和锌的浸出率分别达到76.2%和98.3%,此时两者的浸出率达到最高。刘红斌等[10]采用硫酸直接浸出法回收转炉渣中的钴,研究表明:在浸出过程中,钴和铁的浸出率紧密相关,随着铁浸出率的提高,钴的浸出率也随之提高。采用直接酸浸,铜的浸出效果不理想,且酸浸易与铜渣中的硅酸盐类矿物形成胶状物,难于分离。充氧气可提高铜金属的浸出率。在物料粒度-0.074 mm含量≥90%,浸出温度85~90 ℃,硫酸浓度(25±5)%,液固比6:1,搅拌速度200~350 r/min,浸出时间1.5~2 h,每克矿通入0.8~1.6 L/h空气量的条件下,铜、钴和铁的浸出率分别超过90%、98%和98%。
在酸浸过程中,钙、镁和铁等不希望被浸出的元素容易发生溶解而导致试剂消耗量增大,对经济产生不利影响;另一个不利的因素是二氧化硅,其在浸出过程中易形成硅胶。
为了改善浸出效果,近年来国内外研究者们选择向浸出过程中添加氧化剂,比如:双氧水、液氨、氯酸钠等,用以加速有价金属元素的溶解。孙建军[11]等以硫酸作为浸出剂,开展了氧化剂(双氧水)添加量对常压氧化条件下铜浸出率影响的研究。结果表明:在未添加双氧水的情况下,铜的浸出率较低,硫化铜几乎不溶;随着双氧水的不断加入,铜的浸出率显著增加,氧化剂(双氧水)添加量增加到400 mL/kg时,铜的浸出效果最佳,浸出率为91.2%。亓传铎等[12]在浸出过程中加入氧化剂氯酸钠,在电位稳定在420~450 mV,持续反应8 h后,铜渣中的贱金属和杂质溶解,而金、银几乎全部留在渣中,损失较少,实现铜渣有价金属元素之间的有效分离。黄自力等[13]通过加入氧化剂H2O2实现除铁提铜的效果,铜渣中的铁溶解会对渣中铜浸出带来不利影响,添加H2O2可抑制铁的浸出,促进铜的浸出。结果表明:在温度60 ℃、搅拌速度500 r/min、浸出时间30 min、硫酸浓度60 g/L、双氧水用量100 L/t的条件下,铜的浸出率达到66.9%。
渣中铁消耗硫酸反应式如下:
| $ \text{FeO}+{{\text{H}}_{2}}\text{S}{{\text{O}}_{4}}\to \text{FeS}{{\text{O}}_{4}}+{{\text{H}}_{2}}\text{O} $ | (1) |
向浸出过程中添加双氧水,化学反应式如下:
| $ 2\text{CuS}+7{{\text{H}}_{2}}\text{S}{{\text{O}}_{4}}+{{\text{H}}_{2}}{{\text{O}}_{2}}\to 2\text{CuS}{{\text{O}}_{4}}+7{{\text{H}}_{2}}\text{S}{{\text{O}}_{3}}+{{\text{H}}_{2}}\text{O} $ | (2) |
| $ 2\text{FeS}{{\text{O}}_{4}}+{{\text{H}}_{2}}{{\text{O}}_{2}}+2{{\text{H}}_{2}}\text{O}\to 2\text{FeOOH}+2{{\text{H}}_{2}}\text{S}{{\text{O}}_{4}} $ | (3) |
浸出过程中添加氧化剂可起到调控浸出体系电位的作用,高电位有利于铜的浸出。氧化剂能与铜渣中的某些金属发生氧化还原反应,使其他金属与目的金属发生分离,对提高铜浸出率起到了促进作用。
酸浸出是较传统的浸出方式,其利用浸出剂直接对铜渣进行浸出处理,所需设备条件简单、操作方便,但此法在浸出过程中因缺少药剂或其他工艺条件的辅助,导致试验耗时长、浸出效果不明显、有价金属回收率偏低等问题。通入氧化剂可使不同金属的电位变化,铜渣中的贵贱金属得以有效分离,加速浸出过程中有价金属元素溶解、浸出率提高、浸出效果明显,然而氧化剂在浸出过程中与金属反应时间较长、耗量大,且多数价格昂贵、成本高。
2.1.2 氧压酸浸出针对上述酸浸出存在的一系列缺点,研究者们提出了一种加氧压酸浸出工艺,以降低酸耗,缩短浸出时间。与传统酸浸出工艺相比,氧压酸浸出工艺流程短,浸出效率高,且一般所用的氧化剂多为通入的氧气,因此,此法排放的多余有害物质少,对环境的污染小。
Anand等[14]采用氧压酸浸法,利用氧化和水解作用降低铁的溶解,从而最大限度地分离和回收转炉渣中的铜、镍和钴。在最佳条件下, 铜、镍和钴的浸出率分别达到90%、95%和95%,而铁的浸出率仅有0.8%,取得了良好的分离效果。张永平等[15]采用硫酸氧压浸出含铜转炉渣中的铜,结果表明:在压力0.4 MPa,硫酸初始浓度150 g/L,浸出温度70 ℃,液固比3:1,压缩空气流量0.2 Nm3/h,浸出时间4 h的条件下,铜的浸出率>97%,而炉渣中的绝大部分砷经沉淀在浸出渣中得到富集,有效地回收了铜渣中的砷。
酸浸渣中残留的砷可导致酸耗高,设备腐蚀严重等问题。由此可知,铜渣浸出过程中砷的提取显得十分必要。采用常规的酸浸出难以回收铜冶炼渣中的铜,而氧压酸浸技术在充氧的基础上利用加压实现了对铜渣中砷元素的有效回收利用。但氧压酸浸法可浸出多种有价金属,加大了后续分离提纯的难度,且伴随高资本投入,因此,此法对处理铜冶炼炉渣的研究较少,更适合富矿石的处理,一般在钒钛渣和铜转炉白烟灰中的研究较多。有时也采用碱性浸出以降低Fe、Mg和Ca的高溶解度,但目前国内外对于碱浸出的研究较少,且其对于有价金属的浸出率较酸性浸出低,关于碱浸对多金属废料浸出的研究非常有限。
2.1.3 碳氨-氨体系浸出氨作为有效的浸出剂,已被广泛用于湿法冶金工艺多年。其一方面减少了酸浸过程中的几种腐蚀问题;另一方面,在多数情况下氨浸过程中可去除不溶性的氧/羟基化合物,将Fe的消耗降至最低,从而铜渣中的有价金属与活性含氮基团生成可溶性氨络合物,大大提高了浸出率。
郭勇等[16]采用氨水+碳酸铵溶液湿法浸出贫化炉水淬渣中的铜。首先采用振动研磨将水淬渣粒度降至-0.147 mm,接着在氨水质量浓度60 g/L、碳酸铵添加量与铜渣质量比1:2.5、浸出时间4.0 h的条件下,铜的浸出率达到45%,氨浸溶液中铜的硫化钠沉淀率达到89%。刘慧等[17]进行了重选—酸浸联合流程和重选—氨浸联合流程的对比试验。结果表明:重选—酸浸法获得了57.09%的总回收率,而重选—氨浸法配合助剂使用的条件下,获得了61.54%的总回收率。因此,采用氨浸法效果更好,其总回收率比酸浸法提髙了3%,同时又避免了脉石矿物对酸液的消耗。Bidari等[18]采用硫化铵浸出法回收铜渣中的铜。其中,温度和搅拌速度对铜浸出的影响最为显著,而氨则影响低浓度下的浸出产率。同时,对数据进行了缩芯模型的动力学分析,研究发现:浸出过程是由界面转移和产物层扩散所控制,活化能为49.4 kJ·mol-1。在温度70 ℃、时间4 h、2 mol/L NH3、pH值10.5、搅拌速度900 r/min和矿浆浓度10%(Ws/V)的最佳条件下,Cu的浸出率达到78%。Nadirov等[19]研究了氨溶液处理铜冶炼渣的可行性,采用CCRD和近似法确定了回收铜冶炼渣中锌和铜的最佳条件。实验设计在四个操作参数的五个水平下进行,即NH3的初始浓度、初始Cl-离子浓度、浸出时间和固液比。试验获得了描述金属回收率对操作参数依赖性的两个数学模型,两个模型成功地预测了响应,发现回收锌的最佳工艺参数为:初始CNH317.1%、初始CCl-160 g/L、浸出时间4.56 h和固液比0.39;回收铜的最佳工艺参数为:初始CNH319.9%,初始CCl-160 g/L、浸出时间4.13 h,固液比0.53。结果表明:两者在各自的最佳条件下获得的最大浸出率分别达到81.16%和56.48%。
氨水浸出过程中,铜及其化合物可能与氨水溶液发生的反应式如下[16]:
| $ \begin{align} & 2\text{Cu}+{{\left( \text{N}{{\text{H}}_{4}} \right)}_{2}}\text{C}{{\text{O}}_{3}}+2\text{N}{{\text{H}}_{3}}+0.5{{\text{O}}_{2}}= \\ & \ \ \ \ \ \ \ \ \text{C}{{\text{u}}_{2}}{{\left( \text{N}{{\text{H}}_{3}} \right)}_{4}}\text{C}{{\text{O}}_{3}}+{{\text{H}}_{2}}\text{O} \\ \end{align} $ | (4) |
| $ \text{CuO}+{{\left( \text{N}{{\text{H}}_{4}} \right)}_{2}}\text{C}{{\text{O}}_{3}}+2\text{N}{{\text{H}}_{3}}=\text{Cu}{{\left( \text{N}{{\text{H}}_{3}} \right)}_{4}}\text{C}{{\text{O}}_{3}}+{{\text{H}}_{2}}\text{O} $ | (5) |
| $ \text{Cu}+\text{Cu}{{\left( \text{N}{{\text{H}}_{3}} \right)}_{4}}\text{C}{{\text{O}}_{3}}=\text{C}{{\text{u}}_{2}}{{\left( \text{N}{{\text{H}}_{3}} \right)}_{4}}\text{C}{{\text{O}}_{3}} $ | (6) |
| $ \begin{matrix} \text{C}{{\text{u}}_{2}}{{\left( \text{N}{{\text{H}}_{3}} \right)}_{4}}\text{C}{{\text{O}}_{3}}+{{\left( \text{N}{{\text{H}}_{4}} \right)}_{2}}\text{C}{{\text{O}}_{2}}+2\text{N}{{\text{H}}_{3}}+ \\ 0.5{{\text{O}}_{2}}=2\text{Cu}{{\left( \text{N}{{\text{H}}_{3}} \right)}_{4}}\text{c}{{\text{O}}_{3}}+{{\text{H}}_{2}}\text{O} \\ \end{matrix} $ | (7) |
| $ 2\text{Cu}+8\text{N}{{\text{H}}_{3}}+2{{\text{H}}_{2}}\text{O}+{{\text{O}}_{2}}=2\left[ \text{Cu}{{\left( \text{N}{{\text{H}}_{3}} \right)}_{4}}{{(\text{OH})}_{2}} \right] $ | (8) |
学者们对含铜氧化物和硫化物矿石的氨浸已经进行了大量研究,但由于矿渣的不同和复杂的矿物学组成,氨浸法处理铜炉渣还存在挥发损失量大、易对现场造成污染、选择性差等问题;但是此法的铜回收率较高,无需高温高压,工艺流程简便,生产成本低,为此今后的应用前景广阔。
2.1.4 氯气浸出国内外学者对氯气浸出的研究一直较少,这主要是源于氯气浸出仅对铜渣中的硫化铜矿物具有较好的浸出效果,局限性较大,且浸出过程中产生的氯气不易处理。
Herreros等[20]开展了氯气浸出法回收反射炉和闪速炉炉渣中的铜。结果表明,几乎所有粒径 < 20 μm的硫化物相的铜都可以采用氯气浸出,铜的浸出率达到80%~90%,铁的溶解度为4%~8%。实验中使用的氯气是通过工业次氯酸钠与盐酸或硫酸反应生成的,反应式如下:
| $ \text{NaOCl}+2\text{HCl}\to \text{C}{{\text{l}}_{2}}+\text{NaCl}+{{\text{H}}_{2}}\text{O} $ | (9) |
| $ \text{NaOCl}+\text{NaCl}+{{\text{H}}_{2}}\text{S}{{\text{O}}_{4}}\to \text{C}{{\text{l}}_{2}}+\text{N}{{\text{a}}_{2}}\text{S}{{\text{O}}_{4}}+{{\text{H}}_{2}}\text{O} $ | (10) |
Bese等[21]采用田口方法在饱和氯气水中进行实验。水介质中氯气溶解转炉渣中的铜、铁和锌,其浸出率分别为98.5%、8.97%和25.17%。李泰康等[22]在酸性条件下采用氯气浸出法回收炉渣中的铜、锡、铅和锌。结果表明:反应温度和氯气量对铜渣中金属元素的浸出率影响较大,在最优条件下,锡的浸出率≥82%,铜、铅和锌的浸出率均≥96%。Nadirov等[23]采用氯化铵热处理回收某铜厂铜冶炼渣中的有价金属。结果表明:时间120 min,温度320 ℃,锌和铜的浸出率分别达到91.5%和89.7%。在所研究的温度条件下,铁回收过程中对温度的敏感程度比锌和铜的回收过程更高,对氯化铵浸出后的残渣再次进行氯化铵热处理,最终获得了88.3%的铁总回收率。Olteanu等[24]采用湿法氯化浸出,以新生氯气为浸出剂,在盐酸存在的条件下对HNO3预处理后的固相铜炉渣进行了选择性浸出。结果表明:常温下反应6 h,液固比1:2,盐酸用量4 mL,金的浸出率达到98%。
采用氯气浸出渣中铜可获得高浸出率。但在浸出过程中,一定时间内铁的浸出率较低,随着浸出时间的延长,氯气的消耗量增加,溶液中铁的溶解也会随之增加,与铜一起被浸出,不利于铜渣中各金属之间的分离与回收。因此,如何合理控制浸出时间是需要试验确定的。
2.2 间接浸出对难浸的铜冶炼渣需要适当的预处理,这样可使铜渣中的有价金属转化成各种可溶性盐类,可有效缩短浸出时间,提高有价金属浸出率[25]。焙烧预处理可分为还原焙烧、硫酸化焙烧和氯化焙烧。其中,硫酸化焙烧是最常见的方法,铜渣焙烧后直接用水浸出[26]。
2.2.1 还原焙烧—浸出法在还原焙烧中,熔渣中各种形式的金属被还原成游离金属,然后用浸出工艺回收其中的金属[27, 28]。
Rudnik等[29]采用连续阶段反应从铜转炉渣中选择性地回收铜和钴,同时对合金溶解的机理进行了探究。在添加还原剂(焦粉2.7%和生铁2.0%)和焙烧温度1 425~1 570 ℃的还原条件下炉渣生成Cu-Co-Fe-Pb合金,将此合金在氨-铵盐溶液中电解,电解过程中铁留在阳极泥中,而铜和钴存在于阳极泥、电解质和阴极沉积物中,实现了铜和钴的高纯度选择性回收。最终得到了纯度分别为99.9%和92%的铜和钴。詹保峰等[30]采用焙烧—浸出—磁选法回收铜炉渣中的铁。以碳粉作为还原剂,向铜炉渣中添加20%碳酸钠,在焙烧温度900 ℃、焙烧时间1.5 h的条件下将焙砂磨细至-0.074 mm含量≥90%,用浓度为18.7%的硫酸浸出,浸出渣经480 kA/m的磁选,铁精矿的品位和回收率分为达到61.52%和82.26%。
炉渣还原焙烧预处理可大幅度降低浸出剂用量,并可提高金属总回收率。但铜渣经还原焙烧后有价金属通常以合金形式存在,不利于后续浸出过程,。因此,近年来还原焙烧—浸出法应用甚少。
2.2.2 硫酸化焙烧—水浸法硫酸化焙烧,将含各种相的Cu、Co和Ni炉渣与硫化物或硫酸盐试剂混合,然后在高温下反应后可得到可溶性硫酸盐[31-35],再用水浸出这些可溶性硫酸。用于焙烧的硫化物和硫酸盐试剂主要包括H2S、H2SO4、(NH4)2SO4、Fe2(SO4)3xH2O和黄铁矿[27]。
Dimitrijevic等[36]采用两步提取法从反射炉炉渣中回收铜和铁。首先在150~800 ℃的温度下添加硫酸对炉渣进行焙烧,接着用蒸馏水浸出,结果表明:铜和铁在焙烧过程中溶解的速度非常快,在最初几分钟即可达到完全溶解,铜的回收率最大可达到94%。Arslan等[37]采用硫酸化焙烧和热水浸出相结合的方法从铜冶炼炉和转炉渣中回收铜、钴和锌。在浸出前首先对铜渣进行了热分解作用,从浸出物的金属回收率来看,此过程由于没有铁的溶解,有利于有价金属的分离,但随着焙烧温度升高和时间的延长,铜的溶解度增加。在温度150 ℃、酸渣比3:1、焙烧时间2 h的条件下,分别得到了回收率为88%、87%、93%和83%的铜精矿、钴精矿、锌精矿和铁精矿。
硫酸化焙烧—水浸法易生成溶于水的多金属硫酸盐,需进一步的分离与提纯,并且铁会与铜一起浸出出来,这对后续的浸出液处理是不利的。但硫酸化焙烧—水浸法具有高浸出率,可浸出多种有价金属元素,此法现阶段虽研究较少,但具有广阔的应用前景。氯化焙烧—浸出法能有效地回收铜渣中的铁资源,研究发现铜渣中的高价铁氧化物难以发生氯化反应,铁的氯化损失率较少,而铜的氯化挥发率却很高。因此,通过氯化焙烧可实现铜渣的选择性分离。但氯化焙烧的焙烧温度要比硫酸化焙烧温度高,能耗大。采用氯化焙烧浸出法处理铜冶炼渣的研究极少。
2.3 微生物浸出利用微生物对某些有价金属的生物氧化作用,使金属以离子形式进入到溶液中,再从浸出液中回收有价元素。
Muravyov等[38]研究了用硫酸溶液从铜转炉渣中浸出铜、锌和铁。在不降低嗜酸的化能自养微生物活性的前提对铁进行氧化,微生物在溶液中浸出矿渣。在温度70 ℃、浸出溶液Fe3+的初始浓度10.1 g/L、浆料的固相含量10%的工艺条件下,铜和锌的浸出率分别达到89.4%和39.3%。在此过程中主要发生以下化学反应[38]:
生物氧化得到的硫酸铁溶液浸出金属(M表示金属):
| $ \text{MS}+2\text{F}{{\text{e}}^{3+}}={{\text{S}}^{0}}+{{\text{M}}^{2+}}+2\text{F}{{\text{e}}^{2+}} $ | (11) |
各种嗜酸化能自养微生物导致Fe3+氧化再生成:
| $ 4\text{F}{{\text{e}}^{2+}}+4{{\text{H}}^{+}}+{{\text{O}}_{2}}=4\text{F}{{\text{e}}^{3+}}+2{{\text{H}}_{2}}\text{O} $ | (12) |
Georgiev等[39]在振荡器和搅拌槽的烧瓶中利用化能自养微生物(细菌和古生菌)对铜渣进行浸出。根据细菌的生长和活性的最适宜温度,使用了3个不同种类的化学无机营养类型:(1)在35 ℃下的中温细菌和铁原体属的嗜酸古生菌;(2)在55 ℃下的中度嗜热细菌;(3)在75 ℃下的极度耐热古生菌。结果表明:在矿浆浓度较低(6%~8%)的情况下,古生菌对矿渣的浸出率高于细菌,但在较高的矿浆浓度(10%~20%)下,中度嗜热细菌的效率更高。Tuovinen等[40]分别用含有和不含有嗜中温的铁硫氧化细菌的硫酸盐溶液浸出熔炼炉渣中的铜和锌试验。在温度27 ℃、矿浆浓度10%的同等条件下,向以酸性矿井水为原料的试验培养基分别添加4.5 g/L Fe2+和10 g/L S0无机盐进行了对比试验。结果表明:以S0为基底时生物的浸出率最高,生物浸出的效率取决于添加的S0形成的H2SO4,且浸出来的金属不影响细菌的活性。铜和锌的浸出率分别为68%和3.7%。
目前国内外学者对于微生物浸出工艺已有所研究,微生物浸出虽存在反应速度慢、浸出周期长等缺点,但具备流程短、成本低、设备简单、污染小等优点,应用前景较广阔。
3 结语浸出法处理铜渣的研究方向是制定清洁环保、低耗能、高效率的工艺,提高铜渣中金属的综合回收利用率。
(1) 在湿法提铁研究中,加压酸浸能够抑制铁的浸出,氯化焙烧可使铜和铁实现选择性分离。随着技术的进步,未来湿法提铁、资源化利用铜渣具有广阔的应用前景。
(2) 目前微生物浸出发展进程迅速,对重金属的分离提取及富集有着显著的成效,是最具有前途的新型清洁生态友好技术之一。因此,筛选适用于铜渣浸出的菌种,寻找适宜微生物培养与驯化的条件是今后生物浸出研究热点。
(3) 湿法浸出回收铜渣中的伴生金属效果较好。一方面,应继续加强对热力学和动力学的研究,以期从铜渣中回收其他有价金属。另一方面,寻找更有效、选择性更高的氧化剂及浸出剂,减少药剂用量,以及减少对设备的腐蚀。
| [1] |
余志翠. 选矿技术在铜渣综合利用中的应用[J]. 中国高新技术企业, 2016(28): 157-158. |
| [2] |
王福坤, 黄自力, 高斯, 等. 经改性的电炉贫化铜渣的酸浸-弱磁选试验[J]. 金属矿山, 2018(1): 193-196. |
| [3] |
付强, 马楠. 影响江西某闪速炼铜渣在选矿过程中铜、砷分离的矿物学因素探讨[J]. 有色金属(选矿部分), 2017(6): 1-4. DOI:10.3969/j.issn.1671-9492.2017.06.001 |
| [4] |
郭秀键, 倪晓明, 马丁, 等. 铜渣处理与综合利用[J]. 有色冶金设计与研究, 2017, 38(2): 23-26. DOI:10.3969/j.issn.1004-4345.2017.02.008 |
| [5] |
周松林. 铜冶炼渣选矿[M]. 冶金工业出版社, 2014: 6-7.
|
| [6] |
朱心明, 陈茂生, 宁平, 等. 铜渣的湿法处理现状[J]. 材料导报, 2013, 27(S2): 280-284. |
| [7] |
廖亚龙, 叶朝, 王祎洋, 等. 铜冶炼渣资源化利用研究进展[J]. 化工进展, 2017, 36(8): 3066-3073. |
| [8] |
Basir SMA, Rabah MA. Hydrometallurgical recovery of metal values from brass melting slag[J]. Hydrometallurgy, 1999, 53(1): 31-44. DOI:10.1016/S0304-386X(99)00030-4 |
| [9] |
陈茂生, 朱心明, 许燕, 等. 除硅铜冶炼水淬渣的硫酸化浸出实验[J]. 材料导报, 2014, 28(18): 86-89. |
| [10] |
刘红斌, 蒋伟, 蒋训雄, 等. 铜转炉渣湿法回收钴[J]. 有色金属(冶炼部分), 2012(2): 19-22. DOI:10.3969/j.issn.1007-7545.2012.02.005 |
| [11] |
孙建军, 黄自力, 杨蘖, 等. 铜冶炼渣硫酸浸出回收铜试验研究[J]. 矿产综合利用, 2017(6): 102-107. DOI:10.3969/j.issn.1000-6532.2017.06.022 |
| [12] |
亓传铎, 牌洪坤, 杨守斌, 等. 从冶炼铜渣中进一步提取金银的湿法工艺研究[J]. 黄金科学技术, 2012, 20(5): 88-91. DOI:10.3969/j.issn.1005-2518.2012.05.015 |
| [13] |
黄自力, 刘缘缘, 秦庆伟, 等. 反射炉水淬渣提铜除铁研究[J]. 矿冶工程, 2012, 32(5): 82-85, 89. |
| [14] |
AnandS, 沈洪. 采用加压稀硫酸浸出法从铜炉渣中提取钴、镍和铜[J]. 湿法冶金, 1984(2): 39-42. |
| [15] |
张永平, 雷华志, 周娴, 等. 含铜转炉渣加压酸浸回收铜的试验研究[J]. 有色金属工程, 2017, 7(3): 51-54. DOI:10.3969/j.issn.2095-1744.2017.03.011 |
| [16] |
郭勇, 秦庆伟, 汤海波, 等. 从贫化炉水淬渣中氨浸提铜试验研究[J]. 湿法冶金, 2016, 35(4): 320-323. |
| [17] |
刘慧, 王路平, 臧文优, 等. 新疆某古炼铜炉渣回收铜探索试验研究[J]. 有色金属(选矿部分), 2015(1): 72-75. DOI:10.3969/j.issn.1671-9492.2015.01.017 |
| [18] |
Bidari E, Aghazadeh V. Investigation of copper ammonia leaching from smelter slags:characterization, leaching and kinetics[J]. Metallurgical & materials transactions B, 2015, 46(5): 1-10. |
| [19] |
Nadirov R, Syzdykova L, Zhussupova A. Copper smelter slag treatment by ammonia solution:leaching process optimization[J]. Journal of Central South University, 2017, 24(12): 2799-2804. DOI:10.1007/s11771-017-3694-3 |
| [20] |
Herreros O, Quiroz R, Manzano E, et al. Copper extraction from reverberatory and flash furnace slags by chlorine leaching[J]. Hydrometallurgy, 1998, 49(1/2): 87-101. |
| [21] |
Bese AV, Ata ON, Celik C, et a1. Determination of the optimum conditions of dissolution of copper in converter slag with chlorine gas in aqueous media[J]. Chemical engineering and processing, 2003, 42(4): 291-298. |
| [22] |
李泰康. 氯化法回收鼓风炉炼铜炉渣中有价金属[J]. 有色金属(冶炼部分), 2001(4): 8-10, 15. DOI:10.3969/j.issn.1007-7545.2001.04.003 |
| [23] |
Nadirov RK, Syzdykova LI, Zhussupova AK, et al. Recovery of value metals from copper smelter slag by ammonium chloride treatment[J]. International journal of mineral processing, 2013, 124(22): 145-149. |
| [24] |
Olteanu AF, Dobre T, Panturu E, et al. Experimental process analysis and mathematical modeling for selective gold leaching from slag through wet chlorination[J]. Hydrometallurgy, 2014, 144-145(4): 170-185. |
| [25] |
王红梅, 刘四清, 刘文彪. 国内外铜炉渣选矿及提取技术综述[J]. 铜业工程, 2006(4): 19-22. DOI:10.3969/j.issn.1009-3842.2006.04.006 |
| [26] |
赖祥生, 黄红军. 铜渣资源化利用技术现状[J]. 金属矿山, 2017(11): 205-208. DOI:10.3969/j.issn.1001-1250.2017.11.040 |
| [27] |
Shen H, Forssberg E. An overview of recovery of metals from slags[J]. Waste Management, 2003, 23(10): 933-49. DOI:10.1016/S0956-053X(02)00164-2 |
| [28] |
Virčíková E, Molnár L. Recovery of copper from dump slag by a segregation process[J]. Resources conservation & recycling, 1992, 6(2): 133-138. |
| [29] |
Rudnik E, Burzyńska L, Gumowska W. Hydrometallurgical recovery of copper and cobalt from reduction-roasted copper converter slag[J]. Minerals engineering, 2009, 22(1): 88-95. DOI:10.1016/j.mineng.2008.04.016 |
| [30] |
詹保峰.奥斯麦特炼铜炉渣改性及铜铁回收的研究[D].武汉: 武汉科技大学, 2015. http://cdmd.cnki.com.cn/Article/CDMD-10488-1015582435.htm
|
| [31] |
Tümen F, Bailey NT. Recovery of metal values from copper smelter slags by roasting with pyrite[J]. Hydrometallurgy, 1990, 25(3): 317-328. DOI:10.1016/0304-386X(90)90047-6 |
| [32] |
Candan Hamamci, Berrin Ziyadanog Ullari. Effect of roasting with ammonium sulfate and sulfuric acid on the extraction of copper and cobalt from dopper donverter slag[J]. Separation science, 1991, 26(8): 1147-1154. DOI:10.1080/01496399108050520 |
| [33] |
Recep Ziyadanog Ullari. A new method for recovering Fe(Ⅱ) sulfate, copper, and cobalt from converter slag[J]. Separation science, 1992, 27(3): 389-398. DOI:10.1080/01496399208018888 |
| [34] |
Berrin Ziyadanog Ullari. Recovery of copper and cobalt from concentrate and converter slag[J]. Separation science & technology, 2000, 35(12): 1963-1971. |
| [35] |
Altundoğan HS, Tümen F. Metal recovery from copper converter slag by roasting with ferric sulphate[J]. Hydrometallurgy, 1997, 44(1-2): 261-267. DOI:10.1016/S0304-386X(96)00038-2 |
| [36] |
Dimitrijevic MD, Urosevic DM, Jankovic ZD, et al. Recovery of copper from smelting slag by sulphation roasting and water leaching[J]. Physicochemical problems of mineral processing, 2016, 52(1): 409-421. |
| [37] |
Arslan C, Arslan F. Recovery of copper, cobalt, and zinc from copper smelter and converter slags[J]. Hydrometallurgy, 2002, 67(1): 1-7. |
| [38] |
Muravyov MI, Fomchenko NV. Leaching of nonferrous metals from copper converter slag with application of acidophilic microorganisms[J]. Applied biochemistry & microbiology, 2013, 49(6): 562-569. |
| [39] |
Georgiev P, Nicolova M, Spasova I, et al. Leaching of valuabe metals from copper slag by means of chemolithotrophic archaea and bacteria[J]. Journal of mining and geological sciences, 2017, 60: 127-130. |
| [40] |
Tuovinen OH, Särkijärvi S, Peuraniemi E, et al. Acid leaching of Cu and Zn from a smelter slag with a bacterial consortium[J]. Advanced materials research, 2015, 1130: 660-663. DOI:10.4028/www.scientific.net/AMR.1130.660 |
 2019
2019



