| 铝灰中铝及其氧化物回收方法现状 |
铝灰产生于金属铝的熔炼或电解铝工艺中,由铝熔体表面的不熔混合物及其与添加剂反应生成的物质组成[1-5]。根据欧洲危险废物目录[6],铝灰被归类为有毒和危险废物。直接堆存铝灰不但占用大量耕地,而且其盐分会缓慢积聚在土壤中而导致盐碱化,扰乱周围植物根系正常生理活动[7]。铝灰中的钡、铬、铅也会导致土壤重金属超标,污染地下水。因为铝灰中含有大量AlN,与水反应会产生氨气,污染空气[8-9]。
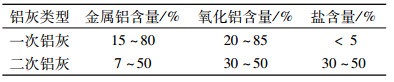
铝灰的分类及其组成参见表 1[10]。铝灰组成非常复杂,主要含有Al、Cl、Na、N等元素。铝灰包括一次铝灰和二次铝灰,一次铝灰可作为二次铝工业的原料,二次铝灰可以从各种铝的废弃物中提取铝后得到[11-12]。与一次铝灰相比,二次铝灰中金属铝的含量较低,氟和氯含量较高,环境危害更大,二次铝灰的无害化处理和回收尤为重要。
| 表 1 铝灰的类型和组成 Table 1 Type and composition of aluminum dross |
 |
不同于其他重金属熔炼产生的炉渣,铝灰一般呈松散的灰状[1]。当铝灰中存在的金属高于70%时,铝灰由松散转变为致密状[13]。Meshram等[10]研究了铝灰混合物的渗透性以及体积收缩率等物理性能,使用50%~90%一次铝灰、膨润土和一定比例水混合而成砖样品。实验结果证明了铝灰混合物的渗透率随着颗粒尺寸的减小而增加[14],而体积收缩率最大为15%,已经满足耐火砖的使用要求。
铝灰的化学性质比较活泼,既可以与酸发生反应,又可以与碱发生反应,这也为湿法处理铝灰提供了多种选择。湿法处理铝灰相关的化学反应如下:
(1) 金属铝与酸和碱发生的反应[15]:
| $ {\rm{2Al + 6}}{{\rm{H}}_3}{{\rm{O}}^ + } + 6{{\rm{H}}_2}{\rm{O}} \to {\rm{2}}{\left[ {{\rm{Al}}{{\left( {{\rm{OH}}} \right)}_6}} \right]^{3 + }} + 9{{\rm{H}}_2} \uparrow $ | (1) |
| $ {\rm{2Al + }}2{\rm{O}}{{\rm{H}}^ - } + 6{{\rm{H}}_2}{\rm{O}} \to {\rm{2}}{\left[ {{\rm{Al}}{{\left( {{\rm{OH}}} \right)}_4}} \right]^ - } + 3{{\rm{H}}_2} \uparrow $ | (2) |
(2) Al2O3是两性金属氧化物,既可以与酸反应,也可与碱反应:
| $ \begin{array}{l} {\rm{A}}{{\rm{l}}_2}{{\rm{O}}_3} + 6{{\rm{H}}^ + } \to 2{\rm{A}}{{\rm{l}}^{3 + }} + 3{{\rm{H}}_2}{\rm{O}}\\ \end{array} $ | (3) |
在溶液环境下:
| $ {\rm{A}}{{\rm{l}}_2}{{\rm{O}}_3} + 2{\rm{O}}{{\rm{H}}^ - } \to 2{\rm{AlO}}_2^ - $ | (4) |
在熔融环境下:
| $ {\rm{A}}{{\rm{l}}_2}{{\rm{O}}_3} + 2{\rm{O}}{{\rm{H}}^ - } + 3{{\rm{H}}_2}{\rm{O}} \to {\rm{2}}{\left[ {{\rm{Al}}{{\left( {{\rm{OH}}} \right)}_4}} \right]^ - } $ | (5) |
(3) AlN的水解反应:AlN与水生成Al(OH)3[15]:
当pH<8时:
| $ {\rm{AlN + 4}}{{\rm{H}}_2}{\rm{O}} \to {\rm{Al}}{\left( {{\rm{OH}}} \right)_3} \downarrow + {\rm{N}}{{\rm{H}}_4}{\rm{OH}} $ | (6) |
当pH>8时:
| $ {\rm{AlN + 4}}{{\rm{H}}_2}{\rm{O}} \to {\rm{Al}}{\left( {{\rm{OH}}} \right)_3} \downarrow + {\rm{N}}{{\rm{H}}_3} \uparrow $ | (7) |
(4) 铝灰中存在少量的Al5O6N和Al4C3等物质,都可以与水发生反应产生大量气体[16]:
| $ {\rm{2A}}{{\rm{l}}_5}{{\rm{O}}_6}{\rm{N + 3}}{{\rm{H}}_2}{\rm{O}} \to 5{\rm{A}}{{\rm{l}}_2}{{\rm{O}}_3} + 2{\rm{N}}{{\rm{H}}_3} \uparrow $ | (8) |
| $ {\rm{A}}{{\rm{l}}_4}{{\rm{C}}_3}{\rm{ + 6}}{{\rm{H}}_2}{\rm{O}} \to 2{\rm{A}}{{\rm{l}}_2}{{\rm{O}}_3} + 3{\rm{C}}{{\rm{H}}_4} \uparrow $ | (9) |
一次铝灰中金属铝含量较高,一般在30%以上。从铝灰中回收Al有着可观的经济效益。目前可用于从铝灰中回收金属铝的方法包括火法回收、筛分法、电选法和碱性浸出法。
1.1 火法回收火法回收铝的原理是基于金属铝的熔点较低,当温度超过金属铝的熔点时,金属铝被熔化成铝液,铝灰中其他物质为固相,在重力作用下实现金属铝的分离[17]。目前通常采用的方法有炒灰回收法[18]、倾动回转窑法、压榨回收法[19]。表 2列举了几种常见的方法及其特点。
| 表 2 铝金属的提取方法(火法) Table 2 Method of extracting aluminum metal (pyrometallurgical method) |
 |
等离子体技术是新发展的技术。Gomez等[20]利用等离子体技术回收铝灰中的金属铝,该方法的优势在于等离子炉中的火焰温度很高,而且废气量明显减少。因为炉温很快达到金属铝熔出温度,金属铝的烧损减少[21]。等离子体技术的缺点在于其设备复杂且耗电量大,大规模铝灰的等离子体处理在经济上是否可行还有待研究[22]。
1.2 筛分法由于金属铝质地较软,通过粉碎和筛分可以回收粗金属铝,通过精细研磨和筛分回收更细的金属铝[15]。该法优点是工艺成熟,设备简单,但是筛分法生产效率低,对环境污染很严重。基于金属铝含量和晶粒尺寸之间关系的筛选技术可以使铝灰残余物的金属铝含量提高,同时降低铝灰残留物的AlN和AlCl3含量。常规方法设计的滚筒筛的筛孔尺寸,没有充分考虑残余物的粒度分布。Hiraki等[23]通过实验发现大于200 μm的铝灰残留物具有较高的金属铝含量,而其AlN和AlCl3含量较低。如果在筛选过程中使用250 μm尺寸的滚筒筛,铝灰残余物中的金属铝质量分数提高了50%,而AlN和AlCl3质量分数都减少了60%。
1.3 电选法电选技术已在再生金属领域广泛应用,电选法回收金属铝的原理是利用铝灰中各物质的电性质差异来实现物料分离。通过对电选设备的转鼓施加高压直流电流的方式使铝灰中的各组分带电荷。由于Al比其他组分更容易带电,使得铝颗粒得到的更多的电荷,受电场力作用粘附于转鼓。转入地线后,铝颗粒因为失去电荷而脱离转鼓,从而实现Al的分离。
Mah等[24]将渣滓粉碎至-840 μm后,使用静电分离器来回收金属铝,其回收率达到70%。Hwang等[25]则采用涡流电分离法,实现对6~10目尺寸金属铝的回收,但是Al的总回收效率还需要进一步提高。
1.4 碱性浸出法二次铝灰中的Al含量较低,一般采取湿法回收金属铝。Murayama等[26]用浓度为2 mol/L的NaOH浸出铝灰5 h,浸出液中Al的相对质量分数为96%,但是Al的浸出率仅为36%。Tsakiridis等[27]通过碱性高压浸出的方法,对二次铝灰进行破碎、筛分、水浸操作后,将铝灰在240 ℃下与260 g/L的NaOH反应100 min,浸出物中Al的质量分数仅为57.5%,残渣中主要成分是α-Al2O3、MgAl2O4、NaAl11O17和CaAl12O19。碱性高压浸出液中硅的含量提高,去除杂质硅也会增加成本[28]。
为了进一步提高Al的提取效率,郭学益等[29]采用低温碱性熔炼法提取铝灰中的Al。在一定的温度下,铝灰中的含铝组分与添加剂Na2O2反应生成可溶于水的碱式盐,达到Al与铝灰中其它物质的分离。优化工艺参数:碱灰质量比1:3,盐灰质量比0.4,熔炼温度为500 ℃,熔炼时间为60 min,此时Al浸出率可高达92.76%。
从酸性溶液中得到金属铝难度较大,而碱性浸出液可以直接利用拜耳法回收Al。因此通常采用碱性浸出法来提取二次铝灰中的Al。
2 回收氧化铝Al2O3因为硬度高、耐磨性好等优异性能一直备受关注[30-32]。目前商业生产Al2O3大部分是使用铝土矿材料,通过拜耳工艺生产[33]。而铝灰中的Al2O3含量较高,具有很大的利用价值。提取Al2O3的路线包括酸性浸出法和碱性提取法。酸浸出剂和碱浸出剂都可将铝灰中的金属铝及其化合物转化为Al3+或AlO2-, 通过向溶液中加入双氧水、碳酸铵、碳酸氢铵、氨水等物质与Al3+或AlO2-生成Al(OH)3沉淀,后者经过煅烧生成Al2O3。
2.1 酸性浸出法酸性浸出法广泛应用于铝灰回收Al2O3中,其中常用的酸浸出剂有硫酸溶液和盐酸[34]。
Saifur等[35]使用HCl作为浸出剂,成功从铝灰中回收Al2O3。在4 mol/L盐酸、120 min浸出时间和100 ℃温度的最佳条件下,回收率最高可达到71%,Al2O3的纯度高达99%。
刘晓红等[36]首先在铝灰中加入H2SO4溶液获得Al2(SO4)3,然后加入NH4HCO3溶液生成碳酸铝铵,最后经过干燥焙烧后得到纳米级别的-Al2O3。在20%质量分数H2SO4溶液,80 ℃浸出温度,3 h浸出时间的最佳条件下,Al的浸出率可达91.5%。该方法工艺简单,不会产生新的废渣。
Dash等[37]通过筛选和筛分的方法初步回收铝灰中的金属铝,接着加入一定浓度的H2SO4溶液将剩余的Al和Al2O3均转变Al2(SO4)3溶液。Al2(SO4)3与氨水发生反应得到无定型的Al(OH)3,最后对Al(OH)3进行高温煅烧处理,得到具有高附加值的α-Al2O3。该研究发现存在于铝灰中的盐会影响Al的浸出。在水浸出除去这些盐后,可以用15%的H2SO4溶解85%左右的Al2O3。将H2SO4浓度增加至50%时,可以溶解95%的Al2O3。
Mahinroosta等[38]采用新型五步浸出工艺,分别是盐酸浸出、共沉淀、纯化、再沉淀和煅烧,第一步加入NaOH溶液,得到富含NaAlO2的溶液。第二步,通过加入一定量的HCl溶液得到Al(OH)3沉淀,最后洗涤Al(OH)3并在700C下煅烧获得α-Al2O3。在38 mm~75 mm铝灰粒径,120 min浸出时间,85 ℃浸出温度,5 mol/L盐酸,20 ml/g液固比的最佳条件下,Al2O3提取率约为83%。实验得到的Al2O3具有纳米尺寸,并且具有高活性,可以应用于吸附和催化等方面。相对于硫酸和硝酸,盐酸与铝灰的反应较为温和。但是不足之处在于其工艺相对复杂,成本较高。酸性浸出法可以合成具有高附加值的Al2O3。与传统拜耳法从高硅原料中提取Al2O3相比,酸性浸出法的Al浸出率更高。
2.2 碱性提取法目前世界上90%以上的Al2O3是由拜耳法生产[39]。其中常用于碱性提取法的浸出剂是NaOH。
Davies等[40]利用拜耳法,首先进行水浸操作回收易溶的盐,如NaCl和KCl。实验使用150 g/L NaOH,分别在100 ℃和145 ℃下处理铝灰15 min,结果表明铝灰中的AlN全部溶解。Al2O3总萃取率约为42%。但是拜耳法液体对于铝灰中的微量杂质很敏感,且Al2O3的提取率较低。
Guo等[41]将铝灰进行水浸预处理,使用一定浓度的NaOH溶液,通过碱性焙烧的方法从铝灰中回收Al并用其合成γ-Al2O3。实验同时也证明了铝灰中氯化物的存在会降低Al的提取效率,而水浸预处理会降低铝灰中NaCl和KCl的含量,将Al的提取率从85%提高到96%。因为铝灰中的Al2O3大部分都是以α-Al2O3的形式存在[42],这种结构晶型完整,活性较低,在常温下难以与酸碱浸出剂发生反应。因此为了提高Al2O3的提取率,欧玉静[43]等将脱盐铝灰和NaOH溶液混合置于坩埚中,在500~800 ℃下烧结,得到的NaAlO2熟料加水溶解,然后过滤得到NaAlO2溶液,通过EDTA返滴定法计算出Al2O3的提取率高达93.26%。在利用碱性提取法回收铝灰中的Al2O3时,可以先经过水浸预处理降低其氯化物的含量,从而促进Al2O3的浸出。碱性提取Al2O3的优点是流程相对简单,作业方便,Al2O3产品质量高。
3 结论铝灰是一种工业固体废料,与此同时也是一种富铝资源,可以作为回收Al及Al2O3的原料。铝灰中Al和Al2O3两种物料含量一般达到70%以上,所以对两种物质回收利用的研究具有很大的经济价值。
回收铝灰中的金属铝时,电选法在国内还不成熟,特别是在提高Al的提取率和减少污染方面。对于一次铝灰中Al的回收,火法回收目前仍是最高效最经济的途径,其中等离子技术污染小,Al的回收效率高,有着很大的发展前景。二次铝灰中Al的含量相对较低,对于二次铝灰中Al的回收,一般选择碱性浸出法。另外,使用湿混料可以促进Al的浸出,还可以通过加入添加剂来提高Al的浸出率,常见的添加剂有NaNO3、Na2O2。
用湿法路线回收铝灰的Al2O3是可行的,且回收得到的Al2O3基本都达到了纳米尺寸,这使其在催化剂、生物载体材料等领域有着广泛的应用。与传统拜耳法从高硅原料中提取Al2O3相比,酸浸法回收Al2O3的效率更高。在不超过浸出剂沸点的温度范围内,可以采用高温烧结法来提高Al2O3的提取率。无论是碱性提取法还是酸性浸出法,铝灰经过水浸出后,铝灰中氯化物含量会降低,Al的浸出率及Al2O3的回收率会大大提高。
| [1] |
吴艳, 辛海霞, 陈若平, 等.铝灰碱浸提取铝工艺研究[C]//2010年全国冶金物理化学学术会议专辑(下册).马鞍山, 2010.
|
| [2] |
吴龙, 胡天麒, 郝以党. 铝灰综合利用工艺技术进展[J]. 有色金属工程, 2016, 6(6): 45-49. DOI:10.3969/j.issn.2095-1744.2016.06.010 |
| [3] |
马英, 杜建伟, 项赟, 等. 铝灰渣中回收氧化铝的研究现状和进展[J]. 轻金属, 2017(2): 29-33. |
| [4] |
王劲松. 浸取熔炼法提取铝灰中铝的技术研究与应用[J]. 世界有色金属, 2013(8): 72-73. |
| [5] |
耿培久, 白斌. 从铝灰中回收金属铝的生产工艺浅析[J]. 有色冶金节能, 2013, 29(4): 4-7. |
| [6] |
Environmental Protection Agency. European waste catalogue and hazardous waste list[M]. Ireland: Environmental Protection Agency, 2002.
|
| [7] |
Shinzato M. C., Hypolito R.. Effect of disposal of aluminum recycling waste in soil and water bodies[J]. Environmental Earth Sciences, 2016, 75(7): 628. DOI:10.1007/s12665-016-5438-3 |
| [8] |
Guo J. Recycling and utilization of the electrolytic aluminium ash and slag[J]. Materials Review, 2013, 40(1): 40-82. |
| [9] |
倪红军, 陈祥, 吕帅帅, 等. 铝渣合成无机材料的研究现状及进展[J]. 现代化工, 2015(11): 19-22. |
| [10] |
Meshram A., Singh K. K.. Recovery of valuable products from hazardous aluminum dross:A review[J]. Resour. Conserv. Recycl., 2018, 130: 95-108. DOI:10.1016/j.resconrec.2017.11.026 |
| [11] |
Shinzato M. C., Hypolito R.. Solid waste from aluminum recyclingprocess:characterization and reuse of its economically valuable constituents[J]. Waste manage., 2005, 25(1): 37-46. |
| [12] |
Hazar A. B. Y., Saridede M. N., çiĝdem M.. A study on thestructural analysis of aluminium drosses and processing ofindustrial aluminium salty slags[J]. Scand. J. Metall., 2005, 34(5): 213-219. |
| [13] |
Manfredi O., Wuth W., Bohlinger I.. Characterizing the physical and chemical properties of aluminum dross[J]. JOM, 1997, 49(11): 48-51. DOI:10.1007/s11837-997-0012-9 |
| [14] |
Adeosun S. O., Sekunowo O. I., Taiwo O. O.. Physical and mechanical properties of aluminum dross[J]. Adv. Mater., 2014, 3(2): 6-10. DOI:10.11648/j.am.20140302.11 |
| [15] |
Bruckard W. J., Woodcock J. T.. Recovery of valuable materials from aluminium salt cakes[J]. Int. J. Miner.Process., 2009, 93(1): 1-5. DOI:10.1016/j.minpro.2009.05.002 |
| [16] |
Tsakiridis P. E.. Aluminium salt slag characterization and utilization-A review[J]. J. Hazard. Mater., 2012, 217-218(none): 1-10. |
| [17] |
张宁燕, 宁平, 谢天鉴, 等. 铝灰有价组分回收及综合利用研究进展[J]. 硅酸盐通报, 2017, 36(06): 1951-1956. |
| [18] |
郑磊.铝灰高效分离提取及循环利用研究[D].长沙: 中南大学, 2010. http://cdmd.cnki.com.cn/Article/CDMD-10533-2010190244.htm
|
| [19] |
李艳, 夏毅敏. 热铝炉渣处理及高效冷却压滤机研制[J]. 湖南有色金属, 2004, 20(5): 46-50. DOI:10.3969/j.issn.1003-5540.2004.05.015 |
| [20] |
Gomez E., Rani D. A., Cheeseman C.R., et al. Thermal plasma technology for the treatment of wastes:A critical review[J]. Journal of Hazardous Materials, 2009, 161(2-3): 614-626. DOI:10.1016/j.jhazmat.2008.04.017 |
| [21] |
李玲玲, 宋明, 靳强. 铝灰回收利用的研究进展[J]. 无机盐工业, 2018, 50(8): 6-10. |
| [22] |
Beheshti R., Moosberg-Bustnes J., Akhtar S., et al. Black dross:processing salt removal from black dross by thermal treatment[J]. JOM, 2014, 66(11): 2243-2252. DOI:10.1007/s11837-014-1178-6 |
| [23] |
Hiraki T, Nagasaka T. An easier upgrading process of aluminum dross residue by screening technique[J]. Journal of material cycles and waste management, 2015, 17(3): 566-573. DOI:10.1007/s10163-014-0283-5 |
| [24] |
Mah K., Toguri J. M., Smith H. W.. Electrostatic separation of aluminum from dross[J]. Conservation & Recycling, 1986, 9(4): 325-334. |
| [25] |
Hwang J. Y., Huang X., Xu Z.. Recovery of metals from aluminum dross and saltcake[J]. Journal of minerals and materials characterization and engineering, 2006, 5(1): 47-62. |
| [26] |
Murayama N., Maekawa I., Ushiro H., et al. Synthesis of various layered double hydroxides using aluminum dross generated in aluminum recycling process[J]. International journal of mineral processing, 2012(110): 46-52. |
| [27] |
Tsakiridis P. E., Oustadakis P., Agatzini-Leonardou S.. Aluminium recovery during black dross hydrothermal treatment[J]. Journal of environmental chemical engineering, 2013, 1(1-2): 23-32. DOI:10.1016/j.jece.2013.03.004 |
| [28] |
徐士尧, 陈维平, 万兵兵, 等. 废铝再生熔炼中铝渣的回收处理工艺进展[J]. 特种铸造及有色合金, 2016, 36(9): 934-938. |
| [29] |
郭学益, 李菲, 田庆华, 等. 二次铝灰低温碱性熔炼研究[J]. 中南大学学报(自然科学版), 2012, 43(3): 809-814. |
| [30] |
Hassanzadeh-Tabrizi S. A., Taheri-Nassaj E., Sarpoolaky H.. Synthesis of an alumina-YAG nanopowder via sol-gel method[J]. Journal of alloys and compounds, 2008, 456(1): 282-285. |
| [31] |
Yoon T. R., Rowe S. M., Jung S. T., et al. Osteolysis in association with a total hip arthroplasty with ceramic bearing surfaces[J]. JBJS, 1998, 80(10): 1459. DOI:10.2106/00004623-199810000-00007 |
| [32] |
冯凌云, 陈晓明. 生物陶瓷材料的生物学性能评价[J]. 武汉工业大学学报, 1996(2): 124-126. DOI:10.3321/j.issn:1671-4431.1996.02.038 |
| [33] |
Silva M. P., Talbot D. E. J.. Essential readings in light metals[M]. Springer international publishing, 2016.
|
| [34] |
Kelmers A. D., Canon R. M., Egan B. Z., et al. Chemistry of the direct acid leach, calsinter, and pressure digestion-acid leach methods for the recovery of alumina from fly ash[J]. Resources and conservation, 1982, 9(82): 271-279. |
| [35] |
Sarker M.S. R., Alam M. Z., Qadir M. R., et al. Extraction and characterization of alumina nanopowders from aluminum dross by acid dissolution process[J]. International journal of minerals, metallurgy, and materials, 2015, 22(4): 429-436. DOI:10.1007/s12613-015-1090-2 |
| [36] |
刘晓红, 刘守信, 邹美琪, 等. 浸取铝灰制取纳米氧化铝新工艺[J]. 无机盐工业, 2009, 41(8): 52-54. DOI:10.3969/j.issn.1006-4990.2009.08.018 |
| [37] |
Dash B., Das B. R., Tripathy B. C., et al. Acid dissolution of alumina from waste aluminium dross[J]. Hydrometallurgy, 2008, 92(1-2): 48-53. DOI:10.1016/j.hydromet.2008.01.006 |
| [38] |
Mahinroosta M., Allahverdi A.. A promising green process for synthesis of high purity activated-alumina nanopowder from secondary aluminum dross[J]. Journal of cleaner production, 2018, 179: 93-102. DOI:10.1016/j.jclepro.2018.01.079 |
| [39] |
许文强, 郭建强. 拜耳法溶出技术及装备的比较选择[J]. 有色矿冶, 2007, 23(6): 55-57. DOI:10.3969/j.issn.1007-967X.2007.06.017 |
| [40] |
Davies M., Smith P., Bruckard W. J., et al. Treatment of salt cakes by aqueous leaching and Bayer-type digestion[J]. Minerals engineering, 2008, 21(8): 605-612. DOI:10.1016/j.mineng.2007.12.001 |
| [41] |
Guo H., Wang J., Zhang X., et al. Study on the extraction of aluminum from aluminum dross using alkali roasting and subsequent synthesis of mesoporous γ-alumina[J]. Metallurgical and materials transactions B, 2018, 49(5): 2906-2916. DOI:10.1007/s11663-018-1341-5 |
| [42] |
EI-Katatny E. A., Halawy S. A., Mohamed M. A., et al. Recovery of high surface area alumina from aluminium dross tailings[J]. Journal of chemical technology & biotechnology, 2000, 75(5): 394-402. |
| [43] |
欧玉静, 李小龙, 智鹏阔, 等. 铝灰中Al2O3的回收工艺[J]. 化工科技, 2018, 26(6): 31-36. |
 2019
2019



