| 白钨矿浮选中方解石对磷酸钠抑制性能的影响及机理研究 |
2. 东北大学 资源与土木工程学院,辽宁 沈阳 110819
2. School of Resource and Civil Engineering, Northeastern University, Shenyang 110819, China
钨是一种重要的稀有金属,在电子、冶金、军工等领域有重要用途。白钨矿是钨的重要载体矿物之一,经常与其它含钙矿物(如方解石、萤石等)共存,在实践中常以浮选的方法回收白钨矿[1]。由于可浮性相近以及矿物间相互作用,白钨矿的含钙脉石矿物的浮选分离一直是选矿研究的热点。
脂肪酸类捕收剂是白钨矿浮选应用最广泛的捕收剂[2],但这类捕收剂在白钨矿浮选中通过羧基与矿物表面的钙离子产生化学吸附或盐沉淀实现矿物的浮选,因此药剂的选择性低,为扩大矿物间的浮选性质差异,通常会通过高选择性的药剂与羧酸类药剂的组合使用[3, 4]、高选择性的抑制剂[5, 6]或者加温的矿浆条件下实现分离。值得注意的是,白钨矿分离的难点除了矿物的可浮性相近,还与矿物间的相互作用有关,矿物间的相互作用会使矿物表面性质相近,降低了矿物间可浮性质的差异[7, 8]以及药剂的选择性[9]。
矿物间的相互作用对浮选分离的影响已有较多研究报道,对于白钨矿浮选体系,矿物表面转化以及钙离子的影响机制均已有报道[9-11]。基于已有的研究,本论文以磷酸钠为调整剂,研究方解石存在与不存在的条件下,考察磷酸钠对白钨矿浮选的影响,并通过浮选溶液化学计算,研究方解石对磷酸钠性能影响的机制。本研究对白钨矿与含钙脉石矿物的高效分离以及浮选过程的调控研究具有一定的指导意义。
1 试验方法 1.1 试验材料白钨矿单矿物样品取自云南省某白钨矿,方解石单矿物样品取自湖南省长沙矿石粉厂,均为结晶良好的块状矿物,手捡出块状固体。取回的块矿样品经手碎后,手选出纯度较高、结晶形态较好的样品,经过再破碎、瓷球球磨后使用标准筛干筛至-106 μm,经去离子水冲洗并烘干后,置于磨口瓶中备用。X射线粉晶衍射分析结果如图 1所示,图 1分析结果表明白钨矿矿样纯度在95%以上, 其中CaO含量13.47%、WO3含量83.73%、SiO2含量2.80%,为高纯度矿样,符合单矿物试验的要求。
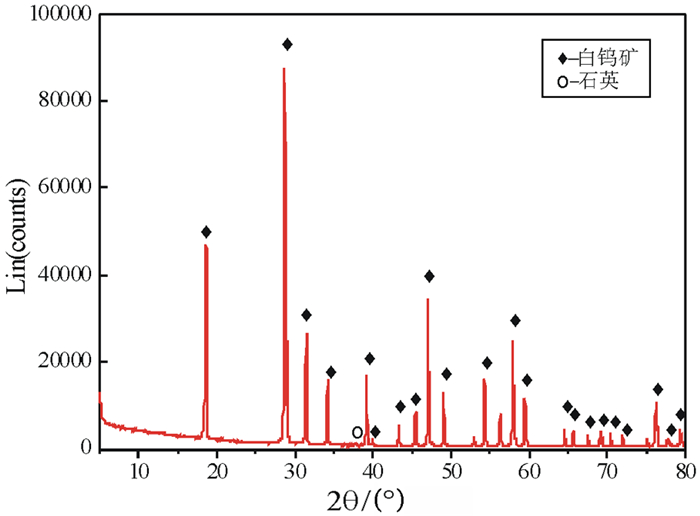 |
| 图 1 白钨矿的XRD图谱分析 Fig.1 XRD analyses spectra of scheelite |
试验所用pH调整剂(HCl和NaOH)、磷酸钠和油酸钠(NaOL)均为化学纯,试验用水为一次蒸馏水。
1.2 浮选试验浮选试验在XFG型挂槽式浮选机中进行,浮选机转速2 000 r/min。称取单矿物2.0 g放入40 mL的浮选槽内,加适量蒸馏水,按照试验要求,分别添加调整剂和捕收剂,添加药剂后搅拌3 min,浮选3 min。所获得的泡沫产品和槽内矿物经过滤、烘干、称重,计算出回收率。
2 试验结果与讨论 2.1 方解石及其溶解离子对磷酸钠抑制性能的影响方解石和磷酸钠对白钨矿回收率的影响如图 2所示。由图 2可知,在较广泛的pH范围内,磷酸钠对白钨矿基本无抑制作用,方解石对白钨矿具有一定的抑制作用,当方解石和磷酸钠同时添加时对白钨矿具有较强的抑制作用。
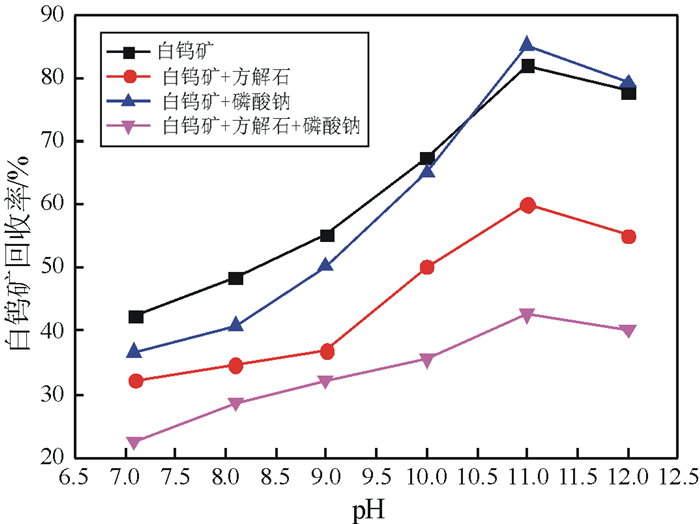 |
| 图 2 方解石和磷酸钠对白钨矿浮选的影响 Fig.2 Effect of sodium phosphate and calcite on the scheelite flotation ([方解石]=2.5 g/L; [NaOL]=1.5×10-4 mol/L; [磷酸钠]=10 mg/L) |
在方解石存在与否的条件下,磷酸钠用量对白钨矿浮选回收率的影响如图 3所示。由图 3可知,方解石对白钨矿具有一定的抑制作用,当方解石不存在时磷酸钠基本不影响白钨矿浮选,然而在方解石的作用下磷酸钠强烈抑制了白钨矿浮选,说明方解石和磷酸钠之间具有协同作用,两者共存时强化了对白钨矿的抑制作用。
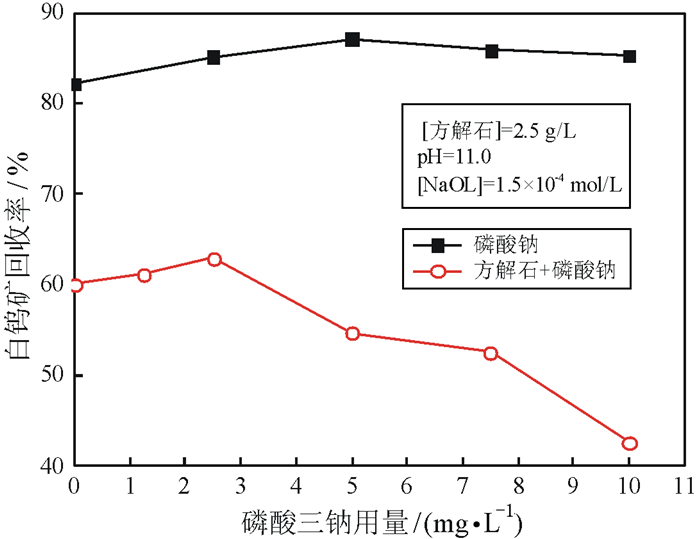 |
| 图 3 磷酸钠用量对白钨矿浮选的影响 Fig.3 Effect of sodium phosphate dosage on the scheelite flotation |
方解石在溶液中溶解会产生大量的钙离子和碳酸根离子,为探索方解石对白钨矿浮选的影响,分别研究了方解石溶解产生的钙离子和碳酸根离子对白钨矿浮选的影响,结果如图 4和图 5所示。由图 4可知,在矿浆pH=11.0的条件下,当磷酸三钠不存在时,碳酸钠对白钨矿具有一定的活化作用,当加入磷酸三钠后碳酸钠对白钨矿的活化作用消失,且白钨矿回收率基本不随磷酸三钠用量的增加而发生变化。图 5表明在无磷酸三钠条件下0~1.0×10-4mol/L的钙离子对白钨矿回收率的影响较小,但磷酸钠在钙离子作用下可强烈抑制白钨矿。由此可见,碳酸钠不影响磷酸钠对白钨矿的抑制作用,而钙离子可强化磷酸三钠对白钨矿的抑制作用。
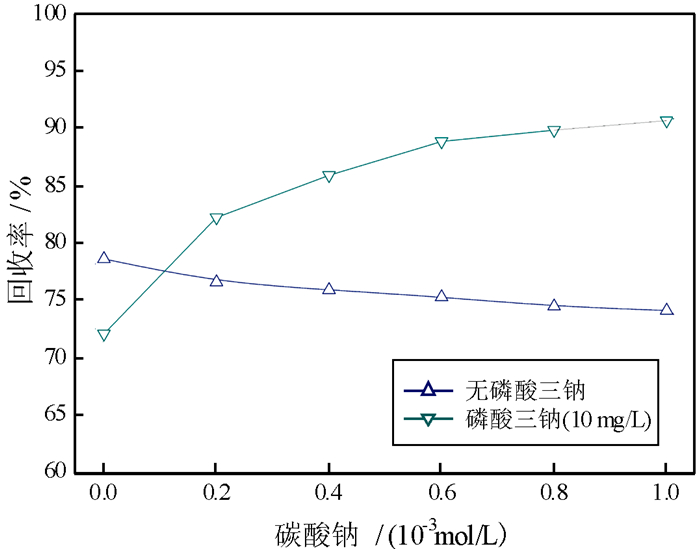 |
| 图 4 有(无)磷酸三钠存在条件下碳酸钠用量对白钨矿浮选回收率的影响 Fig.4 Effect of phosphate on the scheelite flotation as a function of sodium carbonate concentration |
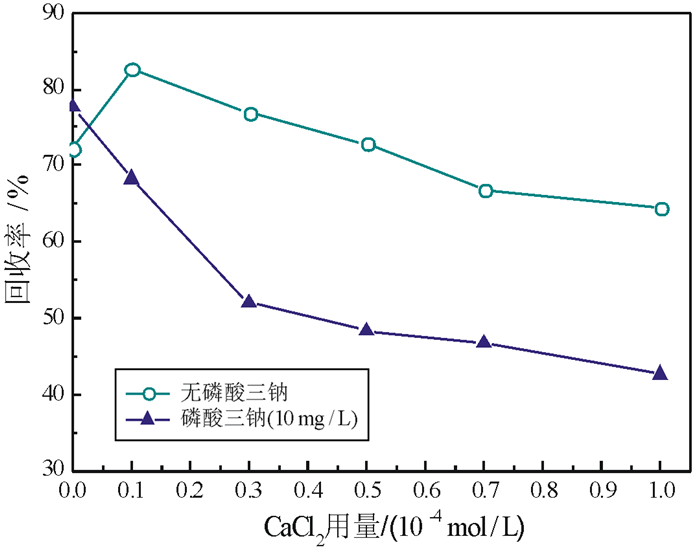 |
| 图 5 有(无)磷酸三钠存在条件下CaCl2用量对白钨矿浮选的影响 Fig.5 Effect of phosphate on the scheelite flotation as a function of CaCl2 concentration |
2.2 方解石对磷酸钠抑制性能影响的机制
方解石和白钨矿均为含钙脉石矿物,无论是混合矿物还是单一矿物,溶液体系中均存在钙离子,由于钙离子可强化磷酸钠对白钨矿的抑制作用,因此需要研究方解石的加入对白钨矿浮选溶液中钙离子浓度的影响。白钨矿溶解平衡为:
| $ \begin{array}{l} {\rm{CaW}}{{\rm{O}}_4} = {\rm{C}}{{\rm{a}}^{2 + }} + {\rm{WO}}_4^{2 - }\\ {K_{{\rm{sp}}\;{\rm{CaW}}{{\rm{O}}_{\rm{4}}}}} = \left[ {{\rm{C}}{{\rm{a}}^{2 + }}} \right]\left[ {{\rm{WO}}_4^{2 - }} \right] \end{array} $ | (1) |
设溶解度为S mol/L, 那么,
| $ \left[ {{\rm{C}}{{\rm{a}}^{2 + }}} \right] = {\rm{S}}/{\alpha _{{\rm{Ca}}}} $ | (2) |
| $ \left[ {{\rm{WO}}_4^{2 - }} \right] = {\rm{S}}/{\alpha _{{\rm{WO}}_4^{2 - }}} $ | (3) |
| $ {\alpha _{{\rm{Ca}}}} = 1 + {10^{{\rm{pH}} - 12.6}} + {10^{2{\rm{pH}} - 25.23}} $ | (4) |
| $ {\alpha _{{\rm{WO}}_4^{2 - }}} = 1 + {10^{{\rm{3}}{\rm{.5}} - {\rm{pH}}}} + {10^{8.2 - 2{\rm{pH}}}} $ | (5) |
由上式得:
| $ {\rm{S}} = \sqrt {{K_{{\rm{sp}}\;{\rm{CaW}}{{\rm{O}}_{\rm{4}}}}}{\alpha _{{\rm{Ca}}}}{\alpha _{{\rm{WO}}_4^{2 - }}}} $ | (6) |
同理可得方解石的溶解度:
| $ {{\rm{S}}_2} = \sqrt {{K_{{\rm{sp}}\;{\rm{CaW}}{{\rm{O}}_{\rm{4}}}}}{\alpha _{{\rm{Ca}}}}{\alpha _{{\rm{CO}}_3^{2 - }}}} $ | (7) |
其中
| $ {\alpha _{{\rm{CO}}_3^{2 - }}} = 1 + {10^{10.33 - {\rm{pH}}}} + {10^{16.68 - 2{\rm{pH}}}} $ | (8) |
由式(6)和(7)计算可得白钨矿和方解石的溶解度,计算结果如图 5所示。
由图 6可知,在图中的pH范围内方解石溶解产生的钙离子总浓度随pH增加而逐渐降低,然后趋于平衡,在pH为11.0时钙离子浓度约为1.0×10-4 mol/L;pH大于5时白钨矿溶解产生的钙离子浓度基本趋于稳定。已有研究表明[12],当pH约为6时钙离子与钨酸根离子浓度基本相等,均为2.2×10-4 mol/L,由于随着pH增加钙离子浓度有所降低,钨酸根离子难度也有所增加,但钨酸根离子与钙离子浓度的乘积为一定值,计算结果与文献值的差异可能是由于氢氧根离子置换钨酸根离子或者矿物溶解过程中钨酸根离子比钙离子优先溶解产生所致,但文献中以及图 6的计算结果足以证明白钨矿溶解的钙离子浓度为(1.0~2.2)×10-5 mol/L。从图 6中白钨矿和方解石溶解产生的钙离子浓度的对比可知,方解石溶解产生的钙离子浓度高于白钨矿,说明方解石加入白钨矿浮选体系后可增加钙离子浓度。
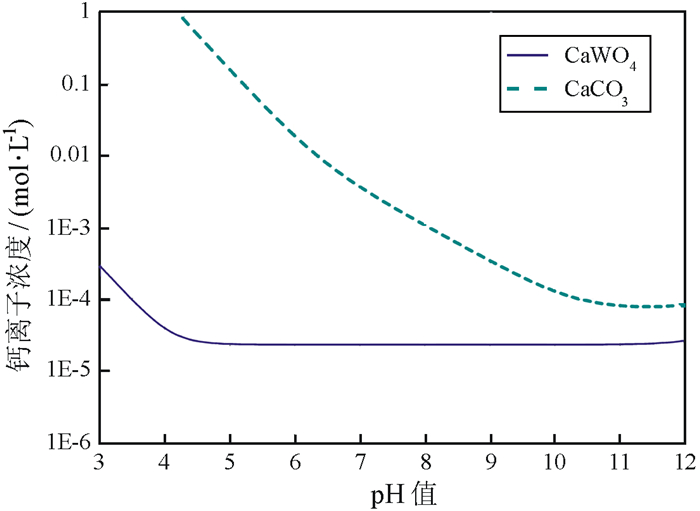 |
| 图 6 白钨矿和方解石溶液中的离子浓度 Fig.6 Ions concentration of scheelite and calcite solution |
方解石加入白钨矿浮选体系后,该浮选体系的溶液化学难以应用式(1)~(5)的计算方法求得,Atademir等测得了该复杂溶液体系钙离子和钨酸根离子的浓度,结果如图 7所示。
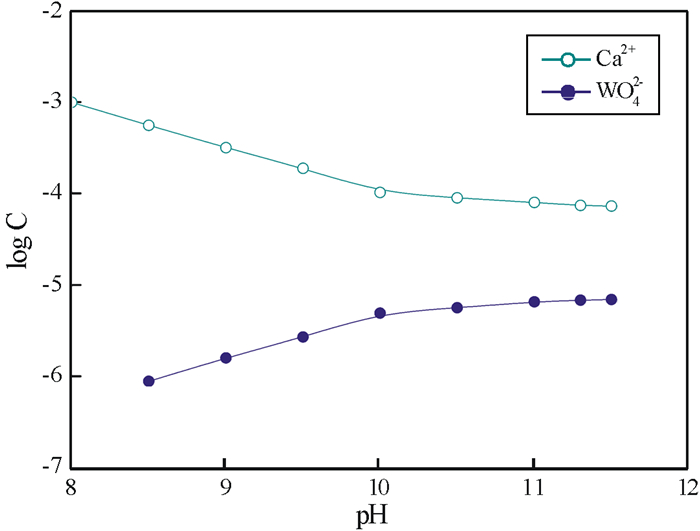 |
| 图 7 白钨矿/方解石混合矿溶液中的离子浓度[12] Fig.7 Ions concentration of scheelite/calcite mixtures |
由图 7可知,白钨矿/方解石混合矿的溶液中钙离子浓度明显高于白钨矿单独存在时的钙离子浓度,且与方解石单独存在时的钙离子浓度基本相等,进一步说明白钨矿浮选体系中加入方解石后增加了钙离子浓度。
方解石溶解后会使白钨矿浮选体系中存在大量碳酸根离子,且可明显增加钙离子浓度。浮选试验表明白钨矿浮选体系中加入碳酸根离子基本不影响磷酸钠的抑制性能,而增加钙离子浓度可明显强化磷酸钠对白钨矿的抑制作用,由此可见,方解石主要通过增加溶液中钙离子浓度的方式强化磷酸钠对白钨矿的抑制作用。
3 结论(1) 磷酸钠对白钨矿浮选的抑制作用较弱,溶液中同时存在方解石时磷酸钠对白钨矿具有明显的抑制作用。方解石溶解产生的碳酸根离子不影响磷酸钠对白钨矿的抑制作用,而溶解产生的钙离子可强化磷酸钠对白钨矿的抑制作用。
(2) 浮选溶液化学研究表明方解石的溶解度大于白钨矿,白钨矿浮选体系中加入方解石后可增加溶液中钙离子的浓度,且增加的钙离子浓度足以强化磷酸钠对白钨矿的抑制作用。
| [1] |
Liu Cheng, Feng Qiming, Chen Wei, et al. Effect of depressants in the selective flotation of scheelite and calcite using oxidized paraffin soap as collector[J]. International Journal of Mineral Processing, 2016, 157(10): 210-215. |
| [2] |
孙伟, 胡岳华, 覃文庆, 等. 钨矿浮选药剂研究进展[J]. 矿产保护与利用, 2000(3): 42-46. |
| [3] |
Gao Y, Gao Z, Sun W, et al. Selective flotation of scheelite from calcite:a novel reagent scheme[J]. International Journal of Mineral Processing, 2016, 154: 10-15. DOI:10.1016/j.minpro.2016.06.010 |
| [4] |
Gao Z, Bai D, Sun W, et al. Selective flotation of scheelite from calcite and fluorite using a collector mixture[J]. Minerals Engineering, 2015, 72: 23-26. DOI:10.1016/j.mineng.2014.12.025 |
| [5] |
邱廷省, 宋宜富, 邱仙辉, 等. 白钨矿浮选体系中大分子有机抑制剂的抑制性能[J]. 中国有色金属学报, 2017, 27(7): 1527-1534. |
| [6] |
张英. 白钨矿与含钙脉石矿物浮选分离抑制剂的性能与作用机理研究[D]. 长沙: 中南大学, 2012.
|
| [7] |
Nordstrom D K, Plununcr L N, Langmuir E, et al. Revised chemical equilibrium data for major water-mineral reactions and their liminations[J]. Chemical Modeling of Aqueous System Ⅱ, 1990, 416: 398-413. DOI:10.1021/symposium |
| [8] |
张治元, 王博, 傅景海. 矿物表面的相互转化对盐类矿物共存体系浮选的影响[J]. 金属矿山, 1995(4): 38-41. |
| [9] |
罗娜, 张国范, 朱阳戈, 等. 六偏磷酸钠对菱锰矿与方解石浮选分离的影响[J]. 中国有色金属学报, 2012, 22(11): 3214-3220. |
| [10] |
沈慧庭, 宫中贵. 白钨矿浮选中方解石的影响及消除影响的方法和机理研究[J]. 湖南有色金属, 1996, 12(2): 32-36. |
| [11] |
Chen wei, Feng Qiming, Zhang Guofan, et al. The effect of sodium alginate on the fotation separation of scheelite from calcite and fluorite[J]. Minerals Engineering, 2017, 113: 1-7. DOI:10.1016/j.mineng.2017.07.016 |
| [12] |
Atademir M R, Kitchener J A, Shergold H L. The surface chemistry and flotation of scheelite Ⅰ:solubility and surface characteristics of precipitated calcium tungstate[J]. Journal of Colloid and Interface Science, 1979, 71(3): 466-476. DOI:10.1016/0021-9797(79)90321-7 |
 2018
2018 

