| 电解锰阳极泥中战略金属回收技术进展 |
锰可以提高合金的强度、韧性、硬度和耐磨性[1],电解金属锰具有纯度高的特点,被广泛用作锰铜合金、锰铝合金、不锈钢的合金添加剂[2-3]。中国电解锰的生产、消费和出口在世界上都占据主导地位[4-5],目前,随着钢铁产量的飙升,电解锰的年产量稳定在150万t左右,占全球电解锰产量的97%以上[6-8],而电解锰的生产需要大量锰矿。我国锰矿总储量约为15.51亿t,占世界总量的6.23%[9-10]。我国贫锰矿储量占现有锰矿总储量的93.6%[11],锰矿石主要以碳酸锰矿石的形式存在,占总矿石储量的66.49%,因此碳酸锰矿石成为我国电解锰生产的主要原料[12]。但是碳酸锰矿石也在不断地开采消耗中变得越来越难以利用,品位越来越低。随着锰矿资源的消耗和电解锰需求的增加,对含锰资源的回收利用研究具有重大意义。
在电解锰的生产过程中,71.9%的锰成为最终产品,12.6%的锰存在于阳极泥中,13.7%的锰进入废渣中[13],每生产1 t电解锰便会产生50~80 kg的阳极泥[14-16],近年来,中国电解锰产量每年约为150万t,因此产生的阳极泥为7.5~12万t。在电解锰阳极泥中,锰的存在形态主要为二氧化锰,锰含量达到45%[17-19],品位已接近锰含量48%以上的富锰矿,非常具有回收利用价值。但是锰阳极泥组成复杂,含有多种杂质,分离回收难度较大,只有少量的电解锰阳极泥直接用作氧化Fe2+的氧化剂,大部分厂家廉价出售或者大量堆存[20],长时间的酸雨冲刷会使堆存的阳极泥中Pb2+渗入地下水系统,严重影响人体健康。因此,研究如何合理有效地回收电解锰阳极泥中有价金属具有重要意义。
电解锰阳极泥中锰和铅为主要元素,目前针对阳极泥中锰铅分离相关人员做了大量研究,主要采取的思路为将阳极泥还原浸出或者经高温焙烧后进行浸出,将四价锰还原为二价使其进入溶液中,铅富集于浸出渣中,也可使用醋酸铵等溶解铅氧化物,锰进入渣中。锡和硒元素在阳极泥中含量较少,所以对其进行回收利用的研究不多,但锡和硒在电子、冶金、化工等方面有重要应用,尤其锡为国家战略资源,极具回收价值。文章将针对电解锰阳极泥中战略金属锰、铅、硒、锡元素的分离回收技术进行探讨。
2 电解锰阳极泥资源概况 2.1 产生机理如图 1所示,电解锰通常以锰含量较低的碳酸锰矿石为原料,经过粉碎、磨细变成矿粉,然后添加至浸取罐,加入硫酸和缓冲剂硫酸铵,通入蒸汽使溶液接近沸腾,使矿粉中的锰浸出进入溶液,为了除去杂质铁,加入二氧化锰粉,继而加入液氨或者石灰乳,调节矿浆pH≈7, 经固液分离滤出残渣,向滤液中添加硫化剂(SDD或乙硫氮)净化溶液,使铁、钴、镍等以硫化物形式富集于渣中,再经二次固液分离除去上一步形成的硫化物沉淀,添加缓冲剂(二氧化硒或二氧化硫)得到电解液[21]。电解时,不断向电解槽中添加电解液,通电电解一段时间,取出附锰阴极板,经过钝化、清洗后,烘干,剥下金属锰,得到锰产品,电解时产生的阳极液,经过收集后重新返回浸取罐[22-23]。
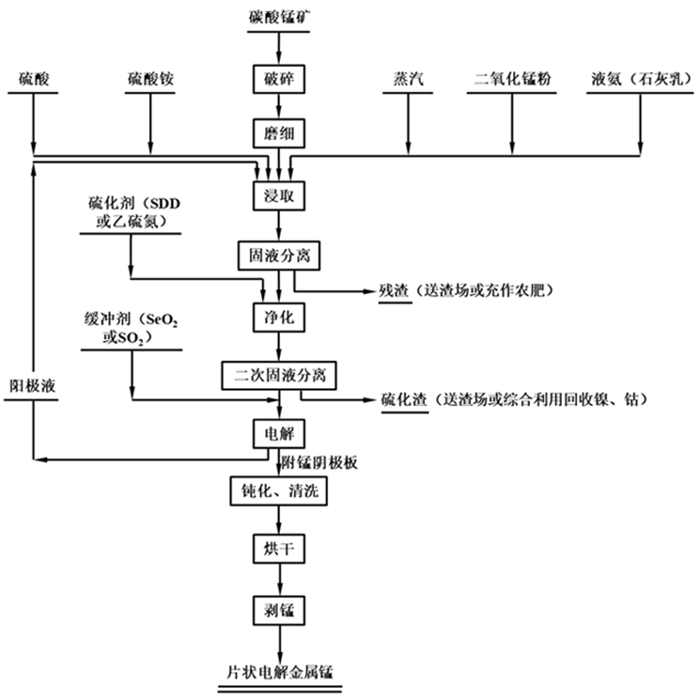 |
| 图 1 电解锰流程 Fig.1 The flow chart of electrolytic manganese |
在电解锰生产的电解过程中,阳极析出氧,伴随着产生少量的黑褐色物质沉积于表面,这种黑褐色物质称为阳极泥。之所以产生阳极泥,是因为电解时少量二价锰在阳极区放电产生二氧化锰沉积在阳极板上[24]。每生产1 t电解锰,便会产生50~80 kg的阳极泥,2020年中国电解锰产量为150.13万t[25],因此2020年产生的阳极泥为7.5~12万t,较往年稍有下降,阳极泥累积量已高达130万t以上。但是锰阳极泥组成复杂,含有多种杂质,分离回收难度较大,使得大部分厂家廉价出售或者大量堆存,所以没有得到合理开发利用,既浪费了宝贵的资源,还可能因处置不当产生严重的环境污染问题[26-28]。
2.2 资源特点 2.2.1 锰铅含量高、活性低电解锰的生产过程中,Mn(Ⅱ)在阳极被氧化为Mn(Ⅳ)的水合氧化物的进程难以避免,由于阳极使用含铅阳极板,铅也被氧化进入阳极泥中[29]。电解锰阳极泥是大小不同的块状物,颜色为黑褐色,白色结晶物硫酸铵嵌入其中,主要元素有Mn、Pb、Se、Sn、Ca、Mg、Fe等[30],元素组成见表 1。锰是电解锰阳极泥中含量最高的金属元素,含量一般为40%~50%,存在形式主要是MnO2,杂质元素主要为铅、钙、镁等,铅是含量最高的杂质金属元素,主要存在形式为铅氧化物,含量达到3%以上[31-32]。
| 表 1 典型电解锰阳极泥主要化学成分 Table 1 Chemical constituents of the typical electrolytic manganese anode slime |

|
电解锰阳极泥中二氧化锰的结构为正八面体结构,由6个氧原子和1个锰原子核配位组成,正是由于这种复杂的网络结构,使得其他阳离子也能嵌入其中[9]。有研究显示,电解锰阳极泥中的锰氧化物不是高活性的MnO2,而是非化学计量形式的氧化物MnOx(1<x<2),这种物质具有很大的晶格缺陷,杂质元素铅、锡等会嵌入其中,使电解锰阳极泥中的二氧化锰为失活状态[33]。有研究[34]分析了锰阳极泥原样的微区,发现阳极泥呈封闭相,以胶状物形式存在。此外,由于铅被锰氧化物包裹,造成铅的浸出活性低。
图 2为电解锰阳极泥的微观形貌和XRD分析,从XRD图中可以看出,电解锰阳极泥结晶度较差,锰主要以MnO2、Mn(OH)4和Mn0.98O2等非化学计量的锰氧化物形式存在。铅以PbO、PbO2和PbSO4的形式存在,硅主要以石英形式存在。由光学显微镜和扫描电镜分析可知,阳极泥结构致密,多呈鲕状结构和层状结构,锰和铅等氧化物相互嵌入。
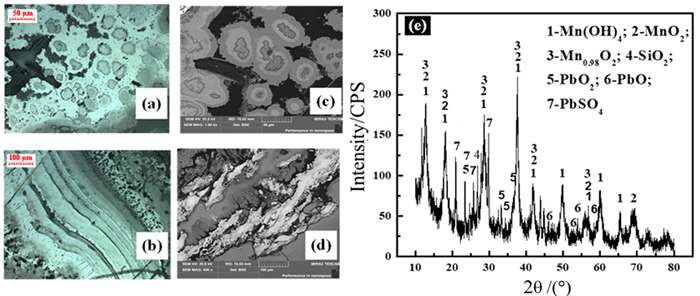 |
| 图 2 电解锰阳极泥原料分析:(a), (b)光学显微镜;(c), (d)SEM;(e)XRD[64] Fig.2 Raw material analysis of the electrolytic manganese anode slime: (a), (b)optical images; (c), (d)SEM; (e) XRD[64] |
2.2.2 硒、锡含量高
硒是一种稀散非金属元素,用途广泛,应用于冶金、玻璃、电子、太阳能等众多领域[35-37]。随着新冠肺炎的肆虐,研究显示,硒可能对新冠肺炎的防治具有重要作用[38],因此硒在市场上的需求持续增加。我国是硒消费大国,占全球消费总量的60%,但是大部分依赖国外进口[39],电解锰行业是国内最大的硒需求行业,每生产1 t电解锰,就需要加入缓冲剂二氧化硒0.9~2.5 kg,这其中有22%的硒进入阳极泥中[40],阳极泥中硒含量一般为0.1%~0.4%,处置不当极易造成环境污染,且硒具有剧毒,过量摄入会出现脱发、生长迟缓、生育力降低等症状。因此,对硒资源的回收利用研究具有重大意义。金属锡广泛应用于电子、化工、航空航天、国防军工等行业[41-43],与钨、锑、稀土并称为我国的四大战略资源,我国锡储量全球第一,是最大的锡出口和消费国。由于电解锰过程中使用含锡阳极板,使得一部分锡也进入电解锰阳极泥中[44],阳极泥中锡含量为0.1%~0.5%,远高于锰冶炼对锡含量的要求。目前,阳极泥中硒、锡资源没有得到回收利用,造成了严重的资源浪费。
3 电解锰阳极泥锰铅分离技术迄今为止,电解锰阳极泥资源回收主要集中于其中的锰、铅等元素,主要路线为选择性浸出、还原浸出、碱熔、还原焙烧等方法,选择性浸出或还原锰、铅物质,使铅进溶液、锰进渣,或者锰进溶液、铅进渣,亦或是铅、锡等杂质挥发进入气相等方式分离回收锰、铅、锡等元素[45-46]。还有研究将电解锰阳极泥中锰制备为二氧化锰、锰酸锂等[47-50]。工艺主要分为还原浸出法[51]、焙烧—浸出法[52-53]、碱熔—浸出法[54]等。由这些方法获得的锰产品为硫酸锰、二氧化锰等,铅产品为铅精矿、醋酸铅、硫化铅等。
3.1 直接还原浸出法阳极泥中的锰为四价,氧化性较强,可选用低价态硫化物、有机物等对其进行还原,发生氧化还原反应后,在硫酸中浸出,得到二价锰溶液,再进行过滤,滤液经过净化处理,即可制得纯度较高的硫酸锰溶液,过滤所得残渣即为铅精矿。
3.1.1 无机还原剂采用HSC Chemistry对MnO2与FeS2、SO2、Fe的反应进行热力学模拟计算,表 2为不同反应的方程式及对应的ΔGθ-T方程式,图 3为不同反应的ΔGθ-T关系图,由上可知,MnO2与FeS2、SO2、Fe常温下即可发生自发反应,产物主要为易溶于水的Mn2+,铅氧化物不易被还原,在硫酸等浸出过程中,会产生PbSO4等沉淀,因此可选用上述无机还原剂对电解锰阳极泥进行锰的选择性浸出。
| 表 2 不同还原剂与MnO2的反应方程式以及对应的ΔGθ-T方程式 Table 2 Reactions of different reducing agents and MnO2 and corresponding ΔGθ-T equations |

|
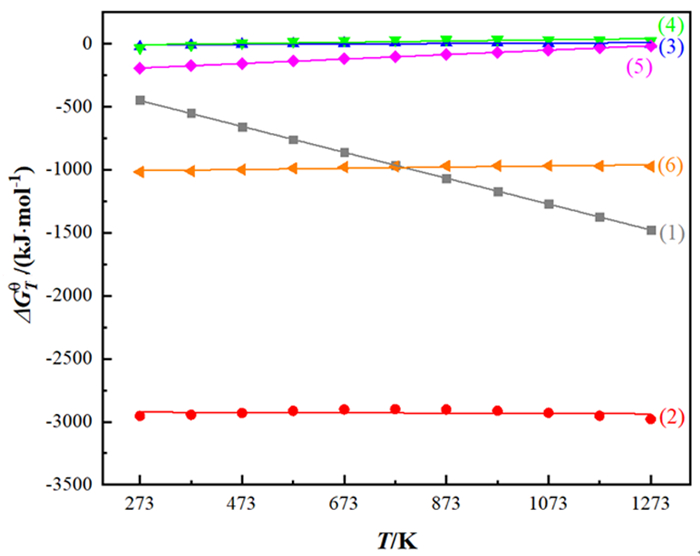 |
| 图 3 不同还原剂与MnO2反应的ΔGθ-T关系 Fig.3 ΔGθ-T diagram for the reaction of different reducing agents and MnO2 |
陈小亮等[55]以硫铁矿为还原剂、硫酸为浸出剂处理电解锰阳极泥,锰主要以MnSO4的形式存在于溶液中,最佳试验条件下,锰的浸出率达到99.1%,该方法具有环境污染小、能耗低、锰回收率高等优点,但是浸出液中引入了Fe、Pb等杂质,还需后续除杂才能利用,且硫铁矿的利用率较低,浸出渣量大,难以回收铅。刘建本等[33]用电解锌厂焙烧尾气处理电解锰阳极泥,将电解锰阳极泥与水混合搅拌成浆,再通入主要成分为SO2的尾气,反应得到MnSO4溶液,研究了反应温度、SO2流量和反应时间的影响,最佳工艺条件下,Mn2+的转化率达到90%以上。此方法充分利用了废弃物电解锰阳极泥和工业尾气SO2,避免了环境污染,但相比其他方法锰的回收率略低。吴焱等[56]对比了铁粉、硫铁矿、菱铁矿和硫酸亚铁浸出电解锰阳极泥的效果,得到结论:还原剂为硫铁矿、菱铁矿、硫酸亚铁时,锰的浸出率效果虽佳,但工艺均存在较大缺陷,不适于电解锰阳极泥的工业化应用,还原剂为铁粉时,锰铅分离效果较好,锰浸出率达到99.43%,但是铁粉价格昂贵,浸出液除铁也比较困难。
采用无机硫化物作还原剂时,锰的回收率较高,但在酸性体系中浸出会产生二氧化硫、硫化氢等气体,同时产生酸性废水、废渣等造成二次污染。
3.1.2 有机还原剂在硫酸体系中,可使大分子有机物(多糖类)水解成小分子有机物(单糖类),锰阳极泥中Mn(Ⅳ)可在其还原作用下变为Mn(Ⅱ)进入溶液中, 从而达到回收阳极泥中锰的效果。
可以选用富含果胶、纤维素等还原物质的橘子皮、木屑等作还原剂,湿法浸出锰阳极泥中的锰,铅富集于浸出渣,从而分离锰铅。体系中发生的主要反应为:
| $ \begin{array}{c} \mathrm{C}_{6} \mathrm{H}_{12} \mathrm{O}_{6}+12 \mathrm{MnO}_{2}+24 \mathrm{H}^{+}= \\12 \mathrm{Mn}^{2+}+6 \mathrm{CO}_{2}+18 \mathrm{H}_{2} \mathrm{O} \end{array} $ | (7) |
| $ \begin{array}{c} \left(\mathrm{C}_{6} \mathrm{H}_{12} \mathrm{O}_{5}\right)_{\mathrm{n}}+13 \mathrm{nMnO}_{2}+26 \mathrm{nH}^{+}= \\13 \mathrm{nMn}^{2+}+6 \mathrm{nCO}_{2}+19 \mathrm{nH}_{2} \mathrm{O} \end{array} $ | (8) |
赵世珍等[57]以木纤维作为还原剂,在硫酸体系中浸出锰阳极泥中的锰,得到硫酸锰溶液,在最优试验条件下,锰浸出率为99.18%,铅的去除率为99.7%以上。此方法锰铅分离效果虽好,但木纤维需要经过预处理,操作复杂,反应周期长。刘贵扬等[58]研究对比了不同有机物(木薯淀粉、玉米秆、废糖蜜和甘蔗渣)对锰阳极泥的浸出,发现除了甘蔗渣对锰的浸出效果不太理想外,其他有机物作为还原剂时,最优条件下锰的浸出率均能达到90%以上,但是,淀粉价格较高,废糖蜜用量和耗酸量大,不适宜用于处理锰阳极泥,玉米秆价格低、来源广且是农作物的废弃物,可以用于对锰阳极泥的处理。
3.2 固态焙烧—浸出法高温焙烧活化电解锰阳极泥,会使阳极泥中锰铅氧化物发生脱氧分解反应,阳极泥产生大量孔洞,有利于锰和铅的浸出[59-61]。固态焙烧—浸出法主要分为空气气氛焙烧和还原气氛焙烧。
3.2.1 空气气氛对锰阳极泥在空气气氛下进行高温焙烧处理,可改变阳极泥中晶体的空间结构,使Mn4+向低价态转变,过程为MnO2→Mn2O3→Mn3O4,高价铅转化为二价铅,离子半径变大,有利于铅在乙酸铵等有机溶剂中的浸出。
Wang等[62]进行了电解锰阳极泥高温焙烧、乙酸铵浸出铅的机理研究,研究发现,高温焙烧改变了铅的高价态,使得铅由四价转化为二价。此时,包覆铅与外部阳极泥之间的致密结构被破坏,形成了带有裂缝的多孔网络结构,有利于铅的浸出,铅氧化物与乙酸铵反应生成醋酸铅存在于溶液中,锰则不与乙酸铵反应,从而分离锰铅,最优工艺参数下,铅的浸出率可达99.3%。其中发生的主要反应如下:
| $ \begin{array}{c} \mathrm{PbO}+\mathrm{CH}_{3} \mathrm{COO}^{-}+2 \mathrm{NH}_{4}^{+}=\\ \mathrm{PbCH}_{3} \mathrm{COO}^{+}+2 \mathrm{NH}_{3}(\mathrm{~g})+\mathrm{H}_{2} \mathrm{O} \end{array} $ | (9) |
| $\begin{array}{c} \mathrm{PbO}+2 \mathrm{CH}_{3} \mathrm{COO}^{-}+2 \mathrm{NH}_{4}^{+}=\\ \mathrm{Pb}\left(\mathrm{CH}_{3} \mathrm{COO}\right)^{2-}+2 \mathrm{NH}_{3}(\mathrm{~g})+\mathrm{H}_{2} \mathrm{O} \end{array} $ | (10) |
| $\begin{array}{c} \mathrm{PbO}+3 \mathrm{CH}_{3} \mathrm{COO}^{-}+2 \mathrm{NH}_{4}^{+}=\\ \mathrm{Pb}\left(\mathrm{CH}_{3} \mathrm{COO}\right)_{3}^{-}+2 \mathrm{NH}_{3}(\mathrm{~g})+\mathrm{H}_{2} \mathrm{O} \end{array} $ | (11) |
| $\begin{array}{c} \mathrm{PbO}+4 \mathrm{CH}_{3} \mathrm{COO}^{-}+2 \mathrm{NH}_{4}^{+}=\\ \mathrm{Pb}\left(\mathrm{CH}_{3} \mathrm{COO}\right)_{4}{ }^{2-}+2 \mathrm{NH}_{3}(\mathrm{~g})+\mathrm{H}_{2} \mathrm{O} \end{array} $ | (12) |
Xie等[63]研究了微波耦合超声从电解锰阳极泥中提取铅的方法,首先进行了阳极泥未焙烧和微波焙烧下铅的浸出试验对比,发现微波辅助焙烧可促进MnO2向Mn2O3和Mn3O4的转化,提高铅的浸出率,乙酸铵浸出过程经超声波强化,可以使颗粒表面光滑,颗粒细化,同时加强了氧化铅的浸出,缩短了浸出反应时间。
3.2.2 还原气氛将电解锰阳极泥在还原气氛下进行焙烧,可强化四价锰向二价锰转变的进程和速度,最终锰和铅都转化为低价态,利用锰和铅离子在酸溶液中的溶解性不同,达到分离锰铅的效果。
Zhang等[64]采用SO2焙烧酸浸法分离锰阳极泥中的锰和铅,在焙烧过程中,SO2将锰阳极泥中锰、铅的氧化物硫化成MnSO4和PbSO4,发生的反应如式(13)~ (19);然后,由于MnSO4和PbSO4在酸溶液中的溶解度不同,可以在随后的酸浸过程中分离出来。在最佳浸出条件下,Mn的浸出率达92.5%,Pb的浸出效率仅为3.21%。此方法锰铅分离效果好,但是可能造成SO2气体污染且能耗较高。
| $ \begin{array}{c} \mathrm{MnO}_{2}+\mathrm{SO}_{2}(\mathrm{~g})=\mathrm{MnSO}_{4} \\3 \mathrm{MnO}_{2}+\mathrm{SO}_{2}(\mathrm{~g})= \end{array} $ | (13) |
| $ \mathrm{Mn}_{2} \mathrm{O}_{3}+\mathrm{MnSO}_{4}+1 / 2 \mathrm{O}_{2}(\mathrm{~g}) $ | (14) |
| $ 2 \mathrm{Mn}_{2} \mathrm{O}_{3}+\mathrm{SO}_{2}(\mathrm{~g})=\mathrm{Mn}_{3} \mathrm{O}_{4}+\mathrm{MnSO}_{4} $ | (15) |
| $ \mathrm{Mn}_{2} \mathrm{O}_{3}+2 \mathrm{SO}_{2}(\mathrm{~g})+1 / 2 \mathrm{O}_{2}(\mathrm{~g})=2 \mathrm{MnSO}_{4} $ | (16) |
| $ \mathrm{Mn}_{3} \mathrm{O}_{4}+3 \mathrm{SO}_{2}(\mathrm{~g})+\mathrm{O}_{2}(\mathrm{~g})=3 \mathrm{MnSO}_{4} $ | (17) |
| $ \mathrm{PbO}_{2}+\mathrm{SO}_{2}(\mathrm{~g})=\mathrm{PbSO}_{4} $ | (18) |
| $ \mathrm{PbO}+\mathrm{SO}_{2}(\mathrm{~g})+1 / 2 \mathrm{O}_{2}(\mathrm{~g})=\mathrm{PbSO}_{4} $ | (19) |
黎应芬等[60]将电解锰阳极泥与硫磺混合,高温还原焙烧,在硫酸中浸出,采用火法—湿法联合工艺分离锰铅,在焙烧过程中,阳极泥中的MnO2被逐步还原成Mn3O4,接着被硫磺和二氧化硫还原为MnS和MnSO4,铅被还原为PbSO4;经硫酸浸出,MnS也转变为MnSO4进入溶液,PbSO4则被富集于渣中。发生的反应如式(20)~(25)所示。最佳工艺条件下,锰的浸出率可达98%,尾渣含铅量30.5%。
| $ 2 \mathrm{~S}+\mathrm{MnO}_{2}=\mathrm{MnS}+\mathrm{SO}_{2}(\mathrm{~g}) $ | (20) |
| $ \mathrm{S}+3 \mathrm{MnO}_{2}=\mathrm{Mn}_{3} \mathrm{O}_{4}+\mathrm{SO}_{2}(\mathrm{~g}) $ | (21) |
| $ \mathrm{S}+4 \mathrm{MnO}_{2}=2 \mathrm{Mn}_{2} \mathrm{O}_{3}+\mathrm{SO}_{2}(\mathrm{~g}) $ | (22) |
| $ \mathrm{MnO}_{2}+\mathrm{S}+\mathrm{O}_{2}(\mathrm{~g})=\mathrm{MnSO}_{4} $ | (23) |
| $ \mathrm{PbO}_{2}+\mathrm{S}=\mathrm{PbS}+\mathrm{SO}_{2}(\mathrm{~g}) $ | (24) |
| $ \mathrm{PbO}+\mathrm{S}+3 / 2 \mathrm{O}_{2}(\mathrm{~g})=\mathrm{PbSO}_{4} $ | (25) |
阳极泥中锰为锰氧化物,将其和强碱混合在高温下焙烧,可将锰氧化为锰酸盐进入溶液,剩余杂质以固态形式存在,从而实现锰铅分离。其中发生的反应为:
| $ 2 \mathrm{MnO}_{2}+4 \mathrm{NaOH}+\mathrm{O}_{2}(\mathrm{~g})=2 \mathrm{Na}_{2} \mathrm{MnO}_{4}+2 \mathrm{H}_{2} \mathrm{O} $ | (26) |
申永强等[54]将电解锰阳极泥与碱混合高温焙烧,MnOx被氧化为可溶于水的Na2MnO4,其他杂质元素则形成不溶于水的盐,经溶解、固液分离后得到纯度较高的锰酸盐溶液,加入少量晶种,再以甲醛为还原剂,加热搅拌后可得初级化学二氧化锰,此法为电解锰阳极泥的回收再利用提供了一种新的思路。
3.4 锰铅分离技术对比表 3为电解锰阳极泥中锰铅分离技术优缺点对比,这些方法的锰铅分离效果均比较理想,但是都有难以避免的缺陷,主要有操作复杂、产生二次污染、能耗高等。因此,今后对固废电解锰阳极泥的探讨应更加深入,如何合理、高效、清洁处理还需大量研究。
| 表 3 电解锰阳极泥中锰铅分离方法 Table 3 Separation methods of manganese and lead from electrolytic manganese anode slime |

|
4 锰阳极泥中硒的分离回收技术
提取硒的主要方法有纯碱焙烧法[65]、硫酸化焙烧法[66]、Na2SO3浸出法[67]等,电解锰阳极泥中提硒的方法主要有氢氧化钠碱浸法、还原浸出法等。
4.1 氢氧化钠碱浸将电解锰阳极泥在碱溶液中浸出,硒氧化物会与氢氧化物发生成盐反应[68],从而实现硒的浸出,发生的反应为:
| $ \mathrm{SeO}_{2}+2 \mathrm{OH}^{-}=\mathrm{SeO}_{3}{ }^{2-}+\mathrm{H}_{2} \mathrm{O} $ | (27) |
曾宪日等[40]以氢氧化钠碱浸法提取阳极泥中的硒,考察了碱浓度、浸出温度、液固比、浸出时间和搅拌速度等对硒浸出率的影响,并且引入超声波辅助浸出,研究了超声波对硒浸出的强化效果。得到结论:超声波可以加快反应进程,降低浸出温度并提高硒的浸出率,最佳工艺条件下,硒浸出率可达到96.11%。
4.2 还原浸出工艺覃兆财等[69]以亚硫酸铵为还原剂、硫酸为浸出剂,回收电解锰阳极泥中的锰和硒,首先将装有一定浓度硫酸溶液的三颈烧瓶置于恒温水浴中,开启搅拌待溶液温度达到设定值后,加入亚硫酸铵和阳极泥,反应一定时间后,抽滤,锰主要以MnSO4的形式存在于溶液中,硒以SeO32-和SeO42-的形式存在于溶液中,铅富集于浸出渣中,在最佳试验条件下,锰的浸出率达到98.78%,硒的浸出率达到93.94%,此方法锰回收率较高,但是硒的回收率不太理想,且反应时间较长。
王雨红等[70]以蔗糖和铁粉为还原剂,硫酸为浸出剂,两段浸出电解锰阳极泥中的锰和硒,锰以Mn2+的形式存在于溶液中,硒被富集于浸出渣中。考察了浸出温度、浸出时间、硫酸浓度、蔗糖用量、铁粉加入量对锰、硒浸出率的影响,其中发生的主要反应有:
| $ \begin{array}{c} 3 \mathrm{MnO}_{2}+6 \mathrm{H}^{+}+\mathrm{MSe}= \\ 3 \mathrm{Mn}^{2+}+\mathrm{M}^{2+}+\mathrm{SeO}_{3}^{2-}+3 \mathrm{H}_{2} \mathrm{O} \end{array} $ | (28) |
| $ \begin{array}{c} 4 \mathrm{MnO}_{2}+8 \mathrm{H}^{+}+\mathrm{MSe}=\\4 \mathrm{Mn}^{2+}+\mathrm{M}^{2+}+\mathrm{SeO}_{4}{ }^{2-}+4 \mathrm{H}_{2} \mathrm{O} \end{array} $ | (29) |
| $ \mathrm{SeO}_{4}^{2-}+2 \mathrm{H}^{+}+\mathrm{Fe}=\mathrm{SeO}_{3}{ }^{2-}+\mathrm{Fe}^{2+}+\mathrm{H}_{2} \mathrm{O} $ | (30) |
| $ \mathrm{SeO}_{3}^{2-}+6 \mathrm{H}^{+}+2 \mathrm{Fe}=\mathrm{Se}{\downarrow}+2 \mathrm{Fe}^{2+}+3 \mathrm{H}_{2} \mathrm{O} $ | (31) |
式中:MSe为硒化物,如MnSe、Ag2Se等。
最佳工艺条件下,锰和硒的浸出率分别为99.31%和0.5%,此方法锰和硒的分离效果较好,但是操作复杂,且成本昂贵。
5 锰阳极泥中锡的分离回收技术常用的回收锡的方法有火法和湿法两种,火法包括硫化挥发法[71]、氯化挥发法[72]、碳热还原法[73]等,汤集刚等[53]以电解锰阳极泥为原料,焦炭为还原剂,将二者混合在回转窑内1 050~1 100 ℃焙烧1 h以脱除铅锡等杂质,焙烧后锰品位由50%提高至70%,证明了还原挥发法将所有重要杂质降至冶炼锰铁合金所要求的水平以下是可能的,此方法虽脱除了大部分锡,但并未将锡回收利用。对于火法回收锡,其中发生的主要反应如下式(32)~(38),由表 4和图 4可知,火法回收锡,只是将锡作为杂质脱除,并未加以利用,且能耗过高,对炉子的侵蚀也比较严重。湿法主要是将SnO2转化为能溶于酸或碱的形态,从而提取锡[74-75]。例如LIU W等[76]采用苏打焙烧—碱浸沉淀法将SnO2转化为CaSnO3,其中发生的反应如式(39)~(41),此法可回收95%以上的锡。
| $ \mathrm{SnO}_{2}+\mathrm{Na}_{2} \mathrm{CO}_{3}=\mathrm{Na}_{2} \mathrm{SnO}_{3}+\mathrm{CO}_{2}(\mathrm{~g}) $ | (39) |
| $ \mathrm{Na}_{2} \mathrm{SnO}_{3}(\mathrm{~s})+3 \mathrm{H}_{2} \mathrm{O}=\mathrm{Na}_{2}\left[\mathrm{Sn}(\mathrm{OH})_{6}\right](\mathrm{aq}) $ | (40) |
| $ \mathrm{Sn}(\mathrm{OH})_{6}^{2-}+\mathrm{CaO}=\mathrm{CaSnO}_{3}+2 \mathrm{OH}^{-}+2 \mathrm{H}_{2} \mathrm{O} $ | (41) |
| 表 4 SnO2转化过程中发生的主要反应[73]及对应的ΔGθ-T方程式 Table 4 Main chemical reactions[73] during the conversion of SnO2and corresponding ΔGθ-Tequations |

|
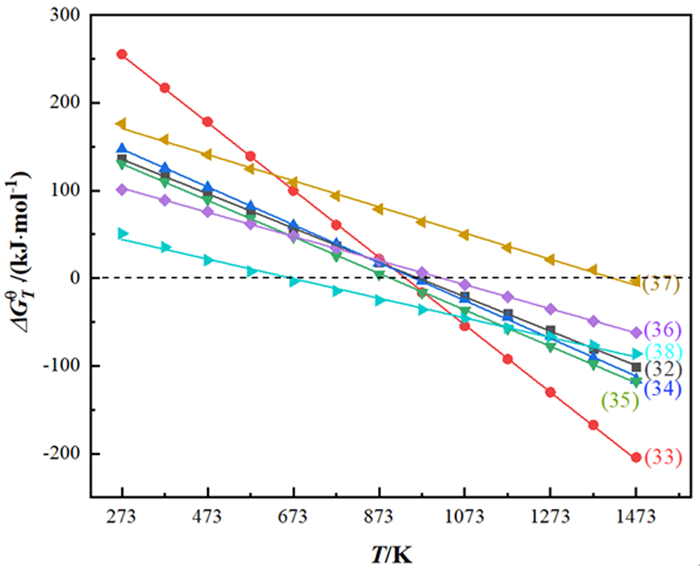 |
| 图 4 SnO2转化过程中反应的ΔGθ-T关系 Fig.4 ΔGθ-T diagram for the main reactions during the conversion of SnO2 |
6 基于硫转化的锰阳极泥锰铅硒锡提取新思路
电解锰阳极泥中锰、铅、硒、锡元素含量较高,具有回收利用价值。对比上述回收锰、铅、硒、锡的方法可知,这四种元素均对硫具有较强的化学亲和性,因此可开发一种基于硫转化的锰铅硒锡分步取技术,反应过程如图 5所示。首先将阳极泥与单质硫混合经高温焙烧,可发生如式(42)~(51)的转化:
| $ \mathrm{MnO}_{2}+2 \mathrm{~S}=\mathrm{MnS}+\mathrm{SO}_{2}(\mathrm{~g}) $ | (42) |
| $ 4 \mathrm{MnO}_{2}+\mathrm{S}+\mathrm{O}_{2}(\mathrm{~g})=\mathrm{MnSO}_{4} $ | (43) |
| $ 4 \mathrm{MnO}_{2}+\mathrm{S}=2 \mathrm{Mn}_{2} \mathrm{O}_{3}+\mathrm{SO}_{2}(\mathrm{~g}) $ | (44) |
| $ 6 \mathrm{MN}_{2} \mathrm{O} 3+\mathrm{S}=4 \mathrm{Mn}_{3} \mathrm{O}_{4}+\mathrm{SO}_{2}(\mathrm{~g}) $ | (45) |
| $ 2 \mathrm{Mn}_{3} \mathrm{O}_{4}+\mathrm{S}=6 \mathrm{MnO}+\mathrm{SO}_{2}(\mathrm{~g}) $ | (46) |
| $ \mathrm{PbO}_{2}+\mathrm{S}=\mathrm{PbS}_{2}+\mathrm{SO}_{2}(\mathrm{~g}) $ | (47) |
| $ \mathrm{PbO}_{2}+\mathrm{S}+\mathrm{O}_{2}(\mathrm{~g})=\mathrm{PbSO}_{4} $ | (48) |
| $ 2 \mathrm{PbO}_{2}+2 \mathrm{~S}=2 \mathrm{PbS}+\mathrm{SO}_{2}(\mathrm{~g}) $ | (49) |
| $ \mathrm{SnO}_{2}+\mathrm{S}+\mathrm{O}_{2}(\mathrm{~g})=\mathrm{SnSO}_{4} $ | (50) |
| $ \mathrm{SeO}_{2}(\mathrm{~s})=\mathrm{SeO}_{2}(\mathrm{~g}) $ | (51) |
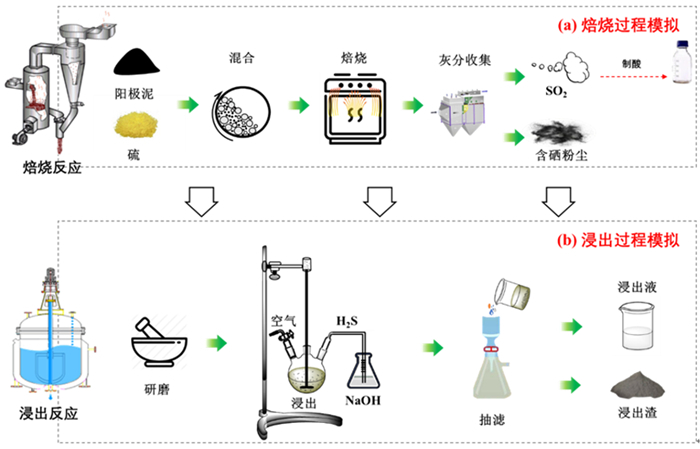 |
| 图 5 反应流程示意图 Fig.5 Schematic diagram of the reaction flow |
再经稀硫酸浸出,MnSO4、MnS、MnO等全部以MnSO4形式进入溶液,锡以SnSO4形式进入溶液,铅以PbSO4和PbS形式析出,固液分离可将锰和锡转移至溶液,铅转移至浸出渣中,通过调节浸出液酸碱度可实现锰锡分离,SeO2易溶于水且高温极易挥发(315 ℃升华),焙烧过程中可进入灰分收集器于气相回收,进一步水洗可实现硒的净化,二氧化硒溶于水的反应如式(52)。
| $ \mathrm{SeO}_{2}+\mathrm{H}_{2} \mathrm{O}=\mathrm{H}_{2} \mathrm{SeO}_{3} $ | (52) |
采用Visual MINTEQ软件对溶液中二价锰(0.01 mol/L)和二价锡离子(0.01 mol/L)的形态分布进行模拟,如图 6所示,在pH<2时,溶液中主要为Mn2+和Sn2+,随着酸碱度增大至pH=8,锰还是以Mn2+形式存在,Sn2+逐渐降低至0,Sn3(OH)42+和SnOH+浓度先升高后降低,随着pH值继续增大,二价锰离子以Mn2(OH)3+的形式存在于溶液中,二价锡离子则逐渐溶出,以Sn(OH)3-的形式存在。对比整个过程不难发现,当pH=6~8时,二价锡离子完全沉淀,锰以Mn2+形式存在于溶液中,可实现锰锡分离。如此通过对电解锰阳极泥硫化还原焙烧、硫酸浸出可实现电解锰阳极泥中锰铅硒锡的分步提取,为电解锰阳极泥的资源化利用提供一种新的途径。
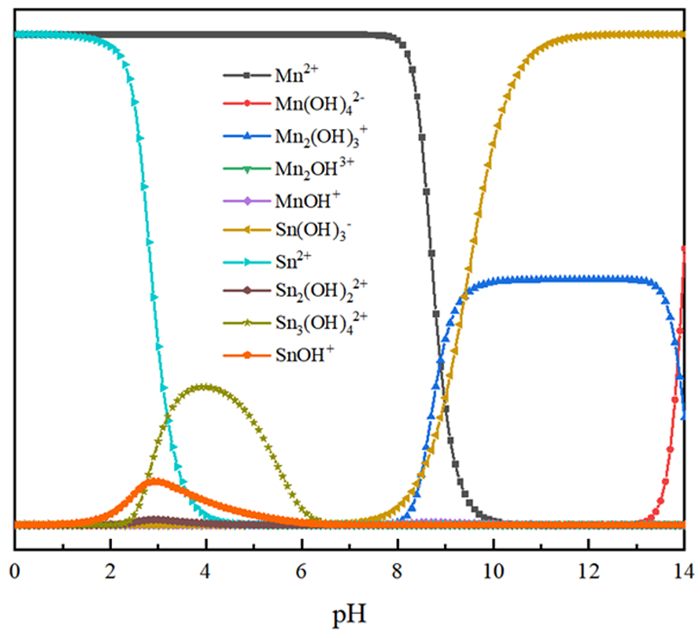 |
| 图 6 不同pH下锰锡离子形态分布图 Fig.6 Morphology distribution of manganese and tin ions at different pH values |
7 结论与展望
电解锰阳极泥中含有大量锰、铅、硒、锡等战略金属元素,综合回收利用价值高。然而,电解锰阳极泥矿物组成与结构复杂,有价组分多、含量高,铅与锰的水合氧化物共生紧密,多呈胶状环带结构,晶形发育不全,综合利用难度大。锰阳极泥中锰铅的分离回收是当前研究的重点,对稀有金属锡、硒的提取研究报道较少。电解锰阳极泥中锰铅分离方法主要有直接还原浸出法、固态焙烧—浸出法、碱熔—浸出法等。电解锰阳极泥中锰铅氧化物交织,焙烧、碱熔预处理以解离锰、铅氧化物的复杂结构,可有效提高锰铅分离效率。电解锰阳极泥中硒的分离回收技术主要有碱浸、还原浸出法等。锰阳极泥中锡的分离回收技术主要包括碳热还原法、硫化挥发法等。目前电解锰阳极泥中锰、铅、锡、硒等有价金属需要不同的工艺单独回收其中的一个或二个金属组元,工艺流程复杂。根据电解锰阳极泥中锰、铅、锡、硒对硫化学元素亲和性,开发基于硫转化的电解锰阳极泥中锰铅锡硒分步提取技术,可为电解锰阳极泥固废的资源化利用提供新的途径。
| [1] |
JOO S, CHOI Y, SHIN H. Hierarchical multi-porous copper structure prepared by dealloying electrolytic copper-manganese alloy[J]. Journal of Alloys and Compounds, 2022, 900: 163423. DOI:10.1016/j.jallcom.2021.163423 |
| [2] |
HE D, SHU J, WANG R, et al. A critical review on approaches for electrolytic manganese residue treatment and disposal technology: reduction, pretreatment, and reuse[J]. Journal of Hazardous Materials, 2021, 418: 126235. DOI:10.1016/j.jhazmat.2021.126235 |
| [3] |
LI P, LUO S, WANG X, et al. Study on the high-efficiency separation of Fe and Mn from low-grade pyrolusite and the preparation of LiMN2O4 materials for lithium-ion batteries[J]. Separation and Purification Technology, 2021, 278: 119611. DOI:10.1016/j.seppur.2021.119611 |
| [4] |
HE D, SHU J, ZENG X, et al. Synergistic solidification/stabilization of electrolytic manganese residue and carbide slag[J]. Science of the Total Environment, 2022, 810: 152175. DOI:10.1016/j.scitotenv.2021.152175 |
| [5] |
YANG T, XUE Y, LIU X, et al. Solidification/stabilization and separation/extraction treatments of environmental hazardous components in electrolytic manganese residue: a review[J]. Process Safety and Environmental Protection, 2022, 157: 509-526. DOI:10.1016/j.psep.2021.10.031 |
| [6] |
HUANG L.Q, BI Y.F, MU L.L, et al. The process and mechanism of electrolytic manganese anode slime lead removal[J]. Advanced Materials Research, 2014, 878: 163-170. DOI:10.4028/www.scientific.net/AMR.878.163 |
| [7] |
WANG Y, GAO S, LIU X, et al. Preparation of non-sintered permeable bricks using electrolytic manganese residue: Environmental and NH3-N recovery benefits[J]. Journal of Hazardous Materials, 2019, 378: 120768. DOI:10.1016/j.jhazmat.2019.120768 |
| [8] |
SHU J, WU Y, DENG Y, et al. Enhanced removal of Mn2+ and NH4+-N in electrolytic manganese metal residue using washing and electrolytic oxidation[J]. Separation and Purification Technology, 2021, 270: 118798. DOI:10.1016/j.seppur.2021.118798 |
| [9] |
黄良取, 黄升谋, 唐疆蜀, 等. 电解锰阳极泥的利用研究进展[J]. 武汉工程大学学报, 2015, 37(10): 5-10. HUANG L, HUANG S, TANG J, et al. Research progress on utilization of electrolytic manganese anode slime[J]. Journal of Wuhan University, 2015, 37(10): 5-10. |
| [10] |
夏熙. 二氧化锰及相关锰氧化物的晶体结构、制备及放电性能(1)[J]. 电池, 2004(6): 411-414. XIA X. Crystal structure, preparation and discharge performance for manganese dioxides and related manganese oxides (Ⅰ)[J]. Battery Bimonthly, 2004(6): 411-414. DOI:10.3969/j.issn.1001-1579.2004.06.009 |
| [11] |
SONG J, ZHU J, ZHANG P, et al. Reduction of low-grade manganese oxide ore by biomass roasting[J]. ActaMetallurgicaSinica-English Letters, 2010(3): 223-229. |
| [12] |
WU Y, SHI B, LIANG H, et al. Magnetic properties of low grade manganese carbonate ore[J]. Applied Mechanics and Materials, 2014, 664: 38-42. DOI:10.4028/www.scientific.net/AMM.664.38 |
| [13] |
DUAN N, FAN W, CHANGBO Z, et al. Analysis of pollution materials generated from electrolytic manganese industries in China[J]. Resources, Conservation and Recycling, 2010, 54(8): 506-511. DOI:10.1016/j.resconrec.2009.10.007 |
| [14] |
ZHANG H, BI Y, CHEN X, et al. Treatment and characterization analysis of electrolytic manganese anode slime[J]. Procedia Environmental Sciences, 2016, 31: 683-690. DOI:10.1016/j.proenv.2016.02.125 |
| [15] |
ZHU R, LONG H, WANG Y, et al. Microwave-assisted recovery of lead from electrolytic manganese anode sludge using tartaric acid and NaOH[J]. Environmental Technology, 2021, 1-15. |
| [16] |
TAO C, LI D, LIU Z, et al. Activation and purification of electrolytic-manganese anode slime and its application[J]. Battery Bimonthly, 2011, 41: 121-124. |
| [17] |
GUO P, TANG J, WANG S, et al. Synergistic effect of reduction leaching of manganese anode slime and oxidation pretreatment of gold concentrate[J]. Materials Research Express, 2019(6): 1065. |
| [18] |
LI K, CHEN J, PENG J, et al. Dielectric properties and thermal behavior of electrolytic manganese anode mud in microwave field[J]. Journal of Hazardous Materials, 2020, 384: 121227. DOI:10.1016/j.jhazmat.2019.121227 |
| [19] |
ZHOU X, LUO C, WANG J, et al. Recycling application of modified waste electrolytic manganese anode slag as efficient catalyst for PMS activation[J]. SCIENCE of the Total Environment, 2021, 762: 143120. DOI:10.1016/j.scitotenv.2020.143120 |
| [20] |
WU Y, SHEN H. Comprehensive recycling of manganese anode slime with modified reductant[J]. Mining and Metallurgical Engineering, 2016, 36(5): 69-72+75. |
| [21] |
FAN X, XI S, SUN D, et al. Mn-Se interactions at the cathode interface during the electrolytic-manganese process[J]. Hydrometallurgy, 2012, 127/128: 24-29. DOI:10.1016/j.hydromet.2012.07.006 |
| [22] |
左小红. 高纯电解锰生产工艺设计探讨[J]. 湖南有色金属, 2003(1): 17-19. ZUO X. Discussion on production process design of high purity electrolytic manganese[J]. Hunan Nonferrous Metals, 2003(1): 17-19. DOI:10.3969/j.issn.1003-5540.2003.01.006 |
| [23] |
ZHANG W, CHENG C Y. Manganese metallurgy review. Part Ⅱ: manganese separation and recovery from solution[J]. Hydrometallurgy, 2007, 89: 160-177. DOI:10.1016/j.hydromet.2007.08.009 |
| [24] |
黄健, 李武斌, 张谊, 等. 一体化组合体电解槽电解锰阳极泥控制机理研究[J]. 广州化工, 2020, 48(15): 76-78. HUANG J, LI W, ZHANG Y, et al. Research on control mechanism of anode mud producing manganese by combined electrolytic device[J]. Guangzhou Chemical Industry, 2020, 48(15): 76-78. DOI:10.3969/j.issn.1001-9677.2020.15.026 |
| [25] |
孙俊. 富铅电解锰渣中锰和铅回收工艺研究[D]. 昆明: 昆明理工大学, 2021. SUN J. Recovery of Mn and Pb from containing lead electrolytic manganese residues[D]. Kunming: Kunming University of Science and Technology, 2021. |
| [26] |
陈玉亮. 电解锰阳极泥中MnO2晶型调控规律及放电性能研究[D]. 重庆: 重庆大学, 2016. CHEN Y. Study on crystal shape control rule of MnO2 and discharge performance for electrolytic manganese anode slime[D]. Chongqing: Chongqing University, 2016. |
| [27] |
XIE Z, CHANG J, TAO C, et al. Polyacrylonitrile-based carbon fiber as anode for manganese electrowinning: anode slime emission reduction and metal dendrite control[J]. Journal of the Electrochemical Society, 2021, 168: 013501. DOI:10.1149/1945-7111/abd608 |
| [28] |
SHU J, LIU R, LIU Z, et al. Leaching of manganese from electrolytic manganese residue by electro-reduction[J]. Environmental Technology, 2017, 38: 2077-2084. DOI:10.1080/09593330.2016.1245789 |
| [29] |
魏汉可, 杨勇, 罗豆, 等. 电解金属锰阳极泥的综合回收利用研究[J]. 中国锰业, 2017, 35(S1): 55-58. WEI H, YANG Y, LUO D, et al. A research on comprehensive recycling of electrolytic manganese anode slime[J]. China's manganese industry, 2017, 35(S1): 55-58. |
| [30] |
严超, 杨勇, 黄冠汉, 等. 电解金属锰阳极泥资源化工程应用研究[J]. 中国锰业, 2017, 35(3): 135-137. YAN C, YANG Y, HUANG G, et al. A study on resource engineering utilization of electrolytic manganese anode slime[J]. China's manganese industry, 2017, 35(3): 135-137. |
| [31] |
LUO S, GUO H, WANG Z, et al. The electrochemical performance and reaction mechanism of coated titanium anodes for manganese electrowinning[J]. Journal of the Electrochemical Society, 2019, 166: E502-E511. DOI:10.1149/2.1071914jes |
| [32] |
LUO S, GUO H, ZHANG S, et al. Comprehensive utilization of metallurgic waste in manganese electrowinning: Towards high performance LiMn2O4[J]. Ceramics International, 2019, 45: 8607-8615. DOI:10.1016/j.ceramint.2019.01.180 |
| [33] |
刘建本, 陈上. 用电解锰阳极泥和含SO2工业尾气制备硫酸锰[J]. 化工环保, 2009, 29(6): 538-540. LIU J, CHEN S. Preparation of manganese sulfate using anode slurry from electrolytic manganese production and industrial exhaust gas containing SO2[J]. Environmental Protection of Chemical Industry, 2009, 29(6): 538-540. DOI:10.3969/j.issn.1006-1878.2009.06.014 |
| [34] |
黄良取. 电解锰阳极泥制备锰酸锂电池正极材料的工艺研究[D]. 武汉: 武汉工程大学, 2014: 83. HUANG L. Research on preparation of manganate cathode materials for lithium batteries with electrolytic manganese anode slime[D]. Wuhan: Wuhan Institute of Technology, 2014: p83. |
| [35] |
陈炳翰, 丁建华, 叶会寿, 等. 中国硒矿成矿规律概要[J]. 矿床地质, 2020, 39(6): 1063-1077. CHEN B, DING J, YE H, et al. Metallogenic regularity of selenium ore in China[J]. Mineral Deposits, 2020, 39(6): 1063-1077. |
| [36] |
FUNARI V, GOMES H I, COPPOLA D, et al. Opportunities and threats of selenium supply from unconventional and low-grade ores: a critical review[J]. Resources, Conservation and Recycling, 2021, 170: 105593. DOI:10.1016/j.resconrec.2021.105593 |
| [37] |
ABOUTALEBI MR, ISAC M, GUTHRIE R I L. The behaviour of selenium impurities during the addition of Se-containing manganese to steel melt[J]. Steel Research International, 2004, 75: 366-372. DOI:10.1002/srin.200405782 |
| [38] |
鲜金利, 童湖云, 蔡正杰, 等. 硒与新型冠状病毒研究进展[J]. 保健医学研究与实践, 2020, 17(5): 12-17. XIAN J, DONG H, CAI Z, et al. Research progress of selenium and novelcoro navirus[J]. Health Medicine Research and Practice, 2020, 17(5): 12-17. |
| [39] |
张栋. 铜阳极泥蒸硒过程中含硒物相变化的研究[D]. 昆明: 昆明理工大学, 2021. ZHANG D. Study on the change of selenium phase in copper anode slime during selenium evaporation[D]. Kunming University of Science and Technology, 2021. |
| [40] |
曾宪日, 王雨红, 屈欣轲, 等. 碱浸回收电解锰阳极泥中硒的研究[J]. 有色金属(冶炼部分), 2016(8): 48-51. ZENG X, WANG Y, QU X, et al. Seleniumre covery from manganese anode slime by alkaline leaching[J]. Nonferrous Metals (Extractive Metallurgy), 2016(8): 48-51. DOI:10.3969/j.issn.1007-7545.2016.08.011 |
| [41] |
彭思尧, 杨建广, 陈冰, 等. 含锡二次资源隔膜电积回收锡新工艺试验[J]. 中国有色金属学报, 2016, 26(12): 2656-2667. PENG S, YANG J, CHEN B, et al. Novel process for tin recovery from stannous secondary resources based on membrane electrodeposition[J]. The Chinese Journal of Nonferrous Metals, 2016, 26(12): 2656-2667. |
| [42] |
韦栋梁, 何绘宇, 夏斌. 对我国锡矿业发展的几点思考[J]. 中国矿业, 2006(1): 58-61. WEI D, HE H, XIA B. Some views on the development of tin industry in China[J]. China Mining Magazine, 2006(1): 58-61. DOI:10.3969/j.issn.1004-4051.2006.01.017 |
| [43] |
马娟, 秦德先, 薛传东. 世界锡矿资源形势预测[J]. 昆明理工大学学报(理工版), 2002(6): 13-17. MA J, QIN D, XUE C. Prediction of the situation for the world tin mines[J]. Journal of Kunming University of Science and Technology, 2002(6): 13-17. DOI:10.3969/j.issn.1007-855X.2002.06.004 |
| [44] |
崔凤平. 电解锰用阳极材料中锡的示波极谱法测定[J]. 冶金分析, 2003(4): 72. CUI F. Determination of tin in anode material by oscillopolarography for electrolytic manganese[J]. Metallurgical Analysis, 2003(4): 72. DOI:10.3969/j.issn.1000-7571.2003.04.030 |
| [45] |
TENG Y, HAN F, ZHAO S, et al. Preparation of manganese sulfate by reduction of electrolytic manganese mud with corn straws[J]. Singapore: Springer Singapore, 2018, 627-636. |
| [46] |
DU B, ZHOU C, LI X, et al. A kinetic study of Mn (Ⅱ) precipitation of leached aqueous solution from electrolytic manganese residues[J]. Toxicological&Environmental Chemistry, 2015, 97: 349-357. |
| [47] |
王强. 玉米秆还原浸出电解锰阳极泥制备化学二氧化锰研究[D]. 南宁: 广西大学, 2015. WANG Q. Study on preparation ofchemicalmanganese dioxide leaching of electrolytic mangane seanode slimer eduction for corn stalk[D]. Nanning: Guangxi University, 2015. |
| [48] |
符磊, 满瑞林, 扶强, 等. 电解锰阳极泥制备锰酸锂[J]. 广东化工, 2018, 45(8): 13-15. FU L, MAN R, FU Q, et al. Preparation of lithium manganate from electrolytic manganese anode slime[J]. Guangdong Chemical Industry, 2018, 45(8): 13-15. |
| [49] |
伍永国. 电解锰阳极渣回收制备一氧化铅和活性二氧化锰[D]. 吉首: 吉首大学, 2020. WU Y. Preparation oflead oxide and active manganese dioxide from electrolyticmanganese anode slag[D]. Jishou: Jishou University, 2020. |
| [50] |
严浩, 彭文杰, 王志兴, 等. 响应曲面法优化电解锰阳极渣还原浸出工艺[J]. 中国有色金属学报, 2013, 23(2): 528-534. YAN H, PENG W, WANG Z, et al. Reductive leaching technology of manganese anode slag optimized by response surface methodology[J]. The Chinese Journal of Nonferrous Metals, 2013, 23(2): 528-534. |
| [51] |
沈慧庭, 覃华, 黄晓毅, 等. 某含锰冶金渣中锰和铅的综合回收研究[J]. 金属矿山, 2009(6): 171-176. SHEN H, TAN H, HUANG X, et al. Research on the comprehensive recovery of manganese and an Mn-bearing metallurgical residue[J]. Metal mine, 2009(6): 171-176. |
| [52] |
ZHANG Y, YOU Z, LI G, et al. Manganese extraction by sulfur-based reduction roasting-acid leaching from low-grade manganese oxide ores[J]. Hydrometallurgy, 2013, 133: 126-132. DOI:10.1016/j.hydromet.2013.01.003 |
| [53] |
汤集刚, 韩至成. 锰阳极泥的工艺矿物学及杂质的脱除研究[J]. 矿冶, 2005(3): 75-78. TANG J, HAN Z. Investigation on process mineralogy of manganese anode slime and impurity removal[J]. Mining&Metallurgy, 2005(3): 75-78. |
| [54] |
申永强, 符智荣, 黄养逢, 等. 电解金属锰阳极泥回收制备化学二氧化锰工艺研究[J]. 中国锰业, 2007(3): 14-16. SHEN Y, FU Z, HUANG Y, et al. The research on manganese anode slime recycle to produce into chemical manganese dioxide[J]. China's Manganese Industry, 2007(3): 14-16. |
| [55] |
陈晓亮, 王海峰, 尤晓宇, 等. 两矿法浸出电解锰阳极渣中锰的研究[J]. 矿冶工程, 2021, 41(3): 92-94. CHEN X, WANG H, YOU X, et al. Leaching of manganese in anode residue from manganese electrolysis[J]. Mining and Metallurgical Engineering, 2021, 41(3): 92-94. |
| [56] |
吴焱, 沈慧庭. 改性无机还原剂还原浸出电解锰阳极泥综合回收锰铅研究[J]. 矿冶工程, 2016, 36(5): 69-72. WU Y, SHEN H. Comprehensive recycling of manganese anode slime with modified reductant[J]. Mining and Metallurgical Engineering, 2016, 36(5): 69-72. |
| [57] |
赵世珍, 韩凤兰, 滕於江, 等. 木纤维还原电解锰阳极泥制备硫酸锰工艺研究[J]. 无机盐工业, 2017, 49(6): 63-65. ZHAO S, HAN F, TENG Y, et al. Study on preparation of manganese sulfate by reduction of electrolytic manganese anode slime with wood fiber[J]. Inorganic Chemicals Industry, 2017, 49(6): 63-65. |
| [58] |
刘贵扬, 沈慧庭, 王强. 电解锰阳极泥有机还原浸出回收锰和铅的研究[J]. 矿冶工程, 2014(4): 92-98. LIU G, SHEN H, WANG Q. Recovery of manganese and lead from manganese electrowinning anode slimeby reduction leaching with organic reductants[J]. Mining and Metallurgical Engineering, 2014(4): 92-98. |
| [59] |
XIE H, ZHANG L, CHEN G, et al. High temperature roasting combined with ultrasonic enhanced extracting lead from electrolytic manganese anode mud[J]. Materials Research Express, 2019, 6(10): 105530. |
| [60] |
黎应芬, 李祥, 叶华, 等. 硫磺还原焙烧-酸浸法提取锰阳极泥[J]. 有色金属(冶炼部分), 2017(8): 13-15. LI Y, LI X, YE H, et al. Recovery of manganese anode slimes by sulfur reduction roasting-acid leaching process[J]. Nonferrous Metals (Extractive Metallurgy), 2017(8): 13-15. |
| [61] |
SHU J, LIU R, LIU Z, et al. Enhanced discharge performance of electrolytic manganese anode slime using calcination and pickling approach[J]. Journal of Electroanalytical Chemistry, 2017, 806: 15-21. |
| [62] |
WANG B, MU L, GUO S, et al. Lead leaching mechanism and kinetics in electrolytic manganese anode slime[J]. Hydrometallurgy, 2019, 183: 98-105. |
| [63] |
XIE H, LI S, GUO Z, et al. Extraction of lead from electrolytic manganese anode mud by microwave coupled ultrasound technology[J]. Journal of Hazardous Materials, 2021, 407: 124622. |
| [64] |
ZHANG Y, WANG J, LIU B, et al. Extraction and separation of Mn and Pb from electrolytic manganese anodic slime (EMAS) via SO2 roasting followed by acid leaching process[J]. JOM, 2020, 72(2): 925-932. |
| [65] |
王晖, 王重庆, 符剑刚. 硒的资源、提取及应用研究现状[J]. 稀有金属与硬质合金, 2013, 41(2): 1-5. WANG H, WANG C, FU J. Research on resource situation, extraction and application of selenium[J]. Rare Metals and Cemented Carbides, 2013, 41(2): 1-5. |
| [66] |
KILIC Y, KARTAL G, TIMUR S. An investigation of copper and selenium recovery from copper anode slimes[J]. International Journal of Mineral Processing, 2013, 124: 75-82. |
| [67] |
ZHENG Y, CHEN K. Leaching kinetics of selenium from selenium-tellurium-rich materials in sodium sulfite solutions[J]. Transactions of Nonferrous Metals Society of China, 2014, 24(2): 536-543. |
| [68] |
LIU W, YANG T, ZHANG D, et al. Pretreatment of copper anode slime with alkaline pressure oxidative leaching[J]. International Journal of Mineral Processing, 2014, 128: 48-54. |
| [69] |
覃兆财, 明宪权, 李春霞, 等. 亚硫酸铵还原浸出电解锰阳极泥中锰和硒的研究[J]. 有色金属(冶炼部分), 2020(10): 55-59. TAN Z, MING X, LI C, et al. Leaching of manganese and selenium from electrolytic manganese anode slime with ammonium sulfiteas reducing agent[J]. Nonferrous Metals (Extractive Metallurgy), 2020(10): 55-59. |
| [70] |
王雨红, 覃兆财, 黄丽燕, 等. 从电解锰阳极泥中两段浸出锰富集硒试验研究[J]. 湿法冶金, 2020, 39(2): 118-122. WANG Y, TAN Z, HUANG L, et al. Two-stage leaching of manganese and enrichment of selenium from electrolytic manganese anode slime[J]. Hydrometallurgy of China, 2020, 39(2): 118-122. |
| [71] |
韦成果. 含锡富渣烟化炉硫化挥发[J]. 有色金属(冶炼部分), 2002(4): 21-22. WEI C. Sulphurationvolatilization of rich tin slag on fuming furnace[J]. Nonferrous Metals (Extractive Metallurgy), 2002(4): 21-22. |
| [72] |
HALSALL P., HODGKIN P.. 从副产品中回收锡和中低品位锡精矿的综合利用[J]. 有色金属(冶炼部分), 1982(8): 31-37. HALSALL P., HODGKINS P.. Comprehensive utilization of tin recovery from by-products and medium and low grade tin concentrate[J]. Nonferrous Metals (Extractive Metallurgy), 1982(8): 31-37. |
| [73] |
后宝明. 碳热还原硫化挥发法从锡中矿回收金属锡的试验研究[J]. 矿冶, 2015, 24(4): 39-42. HOU B. Experiment study on tin recovery from tin middling product by carbothermic reduction and sulfidizing volatilization[J]. Mining&Metallurgy, 2015, 24(4): 39-42. |
| [74] |
钟晨, 陈淑瑜, 梁惠珠. 用低品位锡矿制取锡酸钠的研究[J]. 广东有色金属学报, 1999(1): 37-43. ZHONG C, CHEN S, LIANG H. Study on preparation of sodium stannate from the tin ore of low grade[J]. Journal of guangdong non-ferrous metals, 1999(1): 37-43. |
| [75] |
傅其华. 从低品位锡渣中制取锡酸钠[J]. 有色金属(冶炼部分), 1983(8): 10-12. FU Q. Sodium stannate is prepared from low-grade tin slag[J]. Nonferrous Metals (Extractive Metallurgy), 1983(8): 10-12. |
| [76] |
LIU W, GU K, HAN J, et al. Innovative methodology for comprehensive use of tin anode slime: preparation of CaSnO3[J]. Minerals Engineering, 2019, 143: 105945. |
 2022
2022



