| 酸/热处理对海泡石吸附甲醛的影响及其机理分析 |
2. 韶关学院 旅游与地理学院,广东 韶关 512005;
3. 湖南科技大学 材料科学与工程学院,湖南 湘潭 411201
2. School of Tourism and Geography, Shaoguan College, Shaoguan 512000, Guangdong, China;
3. School of Material Science and Engineering, Hunan University of Science and Technology, Xiangtan 411201, Hunan, China
装修材料与家具中含有大量的胶黏剂,胶黏剂在10~15年内会持续向周围环境释放甲醛,其含量容易超过《居室空气中甲醛的卫生标准》(GB/T 16127—1995)规定的上限0.080 mg/m3,危害人体健康[1]。对空气中甲醛的净化处理方法很多,归纳起来主要有通风换气法、生物净化法、吸附法、催化法等。这些方法各有利弊[2],其中常温催化氧化法是净化空气中甲醛最有前景的方法之一,但目前尚未能达到经济实用的效果[3]。而活性炭吸附法因简便廉价而在生活中常用,但它作为物理吸附法存在无选择性、易饱和、易脱附的局限。总之,目前尚无真正经济实用长效的室内甲醛去除方法。
海泡石作为一种天然的黏土矿物,存在4个与阳离子镁配位组成的八面体的结晶水、8个在晶体宽大孔道内能较自由地进出的沸石水及4个存在于三八面体结构中的羟基水(OH) [4],其特殊的结构对各种极性分子具有良好的吸附性能[5-6]。贺洋[7]和周鹏[8]分别研究了提纯和酸改性对海泡石吸附性能的影响,试验表明通过提纯和酸处理可增强海泡石对甲醛的吸附能力; 但研究中没有涉及到吸附剂的饱和吸附失活和再生问题。本文用酸处理方法作为比较,重点研究热处理温度对海泡石吸附高浓度甲醛效果的影响,并通过多种表征手段探讨相关机理,为用海泡石吸附法长效去除甲醛提供依据。
1 试验与表征方法 1.1 海泡石的加热处理海泡石由湘潭源远海泡石新材料股份有限公司提供,系经湿法物理选矿方法从低含量的沉积型海泡石矿中提纯得到。用烘箱(100~300 ℃)和马弗炉(350~600 ℃)对海泡石进行5 h加热处理后留待进行甲醛吸附试验。
1.2 海泡石酸化处理配制质量分数为15%的盐酸溶液,向溶液中加入质量10%的海泡石粉末,升温至60 ℃保温密闭搅拌8.5 h,然后用去离子水反复洗涤抽滤至滤液pH值达到6为止,在100 ℃烘干滤饼后用南昌通用化验制样机厂的振动磨研磨2 min得酸化海泡石粉。
1.3 甲醛静态吸附试验对海泡石和酸化海泡石均进行了甲醛静态吸附试验,试验前皆在100 ℃烘干。通过电蚊香加热上海阿拉丁生化科技股份有限公司提供的分析纯多聚甲醛,在85 ℃左右分解出干燥纯净的甲醛气体以方便定量。具体试验方法是在直径300 mm的干燥皿(容积约20 L)下层平铺105 ℃烘干的500 g硅胶干燥剂,将用铝箔包裹的多聚甲醛粉末固定于蚊香片位置。在带孔的陶瓷隔板上分散放置5个培养皿和温湿度计,将海泡石粉均分平铺于培养皿底部,电蚊香接通移动电源后迅速盖上涂有真空胶的干燥皿上盖。甲醛预置浓度等于多聚甲醛质量除以干燥皿容积。设海泡石吸附前质量为m0,吸附后质量为m1,没有甲醛(多聚甲醛质量为0)的空白试验测得海泡石吸附后质量为m2,则吸附一定时间的(单位质量)甲醛吸附量(mg/g):
| $ \Delta=\frac{m_{1}-m_{2}}{m_{0}} \times 1000 $ | (1) |
应用日本理学SmartLab9进行粉末X-射线衍射(XRD)检测,具体选择CuKa靶,加速电压40 kV,加速电流150 mA,6(°)/min,连续扫描。傅丽叶红外吸收光谱(FTIR)分析应用Thermo Fisher电子公司生产的Nicolet 6700傅利叶红外光谱仪对用KBr压片的样品进行检测,光谱范围为4 000~400 cm-1。热重分析使用瑞士梅特勒的设备,氮气气氛,氮气流量为40 mL/min,升温速率为10 ℃/min,温度范围为常温~800 ℃。使用美国麦克仪器公司ASAP2460孔径分析仪通过在-196 ℃的氮气吸脱附试验数据得到BET比表面积和孔径特征。扫描电子显微(SEM)分析用德国蔡司的Sigma 500扫描喷金海泡石粉体的二次电子像。
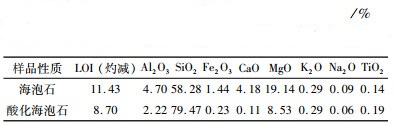
2 结果与讨论 2.1 经不同方式预处理的海泡石化学组成与物相表征比较经X射线荧光光谱分析,酸化前后海泡石的化学组成见表 1。由表 1可知,酸化海泡石的化学组成与酸化前的海泡石相比,灼减量、Al2O3、CaO和MgO显著减少,说明酸化使大量的Al3+和Mg2+被H+取代,CaO则被酸化脱除,并伴随有大量结合水的脱出。
| 表 1 海泡石其及酸化样的化学组成 Table 1 Chemical analysis of sepiolite and the acidized sepiolite |
|
XRD检测(见图 1)表明,海泡石样品分别经100 ℃、200 ℃和400 ℃热处理的样品S100、S200和S400除含有海泡石外,都还有α-石英、滑石和方解石等杂质相,经500 ℃和600 ℃热处理的样品S500和S600中仅海泡石相消失; 酸处理海泡石样品H100(经100 ℃烘干)中海泡石和方解石均消失,仅存石英与滑石。
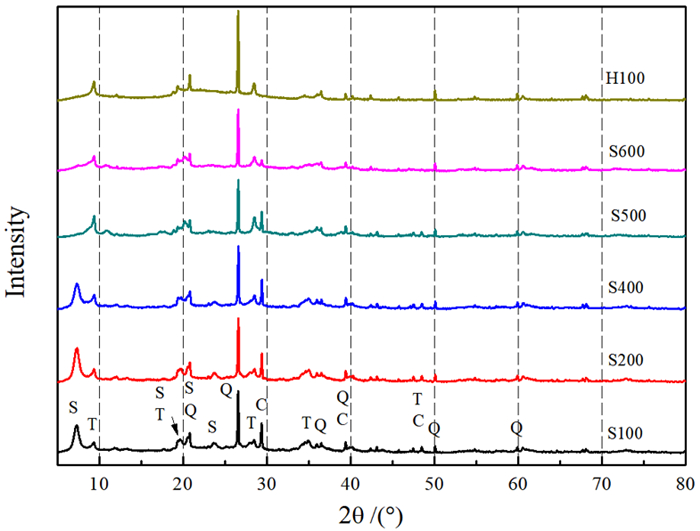 |
| S: 海泡石,Q: α-石英,T: 滑石,C: 方解石 图 1 吸附剂的XRD谱 Fig.1 XRD patterns of adsorbents |
FTIR检测(见图 2)表明,S100、S200和S400具有的对应于海泡石结晶水伸缩振动的3 562 cm-1吸收峰[9]在S500和S600中消失,但对应于结构水的3 675 cm-1吸收峰在后者中更明显; 酸化样品H100中不仅没有3 562 cm-1吸收峰,也缺失其他样品都有因C-O键振动引起的吸收峰(1 430 cm-1)。这说明经≥500 ℃热处理后,海泡石相的结晶水均已烧失,而属于海泡石相与滑石相[10]共有的结构水仍然保留; 经15 %盐酸60 ℃处理8.5 h后,海泡石晶体结构中的Mg被H大量取代,使与Mg络合的结晶水脱失,方解石相也酸解消失。
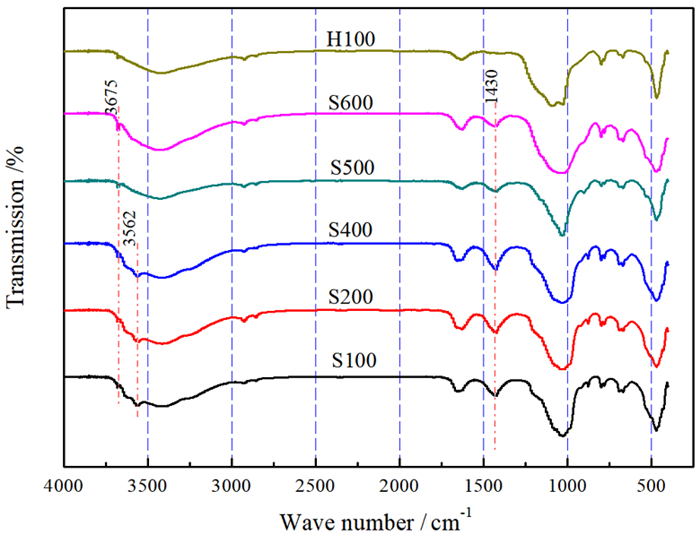 |
| 图 2 吸附剂的FTIR曲线 Fig.2 FTIR spectrum for absorbents |
热重分析(见图 3)发现,酸化海泡石仅在100 ℃处存在吸附水脱出失重,海泡石则在250~300 ℃和620~680 ℃两个温度区间均存在快速失重现象。这与海泡石在250~300 ℃失去一半的结晶水[11],至450 ℃逐渐不可逆地失去剩余的结晶水[4]相一致,而620~680 ℃的失重则对应着方解石的热分解。
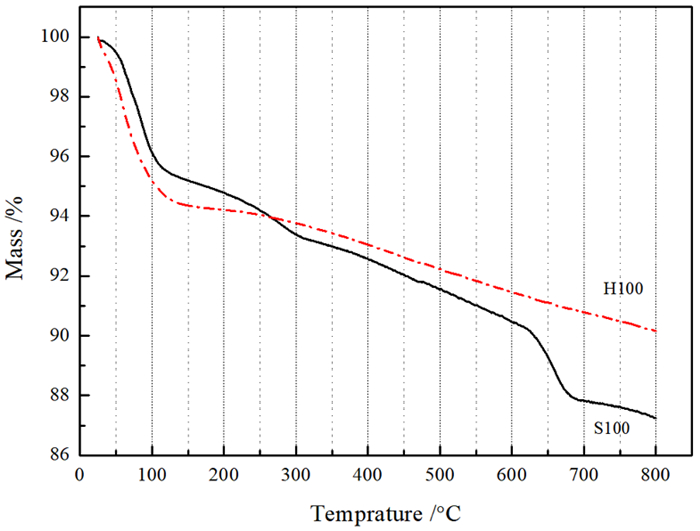 |
| 图 3 海泡石及其酸化样品的热重曲线比较 Fig.3 TGA curves for sepiolite sample and the acidized sepiolite |
BET比表面分析发现,热处理温度对样品的比表面积、孔径及粒度均有明显影响。如图 4所示,在热处理海泡石中,200 ℃处理海泡石的BET比表面积和微孔面积最大,相比之下,经500 ℃和600 ℃热处理的样品比表面积明显减小,且主要因微孔面积显著减小到接近于零所致; 酸处理后100 ℃烘干样品H100的比表面积最大,但微孔面积与100 ℃热处理过的海泡石S100相比减小,故其比表面积的增大主要由外表面的增加引起。从图 5可以看出,500 ℃和600 ℃的热处理海泡石平均孔径与平均粒径增大,但酸处理使平均孔径与平均粒径减小,说明高温热处理会促进粒子团聚,而酸处理促进了海泡石层间拆解,使粒径减小,外表面的增大促成其比表面积增大。
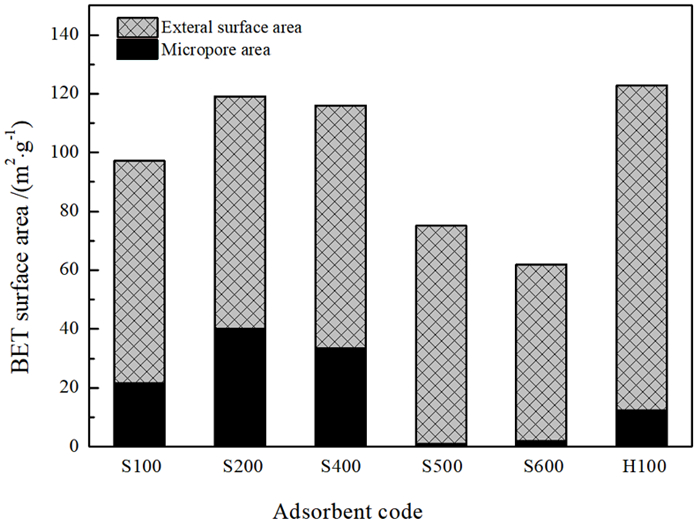 |
| 图 4 吸附剂的BET比表面积及其微孔与外比表面积 Fig.4 BET surface areas, micropore areas and exteral surface areas for adsorbents |
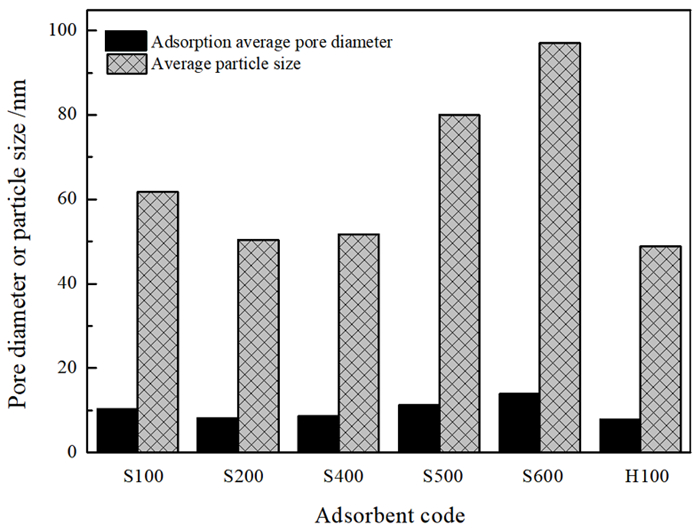 |
| 图 5 吸附剂的平均孔径与平均粒径 Fig.5 Adsorption average pore diameter and average particle size for absorbents |
扫描电镜的二次电子像表明,海泡石主要为粒径数微米的不规则“饼”状团块组成,但其细分散的晶形呈不规则的纤维状或毛发状。酸化海泡石的颗粒粒度和形貌与海泡石类似,但其细分散的纳米级颗粒更多(见图 6),这与BET比表面积分析结果一致。
 |
| 图 6 海泡石(a, b)和酸化海泡石(c, d)的SEM形貌 Fig.6 SEM morphologies for sepiolite (a, b) and acidized sepiolite(c, d) |
2.2 海泡石甲醛吸附量与热处理温度的关系
(1) 海泡石经200 ℃热处理5 h后在干燥皿中冷却至室温,然后在为67 g/m3的干燥皿中吸附6 h,研究海泡石/甲醛的质量比对吸附容量的影响,以确定合理的海泡石/甲醛质量比。试验结果见图 7。由图 7可知,随着海泡石/甲醛质量比升高,200 ℃热处理的海泡石6 h吸附量下降,但该比例从5升高至10时,吸附量下降不大,所以海泡石/甲醛质量比为10是比较合适的试验参数。
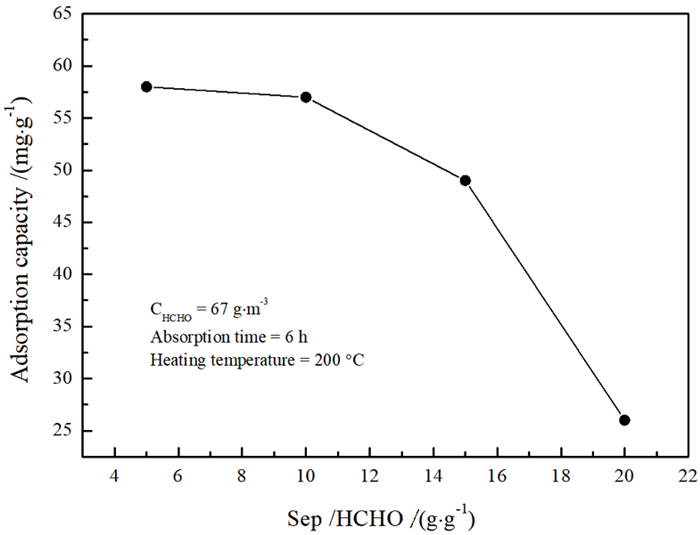 |
| 图 7 海泡石/甲醛质量比对吸附容量的影响 Fig.7 Effects of sepiolite/HCHO mass ratio on adsorption capacity |
(2) 海泡石经200 ℃热处理5 h后在干燥皿中冷却至室温,取海泡石/甲醛质量比为10,吸附时间为6 h,研究甲醛预置浓度对吸附量的影响,以确定合理的甲醛预置浓度。结果表明,海泡石的甲醛吸附量随着甲醛预置浓度的增加而增加,当甲醛预置浓度达到67 g/m3后,继续增大其浓度,甲醛吸附量增幅很小(见图 8)。
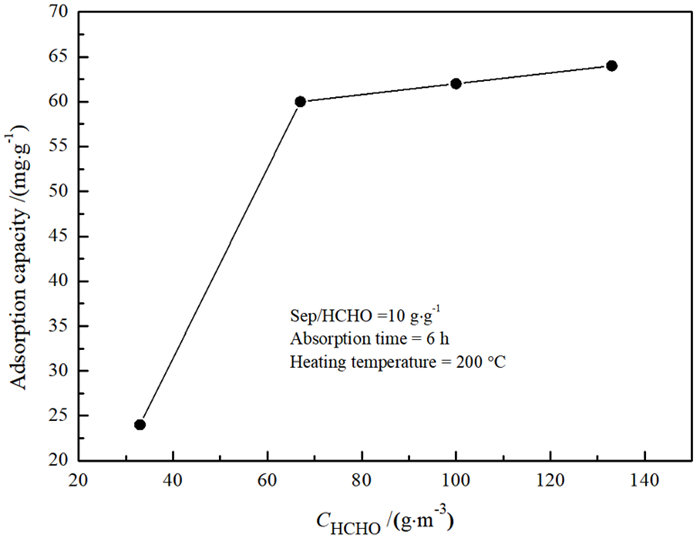 |
| 图 8 甲醛质量浓度对吸附容量的影响 Fig.8 Effects of HCHO concentration on adsorption capacity |
(3) 吸附时间的选择。取海泡石/甲醛质量比为10、甲醛预置浓度为67 g/m3,对100 ℃加热的海泡石进行不同时间的吸附试验,发现海泡石的甲醛吸附量随着吸附时间的增加而增加,吸附时间达到6 h后基本达到吸附平衡,吸附量基本稳定下来(见图 9)。
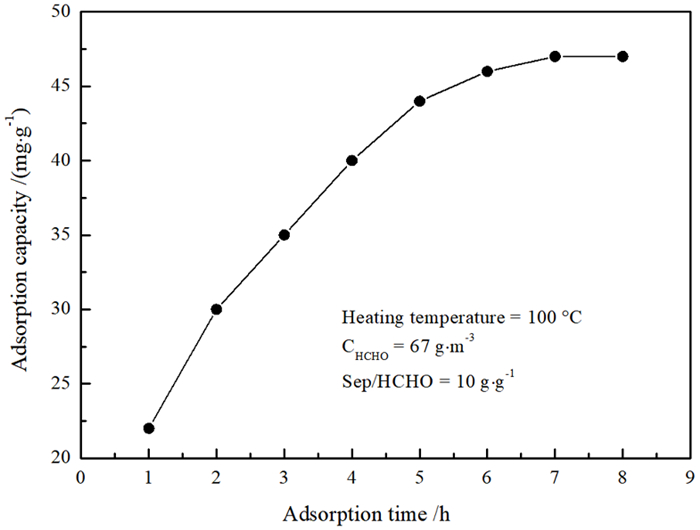 |
| 图 9 吸附时间对吸附容量的影响 Fig.9 Effects of adsorption time on adsorption capacity |
(4) 热处理温度的影响。选择试验条件: 海泡石/甲醛质量比为10、甲醛预置浓度为67 g/m3和吸附时间6 h,检测不同热处理温度下海泡石和酸化海泡石的甲醛吸附量,结果见图 10。由图 10可知,海泡石的热处理温度在100~400 ℃范围内的甲醛吸附量相对稳定,升至450 ℃时吸附量有所下降,≥500 ℃热处理的海泡石的甲醛吸附量显著降低。酸化海泡石的甲醛吸附量明显低于海泡石,仅为海泡石吸附量的1/2~2/3,这和过去认为酸化可以提高其甲醛[8]和挥发性有机物[12]吸附能力的结果明显不同。酸化海泡石在热处理升温至450 ℃时吸附量下降,≥500 ℃热处理后下降更明显,但亦显著高于同处理温度的海泡石。
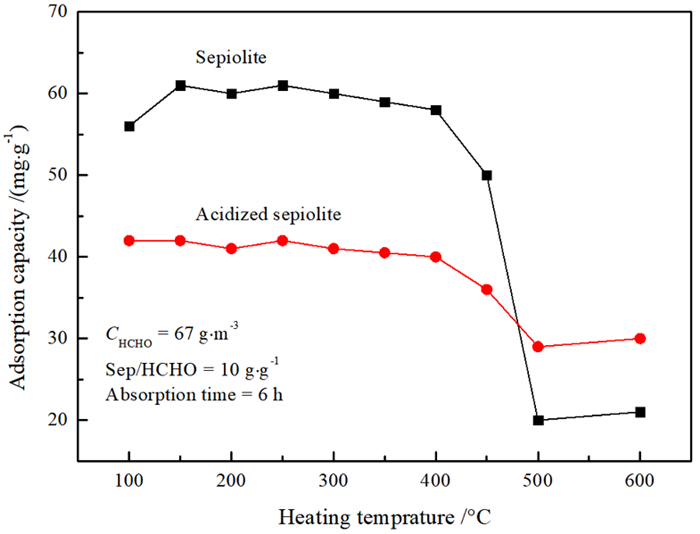 |
| 图 10 热处理温度对吸附容量的影响 Fig.10 Effects of heating temperature on adsorption capacity |
2.3 海泡石甲醛吸附机理探讨
60 ℃酸化使海泡石中大量的Al3+和Mg2+被H+取代,原本与Mg2+结合的结晶水脱出,海泡石的晶体结构瓦解,且平均粒度下降,外表面增加,从而比表面积提高,而其微孔面积则因结构孔坍塌而显著减小,并降低其甲醛吸附量。
≥100 ℃的热处理导致海泡石结构中部分沸石水脱出而留下微孔,≥250 ℃热处理脱出所有的沸石水[4]。同为极性分子的甲醛最容易被结晶水吸附并占位邻近的沸石微孔,而且第一层甲醛分子可能通过氢键与结晶水联接而形成一定的化学吸附。海泡石在≥450 ℃的热处理时不可逆地失去所有的结晶水[4],导致晶体结构畸变,沸石孔坍塌消失,甲醛分子不仅失去与结晶水的化学吸附条件,还无法占位沸石孔形成物理吸附,所以≥500 ℃的高温热处理会严重降低海泡石的甲醛吸附性能。
吸附的甲醛通过升温可以脱附,从而热处理达到甲醛吸附饱和的海泡石可以实现海泡石吸附剂的热再生,温度越高,甲醛脱附越快,当温度高至甲醛的燃点时更可快速氧化消除。但热处理温度不应该超过450 ℃,以保留结构中可恢复的结晶水,以保持其吸附能力,从而延长海泡石质甲醛吸附剂的使用寿命。另一方面,酸化虽然可以一定程度提高其比表面积,但容易引起结晶水脱出和沸石微孔坍塌,严重降低其甲醛吸附性能,故需要审慎设置酸化条件。
3 结论(1) 通过对高浓度甲醛的静态吸附试验发现,在有干燥剂存在的前提下,热处理后的海泡石对空气中的甲醛保持良好的吸附效果,但≥500 ℃的热处理会显著降低海泡石的甲醛吸附性能; 以质量分数15%的盐酸于60 ℃酸化海泡石8.5 h严重降低其甲醛吸附性能。
(2) 推测海泡石相的结晶水对甲醛形成化学吸附,而其沸石孔洞有利于物理吸附的甲醛占位,而综合表征发现,≥500 ℃的热处理和不适当的酸处理会去除海泡石的结晶水,并使沸石孔洞坍塌封闭,是导致其对甲醛吸附能力显著下降的原因。
(3) 海泡石经450 ℃热处理后仍能保持良好的吸附性能,该温度高于甲醛的燃点430 ℃,表明达到甲醛吸附饱和的海泡石经≤450 ℃热处理可以同步脱附和去除甲醛并恢复吸附性能,这对持续反复利用海泡石的吸附性能去除空气中的甲醛具有指导意义。
| [1] |
崔维怡, 王希越, 谭乃迪. 甲醛催化氧化反应机理的研究进展[J]. 精细化工, 2020, 37(10): 1978-1985. CUI W Y, WANG X Y, TAN N D. Research progress in the mechanism of catalytic oxidation of formaldehyde[J]. Fine Chemicals, 2020, 37(10): 1978-1985. |
| [2] |
张永航. 空气中甲醛净化处理的研究进展[J]. 广州化工, 2020, 48(22): 24-27+89. ZHANG Y H. Research progress on formaldehyde purification in air[J]. Guangzhou Chemical Industry, 2020, 48(22): 24-27+89. |
| [3] |
黄慧娟, 尚莉莉, 马建锋, 等. 锰氧化物催化分解室内甲醛的研究进展[J]. 材料导报, 2019, 33: 521-525. HUANG H J, SHANG L L, MA J F, et al. Advances on catalytic oxidation of formaldehyde by manganese oxide[J]. Materials Reports, 2019, 33: 521-525. |
| [4] |
王濮, 潘兆橹, 翁玲宝, 等. 系统矿物学(中册)[M]. 北京: 地质出版社, 1987: 419-421. WANG P, PAN Z L, WEN L B, et al. Systemic Mineralogy(middle volume)[M]. Beijing: Geology Press, 1987: 419-421. |
| [5] |
CORUH S, GEYIKEI F, ELEVLI S. Adsorption of neutral red dye from an aqueous solution onto natural sepiolite using full factorial design[J]. Clays and Clay Minerals, 2011, 59(6): 617-625. DOI:10.1346/CCMN.2011.0590607 |
| [6] |
鲁旖, 仇丹, 章凯丽. 海泡石吸附剂的应用研究进展[J]. 宁波工程学院学报, 2016, 28(1): 17-22. LU Y, QIU D, ZHANG K L. Research progress on application of sepiolite absorbent[J]. Journal of Ningbo University of Technology, 2016, 28(1): 17-22. |
| [7] |
贺洋. 低品质海泡石提纯及吸附性能研究[J]. 非金属矿, 2019, 42(4): 56-57. HE Y. Purification of low quality sepiolite and adsorption capacity research[J]. Non-Metallic Mines, 2019, 42(4): 56-57. |
| [8] |
周鹏. 改性海泡石制备及其对甲醛的吸附行为研究[D]. 武汉: 武汉理工大学, 2019. ZHOU P. Preparation of modified sepiolite and adsorption behavior to formaldehyde[D]. Wuhan: Wuhan University of Technology, 2019. |
| [9] |
宋公保, 彭同江, 董发勤, 等. 海泡石的红外光谱研究[J]. 矿物学报, 1998, 18(4): 525-532. SONG G B, PENG T J, DONG F Q, et al. Infrared spectrometric study of sepiolite[J]. Acta Mineralogica Sinica, 1998, 18(4): 525-532. DOI:10.3321/j.issn:1000-4734.1998.04.019 |
| [10] |
王艳, 王多君, 易丽. 空气气氛中滑石的热分解动力学试验研究[J]. 中国科学院大学学报, 2015, 32(1): 70-73. WANG Y, WANG D J, YI L. Experimental study on thermal decomposition kinetics of talc under the condition of air[J]. Journal of University of Chinese Academy of Sciences, 2015, 32(1): 70-73. |
| [11] |
聂利华, 刘德忠, 姚守拙. 海泡石的物化特性[J]. 湖南大学学报, 1990, 17(1): 106-113. NIE L H, LIU D Z, YAO S C. Physichemieal Properties of sepiolite of Liuyang County in Hunan Province[J]. Journal of Hunan University, 1990, 17(1): 106-113. |
| [12] |
梁伟朝. 海泡石改性及其吸附挥发性有机物机理与过程研究[D]. 石家庄: 河北科技大学, 2016. LIANG W C. Adsorption mechanism and process of VOCs on Modified sepiolite[D]. Shijiazhuang: Hebei University of Science and Technology, 2016. |
 2022
2022



