2. 传化智联股份有限公司, 浙江 杭州 311215
2. Transfar Zhilian Co. Ltd., Hangzhou 311215, China
氟代丙烯酸酯类共聚物具有优异的防水、防油和防污性能,在涂料、织物整理剂等方面得到广泛应用[1-4]。用作织物整理剂的氟代丙烯酸酯类聚合物通常由氟代和非氟代(甲基)丙烯酸酯单体共聚而成。当氟代丙烯酸酯单体的氟代烷链碳原子数不小于6,(甲基)丙烯酸酯的烷链碳原子数不小于12时,共聚物具有结晶性,共聚物中的氟代烷基和长链烷基在涂层表面可以有序排列,通过两者的协同作用得到具有防水、防油和防污效果的涂层[5-7]。乳液聚合是合成织物整理用氟代丙烯酸酯共聚物的主要方法,但由于含氟单体在水中的溶解性极小,不易从单体液滴向胶束扩散,需要加入一定量的有机溶剂或采用特殊的含氟乳化剂来提高其溶解性,导致织物整理使用过程的环境污染[8-9]。与常规乳液聚合相比,加入了助乳化剂的细乳液聚合以稳定的单体液滴为聚合场所,不需要单体的水相扩散,因此特别适用含高疏水性的氟代丙烯酸酯单体参与的聚合[10-12]。
采用活性自由基聚合(living radical polymerization, LRP)可制备结构可控、具有嵌段等特殊拓扑结构的聚合物。根据不同LRP机理制备氟代丙烯酸酯共聚物已有一些报道,如Li等[13]采用原子转移自由基聚合(atom transfer radical polymerization, ATRP)制备了全氟烷基丙烯酸酯-甲基丙烯酸甲酯嵌段共聚物;Zhu等[14]采用ATRP方法合成了聚甲基丙烯酸异辛酸酯-b-1H, 1H-全氟辛基丙烯酸酯和聚甲基丙烯酸异辛酸酯-b-1H, 1H, 2H, 2H-全氟辛基丙烯酸酯共聚物;Zhang等[15-16]采用可逆加成-断裂链转移(reversible addition fragmentation chain transfer polymerization,RAFT)细乳液聚合制备了氟代丙烯酸酯-甲基丙烯酸丁酯无规和嵌段共聚物;Li等[17]采用RAFT溶液聚合制备了聚(甲基丙烯酸甲酯-co-甲基丙烯酸)-b-聚全氟烷基乙基甲基丙烯酸酯共聚物。碘转移聚合是以氟代烷基碘或烷基碘为链调控剂,由普通自由基聚合引发剂引发的LRP,已用于偏氟乙烯等含氟乙烯基单体聚合,及其嵌段共聚物的工业合成[18]。但是,采用碘转移聚合制备织物整理用氟代丙烯酸酯共聚物还少有报道。
本文采用碘转移细乳液聚合方法合成具有优异疏水疏油特性的氟代丙烯酸酯-丙烯酸十八酯共聚物,并研究聚合动力学、聚合活性特性和共聚物涂层的界面性能,为制备结构可控的氟代丙烯酸酯-丙烯酸十八酯共聚物及进一步进行嵌段共聚提供基础。
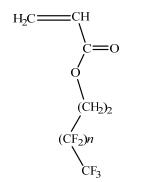
2 实验部分 2.1 实验试剂与仪器氟代丙烯酸酯(fluoroacrylate,FA,工业级,结构见图 1,n=6~10,其中n=8的组成物的质量分数为70.2%),丙烯酸十八酯(stearyl acrylate,SA,百灵威科技有限公司,分析纯),甲基丙烯酸甲酯(methyl methacrylate, MMA,国药集团化学试剂有限公司, 分析纯),十六烷基三甲基溴化铵(hexadecyl trimethyl ammonium bromide,CTAB,国药集团化学试剂有限公司, 分析纯),十六烷(hexadecane,HD,百灵威科技有限公司,分析纯),碘仿(iodoform,CHI3,国药集团化学试剂有限公司, 化学纯),2, 2’-偶氮二异丁基脒二盐酸盐(2, 2'-azobis(2-methylpropionamidine)dihydrochloride,AIBA,百灵威科技有限公司,分析纯),对苯二酚(百灵威科技有限公司,分析纯),甲醇(国药集团化学试剂有限公司,分析纯)。
|
图 1 氟代丙烯酸酯单体结构式 Fig.1 Structure of fluoroacrylate monomer |
将一定量的主乳化剂CTAB溶解于适量去离子水中配成水相,取一定量的助乳化剂HD和碘仿溶于一定量的FA/SA单体混合物中配成油相;将水相和油相混合并磁力搅拌,接着在冰水浴中用超声波细胞粉碎机进行细乳化,得到预乳化液;将预乳液转移到反应釜中,通氮排氧,搅拌下升温至设定聚合温度,用注射器将AIBA引发剂水溶液注入反应釜中,开始聚合,并在不同聚合时间取样,用于聚合转化率测试。
2.3 扩链反应在上述碘封端的氟代丙烯酸酯共聚物乳液中加入定量的MMA单体,待其充分溶胀后,补加AIBA引发剂水溶液,在设定聚合温度下反应,反应结束后用甲醇破乳、抽滤、去离子水反复洗涤、过滤、真空干燥,得到MMA扩链共聚物。
2.4 测试与表征单体转化率:采用称重法测定,在聚合过程中定时称取2~3 g乳液,置于已称重的称量瓶中,滴入约0.1 mL质量分数为5% 的对苯二酚乙醇溶液阻聚,120 ℃下真空干燥至恒重,计算转化率:
| $ {\rm{conversion = }}\frac{{{m_2} - {m_0} - {m_1} \times {w_0}}}{{{m_1} \times w}} \times 100\% $ | (1) |
式中:m2为干燥至恒重后的总质量;m1为称取乳液的质量;m0为空称量瓶质量;w0为细乳液中乳化剂和阻聚剂的质量分数;w为细乳液中未聚合前单体的质量分数。
聚合物平均分子量及分子量分布:采用Waters 1525 / 2414凝胶渗透色谱仪(GPC)测定,样品质量分数为0.3%~0.5%,四氢呋喃为溶剂,以窄分布聚苯乙烯为标样。
聚合物结构:采用傅里叶变换红外光谱仪对共聚物进行结构表征,测试范围4 000~500 cm-1。采用Bruker Avance 500M超导核磁共振仪测定共聚物结构,氘代氯仿为溶剂,四甲基硅氧烷为内标物。
聚合物特性:采用美国TA公司的TA Q500热重分析仪在氮气氛围下分析聚合物的热失重特性,升温速率20 ℃·min-1,温度50~600 ℃。采用NETZSCH5 ASCII型差示扫描量热仪分析聚合物的热转变行为,氮气气氛,测量温度为-50~120 ℃,升温速率10 ℃·min-1。将乳液均匀涂布在洁净的载玻片上,室温下放置24 h,自然干燥成膜,采用德国Dataphysics公司的OCA 20视频光学接触角测量仪进行接触角测量,选择水和正十六烷为参比液体,液滴体积为3.5 μL,每个样品测4~5次,然后根据Owens和Wendt理论[19],通过参比液体在样品表面的接触角计算共聚物的表面张力(如式(2)):
| $ {\gamma _{{\rm{sL}}}}{\rm{ = }}{\gamma _s}{\rm{ + }}{\gamma _L} - 2{\left( {\gamma _s^d\gamma _L^d} \right)^{1/2}} - 2{\left( {\gamma _s^p\gamma _L^p} \right)^{1/2}} $ | (2) |
| $ {\rm{结合Young氏方程}}\ \ \ \ \ \ {\gamma _L}\cos \theta = {\gamma _s} - {\gamma _{sL}} - {\pi _e} $ | (3) |
| $ {\rm{可以得到式(4):}}\ \ \ \ {\gamma _L}\left( {1{\rm{ + }}\cos \theta } \right){\rm{ = }}2{\left( {\gamma _s^d\gamma _L^d} \right)^{1/2}}{\rm{ + }}2{\left( {\gamma _s^p\gamma _L^p} \right)^{1/2}} $ | (4) |
式中:θ为液体与固体表面的接触角;γ为表面张力;γs、γL、γsL分别为固-气、液-气和固-液之间的表面张力;γsd、γsp分别为固体样品表面张力的色散部分和极性部分;γLd、γLp分别为参比液体表面张力的色散部分和极性部分;πe表示在固体表面液体的平衡蒸汽压,由于πe远小于γL,所以πe可忽略不计。以水和十六烷为参比液,其中水的γ、γ d、γp分别为72.8、21.8和51.0 mN·m-1,十六烷的γ、γ d、γ p分别为27.6、27.6和0 mN·m-1[20]。
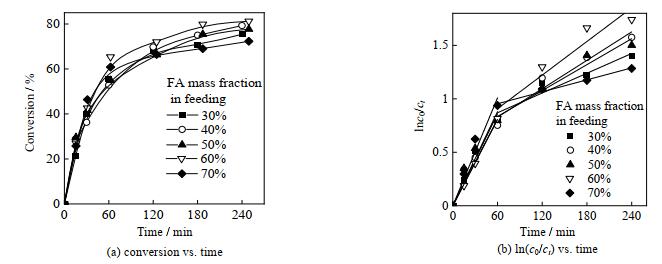
3 结果与讨论 3.1 聚合动力学首先在固定碘仿和引发剂浓度、聚合温度θ条件下,研究单体投料组成对聚合动力学的影响, 得到不同单体组成时聚合转化率、ln(c0/ct) (c0和ct为0和t时刻的单体浓度,mol·L-1)随时间的变化如图 2所示,n(M): n(CHI3): n(AIBA)为单体、CHI3、AIBA的量比,m(FA-SA)为FA和SA混合物的质量。
|
图 2 不同单体投料组成时FA-SA共聚动力学 Fig.2 Kinetics of FA-SA copolymerization with different monomer feeding compositions (n(M): n[CHI3]: n[AIBA]=500:1:1, m(FA-SA)=10 g, θ=60 ℃) |
由图可见,不同投料单体组成时,反应时间240 min后的转化率都能达到70% 以上,ln(c0/ct)与反应时间呈两段线性关系,当投料单体中FA分率由30% 增加至70%,表观速率常数kp1分别为0.014、0.013、0.015、0.014和0.017 min-1,kp2分别为0.003、0.004、0.004、0.006和0.002 min-1,说明单体组成对初期聚合速率影响并不大,但后期反应速率随投料单体中FA估量分数的增加先增大后下降。
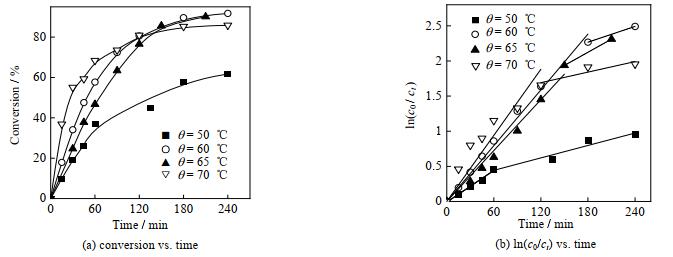
固定FA/SA质量比、碘仿和AIBA引发剂浓度,不同温度下的FA-SA共聚合转化率-时间、ln(c0/ct)-时间关系如图 3所示。
|
图 3 不同聚合温度时FA-SA共聚动力学 Fig.3 Kinetics of FA-SA copolymerization at different temperatures (m(FA): m(SA)=6/4, n(M): n(CHI3): n(AIBA)=500:1:1, m(FA-SA)=10 g) |
由图可见,聚合温度对聚合动力学的影响较大,当温度为50 ℃时,AIBA的分解半衰期远远长于反应时间,聚合速率较慢,最终转化率较低;而温度为60和65 ℃时,聚合反应表现出较大的反应速率,两个温度下表观速率常数kp1分别为0.013和0.012 min-1,kp2分别为0.004和0.006 min-1,并且反应240 min后最终转化率都能达到90% 以上;当温度升高至70 ℃,表观速率常数kp1达到0.013 min-1,反应速率较快,但最终的转化率反而不高,这是由于较高温度下,前期引发剂快速分解产生大量自由基聚合速率大,后期则因引发剂消耗过多,聚合速率下降。此外,较高的聚合温度会影响分子链末端C-I键的断裂,导致部分碘末端失活。因此,为了既能保证较快的反应速率,又保证碘末端少失活,60 ℃为合适的聚合温度。
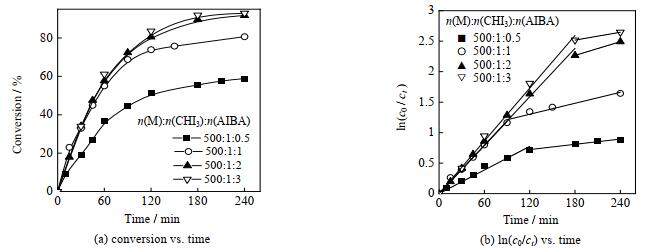
固定其他条件,AIBA引发剂浓度对转化率-时间、ln(c0/ct) -时间的影响如图 4所示。
|
图 4 不同引发剂浓度下FA-SA共聚动力学 Fig.4 Kinetics of FA-SA copolymerization with different initiator concentrations (m(FA): m(SA)=6/4, m(FA-SA)=10 g, θ=60 ℃) |
由图可见,当引发剂浓度较低,仅为碘仿浓度的一半时,聚合速率较低,表观速率常数kp1只有0.006 min-1,反应240 min后转化率仅为60%。这是因为AIBA较少时,分解产生的自由基数目少,自由基进入单体液滴内进行碘转移自由基聚合较弱;随着引发剂浓度不断增大,当引发剂浓度是碘仿浓度的等量、2倍和3倍时,最终反应转化率明显提升(达85%),表观速率常数kp1分别为0.013、0.013和0.014 min-1,由此采用适量的碘仿与催化剂用量,可以有效提高聚合反应速率。
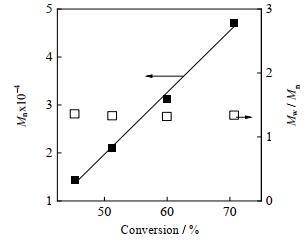
3.2 聚合活性特征的验证当聚合温度为60 ℃,n(M): n(CHI3): n(AIBA)=500:1:1,m(FA): m(SA)=6/4当聚合温度为60 ℃,n(M): n(CHI3): n(AIBA)=500:1:1,m(FA): m(SA)=6/4时,聚合过程取样得到不同转化率共聚物样品,共聚物数均分子量Mn和分子量分布随转化率的变化如图 5所示。可见,共聚物数均分子量随转化率的增大而线性增大,共聚物的分子量分布指数(Mw/Mn)为1.34左右,分布较窄,初步说明碘仿调控的FA-SA细乳液共聚合具有活性特征。
|
图 5 共聚物Mn和Mw / Mn随转化率的变化 Fig.5 Variation of Mn and Mw / Mn of FA-SA copolymers with conversion |
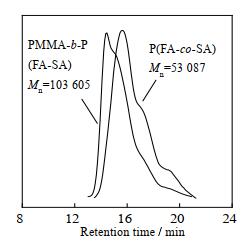
为了进一步证明聚合的活性特征,在得到的共聚物细乳液中加入一定量的MMA单体,并补加引发剂,继续进行聚合反应,加入MMA扩链聚合前后的共聚物GPC曲线如图 6所示。GPC曲线表现为整体向左平移,分子量明显增大,表明含碘末端的FA-SA共聚物仍具有活性特征,可以继续进行引发聚合而得到嵌段共聚物。这为有效制备结构规整、可控的嵌段型氟代丙烯酸酯类织物整理剂提供了新方法。
|
图 6 FA-SA共聚物扩链前后的GPC曲线 Fig.6 GPC curves of FA-SA copolymers and chain-extended product with MMA |
FA-SA共聚物的傅里叶红外光谱、核磁共振氢谱分别如图 7、8所示。
|
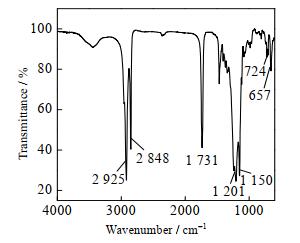
图 7 FA-SA共聚物红外光谱 Fig.7 FT-IR spectra of FA-SA copolymer |
|
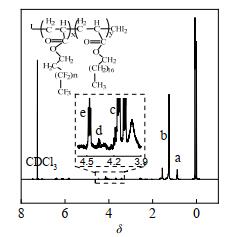
图 8 FA-SA共聚物核磁共振氢谱 Fig.8 1H NMR spectra of FA-SA copolymer |
FA-SA共聚物在吸收峰2 925、2 848 cm-1处分别是─CH3、─CH2的伸缩振动峰,1 731 cm-1处是酯基中的─CO─的强伸缩振动峰,1 200 cm-1处是C─O─C的伸缩振动峰,1 000~1 400 cm-1处表现为C─F的特征吸收峰,724 cm-1处是─(CH2)n─(n≥4)的长链吸收峰,657 cm-1处为C─F的弯曲振动峰,其中在1 640 cm-1处没有出现C═C键吸收峰。
FA-SA共聚物在化学位移δ = 0.8处的a峰对应于SA中的─CH3的核磁共振氢谱,δ =1.3处的b峰对应于SA中的─CH2—的核磁共振氢谱,δ =4.15处的c峰对应于FA和SA中─COO─CH2上氢的化学位移[10],δ =4.37处的d峰对应的是末端的次甲基(─CHI2)上质子氢的特征峰,而图中化学位移在δ=4.47处的e峰对应的是末端的次甲基(─CH2I)上质子氢的特征峰[21]。其中d峰和e峰的峰面积之比Id/Ie为1:2.2,接近理论值1:2,表明得到的共聚物一端为碘原子,另一端是碘仿失去1个碘原子后的残基─CHI2,与碘转移活性自由基聚合机理相符。合成共聚物时的单体投料摩尔比为1:1,通过比较c峰和a峰的相对峰面积可以计算得到Ic/Ia为1.08:0.91,进一步可得n(FA): n(SA)=0.8:1,与投料比(1:1)相当。这是因为细乳液聚合时,单体液滴为聚合场所,基本没有单体向水相扩散,每个单体液滴内的组成和投料基本保持一致。
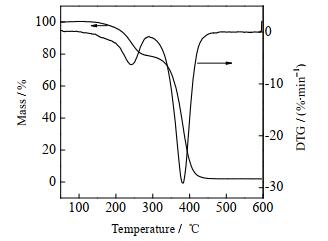
3.4 FA-SA共聚物的特性图 9为典型的FA-SA共聚物的热失重曲线。可见,共聚物的热分解过程可以分为2个阶段:第1阶段的热分解起始温度为210 ℃,最大分解速率时分解温度为243 ℃,热失重速率为6.29 %·min-1,这是由于聚丙烯酸十八酯具有较长的─CH2─侧链,容易先分解,从而形成第1个失重阶段;第2个阶段的热分解起始温度为310 ℃,最大分解速率时分解温度为382 ℃,热失重速率为29.14 %· min-1,这是由于310 ℃后,聚合物主链断裂,开始形成第2个失重阶段。当温度为467 ℃时,共聚物的质量不再变化,体系达到恒量状态,说明在该温度下聚合物已分解完全。含氟链段结构的存在,提高了聚合物的分解温度和耐热性。
|
图 9 FA-SA共聚物的热失重曲线 Fig.9 TG-DTG curve of FA-SA copolymer |
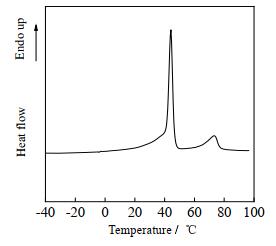
图 10为FA-SA共聚物的典型DSC曲线。可见,在-50~100 ℃并没有出现玻璃化转变区,但在43.8 ℃处,出现了1个强的归属于聚丙烯酸十八酯链段的熔融峰,在71.8 ℃处出现了聚氟代丙烯酸酯链段的熔融峰。
|
图 10 FA-SA共聚物的DCS曲线 Fig.10 DSC curve of FA-SA copolymer |
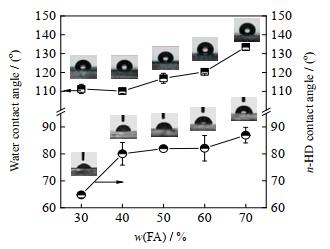
将不同组成的FA-SA共聚物乳液滴在洁净的玻璃片上自然干燥得到乳胶膜,对其进行静态接触角测量,结果如图 11所示,w(FA)为FA的质量分数。当w(FA)=30%~70%,共聚物膜的静态水接触角均大于110°,十六烷的接触角均大于60°,且当单体中w(FA)由30% 增加到70%,水接触角从110°增大到130°,十六烷接触角从65°增大到87°,表现出较好的疏水疏油性。这是由于氟代丙烯酸酯中的C─F键能够显著降低临界表面张力和表面自由能,而且含氟链段有富集趋势,在成膜过程中含氟链段容易向空气界面迁移,从而降低表面自由能。
|
图 11 不同FA含量的水和十六烷的接触角 Fig.11 Water and n-HD contact angle at different FA contents |
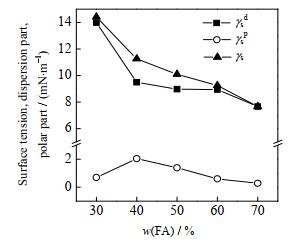
计算得到的FA-SA共聚物的表面张力如图 12所示。可见,随着w(FA)的增加,共聚物的表面张力逐渐降低,表面张力均小于15×10-3 N·m-1,当w(FA)=70% 时,表面张力只有7.66×10-3 N·m-1,表现出极低的表面张力。
|
图 12 不同FA含量共聚物的表面张力值 Fig.12 Surface tension at different FA contents |
以CHI3为链转移剂、AIBA为引发剂、CTAB/HD为主/助乳化剂,成功实现了FA-SA碘转移细乳液共聚合。当n[AIBA]: n[CHI3]=1:1,聚合温度为60 ℃下,FA-SA共聚合反应速率kp1=0.013 min-1,反应240 min转化率达90% 以上。碘封端的共聚物具有活性特征,通过扩链反应可以进一步合成嵌段共聚物。制得的FA-SA共聚物热稳定性良好,静态水接触角为110°~130°,十六烷接触角大于60°,表面张力小于15×10-3 N·m-1,具有优异的疏水疏油特性。
| [1] |
MONDAL S, PAL S, MAITY J. Transparent and double sided hydrophobic functionalization of cotton fabric by surfactant-assisted admicellar polymerization of fluoromonomers[J]. New Journal of Chemistry, 2018, 42(3): 6831-6838. |
| [2] |
GRAHAM P, STONE M, THORPE A, et al. Fluoropolymers with very low surface energy characteristics[J]. Journal of Fluorine Chemistry, 2000, 104(1): 29-36. DOI:10.1016/S0022-1139(00)00224-4 |
| [3] |
YAO W, LI Y, HUANG X. Fluorinated poly(meth)acrylate: Synthesis and properties[J]. Polymer, 2014, 55(24): 6197-6211. DOI:10.1016/j.polymer.2014.09.036 |
| [4] |
TAKAYANAGI T, YAMABE M. Progress of fluoropolymers on coating applications: Development of mineral spirit soluble polymer and aqueous dispersion[J]. Progress in Organic Coatings, 2000, 40(1): 185-190. |
| [5] |
XU W, AN Q, HAO L, et al. Synthesis of self-crosslinking fluorinated polyacrylate soap-free latex and its waterproofing application on cotton fabrics[J]. Fibers and Polymers, 2014, 15(3): 457-464. DOI:10.1007/s12221-014-0457-8 |
| [6] |
MORITA M, OGISU H, KUBO M. Surface properties of perfluoroalkylethyl acrylate/n-alkyl acrylate copolymers[J]. Journal of Applied Polymer Science, 1999, 73(9): 1741-1749. DOI:10.1002/(SICI)1097-4628(19990829)73:9<1741::AID-APP15>3.0.CO;2-F |
| [7] |
AGIRRE A, NASE J, DEGRANDI E, et al. Improving adhesion of acrylic waterborne PSAs to low surface energy materials: Introduction of stearyl acrylate[J]. Journal of Polymer Science Part A: Polymer Chemistry, 2010, 48(22): 5030-5039. DOI:10.1002/pola.24300 |
| [8] |
张庆华, 詹晓力, 陈丰秋. FA/LMA/MMA三元共聚物乳液的合成与性能[J]. 纺织学报, 2005, 26(2): 4-7. ZHANG Q H, ZHAN X L, CHEN F Q. Synthesis and properties of the FA/LMA/MMA copolymer emulsion[J]. Journal of textile research, 2005, 26(2): 4-7. DOI:10.3321/j.issn:0253-9721.2005.02.002 |
| [9] |
JIANG Y, LI L, LIU J, et al. Hydrophobic films of acrylic emulsion by incorporation of fluorine-based copolymer prepared through the RAFT emulsion copolymerization[J]. Journal of Fluorine Chemistry, 2016, 183: 82-91. DOI:10.1016/j.jfluchem.2016.01.010 |
| [10] |
张庆华, 詹晓力, 陈丰秋. 氟代丙烯酸酯三元共聚物细乳液的合成与表征[J]. 高等学校化学学报, 2005, 26(3): 575-579. ZHANG Q H, ZHAN X L, CHEN F Q. Synthesis of fluorinated acrylate ternary copolymer latex by miniemulsion polymerization and characterization[J]. Chemical Journal of Chinese Universities, 2005, 26(3): 575-579. DOI:10.3321/j.issn:0251-0790.2005.03.037 |
| [11] |
ZHANG Q H, LUO Z H, ZHAN X L, et al. Monomer reactivity ratios for fluoroacrylate and butyl methacrylate in miniemulsion copolymerizations initiated by potassium persulphate[J]. Chinese Chemical Letters, 2009, 20(4): 478-482. DOI:10.1016/j.cclet.2008.12.041 |
| [12] |
ZHANG Q, ZHAN X, CHEN F. Miniemulsion polymerization of a fluorinated acrylate copolymer: Kinetic studies and nanolatex morphology characterization[J]. Journal of Applied Polymer Science, 2007, 104(1): 641-647. DOI:10.1002/app.25639 |
| [13] |
LI K, WU P, HAN Z. Preparation and surface properties of fluorine-containing diblock copolymers[J]. Polymer, 2002, 43(14): 4079-4086. DOI:10.1016/S0032-3861(02)00202-1 |
| [14] |
ZHU Y, FORD W T. Novel fluorinated block copolymer stabilizers for dispersion polymerization of cross-linked poly (2-ethylhexyl methacrylate-stat-chloromethylstyrene) in fluorinated solvents[J]. Macromolecules, 2008, 41(16): 6089-6093. DOI:10.1021/ma800111t |
| [15] |
ZHANG Q, WANG Q, LUO Z, et al. Conventional and RAFT miniemulsion copolymerizations of butyl methacrylate with fluoromethacrylate and monomer reactivity ratios[J]. Polymer Engineering & Science, 2009, 49(9): 1818-1824. |
| [16] |
ZHANG Q, ZHAN X, CHEN F, et al. Block copolymers of dodecafluoroheptyl methacrylate and butyl methacrylate by RAFT miniemulsion polymerization[J]. Journal of Polymer Science Part A: Polymer Chemistry, 2007, 45(9): 1585-1594. DOI:10.1002/pola.21930 |
| [17] |
LI X, YANG Y, LI G, et al. Synthesis and self-assembly of a novel fluorinated triphilic block copolymer[J]. Polymer Chemistry, 2014, 5(15): 4553-4560. DOI:10.1039/C4PY00308J |
| [18] |
DAVID G, BOYER C, TONNAR J, et al. Use of iodocompounds in radical polymerization[J]. Chemical Reviews, 2006, 106(9): 3936-3962. DOI:10.1021/cr0509612 |
| [19] |
OWENS D K, WENDT R C. Estimation of the surface free energy of polymers[J]. Journal of Applied Polymer Science, 1969, 13(8): 1741-1747. DOI:10.1002/app.1969.070130815 |
| [20] |
ELLISON A H, ZISMAN W A. Wettability of halogenated organic solid surfaces[J]. The Journal of Physical Chemistry, 1954, 58(3): 260-265. DOI:10.1021/j150513a020 |
| [21] |
KOTANI Y, KAMIGAITO M, SAWAMOTO M. Re(V)-mediated living radical polymerization of styrene: 1ReO2I(PPh3)2/RI initiating systems[J]. Macromolecules, 1999, 32(8): 2420-2424. DOI:10.1021/ma981614f |




