聚氯乙烯(PVC)是由氯乙烯单体(VCM)聚合所得,是我国五大通用塑料之一,广泛应用于日常生活及工业生产中[1-3]。氯乙烯单体的合成是聚氯乙烯生产中的核心工艺。根据我国特殊的“富煤、贫油、少气”的能源结构,我国多采用乙炔氢氯化法制备氯乙烯,过去10年采用该法的产能已达70% [4-6]。过往我国在乙炔氢氯化反应中所使用的反应催化剂为Hg基催化剂,但随着我国签署《关于汞的水俣公约》[7],Hg基催化剂终将被绿色环保的催化剂所取代。Ru基催化剂是Hg基催化剂的潜力替代产品,受到广泛关注。科研工作者验证了Ru基催化剂性能,提出了众多优化方案[8-11],如载体的优化,助剂的引入,通过第二或第三种金属的协同作用等,但还是无法满足工业化的要求。无汞催化剂与高汞催化剂的工艺条件有区别,需要根据基元反应速率的理论计算推测整个反应的动力学规律,通过相关实验确定反应物中各组分物质的量比、反应温度等参数与反应速率之间的关系,以满足反应过程开发[12]。研究Ru催化剂在乙炔氢氯化反应中的动力学,可从反应机理角度了解影响催化剂性能的关键因素,并针对其进行优化。动力学的研究在排除内、外扩散的前提下进行,催化剂的内、外扩散限制是催化反应中一个非常重要的限制因素,它对反应速率、选择性和稳定性都产生重要影响,通过优化催化剂的孔径大小和颗粒大小,可以排除内扩散,通过提高气流主体的线速度可以降低反应物分子在催化剂外表面扩散的阻力,最终降低气流主体与催化剂外表面的浓度差,排除外部扩散[13]。本研究将结合动力学实验、表面积分析仪(BET)、程序升温还原(TPR)、透射电子显微镜(TEM)和程序升温脱附(TPD)表征经高温H2处理后的钌纳米颗粒与高分散钌物种活性中心催化性能的差异。从动力学角度指导Ru催化剂的开发以及选择工业生产中最优的反应条件。
2 实验 2.1 实验材料高纯乙炔气体(摩尔分数x≥ 98.0%)、电子级氯化氢气体(x≥ 99.9%)及高纯氮气(x≥99.9%),上海民星化工科技有限公司;RuCl3(Ru质量分数≥37.0%),上海阿拉丁试剂公司;活性炭(AC),荷兰诺芮特公司;无水乙醇,安徽安特食品股份有限公司。
2.2 实验仪器气相色谱仪(GC9800),上海科创色谱仪器有限公司;质量流量计,北京七星华创电子股份有限公司;温度控制器,厦门宇电自动化科技有限公司;固定床管式反应装置,天津鹏翔科技有限公司;管式炉(SK-2.5-15),天津市泽庆电阻炉工贸有限公司。
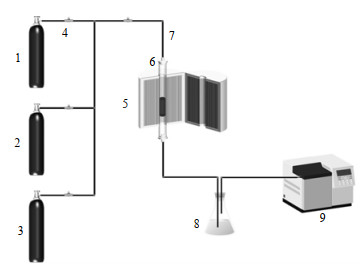
2.3 实验装置如图 1所示,反应管为实验室定制,反应管的长度为43 cm,内径为13 mm,尾气吸收装置中采用NaOH溶液,除去尾气中多余HCl气体。
|
图 1 实验装置图 Fig.1 Schematic diagram of the catalyst evaluation setup 1. acetylene 2. hydrogen chloride 3. nitrogen 4. stop valve 5. temperature control 6. fixed bed reactor 7. reaction tube 8. absorption bottle (NaOH solution) 9. gas chromatograph |
本研究中催化剂均采用等体积浸渍法制备, 等体积浸渍法是一种制备负载催化剂的方法,其特点是使用的浸渍液体体积等于固体载体的孔体积。准确称取0.108 g RuCl3前驱体,溶解静置6 h。后将10.0 g活性炭载体倒入溶液中,充分搅拌均匀,使活性炭充分吸收浸渍液。后将混合后的载体在室温静置6 h后放入鼓风干燥箱中120 ℃干燥12 h。干燥完成后该催化剂为Ru/AC催化剂,Ru的质量为活性炭载体的0.4%。将制备好的Ru/AC催化剂置于管式炉中,在H2摩尔分数为10% 的H2/Ar气氛下,程序升温至1 073 K进行热处理,恒温保持2 h[14-15],然后自然冷却至室温,该催化剂为Ru-NPs/AC。
2.5 催化剂的评价及分析方法在反应管中装入一定量催化剂,在N2氛围的保护下升温至反应温度,通入HCl气体活化30 min,HCl气体的流量为12 mL⋅min−1,最后通入C2H2反应,尾气通过洗气瓶除去未反应的HCl气体,再进行气相色谱分析。反应在原料气物质的量比n(C2H2): n(HCl)=1:1.2的条件下进行评价,气相色谱采用热导检测器,载气为氢气,氢气的流量为40 mL⋅min−1,柱温为160 ℃,进样量为0.3 mL,采用面积归一法测定转化率。催化活性表示为乙炔的转化率XC2H2根据式(1)计算:
| $ X_{\mathrm{C}_2 \mathrm{H}_2}=\frac{n_{\mathrm{in}}\left(\mathrm{C}_2 \mathrm{H}_2\right)-n_{\text {out}}\left(\mathrm{C}_2 \mathrm{H}_2\right)}{n_{\text {out }}\left(\mathrm{C}_2 \mathrm{H}_2\right)} \times 100 \% $ | (1) |
式中:
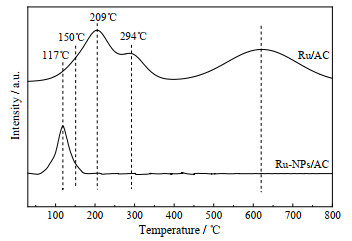
H2-TPR分析显示(见图 2),Ru/AC催化剂在400~700 ℃存在一个分解峰,这主要与载体上的官能团分解有关[16]。由于在升温过程中Ru物种与H2反应,导致含量下降,在100~300 ℃有清晰的还原峰,在150、209和294 ℃的还原峰分别归属于RuOx (x > 2)、RuO2或者Ru/RuOy和RuCl3中的钌物种[11]。与Ru/AC相比,Ru-NPs/AC只在117 ℃有一个明显的峰,这是未与活性炭相互作用的Ru纳米颗粒物质的还原峰[17];这证明在高温处理后,负载在活性炭上的大部分钌物种被还原。
|
图 2 催化剂H2-TPR图 Fig.2 H2-TPR of the catalysts |
为判断Ru/AC及Ru-NPs/AC催化剂中Ru物种的分散形式及反应前后活性中心的颗粒尺寸变化,将催化剂反应前后样品进行TEM测试。测试结果如图 3所示,Ru/AC催化剂中,Ru物种高度分散,活性中心的颗粒尺寸低于TEM的检测限,且催化剂反应后未发现有明显的Ru物种团聚现象,分散度依旧较高。而对于Ru-NPs/AC催化剂则明显观察到1~2 nm Ru纳米颗粒,该催化剂催化活性中心为钌纳米颗粒,催化剂活性中心分散度不如Ru/AC,反应后钌物种尺寸进一步增大,出现团聚。

|
图 3 催化剂TEM图 Fig.3 TEM micrographs of the catalysts |
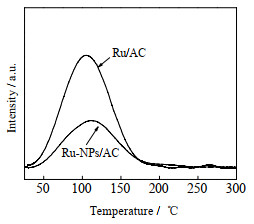
为探究催化剂在反应条件(T = 433 K,GHSVC2H2 = 1 000 h−1) 下对C2H2的吸附性能,将催化剂在反应条件下处理后进行C2H2-TPD测试,结果如图 4所示。2种催化剂均在100~150 ℃出现乙炔的脱附峰。观察乙炔脱附峰的峰面积及脱附温度,可知Ru-NPs/AC催化剂对乙炔的吸附量比Ru/AC催化剂少,吸附温度未出现明显变化。说明Ru活性物种在经过高温H2处理后形成的Ru-NPs/AC催化剂对C2H2的吸附强度不变,吸附量减少。
|
图 4 催化剂C2H2-TPD图 Fig.4 C2H2-TPD profiles of the catalysts |
测定催化剂的本征催化性能时需排除内、外扩散对催化反应的影响[18-19]。Ru/AC及Ru-NPs/AC均为活性炭载体催化剂,如果反应气体在载体的微孔结构中扩散速度过慢,内扩散会限制催化剂的本征反应速率。同理,在气相主体与催化剂表面的传质速度过慢,外扩散会影响催化本征速率。在保证反应条件一致的情况下,改变催化剂颗粒尺寸能有效排除内扩散影响,在保证反应空速一致的条件下,改变反应气体流速可以排除外扩散影响。
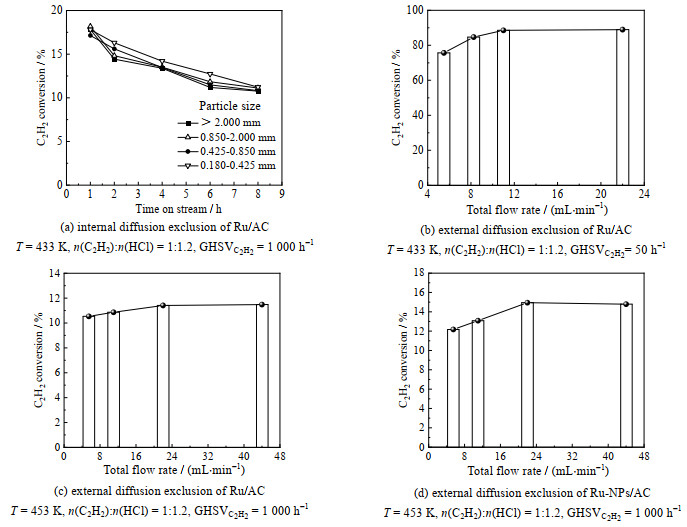
如图 5所示,以Ru/AC催化剂为样本进行评价,由图 5(a)可知反应在温度为433 K,n(C2H2): n(HCl) = 1:1.2,总空速为2 200 h−1的条件下进行,通过减小ROX0.8活性炭载体的粒径消除内扩散影响。结果显示催化剂颗粒尺寸对乙炔氢氯化反应的催化效率几乎无影响,说明Ru物种在活性炭载体上高度分散且均一,即使催化剂颗粒尺寸不同,Ru物种在催化剂载体孔结构中的分布情况依旧相似[20]。由图 5(b)可知在反应温度433 K,n(C2H2): n(HCl) = 1:1.2,总空速为110 h−1的条件下,通过改变反应气体流速,消除外扩散对催化反应的影响。在该催化剂中,在空速不变的条件下,当总流速小于11 mL⋅min−1时,随着乙炔流速减小,乙炔转化率降低,催化反应速率此时受外扩散影响,外扩散速率限制催化反应整体速率。当反应气体总流速高于11 mL⋅min−1时,催化性能几乎不变,外扩散速率对本征反应速率几乎无影响,此条件下的催化反应速率为本征反应速率,催化结果为本征反应结果。由图 5(c)~(d)可知,将反应温度升高至453 K且GHSVt为2 200 h−1的条件下,当反应气体总流速高于22 mL⋅min−1时,外扩散对反应也几乎没有影响。因此以本研究使用的反应装置为前提,以ROX0.8活性炭负载Ru催化剂,催化剂颗粒尺寸对催化反应结果几乎无影响,即内扩散在本系统中可忽略,并且在反应温度为433~453 K,n(C2H2): n(HCl) = 1:1.2,GHSVt= 110~2 200 h−1,当总流速大于22 mL⋅min−1时可认为外扩散对本实验无明显影响,基于此条件下进行催化反应为本征催化反应。
|
图 5 催化剂内外扩散的排除 Fig.5 Elimination of internal and external diffusion for catalyst evaluation |
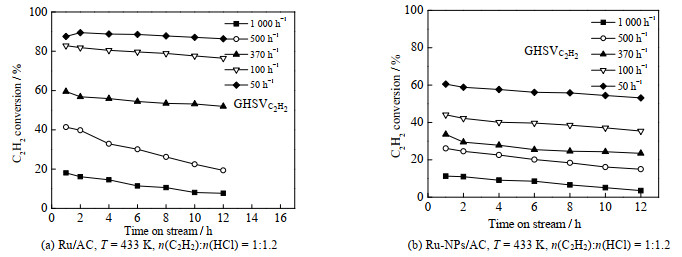
在排除内外扩散的影响下,对比了两种催化剂在不同空速时的催化活性和稳定性。如图 6所示,在433 K时,乙炔空速为50~1 000 h−1,Ru/AC催化剂均比Ru-NPs/AC催化剂显示出更高的活性。其中使用Ru/AC催化剂时,乙炔空速为50~370 h−1,乙炔转化率能够维持在50% 以上。
|
图 6 空速对催化反应的影响 Fig.6 Effects of space velocity on catalytic reaction |
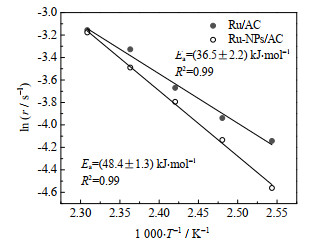
此外,在远离平衡的条件下(乙炔转换率低于10%;乙炔空速为1 000 h−1,n(C2H2): n(HCl) = 1:1.2,温度为393~433 K),测定了表观活化能。实验结果如图 7所示,图中r为反应速率。Ru/AC催化下的表观活化能为(36.5± 2.2) kJ⋅mol−1,这与Wang等[21]、Zhu等[22]报道的Ru/AC催化乙炔氢氯化反应的表观活化能(分别为31.88 kJ⋅mol−1 [21]、38.1 kJ⋅mol−1 [22])基本一致。在相同实验条件下,Ru-NPs/AC催化下的反应表观活化能更高((48.4±1.3) kJ⋅mol−1)。根据TPR分析可知Ru-NPs/AC的活性物种以金属态钌为主,而Ru/AC的活性物种以氧化态钌为主;TEM分析显示Ru-NPs/AC较Ru/AC具有更低分散度、Ru颗粒尺寸更大;此外,C2H2-TRD显示Ru-NPs/AC对于乙炔的吸附更加困难,这些因素都有可能导致Ru-NPs/AC比Ru/AC具有更高活化能。
|
图 7 不同温度反应速率和催化剂表观活化能 Fig.7 Reaction rates at different temperatures and apparent activation energies of the catalysts. Reaction conditions: GHSVC2H2 = 1 000 h−1, n(C2H2): n(HCl) = 1:1.2. The turnover rate at each temperature was measured at reaction time of 3 h. |
需要指出的是,两种催化剂的失活速率随着空速的增加而变大,Ru/AC的失活速率为0.10%⋅h−1~0.86%⋅h−1,Ru-NPs/AC的失活速率为0.62%⋅h−1~0.93 %·h−1。对此,对新鲜的和乙炔氢氯化反应后的(乙炔空速1 000 h−1、温度为433 K、反应12 h)催化剂进行BET表征,结果如表 1所示。
|
|
表 1 催化剂孔道信息 Table 1 Pore information of the catalysts |
由表 1可知,催化活性中心负载到活性炭上之后,载体的比表面积及孔容出现下降,说明活性中心均匀分布在载体孔道内部。反应后催化剂比表面积及孔容明显下降,但平均孔径几乎不变,说明催化剂整体孔道结构出现堵塞。结合催化活性(图 6)可知,载体的孔道部分堵塞是导致催化剂失活的原因之一,反应气体进入孔道内阻力增大,与活性位点接触的概率降低,导致催化性能出现下降。此外,TEM结果显示,反应后Ru-NPs/AC中的钌颗粒尺寸增大,出现团聚现象,这也可能是催化剂失活的原因。
4.3 反应级数的测定及动力学方程的构建反应级数是判断催化反应中各种原料气对反应速率影响程度大小的判断依据之一,因此明确各反应原料气之间的反应级数对反应工艺的优化具有一定的指导作用。乙炔氢氯化反应速率可由经验速率方程(式(2))表示:
| $ r=\frac{\text { 单位时间内被转化的乙炔的物质的量 }\left(\mathrm{mol} \cdot \mathrm{s}^{-1}\right)}{\text { 催化剂中金属的物质的量 }(\mathrm{mol})}=k p_{\mathrm{C}_2 \mathrm{H}_2} p_{\mathrm{HCl}}$ | (2) |
式中:k为表观反应速率常数,s−1⋅atm−(a+b);a为C2H2反应级数,b为HCl反应级数;pC2H2、pHCl为C2H2、HCl的分压,atm,atm为标准大气压,其法定计量单位换算系数为101 325 Pa,后文同。
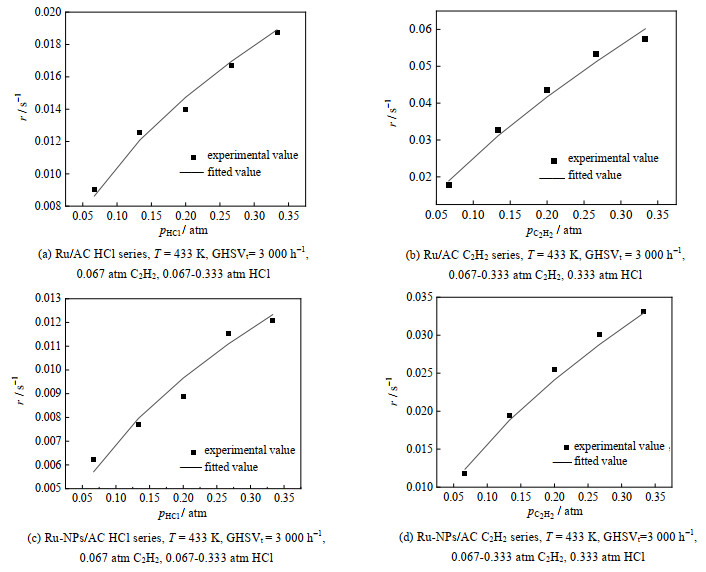
测定催化剂反应级数时,反应温度为433 K,反应的总空速保持在3 000 h−1,N2为平衡气体,通过改变原料气n(C2H2): n(HCl),测定各条件下两种催化剂的反应速率,将反应速率按经验速率方程拟合得出具体原料气的反应级数。对实验测得不同反应气在不同分压下的催化反应速率进行拟合,结果如图 8所示,具体数值及误差如表 2所示。使用Ru/AC催化剂时,HCl的级数为0.49 ± 0.11,C2H2的反应级数为0.72 ± 0.04;使用Ru-NPs/AC催化剂时,HCl的级数为0.48 ± 0.18,C2H2的反应级数为0.61 ± 0.07。Ru/AC催化剂的表观反应速率常数为(0.23 ± 0.02) s−1⋅atm−(a+b),高于Ru-NPs/AC的(0.11 ± 0.02) s−1⋅atm−(a+b),证明了前者具有更高的催化活性。
|
图 8 催化剂的反应级数拟合(各分压下的级数在反应时间为1.5 h时测得) Fig.8 Fitting results of reaction order measurements(The order under each partial pressure was measured at reaction time of 1.5 h) |
|
|
表 2 催化剂动力学参数及误差 Table 2 Kinetic parameters and error margins of the catalysts |
由于Ru/AC具有更高的催化活性、更低的表观活化能,研究者们对其催化下的反应机理进行了深入探究。Jia等[23]曾报道使用Ru@4×N6催化剂时,C2H2和HCl首先吸附在催化剂表面,接着HCl的H1原子向C2H2* (*表示Ru活性位点)的C1原子移动,HCl的Cl原子向相反方向移动,形成第一个中间体IM1,H1原子加入C2H2*的C1上形成C2H3*,Cl原子被C2H3*另一侧的H3原子俘获,由于C2H3*形成后Ru的不饱和配位,被H3俘获的Cl最终被Ru位点吸附,然后,将吸附的Cl原子加入C2H3*中,在此过程中,Cl逐渐攻击C2H3*的C2,生成垂直于催化剂表面的ads-VCM。Cl加成过程为催化过程限速步骤。Zhu等[22]曾报道乙炔在RuCl3上进行氢氯化反应,由4个反应步骤组成,即:(1) C2H2反应物在RuCl3上的吸附,(2) HCl分子在RuCl3-C2H2配合物上的共吸附,(3) 反应物的吸附态转化为C2H3Cl,(4) C2H3Cl的解吸,其中反应的第3步为速率决定步骤。
据此,作者结合上述文献以及所得到的实验结果,推测了Ru/AC催化下的基元反应步骤。由于催化剂的前驱体为RuCl3,在Ru的配位数较低的情况下,HCl分为两步加成到C2H2分子中,反应经历C─C π键的断裂及C─H键和C─Cl键的形成,C─Cl键的形成为催化反应决速步[24]。催化反应主要分为以下步骤,首先为C2H2在催化剂表面的吸附活化,随后气相主体HCl与活化后的C2H2发生加成反应生成氯乙烯,最终氯乙烯从催化剂表面脱附回归气相主体[25-26]。本研究以RuCl3为前驱体制备的催化剂,推测反应步骤具体如下:
| $ \mathrm{C}_2 \mathrm{H}_2 \text { 吸附: }\quad\quad*+\mathrm{C}_2 \mathrm{H}_2 \stackrel{K_{\text {ads, } \mathrm{C}_2 \mathrm{H}_2}}{\rightleftarrows} \mathrm{C}_2 \mathrm{H}_2{ }^* $ |
| $ \mathrm{C}-\mathrm{H} \text { 键形成: }\quad\quad\mathrm{C}_2 \mathrm{H}_2{ }^*+\mathrm{HCl} \stackrel{K_{\mathrm{H}}}{\rightleftarrows} \mathrm{C}_2 \mathrm{H}_3{ }^* \mathrm{Cl} $ |
| $ \mathrm{C}-\mathrm{Cl} \text { 键形成: }\quad\quad\mathrm{C}_2 \mathrm{H}_3{ }^* \mathrm{Cl} \xrightarrow{k_1} \mathrm{C}_2 \mathrm{H}_3 \mathrm{Cl}^* $ |
| $ \mathrm{C}_2 \mathrm{H}_3 \mathrm{Cl} \text { 的脱附: }\quad\quad\mathrm{C}_2 \mathrm{H}_3 \mathrm{Cl}^* \stackrel{K_{\mathrm{VC}}}{\rightleftarrows} \mathrm{C}_2 \mathrm{H}_3 \mathrm{Cl}+* $ |
基于以上推论,假设C─Cl键的形成为催化反应决速步骤[25],根据理想催化反应模型及Langmuir等温吸附模型,可得到反应速率方程(3):
| $ r=\frac{k_1 K_{\mathrm{ads}, \mathrm{C}_2 \mathrm{H}_2} K_{\mathrm{H}} p_{\mathrm{C}_2 \mathrm{H}_2} p_{\mathrm{HCl}}}{1+K_{\mathrm{ads}, \mathrm{C}_2 \mathrm{H}_2} p_{\mathrm{C}_2 \mathrm{H}_2}+K_{\mathrm{ads}, \mathrm{C}_2 \mathrm{H}_2} K_{\mathrm{H}} p_{\mathrm{C}_2 \mathrm{H}_2} p_{\mathrm{HCl}}} $ | (3) |
式中:k1为速率控制步骤速率常数,s−1;Kads, C2H2为乙炔吸附平衡常数,kPa−1;KH为C─H键形成平衡常数,kPa−1。根据式(3),当催化剂部分表面被C2H2和HCl的衍生物(
在排除内、外扩散的影响下,测定Ru/AC及Ru-NPs/AC的相关动力学参数,在Ru/AC催化剂中表观活化能为(36.5 ± 2.2) kJ⋅mol−1,HCl的级数为0.49 ± 0.11,C2H2的级数为0.72 ± 0.04,表观反应速率常数为(0.23 ± 0.02) s−1⋅atm−(a+b)。Ru-NPs/AC催化剂的表观活化能为(48.4 ± 1.3) kJ⋅mol−1,HCl的级数为0.48 ± 0.18,C2H2的级数为0.61 ± 0.07,表观反应速率常数为(0.11 ± 0.02) s−1⋅atm− (a+b)。造成Ru-NPs/AC催化剂表观活化能升高,反应速率降低的主要原因为Ru物种经过高温H2处理后,活性物种性质发生变化,从氧化态的钌为主变成为金属态的钌为主,并且Ru纳米活性物种分散度降低,活性颗粒尺寸增大,易团聚。在催化剂的开发中,可以通过调控催化剂活性中心氧化态,提高Ru活性物种的分散度,提升活性中心对反应原料气的吸附活化能力,进而优化催化剂性能,以符合工业生产需求。
| [1] |
安晓通. 聚氯乙烯行业的生产现状及发展趋势[J]. 化工设计通讯, 2019, 45(5): 205. AN X T. Production status and development trend of PVC industry[J]. Chemical Engineering Design Communications, 2019, 45(5): 205. DOI:10.3969/j.issn.1003-6490.2019.05.147 |
| [2] |
杨惠娣. 聚氯乙烯及其热稳定剂现状与发展趋势[J]. 中国塑料, 2019, 33(4): 111-119. YANG H D. Current situation and development trends of PVC and its stabilizers[J]. China Plastics, 2019, 33(4): 111-119. |
| [3] |
高伟杰. 阻燃聚氯乙烯研究进展及在工程中的应用[J]. 合成材料老化与应用, 2019, 48(5): 132-136. GAO W J. Research progress of flame retardant PVC and their application in engineering[J]. Synthetic Materials Aging and Application, 2019, 48(5): 132-136. |
| [4] |
WANG B L, YUE Y X, PANG X X, et al. Nature of HCl oxidation Au anomalies and activation of non-carbon-material-supported Au catalyst[J]. Journal of Catalysis, 2021, 404: 198-203. DOI:10.1016/j.jcat.2021.09.020 |
| [5] |
王小艳, 王小昌. 电石法聚氯乙烯低汞触媒的研究进展[J]. 中国氯碱, 2017(4): 11-15. WANG X Y, WANG X C. Research progress of calcium carbide PVC low mercury catalyst[J]. China Chlor-Alkali, 2017(4): 11-15. DOI:10.3969/j.issn.1009-1785.2017.04.005 |
| [6] |
WANG B L, JIN C X, SHAO S J, et al. Electron-deficient Cu site catalyzed acetylene hydrochlorination[J]. Green Energy & Environment, 2023, 8(4): 1128-1140. |
| [7] |
《关于汞的水俣公约》生效公告[J]. 电池工业, 2017, 21(3): 53, 32. The Minamata Convention on Mercury[J]. Chinese Battery Industry, 2017, 21(3): 53, 32. |
| [8] |
LI J, ZHANG H Y, CAI M, et al. Enhanced catalytic performance of activated carbon-supported ru-based catalysts for acetylene hydrochlorination by azole ligands[J]. Applied Catalysis A: General, 2020, 592: 117431. DOI:10.1016/j.apcata.2020.117431 |
| [9] |
LI J, ZHANG H Y, LIANG H X, et al. High-efficiency catalysis of Ru-based catalysts assisted by triazine-based ligands containing different heteroatoms (N, O, S) for acetylene hydrochlorination[J]. Molecular Catalysis, 2022, 519: 112142. DOI:10.1016/j.mcat.2022.112142 |
| [10] |
MAN B C, ZHANG H Y, ZHANG C M, et al. Effect of Ru/Cl ratio on the reaction of acetylene hydrochlorination[J]. New Journal of Chemistry, 2017, 41(23): 14675-14682. DOI:10.1039/C7NJ03863A |
| [11] |
ZHANG H Y, LI W, JIN Y H, et al. Ru-Co(Ⅲ)-Cu(Ⅱ)/SAC catalyst for acetylene hydrochlorination[J]. Applied Catalysis B: Environmental, 2016, 189: 56-64. DOI:10.1016/j.apcatb.2016.02.030 |
| [12] |
郭燕燕, 刘鹰, 胡瑞生, 等. 乙炔氢氯化反应非贵金属无汞催化剂的研究进展[J]. 化工进展, 2014, 33(6): 1486-1490. GUO Y Y, LIU Y, HU R S, et al. Research progress of mercury-free catalysts of non-noble metal for acetylene hydrochlorination[J]. Chemical Industry and Engineering Progress, 2014, 33(6): 1486-1490. |
| [13] |
宋静, 金奇杰, 计雯钰, 等. WO3-ZrO2/TiO2-CeO2-MnO2选择性催化还原NO热动力学和反应机理研究[J]. 电力科技与环保, 2022, 38(1): 10-17. SONG J, JIN Q J, JI W Y, et al. Kinetics and reaction mechanism of selective catalytic reduction of NO by WO3-ZrO2 / TiO2-CeO2-MnO2[J]. Electric Power Environmental Protection, 2022, 38(1): 10-17. |
| [14] |
KAISER S K, LIN R H, KRUMEICH F, et al. Preserved in a shell: High-performance graphene-confined ruthenium nanoparticles in acetylene hydrochlorination[J]. Angewandte Chemie International Edition, 2019, 58(35): 12297-12304. DOI:10.1002/anie.201906916 |
| [15] |
KAISER S K, FAKO E, SURIN I, et al. Performance descriptors of nanostructured metal catalysts for acetylene hydrochlorination[J]. Nature Nanotechnology, 2022, 17(6): 606-612. DOI:10.1038/s41565-022-01105-4 |
| [16] |
JIN Y H, LI G B, ZHANG J L, et al. Effects of potassium additive on the activity of Ru catalyst for acetylene hydrochlorination[J]. RSC Advances, 2015, 5(47): 37774-37779. DOI:10.1039/C5RA03466C |
| [17] |
ZHENG S Z, CAO X Y, ZHOU Q, et al. Gas phase hydrogenolysis of methyl difluoroacetate to 1, 1-difluoroethanol over Ru/C catalysts[J]. Journal of Fluorine Chemistry, 2013, 145: 132-135. DOI:10.1016/j.jfluchem.2012.10.014 |
| [18] |
黄柳华, 徐壮, 朱明远, 等. 乙炔氢氯化无汞催化动力学及其反应器优化[J]. 石河子大学学报(自然科学版), 2021, 39(5): 529-536. HUANG L H, XU Z, ZHU M Y, et al. Mercury-free catalytic kinetics of acetylene hydrochlorination and its reactor optimization[J]. Journal of Shihezi University (Natural Science), 2021, 39(5): 529-536. |
| [19] |
WANG B L, ZHANG H F, YUE Y X, et al. Catalytic behavior of au confined in ionic liquid film: A kinetics study for the hydrochlorination of acetylene[J]. Catalysts, 2022, 12(9): 1012. DOI:10.3390/catal12091012 |
| [20] |
XU H, SI J K, LUO G H. The kinetics model and fixed bed reactor simulation of Cu catalyst for acetylene hydrochlorination[J]. International Journal of Chemical Reactor Engineering, 2017, 15(4): 20160165. |
| [21] |
WANG X L, LAN G J, CHENG Z Z, et al. Carbon-supported ruthenium catalysts prepared by a coordination strategy for acetylene hydrochlorination[J]. Chinese Journal of Catalysis, 2020, 41(11): 1683-1691. DOI:10.1016/S1872-2067(20)63616-6 |
| [22] |
ZHU M Y, KANG L H, SU Y, et al. MClx (M = Hg, Au, Ru; x = 2, 3) catalyzed hydrochlorination of acetylene — A density functional theory study[J]. Canadian Journal of Chemistry, 2013, 91(2): 120-125. |
| [23] |
JIA Y M, NIAN Y, ZHANG J L, et al. Theoretical design of ruthenium single-atom catalysts with different substrates for acetylene hydrochlorination[J]. Molecular Catalysis, 2021, 513: 111826. |
| [24] |
HAN Y, SUN M X, LI W, et al. Influence of chlorine coordination number on the catalytic mechanism of ruthenium chloride catalysts in the acetylene hydrochlorination reaction: A DFT study[J]. Physical Chemistry Chemical Physics, 2015, 17(12): 7720-7730. |
| [25] |
汪新鑫, 吴广文, 吴浩, 等. 乙炔氢氯化的低汞催化反应动力学研究[J]. 工业催化, 2014, 22(5): 392-396. WANG X X, WU G W, WU H, et al. Kinetic study of hydrochlorination of acetylene on low-mercury catalyst[J]. Industrial Catalysis, 2014, 22(5): 392-396. |
| [26] |
李阳, 吴广文, 吴浩, 等. 乙炔氢氯化的无汞催化反应动力学研究[J]. 工业催化, 2015, 23(4): 307-312. LI Y, WU G W, WU H, et al. Kinetic study of hydrochlorination of acetylene on non-mercury catalyst[J]. Industrial Catalysis, 2015, 23(4): 307-312. |




