磷石膏是湿法磷酸生产过程中磷矿与硫酸反应生成的副产物,每生产1 t磷酸约产生4~5 t磷石膏,生产l t磷酸二铵约产生2.5~5 t磷石膏[1]。在我国可持续发展政策的压力下,磷石膏废渣已成为中国磷肥工业的一个难题。采用磷石膏分解制硫酸联产水泥是磷石膏综合利用的有效途径之一,但由于SO2浓度低、制酸成本高、产量低、能耗高等缺点大大限制了该技术的推广[2]。在磷石膏的分解方面,Ma等[3, 4]对高硫煤在N2氛围下还原分解磷石膏进行了实验研究,可得到高浓度SO2用于制硫酸联产水泥过程。有文献表明,还原性的气氛有助于CaSO4的分解,Liu等[5]通过热重分析仪在CO2气氛下对煤与CaSO4载氧体的作用机理进行了研究,发现煤与CO2形成的还原性气氛可促进煤焦与CaSO4的反应。Ma等[6]对磷石膏还原分解的反应机理及影响因素进行了研究,同样发现还原性气氛能够促进磷石膏的分解,通过控制煤的颗粒大小、反应温度和加热速率可得到较高含量的CaO和高浓度的SO2。实现我国磷石膏废渣的还原分解需要大量的还原性气体,成本较高。而本文采用的云南当地煤种曲靖褐煤来代替还原性气体还原分解磷石膏,曲靖褐煤具有矿藏量丰富、价格低廉易得等优点,且其较高含量的挥发分可以提供一定量的还原性气氛,从而更有利于磷石膏的还原分解。
本文采用热重-红外联用技术(TG-FTIR)在CO2气氛下对磷石膏和褐煤的反应特性进行了实验研究。通过对反应过程中气体产物浓度的变化规律进行实时在线分析,探究了褐煤与磷石膏在CO2气氛下不同阶段的反应特性,推断磷石膏与褐煤的反应历程。此外,本文还分析了Ca/C摩尔比对磷石膏还原分解过程及产物的影响,为进一步利用云南褐煤还原分解产自云南的磷石膏这种固体废弃物提供相应的理论依据。
2 实验部分 2.1 实验原料磷石膏(Phosphogypsum,PG)来自云南磷化集团有限公司,磷石膏样品中水含量较高,将磷石膏样品在80℃下烘干至恒重,脱除游离水,然后适当破碎后经20目过筛除去大块颗粒后收集备用。磷石膏化学成分如表 1所示,由表 1可知,磷石膏样品中二水硫酸钙含量达到78.07%,含有一定量的SiO2,还含有少量的Fe2O3、Al2O3、F,其余杂质含量很少。实验所用煤种为云南曲靖褐煤,采用空气干燥基方式,其工业分析和元素分析列于表 2。
| 表 1 磷石膏化学成分分析 Table 1 Chemical composition of PG |
| 表 2 褐煤工业分析及元素分析 Table 2 Proximate and ultimate analysis of qujing lignite |
实验采用的热重分析仪为德国耐驰公司的Netzsh STA 409PC(天平灵敏度2 μg,温度准确度<1℃)和Bruker TENSOR 27型傅里叶变换红外光谱分析仪(波长范围400~4000 cm-1)。按照所需不同摩尔比混合后在研钵中充分研磨,收集样品,用于下步热重实验。实验在CO2/N2的混合气氛下进行,其中N2为吹扫气,流量为50 mL⋅min-1,CO2流量为20 mL⋅min-1,程序升温速率为20 K⋅min-1,实验终温为1100℃,反应产生的气体产物通过与热重相连的红外分析仪进行在线检测。实验条件如表 3所示。
| 表 3 实验条件 Table 3 Experimental conditions |
与本文有关的小分子气体的红外波数区间[7]:H2O:1300~1800 cm-1、 3500~3800 cm-1; CO2:2200~2450 cm-1;CO:2000~2200 cm-1;CH4:2900~3100 cm-1;SO2:1300~1400 cm-1。
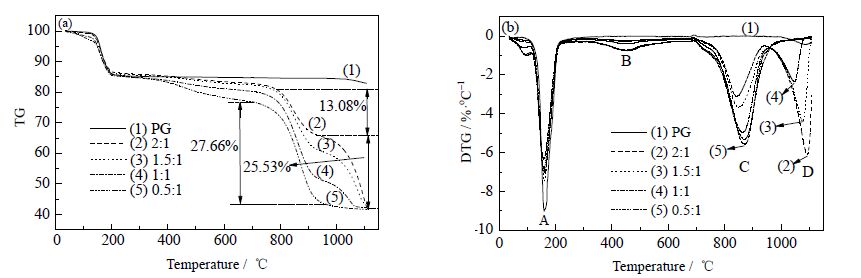
3 结果与讨论 3.1 不同Ca/C摩尔比下TG-FTIR分析分别取Ca/C摩尔比为2、1.5、1等五组在CO2气氛下进行热重-红外联用(TG-FTIR)实验,以CO2为气化剂,具有热量损失少等优点[8],且CO2的引入可以促进煤热解过程的发生,促进羟基、甲基、亚甲基等脱落和芳环结构的开裂,促进挥发分的溢出,降低半焦的产率[9]。磷石膏与褐煤随温度升高的热重曲线如图 1所示。图 1(a)中曲线(1)表示无褐煤加入情况下的磷石膏随温度升高的失重曲线,由曲线(1)可知,磷石膏在CO2气氛下性能较稳定,在200~1100℃,磷石膏的质量由85.14%降低到83.04%,仅仅失重2.10%,磷石膏在这个温度范围内性能稳定,基本不分解。加入褐煤之后,磷石膏在800℃左右即开始失重,说明褐煤的加入可以明显降低磷石膏的还原分解温度。
|
图 1 不同Ca/C 摩尔比条件下的热重曲线 Fig.1 TG (a) and DTG (b) curves with different Ca/C molar ratios |
图 1(b)为不同Ca/C摩尔比条件下磷石膏与褐煤反应的失重速率(DTG)曲线,由图可知,在35~1100℃范围内出现四个失重峰,分别标记为A、B、C、D。第一个失重峰出现在100~200℃;在300~600℃出现第二个失重峰;从700℃开始,出现第三、四个失重峰,且不同Ca/C摩尔比下第三、四个失重峰峰高度、峰值对应的温度也不相同。第三个失重峰随着褐煤添加量的增加即Ca/C摩尔比的减小呈现出不断增加趋势,是因为当褐煤量较低时,产生的还原性气体较少,只能与部分磷石膏反应,因此失重较小。随着褐煤添加量的不断增加,参与反应的磷石膏越来越多直到反应失重达到最大值。第四个DTG失重峰随褐煤添加量的增加即Ca/C摩尔比的减小表现出不断降低的趋势,出现峰值对应的温度也呈现出降低的趋势。
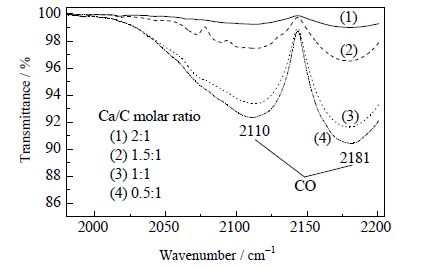
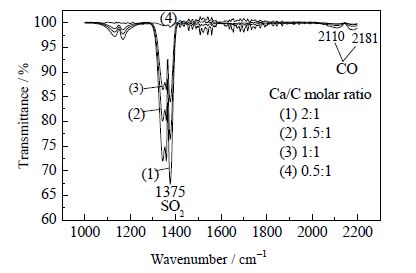
图 2是不同Ca/C摩尔比下第三个DTG曲线峰值对应的红外谱图,从图 2中可以看出,2110 cm-1和2181 cm-1处为C-O键的伸缩振动峰,CO的红外峰强度随褐煤添加量的增加而增加,说明第三个DTG失重是由于煤焦与CO2反应生成CO,CO与热解后的褐煤煤焦均可以与CaSO4发生反应。图 3是不同Ca/C摩尔比下第四个DTG峰值对应的红外谱图,其中1375 cm-1处对应SO2的特征峰(1300~1400 cm-1)。其DTG峰值对应的SO2红外峰强度随着褐煤添加量的增加表现出减弱的趋势,由图 1(b)可知,第四个DTG的峰值也表现出随褐煤添加量的增加而减小的趋势。这说明第四个DTG峰的出现是由于释放SO2引起的失重,生成SO2的量随褐煤添加量的增加而减少。
|
图 2 不同Ca/C 摩尔比下第三个DTG 峰值对应的红外谱图 Fig.2 FTIR spectra of the third DTG peak chemicals produced with different Ca/C molar ratios |
|
图 3 不同Ca/C 摩尔比下第四个DTG 峰值对应的红外谱图 Fig.3 FTIR spectra of the fourth DTG peak chemicals produced with different Ca/C molar ratios |
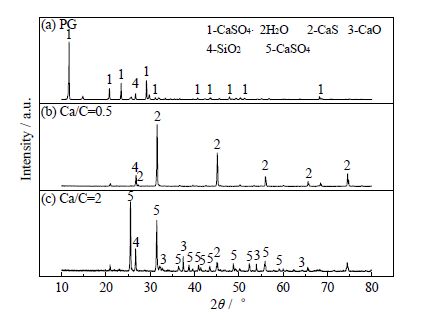
对磷石膏烘干筛分后的原料、Ca/C摩尔比为0.5和2的反应后的固体产物分别进行XRD表征,以确定不同Ca/C摩尔比对磷石膏与褐煤反应后固体产物的影响。所用XRD测试仪为日本理学D/max 2500 PC型X射线衍射仪,Cu靶Kα(λ=0.1540 6 nm)光源,管电压40 kV,管电流100 mA,扫描步长0.02°,扫描范围为10°~80°,所用分析软件为Jade 5.0。测试结果如图 4所示,图 4(a)为经干燥筛分处理后的磷石膏原料XRD谱图,在11.6°、20.7°、29.1°等处出现CaSO42H2O的特征衍射峰,此外还出现SiO2的特征峰;图 4(b)为Ca/C摩尔比为0.5时反应后的XRD谱图,在27.1°、31.6°、44.9°等处出现明显的CaS的特征峰,说明这个摩尔比例下的产物主要为CaS;图 4(c)为Ca/C摩尔比为2时反应后的XRD谱图,由于这个比例磷石膏过量,样品中主要为CaSO4和CaO的物相。
|
图 4 PG 和不同摩尔比反应后产物的XRD 谱图 Fig.4 XRD patterns of PG and solid products with different Ca/C molar ratios |
结合图 3的红外谱图和反应后产物的XRD表征可知,当Ca/C摩尔比为0.5时,磷石膏分解产物中主要为CaS,生成较少的SO2;当Ca/C摩尔比为2时,有较多的SO2生成,磷石膏与褐煤反应产物中CaO居多。为了更好的探究不同摩尔比下的反应历程,选取这两个摩尔比,通过分析不同阶段的质量失重以及四个DTG曲线峰值时间点下对应的红外谱图来确定不同阶段的气体释放规律。
3.3 高Ca/C摩尔比的反应历程由图 1(b)可知,当Ca/C摩尔比为2时,磷石膏与曲靖褐煤反应过程有四个DTG峰,其失重速率分别在157℃、445℃、844℃和1091℃最快。分别选取4个不同温度所在时间点下气体产物的红外谱图:577 s、1265 s、2589 s、3163 s,结合热重分析,确定不同阶段发生的反应。
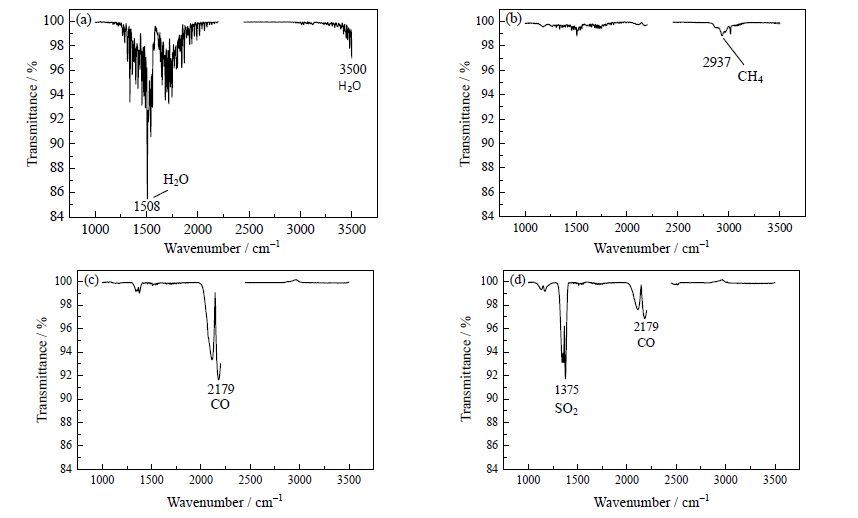
图 5为Ca/C摩尔比为2时,四个DTG曲线峰值时间点下对应的红外谱图。由图 5可知,当温度为157℃时出现水分(波数为1300~1800 cm-1,3500~3800 cm-1)的振动峰,说明第一个DTG峰的出现是由于磷石膏和褐煤中的结合水析出。当温度为445℃时,2937 cm-1处主要对应CH4的特征峰(2900~3100 cm-1),说明此时进行煤热解过程,主要产生CH4和CO等气体。随着温度的升高,磷石膏与褐煤反应的气体产物也发生了变化。由844℃下的红外谱图可知,气体产物中除了少量的SO2外,还存在明显的CO的特征峰(2000~2200 cm-1),说明褐煤煤焦在CO2气氛下气化生成了CO,CO在热力学上更容易与CaSO4发生气-固反应;由于气-固反应比固-固反应速率更快,因此磷石膏与褐煤反应过程不仅有固-固反应,还有气-固反应,是共同作用的结果[10]。此后,当温度升高到1091℃时,主要出现CO和SO2(1300~1400 cm-1)的特征峰,说明第四个DTG峰主要是由于生成SO2失重所导致。
|
图 5 Ca/C=2 时不同DTG 峰值对应的气体红外谱图 Fig.5 FTIR spectra of the four DTG peak chemicals produced with Ca/C molar ratio 2 (a) 157℃, 577 s (b) 445℃, 1265 s (c) 844℃, 2589 s (d) 1091℃, 3163 s |
结合图 1(a)的TG曲线可知,当Ca/C摩尔比为2时,前两个阶段理论失重量为15.6%,实际失重17.28%,实际失重高于理论失重说明这一范围内不仅进行水分析出、褐煤热解过程,煤焦与CO2反应也在同时进行。第三个阶段发生700~1100℃,失重曲线主要分成两段,说明在这个温度范围内发生的反应不止一个。假设700℃开始失重时为经过热解后的煤焦,褐煤煤焦在CO2气氛下先与磷石膏反应生成CaS,直到褐煤被磷石膏消耗完全,这部分的理论失重量为9.50%,而实际失重量13.08%;此时生成的CaS与未反应完全的磷石膏继续反应,理论失重为21.89%,实际失重23.53%。因此,当Ca/C摩尔比为2时,褐煤煤焦先与磷石膏生成CaS,随着温度的升高生成的CaS与未反应完全的磷石膏反应生成CaO。
综上所述,当Ca/C摩尔比为2时,首先进行磷石膏中结合水析出过程和褐煤热解过程,当升高到一定温度后,部分煤焦在CO2氛围下生成CO,CO与剩余煤焦将部分CaSO4还原为CaS。由于这个摩尔比下褐煤所占比例最少因此第三个DTG峰值高度也最小,随着温度的升高,生成的CaS又与未反应完的CaSO4发生反应生成CaO并释放出SO2。可用液态共熔体机理[11, 12]解释CaS与CaSO4之间的反应:在850℃以上的温度,CaSO4与CaS形成液态共熔体,而后S2-、SO42-、 Ca2+反应,生成CaO,同时析出SO2气体。
3.4 低Ca/C摩尔比的反应历程由图 1可知,当Ca/C摩尔比为0.5时,磷石膏与曲靖褐煤反应过程的DTG曲线主要有三个峰,其失重速率分别在156℃、447℃和873℃最快,其中1091℃作为上个摩尔配比的对照温度。为了更好地了解反应历程,同样选取4个不同温度所在时间点下的红外谱图:577 s、1265 s、2563 s、3053 s,结合热重分析,确定不同温度下发生的反应。
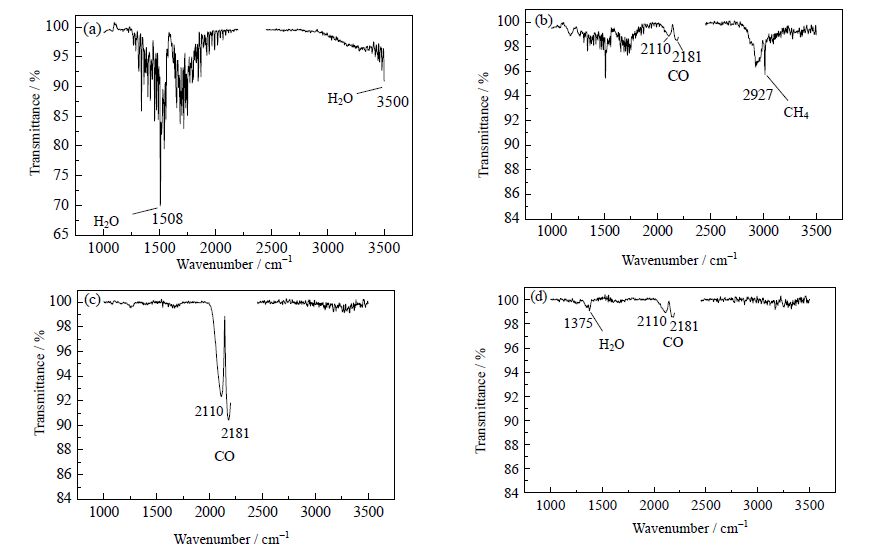
图 6是Ca/C摩尔比为0.5时,DTG曲线峰值时间点下对应的红外谱图。由图 6可知,与Ca/C摩尔比为2时的红外谱图相比,褐煤在所取样品中所占比例增加,图 6(b)、(c)的红外谱图中CH4(2900~3100 cm-1)和CO(2000~2200 cm-1)的特征峰峰值均高于图 5(b)、(c)所对应的红外特征峰峰值。这说明第三个DTG失重是由于部分褐煤与CO2的气化反应生成CO,且CO生成量随褐煤在混合物中比例的增加而增加。磷石膏不仅与CO发生气-固反应,还与褐煤煤焦发生固-固反应。最大的区别在于1091℃下的红外谱图,其SO2特征峰(1300~1400 cm-1)的峰值与图 5(d)中SO2特征峰峰值相比有较大程度的降低,说明Ca/C摩尔比为0.5时SO2释放量很小。
|
图 6 Ca/C=0.5 时不同DTG 峰值对应的气体红外谱图 Fig.6 FTIR spectrum of the four DTG peak chemicals produced with Ca/C molar ratio 0.5 (a) 156℃, 577 s (b) 447℃, 1265 s (c) 873℃, 2563 s (d): 1091℃, 3053 s |
由图 1(a)中Ca/C摩尔比为0.5时的TG曲线可知,由于褐煤在样品中占的比例逐渐增大,在300~700℃之间的质量损失也越来越明显。第三个阶段从700℃开始,磷石膏此时开始与褐煤发生反应,然而不同Ca/C摩尔比下的失重量不同,当温度升高到900℃,Ca/C摩尔比为2和0.5时的失重量差别明显,说明不同的Ca/C摩尔比对应的反应历程不同。当Ca/C摩尔比为0.5时,实际失重为27.66%,理论上在800℃左右开始失重时为经过热解阶段剩下的煤焦,煤焦在CO2气氛下与磷石膏发生反应生成CaS,理论失重为25.97%,因此这个摩尔比下的主要反应为磷石膏与煤焦的作用导致的失重。由图 4(b)的XRD谱图中出现明显的CaS晶型也进一步证实了CaS是Ca/C摩尔比为0.5时的主要产物。
综上所述,当Ca/C摩尔比为0.5时,随着温度的升高煤焦与CO2发生气化反应生成CO。由于CO比煤焦在热力学上更容易与CaSO4反应,并且气-固反应比固-固反应速率更快,因此高温下CO与煤焦可同时与CaSO4反应。磷石膏主要转化为CaS,在褐煤过量的情况下基本没有CaO的生成。
4 结 论本文主要通过热重-红外联用技术研究了褐煤还原磷石膏的反应历程,考察了CO2气氛下不同Ca/C摩尔比对磷石膏还原分解反应的影响。主要得到以下结论:
(1) CO2气氛下,磷石膏在1100℃以内基本不分解,褐煤的加入可以显著降低磷石膏的还原分解温度,磷石膏在800℃下可以与褐煤这种低阶煤发生还原反应。
(2) 由DTG曲线峰值对应的红外谱图可知,CO2气氛下,随着温度的升高,磷石膏与褐煤主要经历三个阶段:水分析出阶段、褐煤热解阶段、煤焦与CO2反应生成的CO与磷石膏反应阶段。其中第三个阶段的反应历程随着褐煤添加量的不同而不同,Ca/C摩尔比不仅影响磷石膏的还原分解过程,还对还原过程产生气相/固相产物有着显著影响。当Ca/C摩尔比为0.5时,产物中主要产物为CaS;当Ca/C摩尔比为2时,产物中CaO含量较高。
| [1] | Rutherford P M, Dudas M J, Samek R A . Environmental impacts of phosphogypsum[J]. Science of the Total Environment , 1994, 149 (1) : 1-38 |
| [2] | YING Guo-liang (应国量). Decomposition characteristics of PG and its fluidization decomposition process for producing sulphuric acid and lime (磷石膏分解特性及其流态化分解制硫酸联产石灰的工艺研究) [D]. Wuhan (武汉): Wuhan Univesity of Technology (武汉理工大学), 2011. |
| [3] | Ma L P, Niu X K, Hou J . Reaction mechanism and influence factors analysis for calcium sulfide generation in the process of phosphogypsum decomposition[J]. Thermochimica Acta , 2011, 526 (1-2) : 163-168 DOI:10.1016/j.tca.2011.09.013 |
| [4] | Zheng S C, Ning P, Ma L P . Reductive decomposition of phosphogypsum with high-sulfur-concentration coal to SO2 in an inert atmosphere[J]. Chemical Engineering Research and Design , 2011, 8 (9) : 2736-2741 |
| [5] | Liu Y Z, Guo Q J, Chen Y . Reaction mechanism of coal chemical looping process for syngas production with CaSO4 oxygen carrier in CO2 atmosphere[J]. Industrial Engineering Chemistry Research , 2012, 51 (31) |
| [6] | Ma L P, Ning P, Zheng S C . Reaction mechanism and kinetic analysis of the decomposition of phosphogypsum via a solid-state reaction[J]. Industrial Engineering Chemistry Resesarch , 2010, 49 (8) : 3597-3602 DOI:10.1021/ie901950y |
| [7] | YANG Ding-guo(杨定国) . Spectrum analysis and application(波谱分析基础及应用)[M]. Beijing (北京): Textile Industry Press(纺织工业出版社), 1993 . |
| [8] | ZHANG Jian-she(张建社), FU Guo-jia(付国家), TIAN Hong-jing(田红景) . Operating parameters analysis of chemical-looping combustion (CLC) with coal/Ca-based oxygen carrier(煤/钙基载氧体化学链燃烧操作参数分析)[J]. Journal of Chemical Engineering of Chinese Universities(高校化学工程学报) , 2012, 26 (2) : 247-253 |
| [9] | GAO Song-ping(高松平), ZHAO Jian-tao(赵建涛), WANG Zhi-qing(王志青) . Effect of CO2 on pyrolysis behaviors of lignite(CO2对褐煤热解行为的影响)[J]. Journal of Fuel Chemistry and Technology(燃料化学学报) , 2013, 4 (3) : 257-264 |
| [10] | ZHENG Da (郑达). Reductive decomposition and reaction mechanism of FGD gypsum (脱硫石膏还原分解特性及反应机理研究) [D]. Nanjing (南京):Nanjing University of Science and Technology (南京理工大学), 2013. |
| [11] | Kamphuis B, Potma A W, Prins W . The reductive decomposition of calcium sulphate-I. Kinetics of the apparent solid-solid reaction[J]. Chemical Engineering Science , 1993, 48 (1) : 105-110 DOI:10.1016/0009-2509(93)80287-Z |
| [12] | XIAO Hai-ping(肖海平), ZHOU Jun-hu(周俊虎), LIU Jian-zhong(刘建忠) . Research on oxidation of CaS under high temperature(高温下CaS氧化反应特性的实验研究)[J]. Journal of Chemical Engineering of Chinese Universities(高校化学工程学报) , 2006, 20 (3) : 494-498 |




