2. 辽宁科技大学 化学工程学院, 辽宁 鞍山 114051
2. School of Chemical Engineering, University of Science and Technology Liaoning, Anshan 114051, China
煤炭是我国的主体能源,在一次能源构成中占比70% 左右[1-2],对保障国民经济快速发展发挥了重要作用。煤燃烧是煤炭最为重要的利用方式,煤燃烧会产生大量含有SO2等污染大气环境的烟气。为了改善大气环境,近年来我国对SO2的排放标准不断提高,要求SO2排放满足小于35 mg⋅m−3(折合氧气6%)的超低排放标准[3]。因此,以石灰石(主要为碳酸钙)为主要脱硫剂的炉内和尾部烟气脱硫技术得到大量应用。
基于石灰石的炉内脱硫是目前最为简单、投资最省的SO2排放控制途径之一[4]。炉内脱硫技术通过在燃烧过程中向炉内加入石灰石脱硫剂将燃煤产生的SO2转化为钙基硫酸盐(主要为CaSO4)以控制SO2排放[5-6]。到目前为止,已有大量关于循环流化床炉内石灰石脱硫的研究[7-11]。研究结果表明,炉内脱硫受多种因素影响,其中Ca与S的物质的量比nCa/ns是最为重要的因素之一。通常,随着nCa/ns增大,脱硫效率增加,但当nCa/ns增大到一定值(通常为3左右)时,脱硫效率趋于稳定[12-16]。对此,谭波等[17]进行了深入分析,认为上述结果多适于实验室研究条件,因为在工业规模循环流化床锅炉观察到在高nca/ns比条件下,由于炉内灰渣量过大导致排渣频繁,使炉内实际“石灰石有效存有量”下降,因而出现脱硫效率随nCa/ns比增大而降低的现象。针对实际工业循环流化床炉内石灰石脱硫过程,谭波等[17]经过对实际锅炉运行数据分析,结合数学模型研究,认为决定脱硫效率的直接因素是“石灰石有效存有量”,而不是石灰石加入量或nCa/ns。研究表明,石灰石有效存有量越大,脱硫效率越高。
石灰石炉内脱硫虽然简单、设备投资成本低,但由于使用石灰石量大,对锅炉效率具有负面影响。此外,石灰石大量使用导致灰渣量增加,加大固废处理压力和成本。刘进强等[18]研究发现,由于炉内脱硫使灰渣中钙和硫含量增加,导致其不再满足作为水泥添加剂使用的技术要求,影响其有效利用途径。Hayhurst等[19]和Zijlma等[20]研究表明,在炉内脱硫时过高的石灰石投入促进燃烧过程中NOx的生成,增加了烟气脱硝的运行成本。目前,炉内脱硫石灰石利用率一般低于40%、石灰石资源浪费严重。可以预见,随着燃煤烟气脱硫规模不断增长,石灰石资源消耗将随之增大,与之对应的开山取石将严重破坏生态环境。因此,为了保障我国生态文明建设的不断发展,急需寻求替代石灰石的脱硫剂,同时研发先进的烟气脱硫技术提高脱硫剂利用效率,克服石灰石炉内脱硫存在的问题。
鉴此,本研究探索利用菱镁矿尾矿废弃物作为脱硫剂实现高效烟气脱硫的可行性。我国菱镁资源丰富,多年来经过开采和浮选加工产生了大量废弃的碎菱镁矿石及浮选尾矿粉料,这些固体废弃物的堆积对环境污染严重,急需寻求有效、高附加值的利用途径。目前,由菱镁矿及其生产的氧化镁已经作为湿法脱硫剂在工业中应用。研究发现,在镁基湿法烟气脱硫工程中,MgO比CaO具有溶解度高、不易结垢,同时脱硫副产物可再生和循环利用的优点[21-26]。然而,镁基湿法脱硫需要优质菱镁矿资源,加之其投资和运行成本高,一直未能被普遍应用。因此,探索菱镁矿尾矿废弃物作为脱硫剂进行烟气脱硫对开拓菱镁矿尾矿废弃物的有效利用途径和研究新式高温烟气脱硫技术都有重要意义。
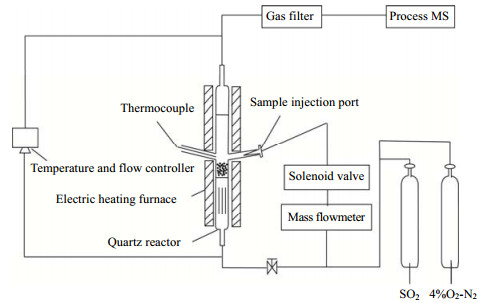
2 实验部分 2.1 实验装置与方法图 1为微型流化床(MFBRA)反应器装置图。MFBRA主要由电加热炉、石英玻璃制微型流化床反应器(直径20 mm)、颗粒脉冲进样系统以及气体在线采集分析系统过程质谱仪(TILON)组成[27]。为了获得菱镁矿浮选尾矿粉作为脱硫剂与SO2气体反应的动态特性,需要反应气体在反应器内及反应器到气体分析系统间保持接近平推流的流动状态,同时脱硫剂加入及其和床料的混合时间远小于反应时间。根据相关研究[28-29],本研究所用微型流化床完全满足这些要求。
|
图 1 微型流化床反应器实验流程图 Fig.1 Schematic diagram of the micro fluidized bed reactor |
实验时,以质量为3 g、粒径为120~180 μm的石英砂作为流化床料,以O2体积分数为4%、N2体积系数为96% 和体积分数为1×10−3的SO2混合气为流化气体,气体体积流量为300 mL⋅min−1。实验时,先将反应器加热到设定反应温度。在反应器温度稳定后,通过脉冲进样系统将质量约20 mg,粒径为74~150 μm干燥菱镁矿浮选尾矿粉快速加入床层中。采用降速法测得床料在实验温度为1023 ~1173 K时的最小流化速度为1.99~1.32 m⋅s−1,实验时床层的流化速度为2.65 m⋅s−1。通过调节颗粒脉冲进样时的气体压力使颗粒加料时间小于0.1 s,减少加料过程对反应结果的影响。通过过程质谱仪实时在线监测反应气体产物中CO2和SO2含量的变化。实验结束后,用一体化自动定硫仪(KZDL-9A)测定脱硫剂中硫的含量。
实验用原料为天然菱镁矿浮选尾矿粉料,取自辽宁省营口嘉晨集团有限公司,其化学成分的质量分数wB见表 1。为防止实验过程中样品受水分的影响,菱镁矿浮选尾矿粉在实验前经过干燥,并放置在干燥器中备用。
|
|
表 1 菱镁矿浮选尾矿化学成分分析表 Table 1 Chemical composition of the magnesite tailings |
菱镁矿颗粒和SO2间的高温反应可以表示为以下2个反应步骤:
(1) 菱镁矿颗粒煅烧反应:
(2) MgO和SO2的硫化反应:
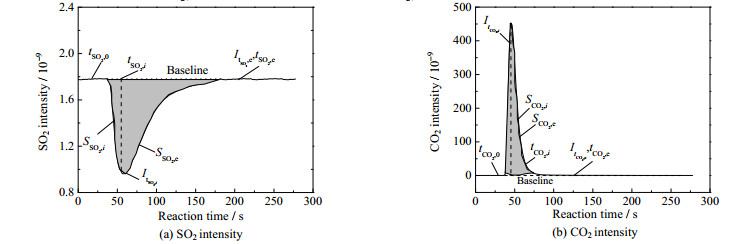
图 2(a)、(b)为实验过程中SO2和CO2气体质谱信号随时间的典型变化曲线。图中,
| $ {S_{{\text{S}}{{\text{O}}_{_{\text{2}}}}{\text{, }}i}}{\text{ = }}\mathop \smallint \nolimits_{{t_{\text{0}}}}^{{t_i}} {\text{(}}{I_{{t_{{\text{S}}{{\text{O}}_{_{\text{2}}}}{\text{, 0}}}}}} - {I_{{t_{{\text{S}}{{\text{O}}_{_{\text{2}}}}{\text{, }}i}}}}{\text{)d}}t $ | (1) |
| $ {S_{{\text{S}}{{\text{O}}_{_{\text{2}}}}{\text{, e}}}}{\text{ = }}\mathop \smallint \nolimits_{{t_{\text{0}}}}^{{t_{\text{e}}}} {\text{(}}{I_{{t_{{\text{S}}{{\text{O}}_{_{\text{2}}}}}}, }}_{_{\text{0}}} - {I_{{t_{{\text{S}}{{\text{O}}_{_{\text{2}}}}{\text{, }}}}_i}}{\text{)d}}t $ | (2) |
| $ {x_{{\text{S}}{{\text{O}}_{\text{2}}}}}{\text{ = }}\frac{{{S_{{\text{S}}{{\text{O}}_{\text{2}}}}}_{{\text{, }}i}}}{{{S_{{\text{S}}{{\text{O}}_{\text{2}}}{\text{, e}}}}}} $ | (3) |
| $ {R_{{\text{S}}{{\text{O}}_{\text{2}}}}}{\text{ = }}\frac{{{\text{d}}{x_{{\text{S}}{{\text{O}}_{\text{2}}}}}}}{{{\text{d}}t}} $ | (4) |
|
图 2 MFBRA-质谱测得SO2和CO2气体产物信号随时间的典型变化及数据其分析方法示意图 Fig.2 Typical signal variations and analysis method of SO2 and CO2 data with time obtained from MFBRA-MS |
由于菱镁矿煅烧分解反应生成CO2一种气体,CO2生成量和菱镁矿所含MgCO3转化量呈正比,因此可以用
| $ {x_{{\text{MgC}}{{\text{O}}_3}}}{\text{ = }}\frac{{{S_{{\text{C}}{{\text{O}}_{\text{2}}}{\text{, }}i}}}}{{{S_{{\text{C}}{{\text{O}}_{\text{2}}}{\text{, e}}}}}} $ | (5) |
菱镁矿粉的煅烧和硫化是气固非均相反应,其反应动力学方程可以表示为
| $ \frac{{{\rm{d}}x}}{{{\rm{d}}t}} = k(T){{ \times }}f(x) $ | (6) |
| $ G(x) = \int {\frac{{{\rm{d}}x}}{{f(x)}}} = k(T){\rm{d}}t $ | (7) |
| ${\rm{由Arrhenius公式可知}}:\ \ \ \ \ \ k(T){\text{ = }}A{\text{ex}}{{\text{p}}_{}}{\text{(}} - \frac{E}{{RT}}{\text{)}}$ | (8) |
在等温反应条件下,将式(8)代入(6)中并两边取对数得到以下方程:
| $ {{{\ln}}_{}}\left( {\frac{{{\rm{d}}x}}{{{\rm{d}}t}}} \right){\text{ = }} - \frac{E}{{RT}}{\text{ + }}{{{\ln}} }\ A{\text{ + }}{{{\ln}} }\ f(x) $ | (9) |
式中:x为转化率;t为反应时间,s;E为活化能,kJ⋅mol−1;R为气体常数,值为8.314 J⋅(mol⋅K)−1;T为反应热力学温度,K;A为指前因子;f(x)为反应机理模型函数、G(x)为f(x)所对应的函数。
实验过程中菱镁矿粉煅烧反应产生的CO2气体体积分数分析和计算方法与上述方法相同。
2.3 气体浓度标定为了获得SO2和CO2气体体积分数的定量变化,采用控制变量法对质谱信号强度进行了标定。具体方法为:向反应器中通入已知的不同体积分数的SO2和CO2气体,待质谱信号值达到稳定不变时,记录信号强度,得到气体实际浓度与质谱信号强度,然后将其关联得到
| $ {\varphi }_{{\text{SO}}_{2}}\text{=0}\text{.003 37}I-\text{0}\text{.338 8} $ | (10) |
| $ {\varphi _{{\text{C}}{{\text{O}}_{\text{2}}}}}{\text{ = 0}}{\text{.008 49}}I - {\text{0}}{\text{.547 6}} $ | (11) |
式中:I为气体物质的信号强度值;
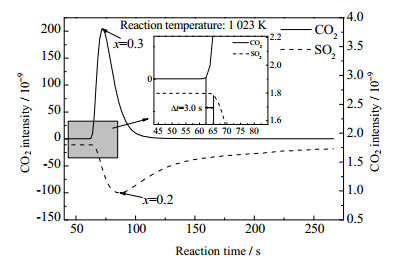
图 3为在反应温度为1 023 K条件下CO2和SO2信号强度随时间的变化关系。图中CO2信号强度开始出现时为煅烧反应开始,CO2信号强度升高后再逐渐降低至0时为煅烧反应停止。同样,SO2信号强度开始降低时为硫化反应开始,SO2信号强度降低后再逐渐恢复到初始值时为硫化反应停止。由图 3可知,在1 023 K反应条件下菱镁矿颗粒首先受热分解,CO2开始产生并快速增加。在CO2开始生成约3 s后,SO2体积分数开始下降,表明硫化反应开始发生。反应进行到t=72.95 s后,菱镁矿煅烧速率达到最大(对应MgCO3颗粒分解转化率为0.3),此时硫化反应速度依然不断增加。在反应时间t=88.05 s时,硫化反应速度达到最大(对应SO2转化率为0.2)。随着反应时间延长,菱镁矿煅烧反应首先终止,随后硫化反应速度逐渐降低直至结束。显然,菱镁矿作为脱硫剂与SO2反应的过程中,同时存在煅烧和硫化2个反应过程,并且煅烧反应先于硫化反应发生(时间差Δt=3.0 s),但在反应过程中煅烧反应和硫化反应同时进行,煅烧反应速度快于硫化反应。
|
图 3 1 023 K下CO2、SO2信号强度随反应时间变化 Fig.3 Variations of CO2 and SO2 concentrations as a function of reaction time at 1 023 K |
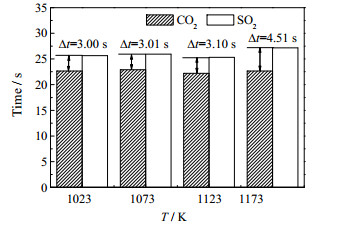
根据图 3所示的方法,获取了不同温度下菱镁矿煅烧与硫化反应开始的时间,其结果示于图 4。由图 4可见,随着温度升高,煅烧反应与硫化反应开始的时间差呈增大的趋势。
|
图 4 不同温度下煅烧与硫化反应开始的时间及其差别 Fig.4 Onset times and discrepancy of calcination and sulfation reactions at different temperatures |
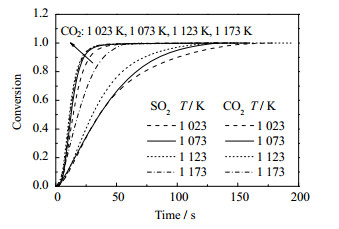
图 5所示为MgCO3颗粒分解转化率和SO2转化率随反应时间的变化关系。可见,在反应初期,MgCO3颗粒分解和SO2脱除转化率均随反应时间快速升高。随着反应接近完成,两者的转化率随时间变化逐渐变缓。随着反应温度的升高,MgCO3颗粒分解和SO2脱除反应速度加快,反应完成所需要的时间相应减小。由于CO2释放完成的反应时间小于SO2脱除完成的反应时间,说明菱镁矿颗粒热分解反应速度比MgO的硫化反应速度快。
|
图 5 不同温度下MgCO3颗粒分解和SO2脱除转化率随时间的变化 Fig.5 Variation of conversions as a function of time at different temperatures |
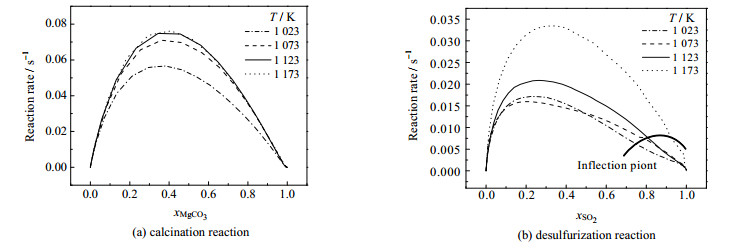
图 6所示为不同反应温度下MgCO3颗粒分解和SO2脱除反应速率与转化率的关系。由图可知,在反应初期MgCO3颗粒分解和SO2脱除反应速度均随其转化率增大而增大,当MgCO3颗粒分解转化率达到0.3~0.4,SO2转化率达到0.2~0.4时,MgCO3颗粒分解和SO2脱除反应速度均达到各自对应的极大值。随着转化率进一步提高,两者反应速度开始下降。当反应温度升高时,MgCO3颗粒分解反应和SO2脱除反应速率均呈增加的趋势。反应温度升高对CO2最大生成速率对应的MgCO3颗粒分解转化率影响不大,但使SO2脱除最大反应速率对应的转化率增大。此外,在转化率达到0.8以上时,反应温度对硫化反应速率影响很小,说明硫化反应速率主要受扩散控制。
|
图 6 不同反应温度下菱镁矿煅烧和硫化反应速率与转化率的关系 Fig.6 Relationship between reaction rate and conversion of magnesite calcination and desulfurization at different temperatures |
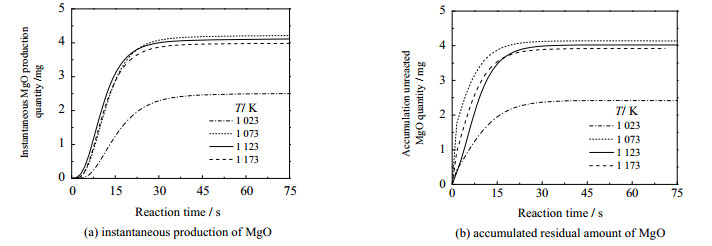
在整个反应过程中,煅烧反应先于硫化反应发生。MgCO3先煅烧生成MgO和CO2,生成的MgO与SO2发生硫化反应,生成MgSO4。在根据以上反应机理,依据实验所实测的MgCO3颗粒分解和SO2消耗随时间的动态变化关系,计算得到MgO的瞬时生成量及MgO累计的剩余量随时间的变化关系(MgO累计的剩余量是MgO生成量和消耗量之差的累积量),结果示于图 7。可见,生成的MgO在反应过程中一直有剩余,所以SO2应优先与反应活性高的MgO发生反应,而与活性较低的MgCO3直接反应的几率很小,说明了上述分析的合理性。
|
图 7 不同温度下菱镁矿脱硫反应过程中瞬时生成和累积剩余MgO质量随反应时间的变化 Fig.7 Profiles of instantaneous and accumulated unreacted MgO at different temperatures |
从上述分析可知,当煅烧和硫化反应进行时,菱镁矿煅烧产生CO2的同时,生成的MgO与SO2反应生成MgSO4。由于MgSO4致密度大,其不断生成将抑制煅烧产生CO2的释放和SO2向颗粒内的扩散。这与其他研究者在石灰石脱硫剂同时煅烧和硫化反应的研究中的现象一致[8, 30-32]。为此,进一步研究菱镁矿煅烧和硫化反应过程中颗粒微观结构的演变特性。
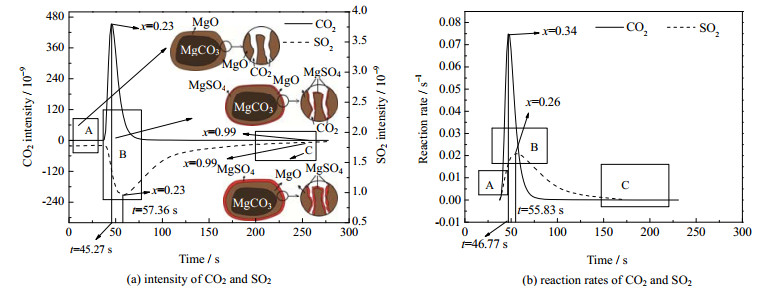
图 8为反应温度为1 123 K下的CO2和SO2信号强度随时间的变化关系。图中A阶段为菱镁矿煅烧反应初期,此时只有颗粒外表面极少部分的MgCO3分解转化为MgO,脱硫剂颗粒内大部分尚未分解。在3.09 s后发生硫化反应。在菱镁矿煅烧的初始阶段,硫化反应生成的MgSO4量较小,对煅烧反应速率几乎没有影响。当反应进行到B阶段时,菱镁矿煅烧反应在45.27 s时CO2的信号强度达到最大值,此时MgCO3颗粒分解转化率为0.23;在46.77 s时MgCO3煅烧反应速度最快,对应的转化率为0.34。在此阶段,颗粒内未分解的MgCO3逐渐减小,颗粒内孔隙依然较大。随着反应持续进行,MgO生成量逐渐增多,与SO2气体接触面积增大,硫化反应速度随之增大,但SO2的信号强度和反应速率均未达到最大值,所以MgSO4的生成对硫化反应的阻碍作用还没有达到控制的程度。当反应继续进行,SO2信号强度在57.36 s、xSO2=0.23时达到最大,反应速率在55.83 s、xSO2=0.26时达到最快。在该阶段,硫化反应速度有了明显的提升。同时,在脱硫剂分解产生的内孔中,MgSO4的生成量增大,覆盖在MgO表面的面积和厚度也不断增加,从而导致MgCO3的煅烧速率逐渐降低,MgO的生成量逐渐减小。在煅烧反应后期(C阶段),煅烧反应几乎结束(xMgCO3 > 0.99),但颗粒内部依然存在少量未分解的MgCO3。在反应后期,颗粒内孔生成速度很慢,说明大部分颗粒内孔壁被MgSO4覆盖堵塞,阻碍了煅烧和硫化反应的进一步进行。此时SO2通过内扩散进入颗粒孔隙内部,与MgO继续发生反应,但反应速率较慢,直至停止。反应结束后,依然有部分MgCO3和大量MgO未发生反应。
|
图 8 在1 123 K下CO2和SO2信号强度和对应反应速率随时间的变化 Fig.8 CO2 and SO2 signal intensities and the corresponding reaction rates at 1 123 K |
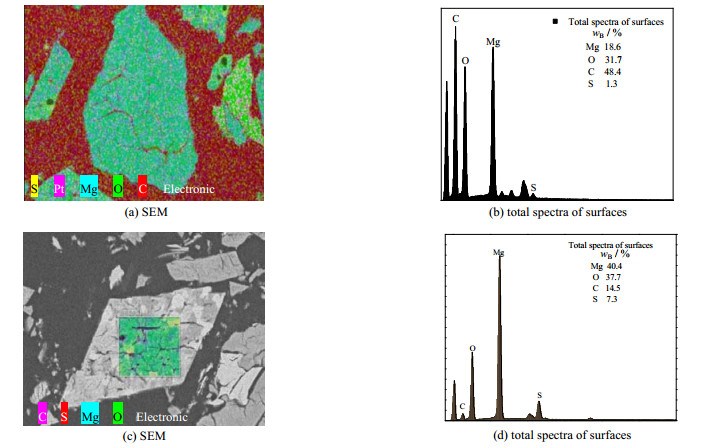
为了验证以上对菱镁矿脱硫反应机理的分析,将脱硫后的脱硫剂进行了扫描电镜能谱(SEM-EDS)分析,如图 9所示,其中图(b)、(d)为(a)、(c)图中切面的总谱图。由图可见,脱硫后的脱硫剂显示明显的内孔结构,Mg元素沿颗粒内孔道分布。从能谱数据可见,脱硫后的脱硫剂中依然存在一定量的C元素和O元素。说明存在明显的MgCO3和MgO,能谱分析结果说明上述分析是合理的。
|
图 9 在1 123 K下菱镁矿颗粒微观结构及元素分布 Fig.9 Microscopic structure and element compositions of a magnesite particle at 1 123 K |
(1) 煅烧反应动力学
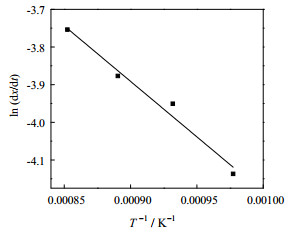
菱镁矿颗粒煅烧反应属于气固非均相反应,通过对不同机理模型[33-35]的拟合分析,发现菱镁矿颗粒的煅烧反应动力学可以用f(x)=4x3/4,G(x)=x1/4描述,据此计算的ln (dx/dt)和1/T示于图 10。可见,ln (dx/dt)~1/T可拟合为一条直线,相关系数为0.989。因此,得到菱镁矿颗粒煅烧反应的活化能E=24.5 kJ⋅mol−1,指前因子为0.291 s−1。
|
图 10 菱镁矿煅烧反应的ln(dx/dt) 与1/T拟合曲线 Fig.10 Fitting curve of ln(dx/dt) vs 1/T of the magnesite calcination reaction |
(2) 硫化反应动力学
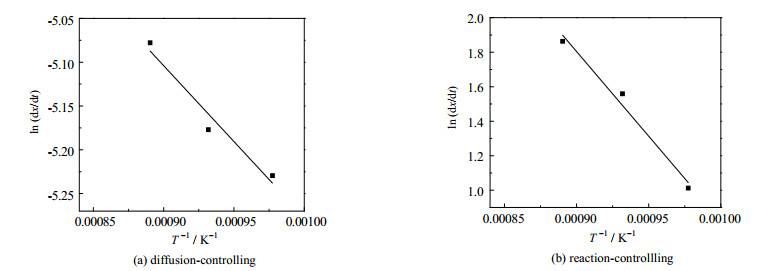
图 11为硫化反应ln (dx/dt)与1/T的拟合结果。由于在硫化反应前期,新生MgO含量大,硫化反应速度很快,反应受SO2气体扩散速度控制,而在硫化反应后期,MgO表面逐渐被MgSO4覆盖导致SO2扩散速度减小,但由于硫化反应活性点位减少,硫化反应成为速度控制步骤。
|
图 11 菱镁矿脱硫反应的ln (dx/dt)与1/T拟合曲线 Fig.11 Fitting curve of ln(dx/dt) vs 1/T of the desulfurization reaction |
因此,对不同反应控制阶段分别进行拟合分析,最终确定硫化反应扩散控制阶段的机理模型是f(x)=4x3/4,G(x)=x1/4,反应控制阶段的机理模型是f(x)=1/2(1−x)3,G(x)=(1−x)−2,计算得到对应平均活化能如表 2所示。可见,硫化反应扩散控制时E=14.41 kJ⋅mol−1;反应控制时E=81.59 kJ⋅mol−1。
|
|
表 2 菱镁矿脱硫反应机理模型和活化能 Table 2 Reaction mechanism and activation energy of the desulfurization reaction |
利用微型流化床反应器研究了菱镁矿浮选尾矿同时煅烧和硫化反应的机理和动力学特性,得到以下主要结论。
(1) 菱镁矿浮选尾矿颗粒与SO2气体反应包含煅烧反应和硫化反应2个过程,硫化反应速率达到最大时所需的时间比煅烧反应速率达到最大时的时间长,且反应速率达到最大时,硫化反应的SO2转化率小于煅烧反应的MgCO3颗粒分解转化率。
(2) 在反应过程中,SO2与MgO发生硫化反应生成的MgSO4会在MgO表面形成一层致密的膜,部分或完全堵塞MgO的孔隙,增加CO2和SO2气体的扩散阻力而抑制煅烧反应和硫化反应进行。
(3) 得到菱镁矿颗粒的煅烧反应动力学函数和活化能;同时发现硫化反应分扩散控制和反应控制这2个阶段,揭示了其对应反应动力学函数和活化能。
本研究成果对认识利用菱镁矿浮选尾矿作为脱硫剂的高温烟气脱硫反应过程机理和特性具有理论意义,对进一步开发该技术的实际应用、提高浮选尾矿的脱硫效率、实现菱镁矿浮选尾矿固废资源的高效利用具有参考意义。
| [1] |
陈鹏. 中国煤炭性质、分类和利用[J]. 燃料化学学报, 2002, 30(1): 71-71. CHEN P. Properties, classification and utilization of coal in China[J]. Journal of Fuel Chemistry and Technology, 2002, 30(1): 71-71. |
| [2] |
国家统计局, 国家统计年鉴2020 [R]. 北京: 中国统计出版社, (2020-09-20) [2022-03-20]. http://www.stats.gov.cn/tjsj/ndsj/2020/indexch.htm. National Bureau of Statistics of China. National Statistical Yearbook 2020 [R]. Beijing: China Statistical Press, (2020-09-20) [2022-03-20]. http://www.stats.gov.cn/tjsj/ndsj/2020/indexch.htm. |
| [3] |
赵永椿, 马斯鸣, 杨建平, 等. 燃煤电厂污染物超净排放的发展及现状[J]. 煤炭学报, 2015, 40(11): 2629-2640. ZHAO Y C, MA S M, YANG J P, et al. Status of ultra-low emission technology in coal-fired power plant[J]. Journal of China Coal Society, 2015, 40(11): 2629-2640. |
| [4] |
陈亮, 王春波, 闫广精. 循环流化床锅炉内石灰石脱硫研究进展[J]. 化工进展, 2019, 38(5): 2451-2460. CHEN L, WANG C B, YAN G J. Research progress of SO2 removal with limestone in CFB boilers[J]. Chemical Industry and Engineering Progress, 2019, 38(5): 2451-2460. |
| [5] |
ÖZDEMIR K, SERINCAN M F. A computational fluid dynamics model of a rotary regenerative heat exchanger in a flue gas esulfurization system[J]. Applied Thermal Engineering, 2018, 143: 988-1002. DOI:10.1016/j.applthermaleng.2018.08.011 |
| [6] |
朱永乐, 赵永华, 张帅, 等. 燃煤电厂脱硫技术进展[J]. 天津化工, 2018, 32(2): 1-3, 6. ZHU Y L, ZHAO Y H, ZHANG S, et al. The research on desulfurization technology in coal-fired power plant[J]. Tianjin Chemical Industry, 2018, 32(2): 1-3, 6. |
| [7] |
孟庆杭. 循环流化床锅炉脱硫提效研究及应用[J]. 节能技术, 2016, 34(1): 68-72. MENG Q H. Research and application on increasing desulfurization efficiency of circulating fluidized bed boiler[J]. Energy Conservation Technology, 2016, 34(1): 68-72. |
| [8] |
陈亮, 王子铭, 王春波. 流化床锅炉内石灰石同时煅烧/硫化反应中煅烧动力学特性[J]. 化工学报, 2017, 68(12): 4615-4624. CHEN L, WANG Z M, WANG C B. Limestone calcination kinetics in simultaneous calcination and sulfation under CFB conditions[J]. CIESC Journal, 2017, 68(12): 4615-4624. |
| [9] |
王海苗. 循环流化床锅炉脱硫系统运行现状分析及优化途径[J]. 内蒙古煤炭经济, 2019(12): 33-34. WANG H M. Analysis and optimization of desulfurization system in circulating fluidized bed boiler[J]. Inner Mongolia Coal Economy, 2019(12): 33-34. |
| [10] |
WANG C, CHEN L, JIA L, et al. Simultaneous calcination and sulfation of limestone in CFBB[J]. Applied Energy, 2015, 155: 478-484. DOI:10.1016/j.apenergy.2015.05.070 |
| [11] |
杨忠凯, 王敬臣, 武宁, 等. 燃煤烟气脱硫技术综述[J]. 河南化工, 2019, 36(3): 3-6. YANG Z K, WANG J C, WU N, et al. Summary on desulfurization technology for coal-fired flue gas[J]. Henan Chemical Industry, 2019, 36(3): 3-6. |
| [12] |
杨玉环, 张媛媛. 钙硫比对CFB锅炉炉内脱硫效率的影响研究[J]. 应用能源技术, 2013(6): 28-32. YANG Y H, ZHANG Y Y. Research on Ca/S influences on in-furnace desulfurization efficiency of CFB boiler[J]. Applied Energy Technology, 2013(6): 28-32. |
| [13] |
何宏舟, 邹峥, 俞金树, 等. 循环流化床锅炉燃烧福建无烟煤炉内脱硫的工业试验研究[J]. 中国电机工程学报, 2010, 30(35): 7-12. HE H Z, ZOU Z, YU J S, et al. An industrial experiment research on the desulfurization of circulating fluidized bed boiler burning Fujian anthracite[J]. Proceedings of the CSEE, 2010, 30(35): 7-12. |
| [14] |
YE Z, WANG W, ZHONG Q, et al. High temperature desulfurization using fine sorbent particles under boiler injection conditions[J]. Fuel, 1995, 74(5): 743-750. DOI:10.1016/0016-2361(94)00011-F |
| [15] |
邹峥, 俞建洪, 何宏舟, 等. 钙硫比对循环流化床锅炉炉内脱硫影响的工业实验[J]. 工业锅炉, 2003(5): 20-22, 39. ZOU Z, YU J H, HE H Z, et al. The effects of Ca/S ratio on desulfurization in CFB boiler firing Fujian anthracite[J]. Industrial Boiler, 2003(5): 20-22, 39. |
| [16] |
张容. 循环流化床锅炉炉内脱硫降低Ca/S技术研究[J]. 内蒙古科技与经济, 2020(18): 89-91. ZHANG R. Study on desulfurization and reduction of Ca/S in circulating fluidized bed boiler[J]. Inner Mongolia Science Technology & Economy, 2020(18): 89-91. |
| [17] |
谭波, 王传志, 司硕, 等. 循环流化床锅炉高效炉内脱硫理论和关键技术[J]. 洁净煤技术, 2020, 26(4): 168-174. TAN B, WANG C Z, SI S, et al. Theory and key technologies of high efficiency desulfurization in circulating fluidized bed boilers[J]. Clean Coal Technology, 2020, 26(4): 168-174. |
| [18] |
刘进强, 刘姚君, 汪澜, 等. CFB-FGD脱硫灰对水泥性能影响及机理研究[J]. 新型建筑材料, 2020, 47(2): 84-87, 91. LIU J Q, LIU Y J, WANG L, et al. Study of the effect and mechanism of CFB-FGD desulfurization ash on cement properties[J]. New Building Materials, 2020, 47(2): 84-87, 91. |
| [19] |
HAYHURST A N, LAWRENCE A D. The effect of solid CaO on the production of NOx and N2O in fluidized bed combustors: Studies using pyridine as a prototypical nitrogenous fuel[J]. Combustion and Flame, 1996, 105(4): 511-527. DOI:10.1016/0010-2180(95)00219-7 |
| [20] |
ZIJLMA G J, JENSEN A D, JOHNSSON J E, et al. NH3 oxidation catalysed by calcined limestone—A kinetic study[J]. Fuel, 2002, 81(14): 1871-1881. DOI:10.1016/S0016-2361(02)00123-0 |
| [21] |
郭如新. 中国镁质资源概况与镁法烟气脱硫[J]. 硫磷设计与粉体工程, 2009(6): 24-29, 6. GUO R X. China's magnesium-based resources and flue gas desulfurization by magnesium oxide[J]. Sulphur Phosphorus & Bulk Materials Handling Related Engineering, 2009(6): 24-29, 6. |
| [22] |
田露, TAHMASEBI A, 李先春, 等. 氧化镁活性及用于烟气脱硫的实验研究[J]. 化工矿物与加工, 2015, 44(4): 22-24, 28. TIAN L, TAHMASEBI A, LI X C, et al. Tests on the activity of magnesium oxide and its application in flue gas desulfurization[J]. Industrial Minerals & Processing, 2015, 44(4): 22-24, 28. |
| [23] |
肖丽聪, 代淑娟. 我国菱镁矿现状及选矿方法的介绍[J]. 有色矿冶, 2017, 33(1): 29-31. XIAO L C, DAI S J. Introduction on the status of magnesite and its beneficiation methods in China[J]. Non-Ferrous Mining and Metallurgy, 2017, 33(1): 29-31. |
| [24] |
袁钢, 马永亮, 汪黎东. 氧化镁烟气脱硫反应特性研究[J]. 环境工程学报, 2010, 4(5): 1134-1138. YUAN G, MA Y L, WANG L D. Study on the characteristics of flue gas desulfurization by magnesium oxide[J]. Chinese Journal of Environmental Engineering, 2010, 4(5): 1134-1138. |
| [25] |
SATOH S, NAKAMURA M, OHIRA Y, et al. Characteristics of desulfurization by magnesite[J]. Kagaku Kogaku Ronbunshu, 2004, 30(5): 661-667. DOI:10.1252/kakoronbunshu.30.661 |
| [26] |
田琳, 连娜, 陈淑江, 等. 菱镁矿对火电厂烟气脱硫效率的影响[J]. 硅酸盐通报, 2014, 33(2): 351-354. TIAN L, LIAN N, CHEN S J, et al. Effect of magnesite on desulfurization efficiency of flue gas in heat-engine plant[J]. Bulletin of the Chinese Ceramic Society, 2014, 33(2): 351-354. |
| [27] |
王芳, 曾玺, 王永刚, 等. 微型流化床与热重测定煤焦非等温气化反应动力学对比[J]. 化工学报, 2015, 66(5): 1716-1722. WANG F, ZENG X, WANG Y G, et al. Comparation of non-isothermal coal char gasification in a micro fluidized bed and thermogravimetric analyzer[J]. CIESC Journal, 2015, 66(5): 1716-1722. |
| [28] |
曾玺, 王芳, 余剑, 等. 微型流化床反应分析的方法基础与应用研究[J]. 化工进展, 2016, 35(6): 1687-1697. ZENG X, WANG F, YU J, et al. Fundamentals and applications of micro fluidized bed reaction analysis[J]. Chemical Industry and Engineering Progress, 2016, 35(6): 1687-1697. |
| [29] |
GENG S, HAN Z, YUE J, et al. Conditioning micro fluidized bed for maximal approach of gas plug flow[J]. Chemical Engineering Journal, 2018, 351: 110-118. DOI:10.1016/j.cej.2018.06.076 |
| [30] |
王子铭, 陈亮, 岳爽, 等. 同时煅烧硫化反应中石灰石微观孔结构演变特性[J]. 化工学报, 2018, 69(5): 2149-2157. WANG Z M, CHEN L, YUE S, et al. Microstructure evolution of procedural products during simultaneous limestone calcination/sulfation[J]. CIESC Journal, 2018, 69(5): 2149-2157. |
| [31] |
陈亮, 王春波. CFB锅炉内石灰石同时煅烧/硫化反应动力学及孔结构演变模拟[J]. 中国电机工程学报, 2019, 39(23): 6952-6963, 7108. CHEN L, WANG C B. Kinetic model of the simultaneous calcination/sulfation reaction and the pore change of limestone in CFB boilers[J]. Proceedings of the CSEE, 2019, 39(23): 6952-6963, 7108. |
| [32] |
郭泰成, 邓菲, 邹潺, 等. O2/CO2气氛下水蒸气对石灰石同时煅烧/硫化的影响[J]. 电力建设, 2016, 37(1): 97-102. GUO T C, DENG F, ZOU C, et al. Effects of steam on simultaneous calcination and sulfation of limestone under O2/CO2[J]. Electric Power Construction, 2016, 37(1): 97-102. |
| [33] |
彭强, 郭玉香, 曲殿利. 菱镁矿热分解的动力学研究[J]. 硅酸盐通报, 2017, 36(6): 1886-1890. PENG Q, GUO Y X, QU D L. Thermal decomposition kinetics analysis of magnesite[J]. Bulletin of the Chinese Ceramic Society, 2017, 36(6): 1886-1890. |
| [34] |
张玉明, 纪德馨, 朱翰文, 等. 微型流化床中萘裂解生成小分子气体的反应动力学研究[J]. 化工学报, 2021, 72(5): 2604-2615. ZHANG Y M, JI D X, ZHU H W, et al. Reaction kinetics of naphthalene cracking into small molecule gas in a micro fluidized bed[J]. CIESC Journal, 2021, 72(5): 2604-2615. |
| [35] |
MAITRA S, MUKHERJEE S, SAHA N, et al. Non-isothermal decomposition kinetics of magnesite[J]. Cerâ mica, 2007, 53(327): 284-287. DOI:10.1590/S0366-69132007000300011 |




