丁酮肟是一种重要的化工产品,广泛应用于涂料、油漆、油墨的防结皮剂,锅炉除氧剂中,也可作为有机合成中间体如硅橡胶类密封剂的原料[1]。目前,国内生产丁酮肟的一种重要方法是酮胺法,该法会副产含有丁酮肟的硫酸铵水溶液,其中丁酮肟的含量大约为(1000~10000) ppm,硫酸铵浓度为0~40%(wt)[2]。由于硫酸铵结晶过程中排放的丁酮肟会污染环境,因此对于硫酸铵水溶液中的丁酮肟应进行分离回收。前期研究表明疏水性离子液体[Bmim][PF6]在萃取回收硫酸铵水溶液中的丁酮肟方面具有良好的效果,相比以前工艺中所用的传统有机溶剂,更为绿色、安全和节能[3]。
传统的萃取工艺多采用混合澄清槽、萃取塔等设备,普遍存在效率低、设备体积大、操作和维修费用高等缺点[4]。为了解决上述问题,亟需开发新的高效萃取分离技术和设备。在过去二十年中,微化工系统一直是一个研究热点[5~8]。与传统设备相比,微化工设备具有比表面积大、高效传质传热、体积小、安全性能高、无放大效应等众多优点[9, 10],因此在化学、化工、材料、食品、医药、环境等多个领域获得了越来越多的应用[11]。微通道是微化工系统的基本组成单位和关键组成部分,通道尺寸范围一般在0.05~1.0 mm。
鉴于微化工设备在传质方面的优越性,本文在自制的T型微通道内进行了离子液体[Bmim][PF6]萃取硫酸铵水溶液中丁酮肟的实验研究,系统考察了各因素对萃取过程的影响,以期对微通道萃取丁酮肟的工业化提供相关的工程基础数据。
2 实验部分 2.1 试剂与仪器1-丁基-3-甲基咪唑六氟磷酸盐([Bmim][PF6],纯度99.0%,C8H15PF6N2,中国科学院兰州化学物理研究所绿色化学与催化中心);丁酮肟(分析纯,纯度99.5%,C4H9NO,国药集团化学试剂有限公司);硫酸铵(分析纯,纯度99.0%,(NH4)2SO4,国药集团化学试剂有限公司);过硫酸铵(分析纯,纯度98.0%,(NH4)2S2O8,国药集团化学试剂有限公司);硫酸高铁铵(分析纯,纯度99.0%,NH4Fe(SO4)2·12H2O,国药集团化学试剂有限公司);浓硫酸(分析纯,纯度98.0%,H2SO4,国药集团化学试剂有限公司);甲醛溶液(分析纯,纯度37.0-40.0%,CH2O,国药集团化学试剂有限公司);去离子水。
SHZ-B水浴恒温振荡器(上海博迅实业有限公司医疗设备厂);FA1004A电子天平(上海精天电子仪器有限公司);LSP01-1A注射泵(保定兰格恒流泵有限公司);DLSB-10/25°低温冷却循环泵(杭州惠创仪器设备有限公司);752型紫外可见分光光度计(上海舜宇恒平科学仪器有限公司);DMA-4500型精密数字密度计(奥地利Anton Paar公司);RS6000旋转流变仪(德国HAAKE公司);PTFE微管(Valco Instruments Company Inc.);不锈钢T型三通接头(Valco Instruments Company Inc.)。
2.2 实验过程 2.2.1 两相物性的测定水相中丁酮肟和硫酸铵的浓度不同,其密度和黏度也不同,为了考察其对萃取过程的影响,需要对不同条件下的两相物性进行测量。本实验采用与实际工业生产中副产的含丁酮肟的硫酸铵水溶液相近的体系,即丁酮肟的浓度为1~10 g·L-1((1000~10000) ppm),硫酸铵质量分数为0~40%(wt),由于丁酮肟浓度较低,对物性的影响较小,可以忽略,故主要测量不同浓度硫酸铵水溶液的密度和黏度,使用的仪器分别是奥地利Anton Paar公司生产的DMA-4500型精密数字密度计和德国HAAKE公司生产的RS6000旋转流变仪,每组数据都重复测量三次,取平均值。体系在293.15 K时的基本物性参数如表 1所示:
| 表 1 实验体系的物性参数(293.15 K) Table 1 Physical properties of experimental systems at 293.15 K |
分配系数K是描述萃取过程中的重要参数,需要先对其进行测定,计算式为液液平衡时离子液体相中丁酮肟浓度与水相中丁酮肟浓度的比值:
| $ K = \frac{{C_{{\rm{IL}}}^{\rm{*}}}}{{C_{{\rm{aq}}}^{\rm{*}}}} $ | (1) |
在实验开始之前,将去离子水和离子液体[Bmim][PF6]在分液漏斗中充分混合后,静置分层,使其互相饱和,这样可以消除在萃取过程中因两相微量的互溶带来的实验误差,分液后的水相再用于配置丁酮肟溶液。取一定丁酮肟浓度的硫酸铵水溶液(丁酮肟浓度为1~10 g·L-1,硫酸铵质量分数为0~40%)与离子液体[Bmim][PF6]各5 mL,分别加入到离心管中,放入水浴振荡器里恒温(293.15 K)振荡,振荡频率设为200 Hz,使两相充分混合。实验发现在萃取时间超过20 min后,水相中丁酮肟的浓度基本不变,萃取过程达到平衡。为了确保达到液液平衡,振荡时间定为30 min,之后停止振荡,静置分层,由于离子液体相的密度大于水相的密度,离心管中上层为水相,下层为离子液体相。取1 mL水相,用去离子水稀释后用分光光度法测定其中所含丁酮肟的浓度。然后再根据总体系丁酮肟的质量守恒,可以计算出离子液体相中丁酮肟的浓度,代入式(1) 中计算分配系数,结果如表 2所示。
| 表 2 丁酮肟在两相中的分配系数(293.15 K) Table 2 Distribution coefficients (K) of butanone oxime in ionic liquid -water two phase systems at 293.15 K |
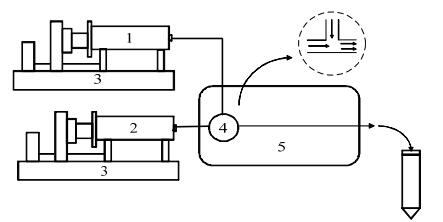
实验装置如图 1所示,微通道为PTFE管,内径为0.75 mm或1 mm,长0.2 m,将一定浓度丁酮肟的硫酸铵水溶液和离子液体[Bmim][PF6]由微注射泵推动进入各自的入口通道,在自制的微混合器(T型三通接头)处混合,然后进入主通道,两相在主通道内进行接触传质后,流出到离心管中。取上层水相,稀释后用紫外可见分光光度计测量其中的丁酮肟浓度。分别调节两相体积流量、流量比、丁酮肟浓度和硫酸铵浓度等条件,考察不同因素对萃取过程的影响。实验装置置于20℃恒温水浴中,避免温度变化影响到实验结果的准确性,另外每次取样时应保证相同的时间间隔,以消除通道外传质对实验带来的影响。
|
图 1 微通道萃取装置示意图 Fig.1 Schematic diagram of the experimental setup 1. aqueous phase 2. ionic liquid phase 3. syringe pump 4.micromixer 5. water bath(20℃) |
参照环己酮肟的测定方法[12],使丁酮肟在酸性条件下水解,生成丁酮和羟胺,在加入过硫酸铵的条件下,羟胺与甲醛反应生成甲酰氧肟酸,甲酰氧肟酸可与三价铁离子生成红色络合物,最大吸收波长为500 nm,在此波长下用紫外可见分光光度计测其吸光度便可得到水相中丁酮肟的浓度。
2.4 实验数据处理微通道的传质性能可用两个参数来表征,即萃取效率Eeff和总体积传质系数kLa。萃取效率是实验过程中丁酮肟的实际萃取量与最大可萃取量的比值,计算公式如下[13]:
| $ {E_{{\rm{eff}}}} = \frac{{{C_{{\rm{IL}}, {\rm{out}}}}-{C_{{\rm{IL}}, \rm{in}}}}}{{C_{{\rm{IL}}, {\rm{out}}}^ *-{C_{{\rm{IL}}, \rm{in}}}}} $ | (2) |
| $ C_{{\rm{IL}}, {\rm{out}}}^ * = K{C_{{\rm{aq, out}}}} $ | (3) |
根据质量守恒定律,微通道的输入量等于输出量加微通道内的累积量,而实验中是在微通道内的液体流动达到稳定状态后才开始取样,因此输入量等于输出量,即为下式:
| $ {Q_{{\rm{aq}}}} \cdot C_{{\rm{aq, in}}}^{} + {Q_{{\rm{IL}}}} \cdot C_{{\rm{IL, in}}}^{} = {Q_{{\rm{aq}}}} \cdot C_{{\rm{aq, out}}}^{} + {Q_{{\rm{IL}}}} \cdot C_{{\rm{IL, out}}}^{} $ | (4) |
其中,Caq, in为微通道入口处水相中丁酮肟浓度,Caq, out为微通道出口处水相中丁酮肟浓度,CIL, in为微通道入口处离子液体相中丁酮肟浓度,在本实验中CIL, in=0,CIL, out为微通道出口处离子液体相中丁酮肟浓度,Qaq为水相的体积流量,QIL为离子液体相的体积流量。
以萃取相(离子液体相)为基准,总体积传质系数kLa定义为下式[13]:
| $ {Q_{{\rm{IL}}}}\left( {C_{\rm{IL}, {\rm{out}}}^{}-C_{\rm{IL}, in}^{}} \right) = {k_\rm{L}}aV\Delta {C_\rm{m}} $ | (5) |
| $ {k_\rm{L}}a = \frac{{{Q_{\rm{IL}}}\left( {C_{\rm{IL}, {\rm{out}}}^{}-C_{\rm{IL}, in}^{}} \right)}}{{V\Delta {C_\rm{m}}}} $ | (6) |
| $ \Delta {C_\rm{m}} = \frac{{\left( {C_{\rm{IL}, in}^ *- C_{\rm{IL}, in}^{}} \right)- \left( {C_{\rm{IL}, \rm{out}}^ *- C_{\rm{IL}, \rm{out}}^{}} \right)}}{{\ln \left[{\left( {C_{\rm{IL}, in}^ *-C_{\rm{IL}, in}^{}} \right)/\left( {C_{\rm{IL}, \rm{out}}^ *-C_{\rm{IL}, \rm{out}}^{}} \right)} \right]}} $ | (7) |
其中,a 为比表面积,V为微通道体积,ΔCm为对数平均浓度差,
为了计算雷诺数,定义两相混合平均密度ρM[14]和平均黏度μM[15]如下:
| $ {\rho _M} = {\left( {\frac{{{\varphi _\rm{aq}}}}{{{\rho _\rm{aq}}}} + \frac{{1-{\varphi _\rm{aq}}}}{{{\rho _{\rm{IL}}}}}} \right)^{-1}} $ | (8) |
| $ {\mu _M} = {\left( {\frac{{{\varphi _\rm{aq}}}}{{{\mu _\rm{aq}}}} + \frac{{1-{\varphi _\rm{aq}}}}{{{\mu _{\rm{IL}}}}}} \right)^{-1}} $ | (9) |
| $ {\varphi _\rm{aq}} = \frac{{{Q_\rm{aq}}}}{{{Q_\rm\rm{aq}} + {Q_{\rm{\rm{IL}}}}}} $ | (10) |
雷诺数ReM的计算式为:
| $ R{e_M} = \frac{{ID \cdot {u_{\rm{M}}}{\rho _\rm{M}}}}{{{\mu _\rm{M}}}} $ | (11) |
| $ {u_{\rm{M}}} = \frac{{{Q_\rm{aq}} + {Q_{{\rm{IL}}}}}}{A} $ | (12) |
其中,φaq为水相的体积分数,ρaq、ρIL分别为水相和离子液体相的密度,μaq、μIL分别为水相和离子液体相的黏度,ID为微通道内径,uM为两相混合流速,A为微通道的截面积。
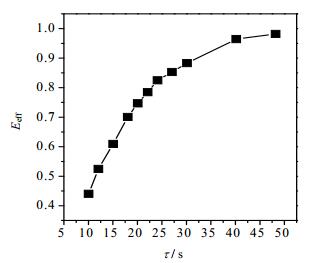
3 结果与讨论 3.1 微通道萃取平衡时间图 2显示了微通道内萃取效率Eeff与停留时间τ的关系,可以看到,在停留时间为50 s时,萃取效率为100%,萃取达到平衡,与传统萃取方式所需的20 min相比,萃取时间大大缩短,这说明微通道有着更高的萃取效率。
|
图 2 丁酮肟萃取效率Eeff与停留时间τ的关系 Fig.2 Effects of the extraction time on extraction efficiency(Eeff) of butanone oxime q = Qaq/QIL=1, ID = 0.75 mm, Caq, in = 10 g·L-1, w[(NH4)2SO4] = 20% |
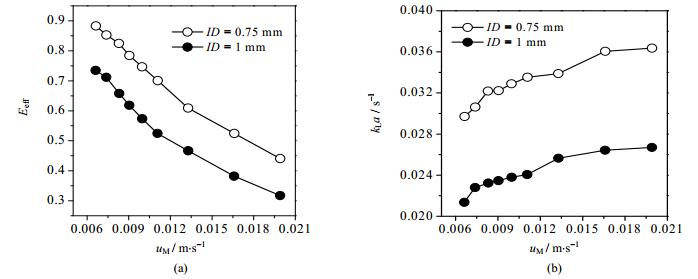
图 3为固定水相与离子液体相的流量比q=1时,总表观流速对萃取效率和总体积传质系数的影响。从图中可以看到,随着总流速的增大,萃取效率减小,总体积传质系数增大。这是因为,两相的总流速越大,输入微通道内的动能(唯一的分散能量来源)越多,使得液滴分散性更好,传质比表面积a增大;另外,流速的增加,导致连续相一侧和分散相一侧的液膜传质系数均增加,总传质系数kL增加,因此,总体积传质系数kLa随着总表观流速的增大而增加。萃取效率随着总表观流速的增加而减小,这是因为停留时间减小的缘故。因此,萃取效率不仅取决于总体积传质系数,也跟停留时间有关,是两者综合作用的结果。
|
图 3 总表观流速对萃取效率(a)及总体积传质系数(b)的影响 Fig.3 Effects of the total flow velocity on extraction efficiency (a) and overall volumetric mass transfer coefficient(b) q = 1, Caq, in = 10 g·L-1, w[(NH4)2SO4] = 20% |
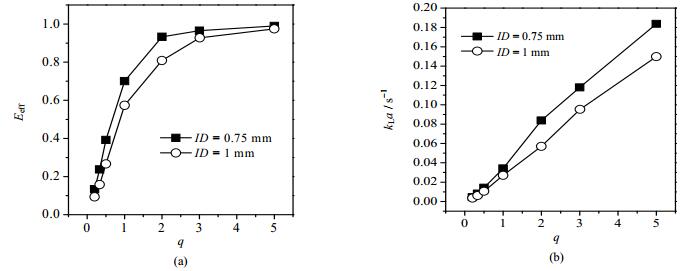
固定总表观流速uM= 0.0113 m·s-1时,萃取效率和总体积传质系数都随着流量比的增大而增大,如图 4所示。总流速相同,流量比越大,即水相(分散相)流速越大,分散相在微通道内的持液量越大,这将导致传质界面的增大,同时离子液体相(连续相)流速减小,分散能力减弱,形成的液柱/液滴尺寸增大,导致比表面积减小,总体积传质系数的增大或减小取决于这两个因素哪个影响更显著,而从图 4(b)来看,显然前者作用更大,即总体积传质系数随着流量比的增大而增大。在相同的总流速,即在相同的停留时间下,萃取效率也越大。
|
图 4 流量比对萃取效率(a)及总体积传质系数(b)的影响 Fig.4 Effects of aqueous-ionic liquid volumetric flux ratio on extraction efficiency (a) and overall volumetric mass transfer coefficient(b) uM = 0.0113 m·s-1, Caq, in = 10 g·L-1, w[(NH4)2SO4] = 20% |
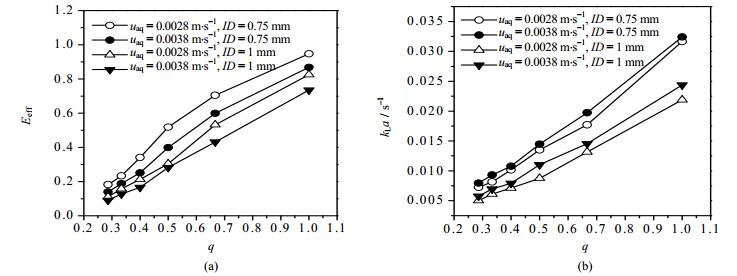
从图 5可以看出,固定水相流速,萃取效率和总体积传质系数随着离子液体相流速的增大(即流量比减小)而减小,离子液体相(连续相)流速增大,微通道内的分散相持液量减小,从而导致了传质界面的减小,总体积传质系数减小,同时停留时间也减小,萃取效率减小。
|
图 5 连续相流速对萃取效率(a)及总体积传质系数(b)的影响 Fig.5 Effects of the continuous phase flow velocity on extraction efficiency(a) and overall volumetric mass transfer coefficient(b) Caq, in= 10 g·L-1, w[(NH4)2SO4] = 20% |
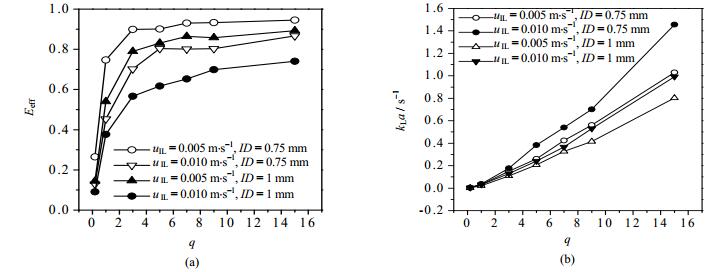
固定离子液体相流速,萃取效率和总体积传质系数随着水相(分散相)流速的增大(即流量比增大)而增大,如图 6所示。随着水相流速的增大,一方面分散相一侧的传质系数增大,另一方面微通道内分散相持液量的增加导致比表面积增大,从而使得总体积传质系数增大。虽然两相在微通道中的接触时间减小,但总体积传质系数增大的影响更大,导致了萃取效率的增大,不过当流量比大到一定程度(从图中看为3左右)时,萃取效率的增大幅度明显变缓,这时接触时间变小的影响就体现出来了。
|
图 6 分散相流速对萃取效率(a)及总体积传质系数(b)的影响 Fig.6 Effects of dispersed phase flow velocity on extraction efficiency (a) and the overall volumetric mass transfer coefficient(b) Caq, in= 10 g·L-1, w[(NH4)2SO4] = 20% |
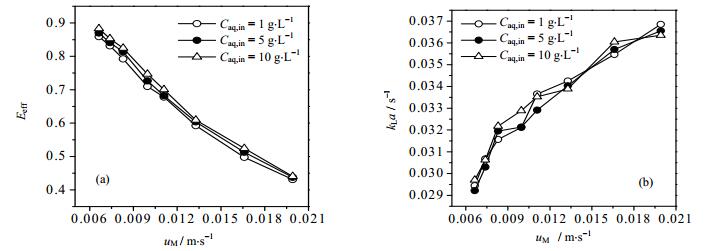
图 7显示了丁酮肟浓度对萃取效率和总体积传质系数的影响,从图中可以看出,固定其它条件时,随着丁酮肟浓度的增加,萃取效率增大。这是因为,溶质初始的浓度差是传质推动力,萃取效率随着传质推动力的增大而增大,而两相的传质推动力取决于丁酮肟浓度。另外,由图 7(b)可以看到,随着丁酮肟浓度的增加,总体积传质系数的变化趋势并不规律,这说明总体积传质系数与丁酮肟的浓度并无直接关系。
|
图 7 丁酮肟浓度对萃取效率(a)及总体积传质系数(b)的影响 Fig.7 Effects of butanone oxime concentration on extraction efficiency (a) and the overall volumetric mass transfer coefficient (b) ID = 0.75 mm, q = 1, w[(NH4)2SO4] = 20% |
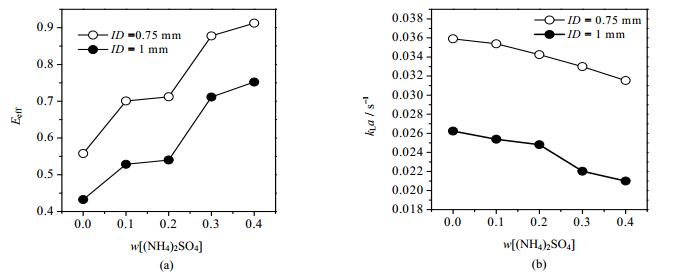
图 8反映了硫酸铵浓度对萃取的影响,随着硫酸铵浓度的增加,萃取效率增大,总体积传质系数减小。这是因为总体积传质系数等于总传质系数乘以比表面积,总传质系数kL的计算式为:
|
图 8 硫酸铵浓度对萃取效率(a)及总体积传质系数(b)的影响 Fig.8 Effects of ammonium sulfate concentration on extraction efficiency (a) and the overall volumetric mass transfer coefficient (b) uM = 0.011 m·s-1, q = 1, Caq, in= 10 g·L-1 |
在考察前几个因素时,都分别在不同内径(0.75 mm/1 mm)的微通道内做了对比实验,从图 3、4、5、6、8均可以看出,在其它条件相同的情况下,随着微通道内径的减小,萃取效率和总体积传质系数都增加。通道尺寸的减小导致所形成液滴的尺寸变小,接触比表面积增大,同时内循环增强,强化了对流传质,加快界面更新,从而使得丁酮肟在相界面的浓度梯度增加,在界面的扩散速度加快,因此总体积传质系数增大,在相同的停留时间内萃取效率也增大。
4 总体积传质系数的关联由于微通道中的液-液两相传质过程较复杂,目前还没有提出相关基于传质理论的微通道内液-液传质模型。Kashid等[14]根据实验结果,关联得到了一种微通道内弹状流液-液传质的总体积传质系数的经验式:
| $ {k_L}a\frac{{{L_{\rm{p}}}}}{{{U_{{\rm{mix}}}}}} = 0.0257C{a^{-0.6}}R{e^{0.05}}{\left( {\frac{{ID}}{{{L_{\rm{p}}}}}} \right)^{-0.1}} $ | (13) |
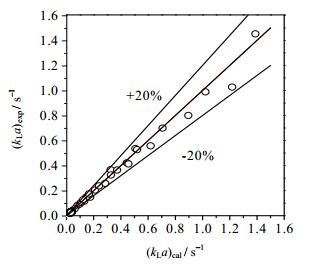
但该关联式中需用到参数液柱长度Lp,而Lp在工业上很难提供,故使用起来并不方便。因此,本文尝试将所得总体积传质系数与流量比、雷诺数以及微通道内径进行关联。所有的数据点是在内径ID为0.75和1 mm的微通道中,通过改变两相的体积流量,将两相流量比q固定在0.2~15,总表观流速 uM固定在0.004~0.16 m·s-1测得,实验中液液两相流流型为弹状流。关联结果如式(14) 所示,图 9显示了微通道萃取硫酸铵水溶液中丁酮肟的总体积传质系数(kLa)的实验值与计算值的比较结果,可以看到两者的误差在±20%之间,平均相对偏差(AAD)为4.85%,最大相对偏差(MAD)为17.9%。偏差的计算式分别为式(15) 和(16):
|
图 9 总体积传质系数kLa实验值与计算值的比较 Fig.9 Comparison of experimental and calculated values of kLa |
| $ {k_L}a = 3.10 \times {10^{-6}}{q^{1.14}}Re_M^{0.19}I{D^{-1.26}} $ | (14) |
| $ AAD = \frac{1}{N}{\sum\limits_{j = 1}^N {\left| {\left( {\frac{{{{\left( {{k_L}a} \right)}_{\exp }}-{{\left( {{k_L}a} \right)}_{{\rm{cal}}}}}}{{{{\left( {{k_L}a} \right)}_{\exp }}}}} \right)} \right|} _{\rm{j}}} $ | (15) |
| $ MAD = {\left| {\frac{{{{\left( {{k_L}a} \right)}_{\exp }}-{{\left( {{k_L}a} \right)}_{{\rm{cal}}}}}}{{{{\left( {{k_L}a} \right)}_{\exp }}}}} \right|_{\max }} $ | (16) |
其中N是实验点数,下标exp和cal分别代表实验值和计算值。
5 结论(1) 在微通道内进行了离子液体[Bmim][PF6]萃取硫酸铵水溶液中的丁酮肟实验,发现萃取达到平衡的时间较传统萃取方式大大缩短,萃取效率显著提高。
(2) 萃取效率与水相/离子液体相流量比、水相流速、丁酮肟和硫酸铵的浓度成正相关,与总表观流速、离子液体相流速和微通道内径成负相关。
(3) 总体积传质系数与总表观流速、水相/离子液体相流量比和水相流速成正相关,与离子液体相流速、微通道内径和硫酸铵浓度成负相关,此外,总体积传质系数与丁酮肟的浓度并无明显关系。通过关联发现,总体积传质系数与流量比的1.14次方成正比,与雷诺数的0.19次方成正比,与微通道内径的1.26次方成反比。此经验关联式的平均相对偏差为4.85%,最大相对偏差为17.9%。
符号说明:
A —微通道截面积,m2
C —丁酮肟浓度,g·L-1
Eeff —萃取效率
ID —微通道内径,m
K —分配系数
kLa —总体积传质系数,S-1
Q —体积流量,μL·min-1
q —水相与离子液体相的流量比
Re —雷诺数
u —流速,m·s-1
ρ —密度,kg·m-3
μ —黏度,Pa·s
上标
* —表示与另一相平衡的状态
下标
aq —水相
cal —计算值
exp —实验值
IL —离子液体相
in —微通道入口
M —混合值
out —微通道出口
| [1] | LI Meng(李猛), LIU Jun-dong(刘俊东), NA Hong-zhuang(那宏壮). Application and advancement in synthesis of 2-butanone oxime(丁酮肟的应用与合成进展)[J]. Chemical Engineer(化学工程师), 2006, 20(7): 42-43. |
| [2] | ZHENG Bo-yu(郑博予), FANG Sheng(房升), HE Chao-hong(何潮洪). Measurement and correlation of densities and viscosities for binary mixtures of methyl ethyl ketoxime with methyl ethyl ketone, cylclohexane, and n-hexane(丁酮肟-丁酮、正己烷、环己烷二元体系密度和黏度的测定及关联)[J]. Journal of Chemical Engineering of Chinese Universities(高校化学工程学报), 2010, 24(6): 911-916. |
| [3] | ZHANG Chen(张宸), CHEN Qiao-li(陈巧丽), WU Ke-jun(吴可君), et al. Liquid-liquid equilibrium of[bmim][PF6]-butanone qxime-water-ammonium sulfate systems([Bmim][PF6]-丁酮肟-水-硫酸铵体系液液平衡的研究)[J]. Journal of Chemical Engineering of Chinese Universities(高校化学工程学报), 2015, 29(6): 1313-1319. |
| [4] | Tegrotenhuis W E, Cameron R J, Butcher M G, et al. Microchannel devices for efficient contact of liquids in solvent extraction[J]. Separation Science & Technology, 1999, 34(6-7): 951-974. |
| [5] | Mason B P, Price K E, Steinbacher J L, et al. Greener approaches to organic synthesis using microreactor technology[J]. Chemical Reviews, 2007, 38(36): 2300-2318. |
| [6] | Roberge D M, Zimmermann B, Rainone F, et al. Microreactor technology and continuous processes in the fine chemical and pharmaceutical industry: is the revolution underway?[J]. Organic Process Research & Development, 2008, 12(5): 905-910. |
| [7] | Pohar A, Si I, Fkkt P. Process Intensification through MicroreactorApplication[J]. Chemical & Biochemical Engineering Quarterly, 2009, 23(4): 537-544. |
| [8] | Ahmed-Omer B, Brandt J C, Wirth T. Advanced organic synthesis using microreactor technology[J]. Organic & Biomolecular Chemistry, 2007, 5(5): 733-740. |
| [9] | Jähnisch K, Hessel V, Löwe H, et al. Chemistry in microstructured reactors[J]. AngewandteChemie International Edition, 2004, 43(4): 406.DOI:10.1002/(ISSN)1521-3773. |
| [10] | CHEN Guang-wen(陈光文), YUAN Quan(袁权). Micro-chemicaltechnology(微化工技术)[J]. Journal of Chemical Industry and Engineering(化工学报), 2003, 54(4): 427-439. |
| [11] | JensenK F. Microchemical systems: status, challenges, and opportunities[J]. AIChE Journal, 1999, 45(10): 2051-2054.DOI:10.1002/(ISSN)1547-5905. |
| [12] | WU Su-fang(吴素芳), LIU Jian-qing(刘建青), XU You-tian(徐有田), et al. Determination of cyclohexanoneoxime in esters by spectrophotometry(分光光度法测定转位酯中环己酮肟)[J]. Chinese Journal of Analytical Chemistry(分析化学), 2002, 30(7): 891. |
| [13] | Sen N, Darekar M, Singh K K, et al. Solvent extraction and stripping studies in microchannels with TBP nitric acid system[J]. Solvent Extraction & Ion Exchange, 2013, 32(3): 281-300. |
| [14] | KashidM N, Gupta A, Renken A, et al. Numbering-up and mass transfer studies of liquid-liquid two-phase microstructuredreactors[J]. Chemical Engineering Journal, 2010, 158(2): 233-240.DOI:10.1016/j.cej.2010.01.020. |
| [15] | Zhao Y, Chen G, Yuan Q. Liquid -liquid two -phase mass transfer in the T -junction microchannels[J]. AIChE Journal, 2007, 53(12): 3042-3053.DOI:10.1002/(ISSN)1547-5905. |




