2. 浙江大学 化学工程与生物工程学院, 浙江 杭州 310027;
3. 浙江树人大学 生物与环境工程学院, 浙江 杭州 310015;
4. 绍兴市环境监测中心站, 浙江 绍兴 312000
2. College of Chemical and Biological Engineering, Zhejiang University, Hangzhou 310027, China;
3. College of Biology and Environmental Engineering, Zhejiang Shuren University, Hangzhou 310015, China;
4. Shaoxing Environmental Monitoring Center Station, Shaoxing 312000, China
氮氧化物(NOx)是主要的大气污染物之一,它会造成酸雨、雾霾等环境污染事件。NOx排放的有效控制对改善我国大气环境质量具有重要意义[1]。随着我国燃煤电厂超低排放技术改造基本完成,工业烟气NOx排放控制的主战场已转移至钢铁、水泥、石化、玻璃等非电行业。用NH3为还原剂的选择性催化还原(SCR)脱硝技术是用于燃煤电厂烟气脱硝的最广泛、成熟且高效的技术。为更大力度地降低非电行业的NOx排放,采用SCR脱硝技术对相关工业炉窑进行提标改造势在必行[2]。SCR脱硝技术的核心在于催化剂的选择,但燃煤电厂所广泛采用的V2O5-WO3/TiO2催化剂运行温度相对较高(350~450 ℃),而非电行业的水泥回转窑、玻璃熔窑、冶金烧结机等产生的烟气对中低温条件下(低于300 ℃)的脱硝有较强的需求[3-4]。烟气再热是一种可选的方法,但会增加大量的能量消耗以及设备投资成本[5-6]。因此,开发具备优异中低温活性的新型SCR烟气脱硝催化剂具有重要意义。
过渡金属中的Mn是SCR烟气脱硝催化剂常见的中低温活性组分,但是锰氧化物易产生N2O[7-9]。近年来,也有学者研究了铬氧化物用于NH3-SCR的脱硝效果,发现它们展现了良好的催化活性[10-11]。构筑复合氧化物体系是提升SCR烟气脱硝催化剂性能的常见手段,由于不同活性组分间的协同作用,往往使得复合体系的性能显著优于单独组分。那么,Mn-Cr复合氧化物的SCR脱硝性能如何?Chen等[12]制备了由CrOx与MnOx物理混合而成的氧化物,发现Cr(0.4)-MnOx在120 ℃时脱硝效率可达98.5%。Gao等[13]用柠檬酸法制备了不同比例的Mn-Cr复合氧化物,发现Mn(3)Cr(2)Ox催化剂性能最佳,在100~225 ℃时脱硝效率接近100%。Mn-Cr除了可形成CrMn2O4物相,也可形成尖晶石型MnCr2O4物相[14]。然而,MnCr2O4的SCR脱硝性能尚不明确。本文探究了以不同方法制备MnCr2O4的可行性,并对它们的脱硝性能进行测试对比,确定最佳的制备条件,同时对催化剂的构效关系进行了探究与分析。
2实验(材料与方法)
2.1 实验材料九水硝酸铬、五水硝酸锰、一水合柠檬酸等试剂均为分析纯,购自国药集团有限公司。
2.2 催化剂制备方法水热合成法的具体步骤:取x mmol硝酸锰和2x mmol硝酸铬前驱体混合并溶于30 mL去离子水中,然后加入3x mmol的尿素,剧烈搅拌至完全溶解。将溶液转移至聚四氟乙烯做内衬的高压反应釜中,在150 ℃下反应12 h。将沉淀用去离子水洗涤3次,在80 ℃下完全烘干。再将烘干的固体粉末置于管式炉中,在600 ℃空气氛围下煅烧4 h,获得最终样品[15]。
沉淀法的具体步骤:取x mmol硝酸锰和2x mmol硝酸铬前驱体混合并溶于30 mL去离子水中,在混合溶液中滴入氨水(20 mL,质量分数为25%),在室温下剧烈搅拌2 h,然后蒸干水分。再将固体粉末置于管式炉中,在600 ℃空气氛围下煅烧4 h,获得最终样品用于下一步测试[16]。
溶胶凝胶法的具体步骤:取x mmol硝酸锰和2x mmol硝酸铬前驱体混合并溶于30 mL去离子水中,在水浴锅60 ℃恒温下剧烈搅拌10 min直至充分溶解,然后加入3.6 x mol的柠檬酸,将混合溶液在90 ℃水浴中剧烈搅拌直至形成黏稠的凝胶,然后将凝胶转移至烘箱,在200 ℃下反应1 h,分解所形成的络合物并获得初步固体产物。最后,将固体产物置于管式炉中,在600 ℃空气氛围下煅烧4 h,获得最终样品[17]。下文中水热法、沉淀法和溶胶凝胶法制备的MnCr2O4催化剂分别用MnCr2O4-W、MnCr2O4-P和MnCr2O4-S表示。
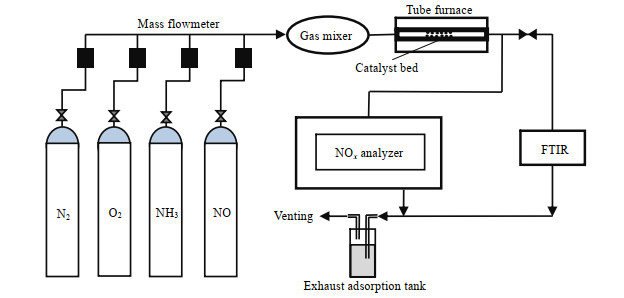
2.3 测试方法如图 1所示,SCR烟气脱硝催化剂活性评价装置由配气系统、催化反应系统和尾气分析系统这三部分组成。其中,配气系统的功能是由钢瓶气配成500×10-6 NOx、500×10-6 NH3、3.6% O2(体积分数)以及N2为载气的模拟烟气,通过质量流量控制器来确定通入气体的流速;催化反应系统包括管式炉和催化剂,反应温度由温控仪精确控制。将催化剂粒径筛分为40~60目,称取相应质量并将催化剂填充于固定床石英反应器(内径6 mm) 中;尾气分析系统包括NO-NO2-NOx分析仪(Thermo Scientific 42i-HL)和FTIR光谱仪(Thermo Scientific, Nicolet 6700),入口和出口的NOx体积分数用NO-NO2-NOx分析仪进行连续在线监测,NH3和N2O的体积分数用FTIR光谱仪定量检测。
|
图 1 SCR烟气脱硝催化剂活性评价装置 Fig.1 Schematic diagram of the evaluation setup for SCR flue gas de-NOx measurements |
脱硝效率和N2选择性通过下式计算,每组数据测三次后取平均值。
| $ {\rm{de - N}}{{\rm{O}}_x}{\rm{ efficiency = }}\left( {1 - \frac{{\varphi {{({\rm{NO)}}}_{\rm out}} + \varphi {{({\rm{N}}{{\rm{O}}_2})}_{\rm out}}}}{{\varphi {{({\rm{NO)}}}_{\rm in}} + \varphi {{({\rm{N}}{{\rm{O}}_2})}_{\rm in}}}}} \right) \times {\rm{100\% }} $ | (1) |
| $ {{\rm{N}}_{\rm{2}}} \ {\rm{ selectivity = }}\left( {\frac{{\varphi {{{\rm{(NO)}}}_{\rm in}} + \varphi {{({\rm{N}}{{\rm{H}}_3})}_{\rm in}} - \varphi {{{\rm{(N}}{{\rm{O}}_2}{\rm{)}}}_{\rm out}} - 2\varphi {{{\rm{(}}{{\rm{N}}_2}{\rm{O)}}}_{\rm out}}}}{{\varphi {{{\rm{(NO)}}}_{\rm in}} + \varphi {{({\rm{N}}{{\rm{H}}_3})}_{\rm in}}}}} \right){\rm{ }} \times {\rm{100\% }} $ | (2) |
式中:φ为稳态时的体积分数,下标“in”和“out”分别为入口和出口。
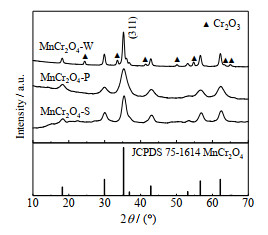
3 实验结果与讨论 3.1 晶型结构通过XRD分析MnCr2O4-W、MnCr2O4-P和MnCr2O4-S的物相组成,结果如图 2所示。MnCr2O4-P和MnCr2O4-S的衍射峰位置与MnCr2O4的PDF标准卡片峰位置完全对应,且未检测到其他杂质峰,说明沉淀法和溶胶凝胶法制得了纯尖晶石型的MnCr2O4。相比之下,水热法制备的MnCr2O4-W为非纯MnCr2O4物相,因为可以观察到明显的Cr2O3杂峰。以上结果表明,通过沉淀法和溶胶凝胶法制备的MnCr2O4纯度要高于水热法,MnCr2O4-W中含有少量Cr2O3杂质,但MnCr2O4仍占主要部分。以最强峰(311)晶面为代表观察样品的衍射峰,可发现MnCr2O4-W的衍射峰最为尖锐,MnCr2O4-S次之,MnCr2O4-P则相对平缓。这说明水热法制备的MnCr2O4-W催化剂的结晶度最高,形成了较大的晶粒。而沉淀法制备的MnCr2O4-P催化剂的结晶度相对最差,所形成的晶粒尺寸最小。
|
图 2 MnCr2O4催化剂的XRD图谱 Fig.2 XRD patterns of MnCr2O4 catalysts |
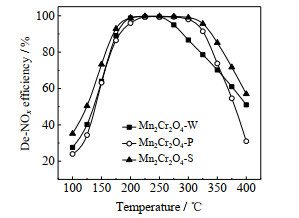
通过测试对比了MnCr2O4-W、MnCr2O4-P和MnCr2O4-S的脱硝效率以及N2选择性,结果分别绘于图 3和4中。可以看出,总的来说MnCr2O4-S催化剂的脱硝效率最高,即催化效率最佳,而MnCr2O4-W和MnCr2O4-P在不同温度区间的脱硝效率不同。在高温段(300 ℃以上),MnCr2O4-P脱硝效率随着温度升高下降较快;此外,在250~350 ℃时,MnCr2O4-P的催化效率显著高于MnCr2O4-W,而在350~400 ℃时,MnCr2O4-W的脱硝效率略高于MnCr2O4-P。由实验结果还可知,在反应空速GHSV = 60 000 h-1时,MnCr2O4-W、MnCr2O4-P和MnCr2O4-S的脱硝效率高于90%的温度窗口T90分别为176~289 ℃、181~327 ℃和169~341 ℃,可见MnCr2O4-S的活性温度窗口相对较宽、较低。
|
图 3 MnCr2O4催化剂的脱硝效率 Fig.3 De-NOx efficiency of MnCr2O4 catalysts |
|
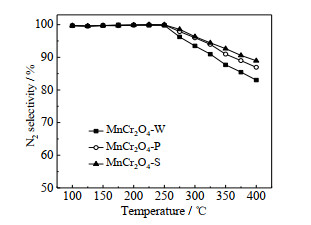
图 4 MnCr2O4催化剂的N2选择性 Fig.4 N2 selectivity of different MnCr2O4 catalysts |
由于SCR过程中NH3的非选择性氧化,常生成N2O这一副产物,对大气环境产生不利影响。N2O的生成可以通过N2选择性来反映,计算式见式(2)。N2选择性测试结果如图 4所示。由图可见,MnCr2O4-W、MnCr2O4-P和MnCr2O4-S催化剂展现出的N2选择性相差不大,在250 ℃以下时,它们的N2选择性均接近100%;在250 ℃以上时,N2选择性随温度升高而缓慢降低。总体上,在250 ℃以上时,MnCr2O4-S的N2选择性略高于MnCr2O4-W和MnCr2O4-P,而且其N2选择性随温度升高而下降,且相对更为平缓。
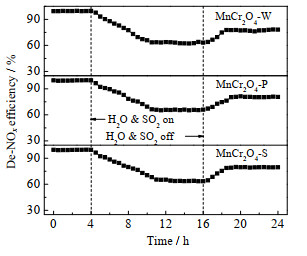
工业烟气即使完成脱硫净化,仍会残留少量SO2,在反应中会形成硫酸铵等物质导致催化剂活性降低。本文测试了在SO2与H2O共存下MnCr2O4-W、MnCr2O4-P和MnCr2O4-S催化剂的脱硝效率变化,选定SO2体积分数为100×10-6,水汽体积分数为5 %,测试温度为250 ℃,如图 5所示,在4 h时通入以上体积分数的SO2 + H2O混合气,待脱硝效率逐步稳定之后,即16 h时切断SO2 + H2O混合气。由图可见,随着SO2 + H2O混合气的持续通入,脱硝效率均逐渐降低,最终稳定在65%左右。切断SO2 + H2O混合气之后,脱硝效率逐渐上升,但未能恢复至新鲜催化剂的水平,最终只升至约80%,这表明MnCr2O4-W、MnCr2O4-P和MnCr2O4-S催化剂的脱硝效率均受到显著影响。一般地,由硫酸铵覆盖活性位点所导致的催化效率损失是可逆的,而活性位点金属离子的硫酸盐化导致的催化效率损失往往不可逆[18]。由此推断,MnCr2O4的失活是由于Mn与Cr离子的硫酸盐化使催化剂的活性位点损失,导致其催化效率发生不可逆损失。
|
图 5 SO2 + H2O存在对MnCr2O4脱硝效率的影响 Fig.5 Effects of SO2 + H2O on the de-NOx efficiency of MnCr2O4 catalysts |
MnCr2O4-W、MnCr2O4-P和MnCr2O4-S催化剂的平均晶粒尺寸、比表面积、平均孔径和孔容积列于表 1。MnCr2O4-W、MnCr2O4-P和MnCr2O4-S的平均晶粒尺寸分别为13.41、10.56和11.09 nm,晶粒尺寸大小规律与XRD衍射峰形状相吻合。对比发现,MnCr2O4-W催化剂的比表面积、平均孔径和孔容积均明显高于MnCr2O4-S催化剂的值,但后者却展现出了更高的催化效率。考虑到SCR催化剂的催化活性由多个因素综合决定,比表面积与孔道结构并不是影响催化活性的唯一因素,例如表面酸性、氧化还原性能等性质在SCR反应中往往也起到更为重要的作用。因此,下面进一步对MnCr2O4-W、MnCr2O4-P和MnCr2O4-S催化剂的微观形貌、表面元素浓度、表面酸性及氧化还原性能等方面进行探究。
|
|
表 1 不同制备方法所得MnCr2O4的平均晶粒尺寸、比表面积、平均孔径和孔容积 Table 1 Mean crystallite size, surface area, mean pore diameter and pore volume of MnCr2O4 prepared by various methods |
图 6为扫描电子显微镜(SEM)照片,显示了水热法、沉淀法和溶胶凝胶法制备的MnCr2O4的微观形貌,其中,(a1)与(a2)、(b1)与(b2)、(c1)与(c2)均为不同放大倍数下的同一组样品。总体来看,三种方法制得的催化剂均由微细颗粒组成,且呈现出无序排列状态,形貌上类似、无显著差异。这表明,在本实验条件下微观形貌对MnCr2O4的SCR催化活性影响较小。

|
图 6 不同方法制备的MnCr2O4催化剂扫描电子显微镜照片 Fig.6 SEM images of MnCr2O4 catalysts prepared by various methods |
为进一步探究不同制备方法所得的MnCr2O4催化剂的表面元素组成和局部化学环境,对样品进行了XPS表征,催化剂表面各元素的摩尔分数列于表 2。由表可见,各样品表面Mn、Cr与O的摩尔分数存在一定差异,其中,MnCr2O4-P表面上Mn的摩尔分数最高(10.35%),MnCr2O4-S表面上Cr与O的摩尔分数最高(26.33%与65.11%)。这说明,沉淀法更易使Mn元素在表面聚集,而溶胶凝胶法更易使Cr与O元素在表面聚集。
|
|
表 2 XPS测试的不同制备方法所得MnCr2O4表面元素摩尔分数 Table 2 The mole fraction of surface element of MnCr2O4 by various methods obtained with XPS |
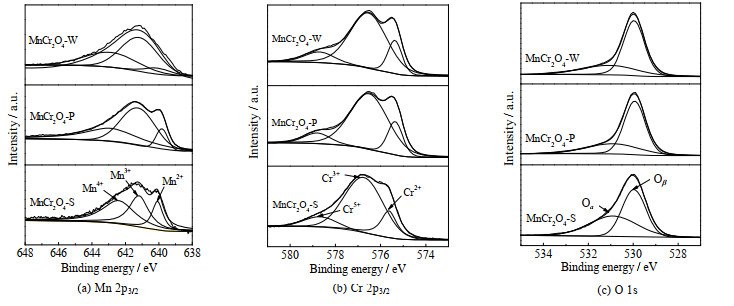
Mn 2p、Cr 2p和O 1s的XPS谱图及分峰拟合结果如图 7所示。Mn 2p3/2的XPS光谱可拟合为Mn2+(结合能为640.0~640.5 eV)、Mn3+ (640.9~641.8 eV)及Mn4+(642.2~643.3 eV)三个峰[19]。Cr 2p3/2的XPS光谱则可拟合为Cr2+(575.2~572.6 eV)、Cr3+(576.4~576.7 eV)和Cr5+ (578.3~578.7 eV)三个峰[20-22]。O 1s的XPS光谱可拟合为两个峰,结合能为531.4~531.6 eV的吸附氧Oα (如O-和O22-)和结合能为529.6~530.2 eV的晶格氧Oβ。Mn4+、Cr5+与Oα物种的富集,有利于促进低温SCR反应[23-26],表 2中列出了Mn4+、Cr5+及Oα的摩尔分数。由表可见,MnCr2O4-S表面的Mn4+、Cr5+和Oα的摩尔分数最高,分别为43.6%、10.9% 和34.5%,其中Mn4+与Oα的比例远高于MnCr2O4-W和MnCr2O4-P,这是MnCr2O4-S的SCR催化效率最高的原因之一。
|
图 7 MnCr2O4催化剂的XPS谱图及分峰拟合结果 Fig.7 XPS spectra and deconvolution results of Mn 2p3/2, Cr 2p3/2 and O 1s of MnCr2O4 catalysts |
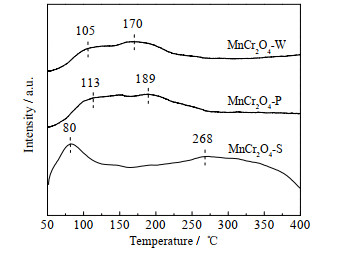
催化剂酸性是催化剂的NH3-SCR性能的一个重要影响因素,本文通过NH3程序升温脱附(NH3-TPD)测试MnCr2O4-W、MnCr2O4-P与MnCr2O4-S的表面酸性。如图 8所示,在50~250 ℃时的脱附峰归属吸附于弱酸位的NH3 (MnCr2O4-W:105、170 ℃;MnCr2O4-P:113、189 ℃;MnCr2O4-S:80 ℃)。在250~400 ℃时的脱附峰归属于吸附于强酸位的NH3 (MnCr2O4-S:268 ℃)[27-28]。可见,尽管MnCr2O4-W催化剂中含有少量Cr2O3杂质,但与MnCr2O4-P的NH3脱附峰型非常相似,二者均以弱酸位NH3脱附峰为主,没有明显的强酸位NH3脱附峰。相比之下,MnCr2O4-S的NH3脱附峰型与MnCr2O4-W、MnCr2O4-P有明显差异,其弱酸位NH3脱附温度仅为80 ℃,远低于MnCr2O4-W、MnCr2O4-P,但其在200~400 ℃时出现了一个明显的宽脱附峰,这表明MnCr2O4-S的强酸位数量要高于MnCr2O4-W和MnCr2O4-P。NH3总脱附量的顺序为MnCr2O4-W < MnCr2O4-P < MnCr2O4-S。以上结果表明,溶胶凝胶法制备的MnCr2O4-S具有数量最多以及酸性最强的酸位点,这与其表现出的最佳催化活性相一致。
|
图 8 MnCr2O4催化剂的NH3-TPD图谱 Fig.8 NH3-TPD profiles of MnCr2O4 catalysts |
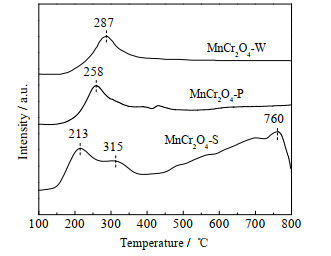
通过H2程序升温还原(H2-TPR)探究所制备催化剂的氧化还原性能,其结果如图 9所示。发现MnCr2O4-W、MnCr2O4-P与MnCr2O4-S的还原峰位置、形状有显著差异。三个样品在150~400 ℃时都有一个大而宽的还原峰,可归于Mn4+→Mn3+→Mn2+与Cr5+→Cr3+→Cr2+在此处的重叠,也即表面吸附氧物种的还原[24, 29-30]。MnCr2O4-S在760 ℃时检测到一个强还原峰信号,而MnCr2O4-W与MnCr2O4-P在此温度附近基本未检测到信号。该信号可归于Mn2+→Mn0与Cr2+→Cr0在此处的重叠,即表面晶格氧物种的还原[31]。H2总消耗量的顺序为MnCr2O4-W < MnCr2O4-P < MnCr2O4-S。这表明,溶胶凝胶法制备的MnCr2O4-S的可还原物种的量是最多的。另外,观测到MnCr2O4-S的低温段主峰的还原温度(213 ℃)略低于MnCr2O4-W (287 ℃)和MnCr2O4-P (258 ℃),说明MnCr2O4-S的可还原性最强,MnCr2O4-P次之,MnCr2O4-W最弱。这说明,MnCr2O4-S的可还原性要强于水热法与沉淀法制备的MnCr2O4。因此,MnCr2O4-S表面存在最丰富的、可还原性最强的物种,使其展现出了最佳的催化活性。
|
图 9 MnCr2O4催化剂的H2-TPR图谱 Fig.9 H2-TPR profiles of MnCr2O4 catalysts |
(1) 通过沉淀法和溶胶凝胶法均可制得较纯的尖晶石相MnCr2O4,相比之下,水热法制备的MnCr2O4中存在少量的Cr2O3杂质;
(2) MnCr2O4-S催化剂总体上脱硝性能优于MnCr2O4-W、MnCr2O4-P催化剂,在GHSV=60 000 h-1时,MnCr2O4-S的T90为169~341 ℃,其N2选择性也略高于MnCr2O4-W和MnCr2O4-P;
(3) 在本实验条件下,MnCr2O4催化剂的比表面积、微观形貌等物理性质对其脱硝活性影响较小,主要由于催化剂表面较高摩尔分数的活性物种、较强的酸性与可还原性等化学性质使得MnCr2O4-S展现出最佳的脱硝活性。
| [1] |
KIM C H, QI G, DAHLBERG K, et al. Strontium-doped perovskites rival platinum catalysts for treating NOx in simulated diesel exhaust[J]. Science, 2010, 327(5973): 1624-1627. DOI:10.1126/science.1184087 |
| [2] |
王韵杰, 张少君, 郝吉明. 中国大气污染治理: 进展·挑战·路径[J]. 环境科学研究, 2019, 32(10): 1755-1762. WANG Y J, ZHANG S J, HAO J M. Air pollution control in China: Progress, challenges and future pathways[J]. Research of Environmental Sciences, 2019, 32(10): 1755-1762. |
| [3] |
刘芳. 焦化厂焦炉烟气脱硫脱硝工艺技术分析[J]. 中国资源综合利用, 2019, 37(9): 90-92. LIU F. Technical analysis of flue gas desulfurization and denitrification process in coking plant[J]. China Resources Comprehensive Utilization, 2019, 37(9): 90-92. DOI:10.3969/j.issn.1008-9500.2019.09.028 |
| [4] |
费明明, 崔雷, 苏传好, 等. 水泥窑烟气脱硝技术现状及展望[J]. 水泥技术, 2019(3): 89-94. FEI M M, CUI L, SU C H, et al. Present situation and prospect of exhaust gas denitrification technology in cement kiln[J]. Cement Technology, 2019(3): 89-94. |
| [5] |
LIU C, CHEN L, LI J, et al. Enhancement of activity and sulfur resistance of CeO2 supported on TiO2-SiO2 for the selective catalytic reduction of NO by NH3[J]. Environmental Science & Technology, 2012, 46(11): 6182-6189. |
| [6] |
XU L, WANG C, CHANG H, et al. New insight into SO2 poisoning and regeneration of CeO2-WO3/TiO2 and V2O5-WO3/TiO2 catalysts for low-temperature NH3-SCR[J]. Environmental Science & Technology, 2018, 52(12): 7064-7071. |
| [7] |
FANG D, HE F, LIU X Q, et al. NH3-SCR performance and applicability of Mn-based spinels over TiO2 catalyst[J]. Materials Science Forum, 2018, 921: 29-34. DOI:10.4028/www.scientific.net/MSF.921.29 |
| [8] |
YANG S, QI F, XIONG S, et al. MnOx supported on Fe-Ti spinel: A novel Mn based low temperature SCR catalyst with a high N2 selectivity[J]. Applied Catalysis B: Environmental, 2016, 181: 570-580. DOI:10.1016/j.apcatb.2015.08.023 |
| [9] |
FANG D, XIE J, MEI D, et al. Effect of CuMn2O4 spinel in Cu-Mn oxide catalysts on selective catalytic reduction of NOx with NH3 at low temperature[J]. RSC Advances, 2014, 4(49): 25540-25551. DOI:10.1039/c4ra02824d |
| [10] |
LI S, WANG X, TAN S, et al. CrO3 supported on sargassum-based activated carbon as low temperature catalysts for the selective catalytic reduction of NO with NH3[J]. Fuel, 2017, 191: 511-517. DOI:10.1016/j.fuel.2016.11.095 |
| [11] |
GUO M, LIU Q, ZHAO P, et al. Promotional effect of SO2 on Cr2O3 catalysts for the marine NH3-SCR reaction[J]. Chemical Engineering Journal, 2019, 361: 830-838. DOI:10.1016/j.cej.2018.12.100 |
| [12] |
CHEN Z, YANG Q, LI H, et al. Cr-MnOx mixed-oxide catalysts for selective catalytic reduction of NOx with NH3 at low temperature[J]. Journal of Catalysis, 2010, 276(1): 56-65. DOI:10.1016/j.jcat.2010.08.016 |
| [13] |
GAO F, TANG X, YI H, et al. Improvement of activity, selectivity and H2O & SO2-tolerance of micro-mesoporous CrMn2O4 spinel catalyst for low-temperature NH3-SCR of NOx[J]. Applied Surface Science, 2019, 466: 411-424. DOI:10.1016/j.apsusc.2018.09.227 |
| [14] |
SLOCZYNSKIL J, JANAS J, MACHEJ T, et al. Catalytic activity of chromium spinels in SCR of NO with NH3[J]. Applied Catalysis B: Environmental, 2000, 24(1): 45-60. DOI:10.1016/S0926-3373(99)00093-4 |
| [15] |
WANG Y, ARANDIYAN H, LIU Y, et al. Template-free scalable synthesis of flower-like Co3-xMnxO4 spinel catalysts for toluene oxidation[J]. ChemCatChem, 2018, 10(16): 3429-3434. DOI:10.1002/cctc.201800598 |
| [16] |
WANG X, LAN Z, ZHANG K, et al. Structure-activity relationships of AMn2O4 (A = Cu and Co) spinels in selective catalytic reduction of NOx: Experimental and theoretical study[J]. The Journal of Physical Chemistry C, 2017, 121(6): 3339-3349. DOI:10.1021/acs.jpcc.6b10446 |
| [17] |
CHEN J, SHI W, YANG S, et al. Distinguished roles with various vanadium loadings of CoCr2-xVxO4 (x=0-0.20) for methane combustion[J]. The Journal of Physical Chemistry C, 2011, 115(35): 17400-17408. DOI:10.1021/jp202958b |
| [18] |
HUANG J, TONG Z, HUANG Y, et al. Selective catalytic reduction of NO with NH3 at low temperatures over iron and manganese oxides supported on mesoporous silica[J]. Applied Catalysis B: Environmental, 2008, 78(3): 309-314. |
| [19] |
THIRUPATHI B, SMIRNIPTIS P. Co-doping a metal (Cr, Fe, Co, Ni, Cu, Zn, Ce, and Zr) on Mn/TiO2 catalyst and its effect on the selective reduction of NO with NH3 at low-temperatures[J]. Applied Catalysis B: Environmental, 2011, 110: 195-206. DOI:10.1016/j.apcatb.2011.09.001 |
| [20] |
CHEN Z, YANG Q, LI H, et al. Cr-MnOx mixed-oxide catalysts for selective catalytic reduction of NOx with NH3 at low temperature[J]. Journal of Catalysis, 2010, 276(1): 56-65. DOI:10.1016/j.jcat.2010.08.016 |
| [21] |
RUSSO N, FINO D, GUIDO S, et al. Studies on the redox properties of chromite perovskite catalysts for soot combustion[J]. Journal of Catalysis, 2005, 229(2): 459-469. DOI:10.1016/j.jcat.2004.11.025 |
| [22] |
BIESINGER M, PAYNE B, GROSBENOR A, et al. Resolving surface chemical states in XPS analysis of first row transition metals, oxides and hydroxides: Cr, Mn, Fe, Co and Ni[J]. Applied Surface Science, 2011, 257(7): 2717-2730. DOI:10.1016/j.apsusc.2010.10.051 |
| [23] |
ZHANG L, SHI L, HUANG L, et al. Rational design of high-performance DeNOx catalysts based on MnxCo3-xO4 nanocages derived from metal-organic frameworks[J]. ACS Catalysis, 2014, 4(6): 1753-1763. DOI:10.1021/cs401185c |
| [24] |
FANG C, ZHANG D, CAI S, et al. Low-temperature selective catalytic reduction of NO with NH3 over nanoflaky MnOx on carbon nanotubes in situ prepared via a chemical bath deposition route[J]. Nanoscale, 2013, 5(19): 9199-9207. DOI:10.1039/c3nr02631k |
| [25] |
KIJLSTRAL W S, BRANDS D, SMIT H, et al. Mechanism of the selective catalytic reduction of NO with NH3 over MnOx/Al2O3 Ⅱ. Reactivity of adsorbed NH3 and NO complexes[J]. Journal of Catalysis, 1997, 1(171): 219-230. |
| [26] |
HU H, CAI S, LI H, et al. In situ DRIFTs investigation of the low-temperature reaction mechanism over Mn-doped Co3O4 for the selective catalytic reduction of NOx with NH3[J]. The Journal of Physical Chemistry C, 2015, 119(40): 22924-22933. DOI:10.1021/acs.jpcc.5b06057 |
| [27] |
WAN Y, ZHAO W, TANG Y, et al. Ni-Mn bi-metal oxide catalysts for the low temperature SCR removal of NO with NH3[J]. Applied Catalysis B: Environmental, 2014, 148-149: 114-122. DOI:10.1016/j.apcatb.2013.10.049 |
| [28] |
JIN R, LIU Y, WU Z, et al. Low-temperature selective catalytic reduction of NO with NH3 over MnCe oxides supported on TiO2 and Al2O3: A comparative study[J]. Chemosphere, 2010, 78(9): 1160-1166. DOI:10.1016/j.chemosphere.2009.11.049 |
| [29] |
KIM D, IHM S. Application of spinel-type cobalt chromite as a novel catalyst for combustion of chlorinated organic pollutants[J]. Environmental Science & Technology, 2001, 35(1): 222-226. |
| [30] |
ZHAO X, HUANG L, LI H, et al. Promotional effects of zirconium doped CeVO4 for the low-temperature selective catalytic reduction of NOx with NH3[J]. Applied Catalysis B: Environmental, 2016, 183: 260-281. |
| [31] |
LIAN Z, LIU F, HE H. Enhanced activity of Ti-modified V2O5/CeO2 catalyst for the selective catalytic reduction of NOx with NH3[J]. Industrial & Engineering Chemistry Research, 2014, 53(50): 19506-19511. |




