在化工生产过程中,通常会产生一些有机废液,这些废液成分复杂且难以处理。目前,最常规的处理方法是将废液运到城市危废处理中心直接焚烧。然而,在废液量大、燃烧热值高、有毒物质含量低的情况下,将废液外运至危废处理中心不仅处理费用高,而且损失了废液所含的热量。某环氧氯丙烷生产企业,在生产工艺中产生1200 kg·h-1的废液,其主要成分为甘油、丙烯醛、甲苯以及NaCl等盐类。如果该废液在焚烧炉内直接燃烧,则废液中的盐会在燃烧过程中高温气化,气态的盐遇冷后会沉积在余热锅炉水冷壁管和各受热面上,堵塞烟道并对受热面造成严重的腐蚀[1-5]。
事实上在许多化工工艺中都会用到盐,如何处理含盐有机废液是个具有一定普遍性的问题。国内外相关研究人员提出了多种处理方法。Olazar等[6]用流化床技术焚烧含盐废液,利用流化床低床层温度的优势,减少废液中碱金属盐的蒸发。这种方法虽能有效减少碱金属盐对余热锅炉受热面的危害,但是过低的焚烧温度不足以充分分解废液中有毒物质,会增加对环境的二次污染[7]。Bhattacharya等[8]通过向床料中添加石灰石、高岭土等添加剂,使熔点较低的碱金属盐转化为高熔点的共晶体,有效防止了盐的熔融和蒸发。除了焚烧法之外,还有微生物法、磁分离法和离子交换法等处理方式[9-11]。但这些方法多处于研究阶段,由于技术和成本等多种原因还没有真正实现工业化应用。
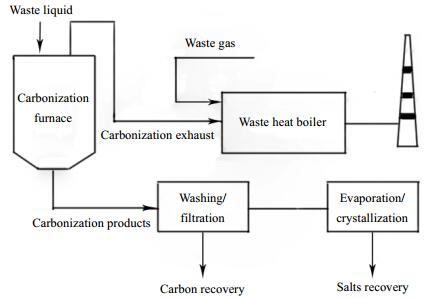
针对该环氧氯丙烷生产企业废液量大、废液热值高、有毒物质含量低、含盐量高等特点,笔者所在团队提出了将含盐有机废液在低于480℃下进行低温炭化的处理方案,具体工艺流程如图 1所示。废液在炭化炉中低温炭化,所产生的炭化尾气(含多种有机物)送入现有的焚烧炉内燃烧,炭化后的固体产物经洗涤过滤后回收炭,经蒸发结晶回收盐。该方案既可利用废液的焚烧热,防止废液中的盐熔融和蒸发对余热锅炉产生危害,又可回收废盐再利用,具有环境保护和综合利用双重效果。
|
图 1 含盐废液炭化处理流程 Fig.1 Carbonization process of the salty liquid wastes |
本文采用热重-红外(TG-FTIR)联用的方法对甘油法制备环氧氯丙烷所产生的废液进行热解特性研究,探究升温速率对热解的影响并运用热分析动力学对废液的热解过程进行分析,获得其热解所需的活化能并建立相应的动力学方程,为炭化炉的数值计算提供基本参数。在炭化试验台上对废液进行热解试验,获得废液炭化的最佳温度与时间,并对炭化后的产物进行微观分析。研究结果可为炭化炉的设计提供重要依据。
2 实验材料和方法 2.1 实验材料实验材料取自某化工厂采用甘油法生产环氧氯丙烷所排放的废液,外观为棕红色黏稠状液体,主要成分是甘油、丙烯醛、甲苯以及NaCl等盐类。
2.2 热重分析使用德国耐驰仪器制造有限公司的STA 449 F5型热重分析仪对样品进行分析。样品质量为(20±0.1) mg,采用氮气(纯度99.99%)作为载气气流,流量为20 mL·min-1。分别以5、10和15℃·min-1的升温速率对样品加热至700℃。
2.3 红外分析利用德国BRUKER公司的VERTEX 70型傅立叶红外光谱分析仪(FT-IR)对热解过程中析出的气相产物进行分析。
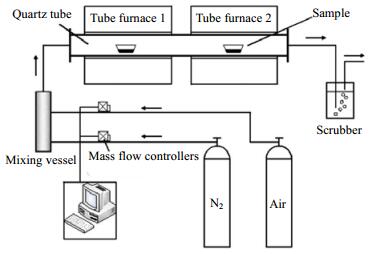
2.4 炭化实验炭化实验在炭化试验台上进行,炭化试验台系统如图 2所示。加热主体由两段独立控温的管式炉组成,可同时在两个不同温度下对样品进行加热。氮气(纯度99.99%)通过流量控制器后进入石英管,流量为75 mL·min-1,石英管末端布置有吸收瓶,用来吸收尾气。称取2 g废液,置于灰皿中,将灰皿快速推入已升至预设温度的石英管试验段。试验温度分别为280,300,320,340,360,380,480和580℃。其中,在380℃及以上温度下对废液分别炭化0.5、1和1.5 h后取出灰皿并冷却称重,计算产炭率。其余温度主要是观察废液的形态变化,每隔10 min观察一次。
|
图 2 炭化试验系统 Fig.2 Schematic diagram of the carbonization system |
采用日本Hitachi公司生产的SU8010型场发射扫描电子显微镜观察炭化产物的微观结构;美国EDAX公司的TEAM Apollo XL型能谱分析仪对炭化产物的组成元素进行分析;德国BRUKER公司的D2 PHASER型X-射线衍射仪对炭化产物进行物相分析,扫描范围为10°~80°。
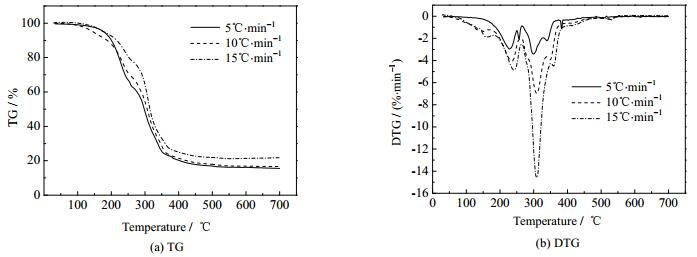
3 实验结果与讨论 3.1 废液热解过程分析图 3为样品在5、10和15℃·min-1的升温速率下热失重(TG)曲线与热失重速率(DTG)曲线。由图可见,在不同升温速率下,废液的失重趋势基本一致,但失重速率有较大差异。以15℃·min-1的TG、DTG曲线为例,该有机废液的热解过程主要可以分为4个阶段。结合图 5气相析出物的测定结果,对热解过程分析如下:
|
图 3 不同升温速率下废液的TG与DTG曲线 Fig.3 TG and DTG curves of liquid wastes under different heating rates |
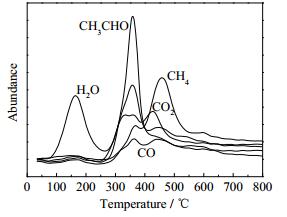
|
图 5 热解过程中析出的气相组分 Fig.5 Volatiles obtained in the pyrolysis process |
第一阶段:从室温到110℃左右,该阶段下TG曲线基本不变,说明废液中游离水含量较少。
第二阶段:从110到260℃,DTG曲线出现一个较大的波动峰,在230℃左右到达顶峰。该阶段的温度较低,废液中的丙三醇发生脱水反应,生成多种羰基化合物,水分的析出导致该阶段质量下降。
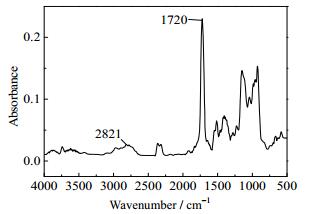
第三阶段:从260到380℃左右,这是整条TG曲线下降幅度最大的一个阶段。其中,在310℃时下降速率到达最大。该阶段的温度较高,反应剧烈,析出大量气体。由红外谱图(图 4)可以看出,在2821 cm-1处有明显的特征峰,这是醛基中C-H键伸缩振动和C-H键弯曲振动所导致的,而1720 cm-1处的特征峰也进一步证明了醛基的存在,结合其余特征峰,判断主要的气相析出物为乙醛。该阶段析出的气相产物还包括水分与少量甲烷、一氧化碳、二氧化碳。由此推断在该阶段中,脱水反应后废液中部分羰基化合物在高温下发生了质子转移,导致乙醛的产生,另一部分羰基化合物在高温下继续脱水,生成其他醛类。甲烷与一氧化碳的存在则说明该阶段下废液中的醛基化合物已逐渐开始分解。二氧化碳的析出规律与一氧化碳类似,主要是由有机物中含氧官能团的热解所导致的。
|
图 4 第三阶段主要气相析出物的红外谱图 Fig.4 FT-IR spectra of main volatiles from the third stage |
第四阶段:当温度高于380℃后,质量变化缓慢。该阶段下醛基化合物大量分解,产生甲烷等小分子气体。在温度进一步升高后C-H键开始断裂,产物表面的官能团数量进一步减少,结构趋于稳定,逐渐向石墨化发展[12]。
3.2 升温速率对废液热解的影响从图 3(a)可以看出,在3种不同升温速率下,废液的失重趋势基本一致。但也可以发现,随着升温速率的增大,最终产物的质量也有所提高(从5℃·min-1时的15.6%升至15℃·min-1时的21.7%)。结合DTG曲线,当升温速率为5℃·min-1时,在255与382℃处有两个较小的波动峰,而当升温速率为10与15℃·min-1时,这两个波动峰消失了。这表明较大的升温速率抑制了某些中间反应的发生,不利于一些挥发份的析出。此外,不同的升温速率会影响波动峰出现的位置及其最大峰值。结合表 1可发现,在第二阶段与第三阶段中,随着升温速率的提高,挥发份析出时的峰值温度也随之升高。
|
|
表 1 不同升温速率下废液热解数据 Table 1 Pyrolysis results of liquid wastes at different heating rates |
通过热分析动力学获得描述反应的“动力学三因子”,即模型函数f (α),指前因子A以及活化能E。反应速率可由微分形式表达:
| $ \frac{{{\rm{d}}\alpha }}{{{\rm{d}}t}} = kf(\alpha ) $ | (1) |
其中变化率α可根据热重曲线求得:
| $\alpha = \frac{{{m_0} - m}}{{{m_0} - {m_\infty }}}$ | (2) |
式中:m0代表初始质量,m代表t时刻的质量,m∞为最终质量。
在大多数情况下,Arrhenius公式可用来描述反应速率常数k与热力学温度T之间的关系:
| $ k = A{e^{ - E/RT}} $ | (3) |
其中:E为反应的活化能;A为指前因子。
将式(3)代入式(1)中,可得:
| $\frac{{{\rm{d}}\alpha }}{{{\rm{d}}t}} = A{e^{ - E/RT}}f\left( \alpha \right)$ | (4) |
令升温速率为β,β = dT/dt,则式(4)可改写为:
| $\frac{{{\rm{d}}\alpha }}{{{\rm{d}}T}} = \frac{A}{\beta }{e^{ - E/RT}}f\left( \alpha \right)$ | (5) |
使用Coats-Redfern方法对式(5)进行积分,简化后可得:
| $\ln \frac{{g\left( \alpha \right)}}{{{T^2}}} = \ln \frac{{AR}}{{\beta E}} - \frac{E}{{RT}}$ | (6) |
其中:
| $g\left( \alpha \right) = \int_0^a {{\rm{d}}\alpha /f(\alpha )} $ | (7) |
利用最概然机理函数的方法,以ln g(α)/T2为纵坐标,-1/T为横坐标作图,选择能使拟合直线线性度最好的g(α)作为机理函数,则E/R为斜率,ln AR/βE为截距,从而可以求得活化能E和指前因子A。
对于一般的热解反应,f (α)可由下式表达[13]:
| $f(\alpha ) = {(1 - \alpha )^n}$ | (8) |
根据前文分析,有机废液热解主要发生在第二阶段和第三阶段。无论是单步反应还是多步反应,若存在多个DTG失重峰,不同峰之间往往存在着不同的反应机理[14]。因此,对第二阶段和第三阶段分别进行动力学拟合,计算拟合曲线值和真实值之间的标准差,标准差SD定义为:
| ${\rm{SD}} = \sqrt {\frac{{\sum\limits_{i = 1}^n {{{\left| {G{{(\alpha )}_{{\rm{ce}}}} - G{{(\alpha )}_{{\rm{ni}}}}} \right|}^2}} }}{n}} $ | (9) |
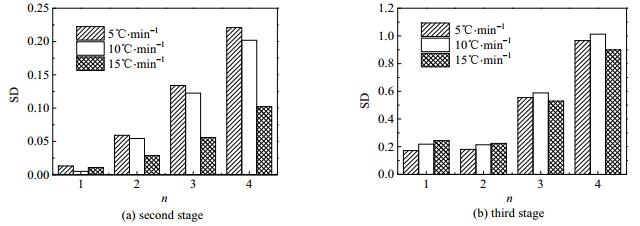
式中:G(α)ce为真实值,G(α)ni为拟合曲线值。结果如图 6所示。从图中可以看出,在第二阶段,选取n =1时的拟合曲线标准差最小。在第三阶段,选取n = 2时的拟合曲线标准差最小。因此,第二阶段的热解过程符合一级动力学模式,最适合的机理函数为f(α) = (1-α),说明该阶段的热解速率与反应物的浓度呈正比。第三阶段的热解过程符合二级动力学模式,最适合的机理函数为f(α) = (1-α)2,热解速率与反应物浓度的二次方成正比。
|
图 6 不同反应级数下拟合曲线标准差 Fig.6 Standard deviations of the fitting curves for different reaction orders |
将不同阶段下的变化率α分别代入所选择的机理函数,以ln g(α)/T2为纵坐标,-1/T为横坐标作图并对其进行拟合,根据拟合方程可得斜率E/R,截距ln AR/(βE),从而求得活化能E和指前因子A。
由表 2可得,各阶段拟合的R2均在0.98以上,说明拟合效果良好,所选用的反应机理函数合理。同时可以看出,阶段二的反应活化能明显低于阶段三的反应活化能,这是因为阶段二主要发生脱水反应。而在第三阶段,有机物开始交联并发生质子转移反应,所需的活化能较大。此外,随着升温速率的提高,相同阶段的反应活化能上升,说明升温速率的提高不利于热解反应的进行,也为DTG曲线中失重峰出现的位置随升温速率的升高而向高温区发生轻微偏移这一现象提供了理论依据。
|
|
表 2 不同升温速率下废液热解数据 Table 2 Pyrolysis results of liquid wastes at different heating rates |
废液在280~380℃下炭化实验结果见图 7。随着炭化温度的升高,废液的颜色逐渐加深,黏稠度降低,表面裂纹增多。具体表现为当温度为280℃时,废液经过30 min后仍呈棕红色黏稠状液体,表面仅产生少量气孔。当温度为300℃时,废液在热解过程中产生较多气泡,经过30 min后,废液已呈固体状。随着温度的进一步提高,废液固化所需的时间缩短,表面的气孔增多直至出现裂纹,颜色也逐渐由320℃时的淡黄色向黑色转变。继续提高温度至360℃后,产物呈现出黑色,表面裂纹状态与340℃时一致,但与380℃时的状态仍有一定差异,从图中可以明显看到,380℃时的炭化产物呈片状,裂纹也更大。

|
图 7 废液在280~380℃下炭化30 min后的表面形态 Fig.7 Surface morphology of liquid waste after carbonization for 30 min at 280~380℃ |
产炭率是指经炭化后剩余产物的质量占原材料质量的百分比。废液在不同温度和不同时间下的产炭率如表 3所示。从表中可看出,当炭化温度为380℃时,随着炭化时间的增加,产炭率由0.5 h时的23.1%下降至1.5 h的18.2%,下降幅度达4.9%。当炭化温度分别为480和580℃时,产炭率随着炭化时间的提升也有微小的下降。这说明在同一炭化温度下,炭化时间越长,产炭率越低。此外,在相同的炭化时间下,随着炭化温度的上升,产炭率下降,这与Lua[15]和林珈羽[16]的研究结果一致,具体表现为当炭化时间为1.5 h时,380℃下的产炭率为18.2%,而480与580℃下的产炭率则分别为16.1%与15.6%。
|
|
表 3 不同温度和时间下废液产炭率 Table 3 Char yields of liquid wastes under different temperatures and times |
废液在580℃下炭化1.5 h后的剩余产物呈片状,质地较脆,可轻易从灰皿中剥离。利用扫描电镜对其进行微观形貌分析,由图 8可见,炭化产物表面存在大量的片状结晶体,且在片与片之间夹杂着一些不规则的絮状物。根据絮状物的位置选取图 8所示的区域1和区域2进行EDS分析,结果如表 4所示。区域1的主要组成元素为O、Na、P、Cl,没有检测到C元素,由此推断出产物中的片状晶体为废液在热解过程中析出的盐。

|
图 8 炭化产物的微观表面形貌 Fig.8 SEM micrographs of char surface |
|
|
表 4 炭化产物的EDS分析(At.%) Table 4 Results of EDS analysis of char (At.%) |
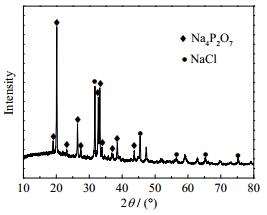
在所选的两个区域中,Na、P、O的原子数比均为3:1:4左右,且P元素的含量远高于Cl元素,说明产物中的盐不仅仅以NaCl的形式存在,还可能存在Na4P2O7或者Na3PO4。利用XRD对产物中的晶相进行检测,结果如图 9所示,经谱图对比,晶相的主要成分为Na4P2O7和NaCl。XRD并没有检测出明显的石墨峰,说明产物中的碳主要以无定形态存在。
|
图 9 炭化产物的XRD分析 Fig.9 XRD patterns of char |
由上述分析可得,该炭化产物为脆性片状物,包含Na4P2O7、NaCl与无定形碳三部分,经简单破碎后可通过洗涤过滤、蒸发结晶等方法分别回收利用。分离的Na4P2O7和NaCl经提纯后可作为工业用盐,剩下的无定形碳可作为黑色染料,用于制造油墨、油漆,或经活化处理后作为吸附剂使用。
4 结论利用热重-红外联用的方法对甘油法制环氧氯丙烷所产生的含盐废液的热解特性进行了研究,并对炭化产物进行详细表征,得到以下结论:
(1) 该有机废液发生热解反应的主要温度区间为110~380℃,在110~260℃内主要发生脱水反应,在260~380℃内发生质子转移反应,热解气的主要成分为乙醛、甲烷。
(2) 热分析动力学研究表明:热解的第二阶段符合一级动力学模式,第三阶段符合二级动力学模式。获得了两个阶段的活化能与指前因子数值,可为炭化炉的数值模拟提供基础参数。
(3) 在炭化温度为280℃时,即使经过1 h以上的时间,废液仍然是黏稠液体,随着温度不断提高,从液体变为固体的时间不断缩短。在380℃时,废液经5 min左右即变硬,且表面为深黑色。TG曲线也表明,样品剩余质量在380℃之后已基本稳定,表明炭化已基本完成。综合考虑各个因素,炭化炉设计温度应高于380℃。但过高的温度会增加炭化炉设计难度和成本,建议不高于480℃。
(4) 炭化后的固态产物主要为氯化钠、焦磷酸钠以及一些无定形碳。可通过洗涤过滤、蒸发结晶的方法分别回收利用。
符号说明:
|
|
| [1] | Chatha S S, Sidhu H S, Sidhu B S. High temperature hot corrosion behavior of NiCr and Cr3C2-NiCr coatings on T91 boiler steel in an aggressive environment at 750℃[J]. Surface & Coatings Technology, 2012, 206(19-20): 3839-3850. |
| [2] | Lith S C V, Frandsen F J, Montgonery M, et al. Lab-scale investigation of deposit-induced chlorine corrosion of superheater materials under simulated biomass-firing conditions. Part 1:exposure at 560℃[J]. Energy & Fuels, 2009, 23(7): 3457-3468. |
| [3] | WANG Yong-zheng(王永征), ZHANG Ke(张科), JIANG Lei(姜磊), et al. Study on sulfur-chlorine synergistic corrosion in biomass and coal co-firing(生物质混煤燃烧过程中硫氯协同腐蚀特性研究)[J]. Journal of Chemical Engineering of Chinese Universities(高校化学工程学报), 2015, 29(6): 1422-1429. DOI:10.3969/j.issn.1003-9015.2015.06.020. |
| [4] | MU Lin(穆林), ZHAO Liang(赵亮), YIN Hong-chao(尹洪超). Fouling and slagging characteristics in wastewater incinerator(化工废液焚烧炉内积灰结渣特性)[J]. CIESC Journal(化工学报), 2012, 63(11): 278-284. |
| [5] | Lehmusto J. High temperature corrosion of superheater steels by KCl and K2CO3 under dry and wet conditions[J]. Fuel Processing Technology, 2012, 104(6): 253-264. |
| [6] | Olazar M, Aguado R, Sanchez J L, et al. Thermal processing of straw black liquor in fluidized and spouted bed[J]. Energy & Fuels, 2002, 16(6): 1417-1424. |
| [7] | Eyk P J V, Kosminski A, Ashman P J. Control of agglomeration and defluidization during fluidized-bed combustion of south Australian low-rank coals[J]. Energy & Fuels, 2011, 26(1): 118-129. |
| [8] | Bhattacharya S P, Harttig M. Control of agglomeration and defluidization burning high-alkali, high-sulfur lignites in a small fluidized bed combustor-effect of additive size and type, and the role of calcium[J]. Energy & Fuels, 2003, 17(4): 1014-1021. |
| [9] | Svoboda J. A realistic description of the process of high-gradient magnetic separation[J]. Minerals Engineering, 2001, 14(11): 1493-1503. DOI:10.1016/S0892-6875(01)00162-5. |
| [10] | Lu J, Ma Y, Liu Y, et al. Treatment of hypersaline wastewater by a combined neutralization-precipitation with ABR-SBR technique[J]. Desalination, 2011, 277(1): 321-324. |
| [11] | Kazemimoghadam M. New nanopore zeolite membranes for water treatment[J]. Desalination, 2010, 251(1-3): 176-180. DOI:10.1016/j.desal.2009.11.036. |
| [12] | King P, Rakesh N, Lahari S B, et al. Biosorption of zinc onto Syzygium cumini L.:equilibrium and kinetic studies[J]. Chemical Engineering Journal, 2008, 144(2): 181-187. DOI:10.1016/j.cej.2008.01.019. |
| [13] | HU Rong-zu(胡荣祖). Thermal analysis kinetics(热分析动力学)[M].Beijing(北京): Science Press(科学出版社), 2008. |
| [14] | NING Xun-an(宁寻安), ZHANG Ning(张凝), LIU Jing-yong(刘敬勇), et al. The co-combustion characteristics of coal and paper mill sludge and its kinetics(造纸污泥混煤燃烧特性及动力学研究)[J]. Acta Scientiae Circumstantiae(环境科学学报), 2011, 31(7): 1486-1492. |
| [15] | LUA A C, TING Y. Effects of vacuum pyrolysis conditions on the characteristics of activated carbons derived from pistachio-nut shells[J]. Journal of Colloid And Interface Science, 2004, 276(2): 364-372. DOI:10.1016/j.jcis.2004.03.071. |
| [16] | LIN Jia-yu(林珈羽), ZHANG Yue(张越), LIU Yuan(刘沅), et al. Structure and properties of biochar under different materials and carbonization temperatures(不同原料和炭化温度下制备的生物炭结构及性质)[J]. Chinese Journal of Environmental Engineering(环境工程学报), 2016, 10(6): 438-444. |




