羊毛脂是附着在羊毛上的一种分泌油脂,主要由胆固醇、羊毛甾醇、高级脂肪醇等醇类物质与大约等量的高级脂肪酸组成,其中胆固醇的含量可达12 %以上[1]。胆固醇在化妆品、医药卫生和液晶材料等领域有着十分广泛的应用[2-5],而天然羊毛脂资源丰富,所以,通过天然羊毛脂皂化分解提取胆固醇产品,具有很好的应用价值。
羊毛脂和普通油脂相比性质更加稳定,只能在强碱性条件下皂化分解。Kohji等[6]选择用二价金属(氢)氧化物直接参与皂化得到二价金属皂,但由于金属盐和二价氢氧化物的溶解度低,反应需高温、高压条件下在釜式反应器中进行,实验条件苛刻;毛法根等[7]在碱水环境中对羊毛脂进行皂化,由于生成的羊毛脂酸盐产生乳化现象,导致皂化收率低于90 %;也有部分研究选择在碱水环境下,通过加入某些助剂优化反应,比如英国Marchon公司在其专利[8]中提到加入二甲基苯磺酸钠作为助剂,能够很好地解决乳化过程产生的泡沫;Robinson等[9]则在皂化过程中加入三辛基甲基氯化铵作为相转移催化剂来提高皂化速率,最终羊毛醇的收率为49 %。
目前工业生产上大多采用釜式反应器,以低级醇作为溶剂在低温低压的温和条件下,反应6~8 h达到较高的皂化收率[10],但存在反应时间长、生产效率低等问题。管式反应器作为一种新兴反应设备,具有传热和传质效率高的优势,能提高反应速度,且由于在线反应量较小而使得反应过程安全可控[11-12]。
本研究采用管式反应器完成羊毛脂皂化过程,对整套实验装置进行了设计,并对反应温度、反应压力、停留时间、溶剂和碱用量等关键影响因素进行了探究。此外,还将皂化副产物提纯得到的羊毛醇和羊毛酸[13-14]通过酯化反应,再经过脱色脱酸得到精制的羊毛脂产品,该产品具有一定市场价值,可作为联产产物。在此过程中,考虑到国内外有关羊毛醇和羊毛酸合成羊毛脂的工艺研究鲜有报道,参考了其他高级脂肪酸酯的合成方法[15-16],对酯化合成羊毛脂工艺进行了研究。
2 实验部分 2.1 主要试剂羊毛脂为工业品,羊毛甾醇为化妆品级,均由浙江花园生物高科股份有限公司提供;氢氧化钾、无水乙醇、甲苯、盐酸、乙醚、环己烷、氯化钙均为分析纯,过氧化氢购自国药集团化学试剂有限公司,质量分数为30 %;重铬酸钾、氯化钴、三氯化铁、氯铂酸钾、碳酸钾、九水偏硅酸钠均为分析纯,购自上海麦克林生化科技有限公司。
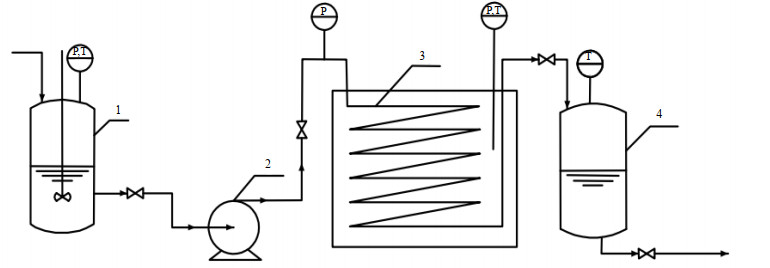
2.2 羊毛脂管道化皂化 2.2.1 实验装置实验装置如图 1所示[17]。进料釜1用来混合反应物料;微量计量螺杆泵2 (RV0.43,上海闪驰泵业有限公司)用来输送反应物料到反应管道3,管道全长130 m、内径为4 mm、体积为316 L、不锈钢材质、呈螺旋排管状;油浴锅(HH-S,金坛市杰瑞尔电器有限公司) 用来加热反应管道。管式反应器末端连有缓冲接收釜4 (250 mL,30 MPa)。
|
图 1 羊毛脂管道化皂化实验装置 Fig.1 Experimental setup of pipeline saponification of lanolin 1. feed tank 2. micro metering screw pump 3. tubular reactor 4. buffer receiving autoclave |
向管道内通入一定压力氮气,保证进料过程稳定。称取无水乙醇、羊毛脂和氢氧化钾,在热水浴下充分溶解混合后,作为反应物料通过微量计量螺杆泵送入管式反应器内部,管式反应器在油浴锅中加热。进料速度通过微量计量螺杆泵控制,出料速度通过出口阀门开度控制,待反应完全稳定后从缓冲接收釜出口取样分析。
2.2.3 分析方法通过酸值测定和分解产物中胆固醇含量的检测来判断皂化反应收率,即羊毛脂的分解程度。首先将产物进行预处理。取产物约10 g于圆底烧瓶中,加甲苯50 mL、盐酸10 mL和少量水,在75 ℃水浴条件下搅拌30 min使其酸化完全。取出,倒入分液漏斗中,用大约3倍的样品量的75 ℃热水水洗多次,至水相呈中性,以使样品中不含钙离子。弃去水相,有机相则用真空旋蒸法除去甲苯。
然后进行产物酸值测定[18]。称取预处理后样品约1 g置于锥形瓶中,加无水乙醇与乙醚以体积比1:1配成的混合液50 mL (临用前加酚酞指示液1.0 mL,用氢氧化钠滴定液调至微显粉红色),振摇至完全溶解,用氢氧化钠滴定液滴定。由式(1)计算供试品酸值:
| $ 供试品酸值=\frac{56.1\times V\times c}{m}$ | (1) |
式中:供试品酸值,mg·g-1;V为氢氧化钠滴定液体积,mL;c为氢氧化钠滴定液浓度,mol·L-1;m为供试品质量,g。
再进行产物胆固醇含量检测[18-19]。配制一定浓度的胆固醇标准品溶液和供试品溶液,用液相色谱检测,根据色谱图面积按照外标法计算胆固醇质量分数。色谱条件如下:C18色谱柱(4.6mm × 250mm),紫外检测器检测波长为205 nm,流动相为甲醇,柱温为35 ℃,进样量为20 μL。
2.3 羊毛脂合成工业羊毛脂的皂化产物经过钙化沉淀、上清液提取、钙皂转化等一系列分离操作可得到胆固醇、羊毛酸和羊毛醇等产品。将其中羊毛酸和羊毛醇经过酯化反应可生成羊毛脂。羊毛脂作为产品出售时,其色度和酸值是判断产品是否合格的重要指标,故需要对羊毛脂进行脱色脱酸处理。
2.3.1 实验步骤称取羊毛酸、羊毛醇、羊毛甾醇和氢氧化钾于三口烧瓶中,打开磁力搅拌和加热装置,设定温度为70 ℃,待原料完全熔化后,打开隔膜泵抽至真空并持续30 min,将体系内残留的溶剂、水、空气抽除,升温至设定温度下开始反应。
2.3.2 色度测定方法羊毛脂的色度采用加德纳色度法判断,这是一种用于判断黄色深浅的一维度量方法,通常需先配制加德纳色度系列标准溶液,再将得到的羊毛脂处理后进行颜色比对。
(1) 加德纳色标的配制
用到的试剂包括盐酸、重铬酸钾、氯化钴、三氯化铁和氯铂酸钾。将盐酸与蒸馏水按照体积比1:17混合得到稀盐酸溶液,将氯化钴、三氯化铁分别与稀盐酸按照质量比1:3、5:1.2混合得到氯化钴溶液和三氯化铁溶液,将790 mg氯铂酸钾用盐酸溶解后配制成100 mL溶液,再将氯铂酸钾溶液按一定浓度梯度稀释得到加德纳1~8号色标,将三氯化铁与氯化钴溶液也按照一定浓度梯度稀释,得到加德纳9~18号色标,色标应放置在避光处,每半年用参比溶液校核一次。
(2) 色度测定
先将羊毛脂快速加热熔化并导入比色管中,然后与加德纳色标溶液的比色管并列放置,在白天的散射光下从侧面目测,比较颜色,以试样溶液颜色相同或最接近的色标号码表示试样的颜色。为了更精确地对颜色进行判断,当颜色在7和8之间时,则可表示为7、7+、8-、8等。
2.4 羊毛脂脱色与脱酸根据杭州洛神科技有限公司制定的Q/LS 001-2015企业标准,羊毛脂产品的色度指标应小于8、酸值小于1 mg·g-1。合成羊毛脂先用质量分数为30 %的过氧化氢溶液脱色,脱色后酸值上升至10 mg·g-1左右;再采用质量分数为2 %的碳酸钾除酸,然后以2倍的异丙醇溶液(体积分数为30 %)为溶剂,反应1 h。加入少量九水偏硅酸钠,静置分层,除去水层,水洗3次后测得产品的酸值为0.8 mg·g-1,达到要求。
3 结果与讨论 3.1 皂化过程影响因素探究 3.1.1 反应机理羊毛脂性质比其他脂类物质更加稳定,皂化生成的羊毛酸、羊毛醇中具有长碳链结构,导致其在醇溶液中的溶解度降低,也会产生乳化现象,从而对传质过程产生干扰、影响反应收率。图 2为皂化反应机理[20-21],反应分为加成、消去两步进行。第一步是亲核加成反应,强亲核试剂氢氧根离子进攻正电性的羰基碳原子,形成带负电的中间体,该步骤是两步反应速度的控制步骤;第二步是脱除R2O-基团后生成羊毛酸盐和醇。

|
图 2 皂化过程反应机理 Fig.2 Mechanism of saponification reaction |
为了得到较优的反应工艺条件,对温度、压力、进料速度、溶剂和碱的用量等因素进行探究。
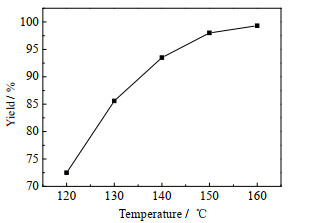
3.1.2 反应温度与反应压力温度是影响反应速度的重要因素之一,提高反应温度能显著提升反应速度。当原料乙醇、羊毛脂、氢氧化钾质量比为3:1:0.11、反应压力为1.40 MPa、进料速度为2.5 L·h-1时,不同温度下反应收率如图 3所示。
|
图 3 温度对反应的影响 Fig.3 Effect of temperature on reaction |
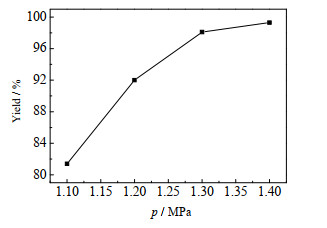
由图可见,羊毛脂皂化反应收率随温度升高而逐渐提高,原因有:①反应温度越高,皂化速率越快;②羊毛脂微溶于冷乙醇,易溶于热乙醇[22],而温度升高能降低反应液黏度,增强其在管道中的流动性;③温度升高可以有效解决皂化产物产生的乳化现象,减少传质阻力带来的影响。但是,过高的温度会造成能源损耗、增加经济成本,且伴随高温产生的高压也会增加反应器的压力负担。最终反应温度优化结果为160 ℃,在此温度下,保持其他条件不变,不同压力p下的反应收率如图 4所示。
|
图 4 160℃下压力对反应的影响 Fig.4 Effect of pressure on reaction at 160 ℃ |
当管道内压力高于反应温度下反应体系的泡点压力时,可认为此时反应体系为液相,羊毛脂和碱都溶解在液相中反应,此时反应过程传质阻力小、皂化速率更快、收率更高;当压力低于该值时,部分乙醇溶剂处于气相,而气相中皂化收率受传质效果影响会有明显下降。160 ℃时乙醇的饱和蒸气压为1.27 MPa,而此时反应尚未达到最优反应条件,这是因为其他低沸点成分的存在,导致乙醇实际分压低于1.27 MPa。最终反应压力优化结果为1.40 MPa。
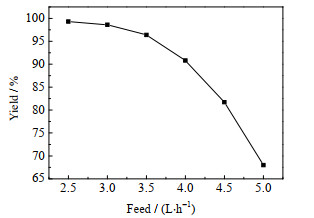
3.1.3 停留时间当管式反应器长度一定时,进料速度越慢,原料在管路中的停留时间越长,收率越高,但也会降低单位时间内的产能,所以,在确保高收率情况下,进料速度越快越好。在最优反应温度和压力、原料投料比保持不变条件下,不同进料速度的反应结果如图 5所示。由图可见,随进料速度降低,即反应物在管道内停留时间变长,反应收率越来越高。而进料速度过慢也会导致羊毛脂在其他未做加热处理的仪器设备中析出,尤其在进料泵中易发生堵塞现象。最终进料速度优化结果为2.5 L·h-1,该进料速度下羊毛脂在管道中的停留时间为40 min。
|
图 5 进料速度对反应的影响 Fig.5 Effect of feed rate on reaction |
高温下羊毛脂和碱在低级醇中的溶解度更高[22]。考虑到乙醇具有来源广泛、价格低廉、毒性低等优点,选择乙醇作为反应溶剂。
在后续的皂化产物分离过程中,需向皂化反应生成的羊毛酸盐中加入氯化钙以便钙化形成羊毛酸钙沉淀。实验研究发现,羊毛酸钾比羊毛酸钠、氯化钙的反应活性更好,更易生成沉淀,有利于后续分离,故选择氢氧化钾作为皂化反应原料碱。
反应过程中加入的乙醇量越多,溶解的羊毛脂和氢氧化钾的量越多、溶液黏度越小,有利于皂化反应进行,但会增加经济成本。在最优反应温度、反应压力和进料速度条件下,不同乙醇和碱加入量下的反应结果如表 1、2所示。最终确定乙醇和羊毛脂的质量比m(C2H5OH):m(lanolin)为3:1、碱和羊毛脂的质量比m(KOH):m(lanolin)为0.11:1。
|
|
表 1 乙醇的量对反应的影响 Table 1 Effect of ethanol on the reaction |
|
|
表 2 碱的量对反应的影响 Table 2 Effect of alkali on the reaction |
将原料羊毛酸和羊毛醇按质量比1:1进行投料,对酯化过程反应温度、反应时间和碱用量(以羊毛醇添加量为基准) 进行正交探究,以产物的酸值和颜色作为判断标准,得到如表 3所示的实验结果。表中酸值越小意味着酯化反应越完全,颜色等级由浅到深依次为较浅、中等和较深。
|
|
表 3 不同条件下的酯化反应结果 Table 3 Esterification results under different conditions |
由表 3可见,添加一定量的碱催化剂,酯化反应活性得到较大提高;提高反应温度、延长反应时间和增大碱用量都可以提高酯化反应收率;高温下长时间反应和碱用量增加会导致产品颜色更深,对后续脱色过程产生困扰。
综合各种因素,最终选择碱添加量为羊毛醇质量的4%,先在180 ℃下反应4 h,再升温到200 ℃反应4 h,此时得到的产物酸值为5.1、色度为中等。在此条件下,改变原料羊毛酸、羊毛醇、羊毛甾醇的质量比进行反应,反应结果列于表 4。由表中1、2、3组实验结果可见,羊毛酸与羊毛醇质量比由1.0增到1.1时,酸值变化不大,继续增大到1.2后,酸值增大明显,表明有较多的羊毛酸剩余,最终确定羊毛酸的添加量为羊毛醇的1.1倍;由表中4、5组实验结果可见,原料中羊毛甾醇的存在会影响羊毛脂产品的形状,较软的产物熔点会更低。根据Q/LS 001-2015标准,羊毛脂产品熔点标准为38~44 ℃。
|
|
表 4 不同投料比下的酯化反应结果 Table 4 Reaction results at different feed ratios |
将羊毛甾醇作为原料参与合成羊毛脂反应,以熔点为检测指标考察羊毛甾醇添加量的影响,其余条件不变,羊毛酸与羊毛醇投料质量比为1.1:1,实验结果列于表 5。
|
|
表 5 羊毛甾醇添加量对熔点的影响 Table 5 Effect of the lanosterol on the melting point |
由于羊毛甾醇价格与其他原料相比更昂贵,综合原料成本、混合后得到的产物熔点等因素,优选的工艺条件为羊毛甾醇添加量为羊毛醇质量的5 %。
3.3 羊毛脂脱色条件探究本次选择过氧化氢溶液(质量分数为30%)作为脱色剂对合成羊毛脂进行脱色处理,实验结果列于表 6。表中第4组为两次脱色且均为常压脱色,第5组为先常压再减压脱色。由表中3、4、5组实验结果可见,在过氧化氢用量相同条件下,两次脱色比一次脱色效果更好;先常压再减压脱色效果优于两次均为常压脱色的效果,产品色度可达到8-,满足指标要求。
|
|
表 6 不同过氧化氢用量下的脱色效果 Table 6 Decolorization effect under different amounts of hydrogen peroxide |
(1) 研究了羊毛脂管道化皂化反应工艺,相比于传统的釜式反应,管式反应过程连续稳定、便于自动化控制,且在线反应量小,保证了工艺更高安全系数,高温条件下皂化反应速度更快、生产能力大,具有较好的工业应用价值。最终确定的工艺条件:乙醇、羊毛脂、氢氧化钾质量比为3:1:0.11、反应温度为160 ℃、反应压力为1.40 MPa、停留时间为40 min,该条件下皂化收率可达99.3 %。
(2) 研究了皂化副产物羊毛酸和羊毛醇通过酯化反应联产羊毛脂的工艺,最终确定的工艺条件:羊毛酸、羊毛醇、氢氧化钾、羊毛甾醇质量比为1.1:1:0.04:0.05、180 ℃下反应4 h、再升温至200 ℃反应4 h,将得到的羊毛脂粗品用质量分数为30 %的过氧化氢脱色两次,再用质量分数为2 %的碳酸钾除酸,最后得到精制的羊毛脂产品,售出该产品可实现产业效益最大化。
| [1] |
张星华. 羊毛脂中胆羊毛甾醇的分离提取工艺[D]. 天津: 天津大学, 2010. ZHANG X H. Process for extracting cholesterol from lanolin[D]. Tianjin: Tianjin University, 2010. |
| [2] |
BOGDANOV A L. Research on the effect of lanolin on rheological and tribotechnical characteristics of complex calcium grease[J]. Journal of Friction and Wear, 2019, 40(3): 266-269. DOI:10.3103/S1068366619030024 |
| [3] |
JACKSON K, DENNIS C. Lanolin for the treatment of nipple pain in breastfeeding women: A randomized controlled trial[J]. Maternal & Child Nutrition, 2017, 13(3): 1-10. |
| [4] |
FU F F, ZHOU B Q, OUYANG Z J, et al. Multifunctional cholesterol-modified dendrimers for targeted drug delivery to cancer cells expressing folate receptors[J]. Chinese Journal of Polymer Science, 2019, 37(2): 129-135, 197-202. DOI:10.1007/s10118-019-2172-9 |
| [5] |
HARTONO D, HO DY, YANG K L, et al. The effect of cholesterol on protein-coated gold nanoparticle binding to liquid crystal-supported models of cell membranes[J]. Biomaterials, 2010, 31(11): 3008-3015. DOI:10.1016/j.biomaterials.2010.01.003 |
| [6] |
KOHJI I, KATSUNCI D. Wool alcohols and fatty acids: JP, 76139806[P]. 1976-12-01.
|
| [7] |
毛法根, 郑筱凤. 从羊毛脂中制取羊毛酸两价金属皂: CN, 86100362[P]. 1987-08-05. MAO F G, ZHENG X F. Preparation of lanolin divalent metal soap from lanolin: CN, 86100362[P]. 1987-08-05. |
| [8] |
ADOLF K, THOMAS T. Manufacture of alcohols from esters: GB, 1002975[P]. 1965-09-02.
|
| [9] |
ROBINSON B, SAFDAR A. Saponification of fats and oils: GB, 2170507[P]. 1986-08-06.
|
| [10] |
沈涛. 羊毛脂中胆固醇的提取[D]. 北京: 北京化工大学, 2016. SHEN T. The extraction of cholesterol from lanolin[D]. Beijing: Beijing University of Chemical Technology, 2016. |
| [11] |
SHEN T, OU Y B, QIAN C, et al. Aminolysis of ethyl acetate in continuous flow and its reaction kinetics[J]. Chinese Journal of Chemical Engineering, 2019, 27(12): 2948-2952. DOI:10.1016/j.cjche.2019.03.015 |
| [12] |
何爽, 罗勇, 初广文, 等. 螺旋盘管反应器内黏性流体微观混合性能研究[J]. 高校化学工程学报, 2014, 28(3): 497-502. HE S, LUO Y, CHU G W, et al. Micromixing efficiency of viscous fluids in a helical tube reactor[J]. Journal of Chemical Engineering of Chinese Universities, 2014, 28(3): 497-502. DOI:10.3969/j.issn.1003-9015.2014.03.010 |
| [13] |
许菲菲. 从羊毛脂中提取胆羊毛甾醇的工艺研究[D]. 杭州: 浙江大学, 2005. XU F F. Study on extraction craft of isolation of cholesterol from lanolin[D]. Hangzhou: Zhejiang University, 2005. |
| [14] |
PEI H R, MA X T, PAN Y, et al. Separation and purification of lanosterol, dihydrolanosterol, and cholesterol from lanolin by high-performance counter-current chromatography dual-mode elution method[J]. Journal of Separation Science, 2019, 42(12): 2171-2178. DOI:10.1002/jssc.201900063 |
| [15] |
NIE J, SHEN J, SHI Y Y, et al. Synthesis of trimethylolpropane esters by base-catalyzed transesterification[J]. European Journal of Lipidence and Technology, 2020, 122(3): 1-10. |
| [16] |
IVAN-TAN C T, ISLAM A, YUNUS R, et al. Screening of solid base catalysts on palm oil based biolubricant synthesis[J]. Journal of Cleaner Production, 2017, 148: 441-451. DOI:10.1016/j.jclepro.2017.02.027 |
| [17] |
钱超, 辛宇, 阮建成, 等. 管道反应器皂化羊毛脂提取胆固醇的方法: CN, 109851654[P]. 2020-06-16. QIAN C, XIN Y, RUAN J C, et al. Method for extracting cholesterol by saponifying lanolin in pipeline reactor: CN, 109851654[P]. 2020-06-16. |
| [18] |
国家药典委员会. 中华人民共和国药典[M]. 北京: 中国医药科技出版社, 2015. Chinese Pharmacopoeia Commission. Pharmacopoeia of the People's Republic of China[M]. Beijing: China Medical Science Press, 2015. |
| [19] |
朱京科, 胡六江. 高效液相色谱/蒸发光散射检测法分析羊毛脂中的胆甾醇[J]. 精细石油化工, 2004, 5(5): 51-53. ZHU J K, HU L J. Determination of cholesterol in lanolin by high performance liquid chromatography and evaporation light scattering detector[J]. Speciality Petrochemicals, 2004, 5(5): 51-53. |
| [20] |
DARJA P, ANDREJA G. Saponification reaction system: a detailed mass transfer coefficient determination[J]. Acta Chimica Slovenica, 2015, 62(1): 237-241. |
| [21] |
ISSARA C, CHAKRIT T, SONGTHAM P, et al. Investigation of saponification mechanisms in biodiesel production: Microscopic visualization of the effects of FFA, water and the amount of alkaline catalyst[J]. Journal of Environmental Chemical Engineering, 2020, 8(2): 1-18. |
| [22] |
陈蔚. 胆固醇和24-去氢胆固醇的溶解度[D]. 杭州: 浙江大学, 2010. CHEN W. Solubilities of cholesterol and desmosterol[D]. Hangzhou: Zhejiang University, 2010. |




