2. 四川大学 化学工程学院,四川 成都 610065
2. School of Chemical Engineering, Sichuan University, Chengdu 610065, China
锂离子电池作为最具前景的新能源材料被广泛应用于便携式电子设备、大型储能设备、电动汽车(EVs)和混合动力汽车(HEVs)[1~3]。为了满足人们对高能量日益增长的需求,制备性能优异的锂离子电池正极材料尤为重要。在这些正极材料中,层状三元正极材料LiNixCoyMn1-x-yO2因其低毒性、低成本和高容量引起了人们广泛关注,其中LiNi1/3Co1/3Mn1/3O2被认为是最有可能替代商业化LiCoO2的正极材料之一[4~6]。然而,LiNi1/3Co1/3Mn1/3O2材料也存在缺陷,如在电化学循环过程中,由于电池的内阻增大导致倍率和循环性能较差[7, 8]。目前,结合高功率的尖晶石材料来制备一种异质结构的尖晶石/层状复合材料的思路被认为是非常可行的[9~12],因为尖晶石材料具有高的Li+扩散系数(10-11~10-9 cm2·s-1)和三维锂离子扩散通道(3D)可以提高Li+的扩散迁移速率[13, 14],因而其倍率性能优异;并且尖晶石相和层状相的晶体结构类似,两者的氧原子都是呈立方密堆积结构[9~11],具有很好的兼容性。Wu等[11]对层状富锂材料Li1.2Mn0.6Ni0.2O2采用原位诱导生长法成功制备得到了一种异质结构的尖晶石/层状复合材料,借助尖晶石相的三维锂离子扩散通道,使得材料的电化学性能显著提升,在2.0~4.8 V,5 C时(1 C = 180 mA·g-1),放电比容量仍能达到218.9 mAh∙g-1。Xia等[9]采用在富锂材料0.33Li2MnO3·0.67Li[Mn1/3Ni1/3Co1/3]O2表面原位碳化还原的方法制得了层状@尖晶石@碳层的异质复合结构材料,显著提高了材料的倍率性能和循环稳定性,在2.0~4.8 V,0.1 C时的首次放电比容量高达334.5 mAh∙g-1,且在30 C的高倍率下,其放电比容量还能保持在122.7 mAh∙g-1。Song等[10]通过碳黑对富锂材料Li(Li0.2Mn0.54Ni0.13Co0.13)O2的表面进行改性处理,制得了表面为尖晶石相,内部为层状相的异质结构材料,并展现出了优异的电化学性能,在2.0~4.8 V,0.05 C时的首次库伦效率由原始材料的78%增加至93.4%,且在10 C时的放电比容量高达100 mAh∙g-1以上。
鉴于异质复合结构材料的优势明显,且目前尚未有相关文献报道对层状三元材料与尖晶石材料的异质复合结构进行研究,故本文采用草酸盐共沉淀法制备得到了一系列(x = 0.1, 0.2, 0.3, 0.4, 0.5) 异质结构的尖晶石/层状复合正极材料LiNi1/3Co1/3Mn1/3O2,考察了晶体结构、形貌和电化学性能随着x值的变化情况,并从中优选出了一组最佳比例值的复合材料。
2 实验 2.1 材料合成将化学计量比的Ni(NO3)2·4H2O、Co(NO3)2·6H2O和Mn(CH3COO)2·4H2O溶于去离子水中配成浓度为1 mol∙L-1的溶液。以1 mol∙L-1的C2H2O4·2H2O和1.5 mol∙L-1的C6H8O7·H2O分别作为沉淀剂和络合剂。将这三种溶液在搅拌速度为500 r∙min-1条件下缓慢加入到反应器中,反应温度为65℃,pH值为4.0±0.2。制得的前驱体沉淀用去离子水清洗数次后在100℃干燥一晚上。最后与过量5%的Li2CO3混合研磨,再在450℃下预烧6 h,850℃下煅烧12 h得到LiNi1/3Co1/3Mn1/3O2。
为了制得异质结构的层状/尖晶石复合材料,本文将上述步骤得到的LiNi1/3Co1/3Mn1/3O2材料加入到Mn(CH3COO)2·4H2O溶液中搅拌混合均匀,再采用减压蒸馏方式除去多余的水分,使得Mn(CH3COO)2·4H2O能够在沸腾和搅拌的共同作用下均匀包裹在LiNi1/3Co1/3Mn1/3O2颗粒表面。最后在750℃下煅烧6 h制得异质结构的尖晶石/层状复合材料。本文以LiNi1/3Co1/3Mn1/3O2的摩尔量为基准,按照n(Mn(CH3COO)2·4H2O):n(LiNi1/3Co1/3Mn1/3O2)分别为x = 0.1、0.2、0.3、0.4、0.5,制备得到了五组异质结构的复合材料。
2.2 样品的表征与电化学测试样品的晶体结构采用X-射线衍射(XRD)分析,仪器为菲利普公司PW1730多晶转靶X-射线仪(Cu Kα靶,λ = 1.5418 Å),扫描角度范围为10~70°。颗粒的形貌和粒径采用日本日立(Hitachi)S-4800的扫描电子显微镜(SEM)进行表征和分析。采用日本电子JEM-2100高分辨透射电镜(TEM)对样品的微观结构进行表征和分析。X-射线光电子能谱(XPS,ESCALAB 250Xi,Al Kα,hν = 1486.68 eV)用于分析Ni、Co、Mn元素的价态情况,测得的元素结合能用C1s = 284.60 eV进行校正。
将正极材料、乙炔黑、黏结剂(PVDF)按80:13:7的质量比例均匀混合,并加入适量的N-甲基吡咯烷酮调成糊状。将湿浆料涂在铝箔上,在100℃下真空干燥10 h。把这些涂有浆料的铝箔切成直径为14 mm的圆片,并在20 MPa下压实得到电池的正极片,每个片上负载的活性物质量为3~4 mg∙cm-2。最后在充满氩气的手套箱中,将正极片、锂片(负极)、隔膜(Celgard 2400)、电解液LiPF6(1 mol·L-1)/碳酸乙烯酯(EC)+碳酸二甲酯(DMC) (体积比1:1) 组装成CR2032扣式电池。本文采用深圳Neware公司的BTS-5 V 20 mA充放电测试仪进行电性能测试,充放电电压为2.7~4.5 V,1 C = 180 mA∙g-1。采用德国Zennium IM6电化学工作站对电池的电化学阻抗谱(EIS)进行测试,测试频率范围在100 kHz~10 mHz,扰动电压为5 mV,得到的数据用Zview 2软件进行电化学元件模型数值拟合分析。
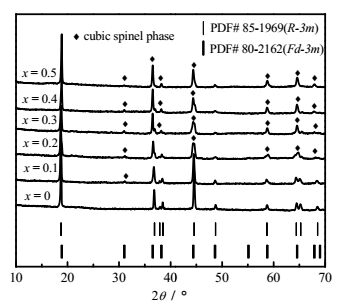
3 结果与讨论 3.1 材料结构和形貌分析图 1为样品的XRD图。由图可发现在x = 0时,样品为纯相的层状结构LiNi1/3Co1/3Mn1/3O2材料,没有其他杂峰存在,所有的衍射峰均能很好地索引为六方α-NaFeO2结构,R3m空间群[15]。随着x值增大,层状结构的衍射峰逐渐减少,峰强变弱,而材料中的尖晶石相特征衍射峰(Fd3m)[16]越来越明显(如图中标记所示),到x = 0.5时,尖晶石相的衍射峰大量存在。XRD结果表明采用此方法成功制得了两相共存的尖晶石/层状复合材料。
|
图 1 样品的XRD图 Fig.1 XRD patterns of samples |
图 2为样品的SEM图。由图可发现,这六种材料的颗粒形貌基本没有变化,都是由球形或类球形结构的一次颗粒无规则团聚而成。

|
图 2 样品的SEM图 Fig.2 SEM micrographs of the samples (a) x = 0 (b) x = 0 (c) x = 0.2 (d) x = 0.3 (e) x = 0.4 (f) x = 0.5 |
图 3(a)和3(b)分别为x = 0和x = 0.2两样品的TEM图以及相应的傅里叶变换图(FFT)。由图 3(a)可发现x = 0的样品为单晶,且相应的FFT图显示出典型的六方晶体结构。由图 3(b)可看出x = 0.2的样品是由两部分组成,且存在明显的相分界线。经傅里叶变换(FFT)可发现,材料表面为立方结构的尖晶石相(厚度约为8 nm左右),内部为六方晶体结构(与图 3(a)中的晶体结构一致)。由TEM结果进一步证实成功制得了外层为尖晶石相,内层为层状结构相的异质复合结构材料。

|
图 3 TEM和相应的FFT图 Fig.3 TEM micrographs and corresponding FFT patterns (a) x = 0 (b) x = 0.2 |
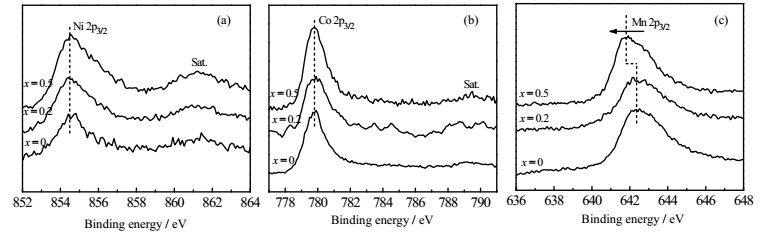
为了研究尖晶石/层状异质结构材料中Ni、Co、Mn的价态及其变化规律,选取x = 0、0.2和0.5的材料进行X射线光电子能谱(XPS)测试,如图 4所示。图 4(a)和4(b)分别为Ni 2p3/2和Co 2p3/2的XPS图,由图可发现这几种材料中的Ni和Co价态未发生改变,其结合能分别在854.5和779.8 eV,对应Ni为+2价,Co为+3价。图 4(c)中x = 0材料的Mn 2p3/2的结合能在642.5 eV,对应Mn4+,但随着x的增大,其结合能值向低结合能方向移动,说明有低于+4价的Mn产生,其原因可归结于表面的Fd3m型尖晶石相的增加(如图 1中XRD分析),因为Fd3m型尖晶石相材料中本身就存在部分+3价Mn原子[10, 12],所以表面的Mn元素价态呈现降低的趋势。此外,采用XPS表征对这三个材料的表面化学成分进行拟合分析,结果表明x = 0材料的表面化学式为LiNi0.34Co0.27Mn0.36O2;x = 0.2材料的表面化学式为LiNi0.46Co0.38Mn1.30O4 (Li[Ni0.23Co0.19Mn0.65]2O4);x = 0.5材料的表面化学式为LiNi0.12Co0.22Mn1.81O4 (Li[Ni0.06Co0.11Mn0.905]2O4)。可以发现,对于x = 0.2和0.5的材料表面化学成分都可由尖晶石材料的通式LiM2O4 (M = Ni, Co, Mn)表示,式中Mn的比例随着x值的增大而增大,而Ni、Co的比例随着x值的增大而降低。XPS结果再次证明成功合成了表面为尖晶石相的异质结构复合材料。
|
图 4 x = 0, 0.2, 0.5样品的XPS图 Fig.4 XPS spectra of (a) Ni 2p3/2; (b) Co 2p3/2; (c) Mn 2p3/2 for x = 0, 0.2, 0.5 samples |
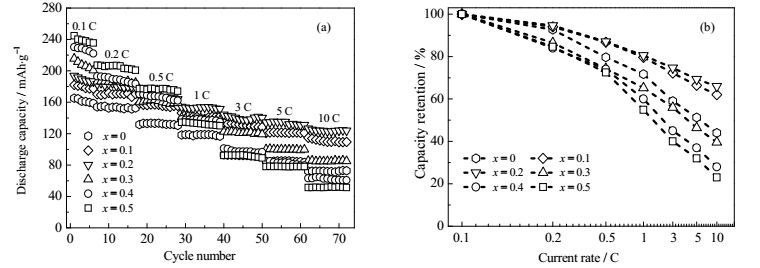
图 5(a)为材料在2.7~4.5 V下的倍率循环图。由图可发现在0.1 C时,随着x值增大,材料的放电比容量就越高,在x = 0、0.1、0.2、0.3、0.4、0.5分别对应的放电比容量为:165、182、194、216、230、244 mAh∙g-1。但随着电流密度的逐渐增大,x值越大的材料,容量衰减反而越快,在10 C时,x = 0.4和0.5材料放电比容量仅仅为63和51 mAh∙g-1,而x = 0.1和0.2材料表现出了优异的倍率性能,在10 C时的放电比容量分别为114和126 mAh∙g-1。图 5(b)为材料在不同倍率下的容量保持率。由图可以直观地看出x = 0.1和0.2材料具有最优异的容量保持率。x = 0.2材料在0.2、0.5、1、3、5和10 C相对于0.1 C的容量保持率分别为:94.6%、87.1%、80.7%、74.7%、69.3%和66.4%,相比于x = 0的原始样品在不同倍率下的容量保持率92.7%、79.7%、71.7%、59.2%、51.3%和44.2%有较大提高。由电化学性能结果可合理地推断材料中较少含量的尖晶石相可以使得主体材料晶体结构更加稳定,不易坍塌,而较多的尖晶石相反而会加剧材料晶体结构的恶化。尖晶石相具有三维锂离子扩散通道(3D)能够提供更快的Li+迁移速率,减少Li+脱嵌晶格的阻力,提高材料的倍率性能,但同时因为Jahn-Teller效应[17~20],即:Mn3+→ Mn2++ Mn4+,生成的Mn2+易与电解液发生副反应,导致主体材料结构恶化,故而对于异质结构的层状/尖晶石复合材料电性能的影响主要取决于尖晶石相的那一方面作为主导,而这又与复合材料中的尖晶石含量密切相关。
|
图 5 样品在不同倍率下的(a)倍率性能; (b)容量保持率 Fig.5 Different rates of the samples of (a) rate capability; (b) capacity retention |
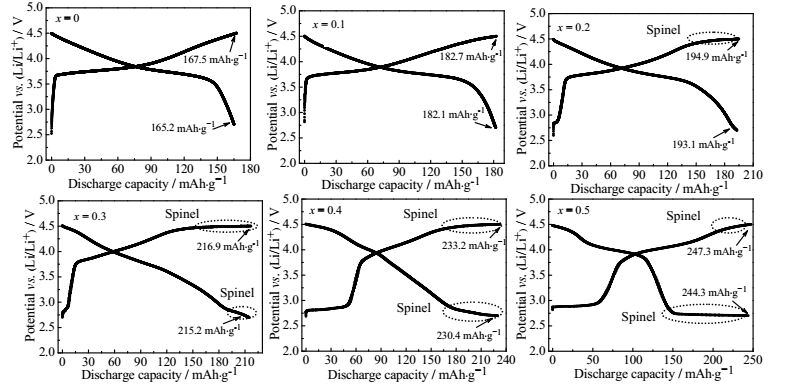
图 6为样品在2.7~4.5 V,0.1 C下的首次充/放电曲线图。由图发现在x = 0、0.1时,材料的充/放电曲线基本一致,但当x继续增大到0.2时,即复合材料中的尖晶石相含量进一步增加,在4.5 V左右逐渐可观察到尖晶石相的充电平台。在x = 0.3、0.4、0.5材料的充/放电曲线中,2.7和4.5 V左右的尖晶石相特征氧化还原反应平台十分明显[17],并可以发现这两个尖晶石相的特征充放电平台对这三个材料的总容量贡献很大,因此这三个比例下的异质结构材料Jahn-Teller效应会相对严重,造成晶体结构在长期的电化学循环过程中不稳定,电化学性能变差。
|
图 6 样品在0.1 C的首次充/放电曲线图 Fig.6 Initial charge/discharge curves of the samples at 0.1 C |
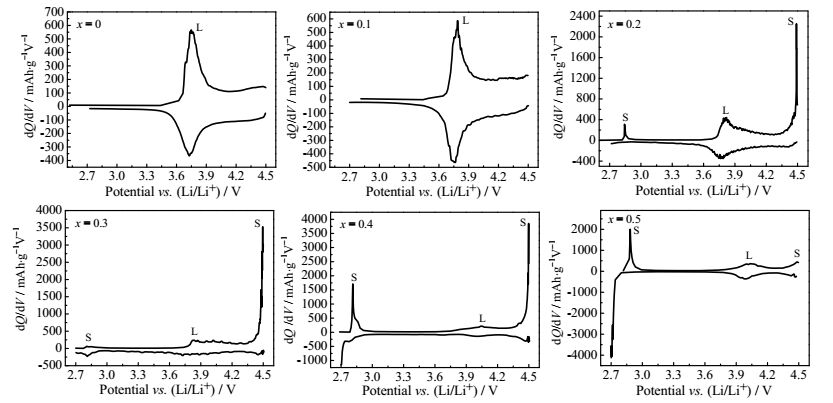
为了更直观地研究尖晶石/层状异质结构材料的电极反应,对样品在0.1 C的首次充/放电曲线(图 6)进行微分处理得到相应的容量与电压微分(dQ/dV)曲线,如图 7所示,图中L表示层状相,S表示尖晶石相。由图可发现,随着x值的增大,尖晶石相的氧化还原峰逐渐出现,并且对充放电比容量的贡献也逐渐变大。x = 0.2、0.3、0.4、0.5时,在2.8 V左右的峰对应尖晶石相中Mn3+/4+的氧化还原反应[10, 12, 14],4.5 V左右的峰对应尖晶石相中Ni2+/4+的氧化还原反应[10, 12, 14]。在x = 0.4、0.5时,材料在2.8 V左右的Mn3+/4+氧化还原峰峰强明显增加,说明在这两个材料中尖晶石相的Mn3+/4+对比容量的贡献较大。在x = 0.5时,4.5 V左右的Ni2+/4+氧化还原峰峰强下降明显,这与尖晶石相LiM2O4中的Ni和Mn元素比例有关,随着x值的增大,尖晶石相中的Mn含量增多,而Ni含量降低(前面XPS分析结果已证实该现象)。
|
图 7 样品在0.1 C的首次充/放电容量与电压微分(dQ/dV)曲线 Fig.7 Differential capacity (dQ/dV) as a function of voltage curves of the samples at 0.1 C (first cycle) |
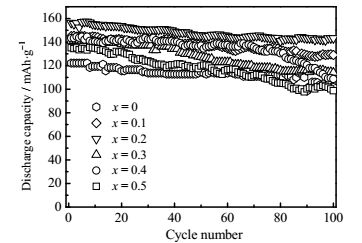
图 8为材料在2.7~4.5 V,1 C下循环100次的循环性能图。由图可以看出,x = 0.2材料的循环稳定性最佳,放电比容量最高。x = 0、0.1、0.2、0.3、0.4、0.5材料在1 C下循环100次后的容量保持率分别为:83%、89%、92%、81%、76%、73%,放电比容量分别为:101、129、144、114、109、99 mAh∙g-1。综合上述电化学性能测试结果可得出x = 0.2的异质结构尖晶石/层状复合材料具有最好的倍率循环性能,此时尖晶石相和主体层状相达到最优的比例,使得尖晶石相的三维锂离子扩散通道优势可以缓解其本征缺陷Jahn-Teller效应,达到了扬长避短的作用。
|
图 8 样品的循环性能 Fig.8 Cycle performance of samples |
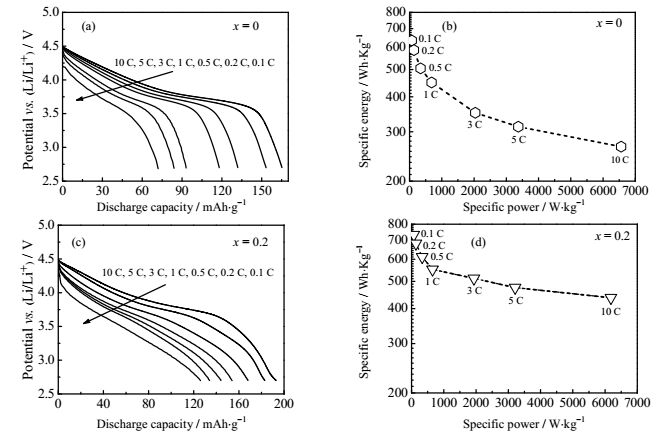
图 9为x = 0和0.2样品在不同倍率下的放电曲线图以及相应的Ragone能量密度图。由图 9(a)(c)可以观察到,随着电流密度的增加,材料的平均放电平台都有一定程度的下降,这种现象是由于电池内阻随着电化学循环的进行而不断增大所引起,使得电池极化严重,不可逆程度变大。x = 0.2样品的放电平台衰减相对较小,说明材料的极化现象不严重,可逆性较好。图 9(b)(d)为样品的Ragone图,比能量密度(Es)和功率密度(Ps)可由下式进行计算:Es= QV= ∫ Q(V) dV,Ps = IV=I ∫ dV[21, 22],其中Q、V和I分别代表比容量(mAh·g-1)、电压(V)和电流密度(mA·g-1)。x = 0样品在0.1 C时的能量密度为635.12 Wh∙kg-1,在10 C时的能量密度为264.38 Wh∙kg-1;而x = 0.2的样品在0.1 C时能量密度为733.44 Wh·kg-1,在10 C时的能量密度为437.21 Wh·kg-1,显示出该电极材料在高功率密度工作时仍能保持较高的能量密度。
|
图 9 不同倍率的放电曲线和相应的ragone曲线 Fig.9 Discharge curves at different rates and corresponding ragone plots |
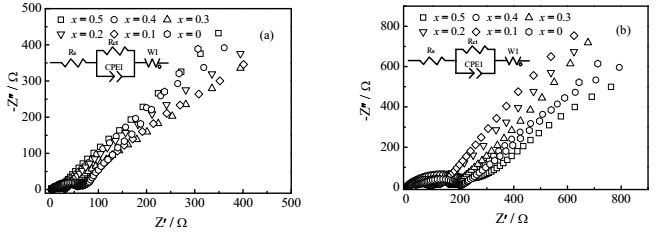
图 10(a)为原始样品的电化学阻抗图谱(EIS),图 10(b)为样品经过倍率循环性能测试后的EIS图。内嵌图为经Zview软件拟合的等效电路图,样品的阻抗谱都由高频区的一个半圆和低频区的一条斜线组成。在高频区阻抗谱与Zx轴的截距表示电池固有阻抗(Rs),主要来源于电解液阻抗、隔膜阻抗等。半圆代表电极材料和电解液之间的界面阻抗(Rct),代表Li+界面反应的难易程度,越小表明反应越易进行。斜线表示Warburg阻抗(W1),表明Li+在固相中的扩散阻力[23~25]。经拟合得到的Rct值列于表 1。Rct1代表图 10(a)拟合的阻抗值,Rct2代表图 10(b)拟合的阻抗值。由拟合数据可发现Rct1随着x的增大而减少,其原因可归结于材料中的尖晶石相含量越来越多,且尖晶石相的Rct值本来就很小[10]。由拟合的Rct2值可发现这种尖晶石相的优势并未在倍率循环测试之后的x = 0.3、0.4、0.5样品中得以延续。ΔR (= Rct2-Rct1)可直接看出x = 0.2材料的阻抗增值最小,而尖晶石含量较多的x = 0.3、0.4、0.5样品阻抗增值较大,这个结果与倍率循环测试结果相符合,这也是材料电化学性能差异的根本原因。
|
图 10 EIS图 Fig.10 EIS plots (a) the pristine samples (b) the samples after rate capacity examination |
| 表 1 EIS等效电路图拟合结果 Table 1 Fitting impedance parameters of the equivalent circuit |
本文采用草酸盐共沉淀法制备了x = 0.1、0.2、0.3、0.4、0.5五组不同异质结构的尖晶石/层状复合LiNi1/3Co1/3Mn1/3O2正极材料,考察了晶体结构、形貌和电化学性能随着x值不同的情况,并从中优选出了一组最佳比例值的复合材料。XRD结果表明成功制得了这种两相共存的异质结构材料,且随着x值的增大,材料中的尖晶石相成份逐渐增多。电化学性能结果表明在x = 0.2的复合材料具有最好的倍率性能和循环性能,此时尖晶石相和主体层状相达到最佳的比例,使得尖晶石相的三维锂离子扩散通道优势可以缓解其本征缺陷Jahn-Teller效应。该材料在0.1和10 C时的能量密度分别为733.44和437.21 Wh∙kg-1,具有应用于电动车等商业化高功率密度锂离子电池中的潜力。
| [1] | Dunn B, Kamath H, Tarascon J M. Electrical energy storage for the grid: a battery of choices[J]. Science, 2011, 334(6058): 928-935.DOI:10.1126/science.1212741. |
| [2] | Tarascon J M, Armand M. Issues and challenges facing rechargeable lithium batteries[J]. Nature, 2001, 414(6861): 359-367.DOI:10.1038/35104644. |
| [3] | Manthiram A, Murugan A V, Sarkar A, et al. Nanostructured electrode materials for electrochemical energy storage and conversion[J]. Energy & Environmental Science, 2008, 1(6): 621-638. |
| [4] | Hua W B, Guo X D, Zheng Z, et al. Uncovering a facile large-scale synthesis of LiNi1/3Co1/3Mn1/3O2 nanoflowers for high power lithium-ion batteries[J]. Journal of Power Sources, 2015, 275: 200-206.DOI:10.1016/j.jpowsour.2014.09.178. |
| [5] | XIA Shu-biao(夏书标), ZHANG Ying-jie(张英杰), DONG Peng(董鹏), et al. Solid synthesis of LiNi0.80Co0.15Al0.05O2 cathode with fine-sized materials and its structure and electrochemical properties(高倍率性能锂离子电池Li[Ni1/3Co1/3Mn1/3]O2正极材料的制备及其电化学性能)[J]. Journal of Chemical Engineering of Chinese Universities(高校化学工程学报), 2015, 29(2): 425-431. |
| [6] | Xu Z L, Xiao L L, Wang F, et al. Effects of precursor, synthesis time and synthesis temperature on the physical and electrochemical properties of Li(Ni1-x-yCoxMny)O2 cathode materials[J]. Journal of Power Sources, 2014, 248: 180-189.DOI:10.1016/j.jpowsour.2013.09.064. |
| [7] | ZHANG Ji-bin(张继斌), HUA Wei-bo(滑纬博), ZHENG Zhuo(郑卓), et al. Preparation and electrochemical performance of LiNi1/3Co1/3Mn1/3O2 cathode material for high-rate lithium-ion batteries(高倍率性能锂离子电池Li[Ni1/3Co1/3Mn1/3]O2正极材料的制备及其电化学性能)[J]. Acta Physico-Chimica Sinica(物理化学学报), 2015, 31(5): 905-912.DOI:10.3866/PKU.WHXB201503091. |
| [8] | WANG Hai-yan(王海燕), TANG Ai-dong(唐爱东), HUANG Ke-long(黄可龙), et al. Preparation and rate capability study of LiNi1/3Co1/3Mn1/3O2 as cathode material(LiNi1/3Co1/3Mn1/3O2正极材料的制备与倍率性能研究)[J]. Chinese Journal of Inorganic Chemistry(无机化学学报), 2008, 24(4): 593-599. |
| [9] | Xia Q B, Zhao X F, Xu M Q, et al. A Li-rich layered@spinel@carbon heterostructured cathode material for high capacity and high rate lithium-ion batteries fabricated via an in situ synchronous carbonization-reduction method[J]. Journal of Materials Chemistry A, 2015, 3(7): 3995-4003.DOI:10.1039/C4TA05848H. |
| [10] | Song B H, Liu H W, Liu Z W, et al. High rate capability caused by surface cubic spinels in Li-rich layer-structured cathodes for Li-ion batteries[J]. Scientific Reports, 2013, 3: 3094.DOI:10.1038/srep03094. |
| [11] | Wu F, Li N, Su Y F, et al. Spinel/layered heterostructured cathode material for high-capacity and high-rate Li-ion batteries[J]. Advanced Materials, 2013, 25(27): 3722-3726.DOI:10.1002/adma.v25.27. |
| [12] | Zheng Z, Hua W B, Yu C, et al. Heterogeneous intergrowth xLi1.5Ni0.25Mn0.75O2.5·(1-x)Li0.5Ni0.25Mn0.75O2 (0 ≤ x ≤ 1) composites: synergistic effect on electrochemical performance[J]. Dalton Transactions, 2015, 44(32): 14255-14264.DOI:10.1039/C5DT01678A. |
| [13] | Amine K, Liu J, Belharouak I, et al. Advanced cathode materials for high-power applications[J]. Journal of Power Sources, 2005, 146(1-2): 111-115.DOI:10.1016/j.jpowsour.2005.03.227. |
| [14] | Santhanam R, Rambabu B. Research progress in high voltage spinel LiNi0.5Mn1.5O4 material[J]. Journal of Power Sources, 2010, 195(17): 5442-5451.DOI:10.1016/j.jpowsour.2010.03.067. |
| [15] | Li J, Xiong S, Liu Y, et al. Uniform LiNi1/3Co1/3Mn1/3O2 hollow microspheres: designed synthesis, topotactical structural transformation and their enhanced electrochemical performance[J]. Nano Energy, 2013, 2(6): 1249-1260.DOI:10.1016/j.nanoen.2013.06.003. |
| [16] | Idemoto Y, Narai H, Koura N. Crystal structure and cathode performance dependence on oxygen content of LiMn1.5Ni0.5O4 as a cathode material for secondary lithium batteries[J]. Journal of Power Sources, 2003, 119-121(6): 125-129. |
| [17] | CHEN Ming-zhe(陈明哲), GUO Xiao-dong(郭孝东), ZHONG Ben-he(钟本和), et al. High energy density spinel LiCr0.2Ni0.4Mn1.4O4 cathode material prepared by spray pyrolysis method(喷雾热解制备高能量密度尖晶石LiCr0.2Ni0.4Mn1.4O4正极材料)[J]. Journal of Inorganic Materials(无机材料学报), 2014, 29(9): 917-923. |
| [18] | Park S H, Oh S W, Kang S H, et al. Comparative study of different crystallographic structure of LiNi0.5Mn1.5O4-δ cathodes with wide operation voltage[J]. Electrochimica Acta, 2007, 52(25): 7226-7230.DOI:10.1016/j.electacta.2007.05.050. |
| [19] | Xiao J, Chen X, Sushko P V, et al. High-performance LiNi0.5Mn1.5O4 spinel controlled by Mn3+ concentration and site disorder[J]. Advanced Materials, 2012, 24(16): 2109-2116.DOI:10.1002/adma.201104767. |
| [20] | Zheng J, Xiao J, Yu X, et al. Enhanced Li+ ion transport in LiNi0.5Mn1.5O4 through control of site disorder[J]. Physical Chemistry Chemical Physics, 2012, 14(39): 13515-13521.DOI:10.1039/c2cp43007j. |
| [21] | Zhu Z, Yan H, Zhang D, et al. Preparation of 4.7 V cathode material LiNi0.5Mn1.5O4 by an oxalic acid-pretreated solid-state method for lithium-ion secondary battery[J]. Journal of Power Sources, 2013, 224: 13-19.DOI:10.1016/j.jpowsour.2012.09.043. |
| [22] | Shaju K M, Bruce P G. Macroporous LiNi1/3Co1/3Mn1/3O2: a high-power and high-energy cathode for rechargeable lithium batteries[J]. Advanced Materials, 2006, 18(17): 2330-2334.DOI:10.1002/(ISSN)1521-4095. |
| [23] | Li Q, Li G S, Fu C C, et al. K+-doped Li1.2Mn0.54Co0.13Ni0.13O2: a novel cathode material with an enhanced cycling sability for lithium-ion batteries[J]. Acs Applied Materials & Interfaces, 2014, 6(13): 10330-10341. |
| [24] | Li B H, Han C P, He Y B, et al. Facile synthesis of Li4Ti5O12/C composite with super rate performance[J]. Energy & Environmental Science, 2012, 5(11): 9595-9602. |
| [25] | Wang L, Zhao J, He X, et al. Electrochemical impedance spectroscopy (EIS) study of LiNi1/3Co1/3Mn1/3O2 for Li-ion batteries[J]. International Journal of Electrochemical Science, 2012, 7(1): 345-353. |




