2. 浙江省生物燃料利用技术研究重点实验室,浙江 杭州 310014;
3. 石油和化工行业生物柴油技术工程实验室,浙江 杭州 310014;
4. 英国阿斯顿大学化学工程与应用化学系 伯明翰 B4 7ET
2. Zhejiang Province Key Laboratory of Biomass Fuel, Hangzhou 310014, China;
3. Biodiesel Laboratory of China Petroleum and Chemical Industry Federation, Hangzhou 310014, China;
4. Chemical Engineering and Applied Chemistry, Aston University, Aston Triangle, Birmingham B4 7ET, UK
层状双氢氧化物(layered double hydroxide,LDHs)是一种层状结构的无机功能材料,已被用于吸附捕集温室气体CO2 [1~5]。前期研究发现,对LDHs进行氨基改性可得到具有良好CO2吸附性能的固体吸附材料[6~8],且CO2吸附容量随材料的氨基负载量的增大而增大。常用的氨基改性方法有阴离子表面活性剂法和超声剥落法。阴离子表面活性剂法制备改性LDHs过程中,氨基硅烷在特定pH下质子化,通过静电作用与阴离子表面活性剂结合,以盐的形式插入层间,经萃取去除阴离子表面活性剂实现氨基负载。Wang等[6]采用该方法,以3-氨丙基三甲氧基硅烷为改性剂制备的Mg-Al LDH的氨基负载量可达3.62 mmol·g-1,25℃纯CO2环境下吸附容量达1.39 mmol·g-1,为文献报道LDHs吸附容量的最高值。该方法萃取过程中阴离子表面活性剂的去除率已高于80%,氨基负载量提升空间有限。超声剥落法制备改性LDHs过程中,通过对已被阴离子表面活性剂插层的LDHs超声处理,使得LDHs层板剥落,氨基硅烷取代部分阴离子位点并与层板上羟基发生反应,从而实现氨基负载。该方法存在剥落效率低、剥落下来的阴离子表面活性剂和氨基硅烷竞争插层的不足[7]。姜哲等[8]采用超声剥落法,以N-氨乙基-γ-氨丙基三甲氧基硅烷为改性剂制备的Mg-Al LDH氨基负载量最高为2.71 mmol·g-1,30℃纯CO2环境下吸附容量为0.69 mmol·g-1。综上,单一采用阴离子表面活性剂法或剥落法都难以进一步提高LDHs的氨基负载量,限制了其在吸附捕集CO2中的应用。
因此,本研究提出一种复合改性方法,将阴离子表面活性剂法和剥落法有机结合,制备具有较高氨基负载量的LDHs,利用XRD、FT-IR、EA和TG等手段对制备的材料进行表征,考察氨基负载量对LDHs CO2吸附性能的影响规律,优选出吸附性能优良的氨基改性层状双氢氧化物,考察吸附温度等对其吸附性能的影响,并研究了其循环再生性能。
2 实验材料和方法 2.1 主要试剂六水合硝酸镁(Mg(NO3)2·6H2O,AR)购自上海泗联化工厂;九水合硝酸铝(Al(NO3)3·9H2O,AR)购自上海振兴试剂厂;氢氧化钠(NaOH,AR)购自西陇化工股份有限公司;甲苯(C7H8,AR)购自杭州化学试剂有限公司;3-氨丙基三甲氧基硅烷(C6H17NO3Si,97%)和N-氨乙基-γ-氨丙基三甲氧基硅烷(C8H22N2O3Si,95%)购自阿拉丁;十二烷基磺酸钠(C12H25NaO3S,97%)购自国药集团;无水乙醇(C2H5OH,AR)购自安徽安特食品股份有限公司。
2.2 样品制备复合氨基改性Mg-Al LDH制备分两步进行。第一步,采用共沉淀法[6]制备阴离子表面活性剂插层的氨基改性Mg-Al LDH。取3.99 g六水合硝酸镁和1.95 g九水合硝酸铝,按3:1(mol)配制水溶液A;取一定量的氨基硅烷、十二烷基磺酸钠溶于50 mL无水乙醇和100 mL去离子水的混合液得到溶液B;其中n(M)2+:n(M3+):n(阴离子表活性剂):n(氨基硅烷) = 3:1:2:6;将A液缓慢加入到B液中,剧烈搅拌;反应温度通过水浴保持在70℃;反应溶液的pH值由pH自动控制加液机调节,稳定在10±0.1;滴加完毕后,70℃下陈化4 h;抽滤、洗涤、干燥得到阴离子表面活性剂插层的氨基改性Mg-Al LDH。以3-氨丙基三甲氧基硅烷(N1)和N-乙基-γ-氨丙基三甲氧基硅烷(N2)为改性剂制备的阴离子表面活性剂插层的氨基改性Mg-Al LDH分别记为Mg-Al DS/N1,Mg-Al DS/N2。第二步,采用超声剥落法[8]对阴离子表面活性剂插层的氨基改性Mg-Al LDH再改性。将1.0 g Mg-Al DS/N1 (Mg-Al DS/N2)和100 mL甲苯置于250 mL烧瓶中,超声5 h;超声结束后,按照氨基硅烷和甲苯体积比分别为0:100、1:100、2:100、3:100、4:100、5:100加入氨基硅烷;保持搅拌,70℃下反应20 h;抽滤、洗涤、干燥得到二次氨基改性Mg-Al LDH,改性过程中以N1为改性剂、氨基硅烷按氨基硅烷和甲苯体积比0:100加入制备的二次氨基改性Mg-Al LDH记为Mg-Al N1(0),其它产物以此类推标记为Mg-Al N1(1)、Mg-Al N1(2)、Mg-Al N1(3)、Mg-Al N1(4)、Mg-Al N1(5)、Mg-Al N2(0)、Mg-Al N2(1)、Mg-Al N2(2)、Mg-Al N2(3)、Mg-Al N2(4)、Mg-Al N2(5)。
2.3 样品表征采用X射线衍射(Bruker AXS D8 Advance型,德国)分析样品结构,扫描角(2θ) 2~65°;采用红外傅里叶变换光谱仪(TENSOR Ⅱ型,德国BRUKER公司)测定样品的表面官能团信息,测试条件为:分辨率4 cm-1,光谱范围400~4000 cm-1,扫描次数64次;采用元素分析仪(Vario Macro Cube型,德国)测定样品的C、H、N、S元素的质量分数,根据改性前后N元素的质量分数计算氨基负载量;采用热重分析仪(TG209F3型,德国)测定样品热稳定性,测试程序:取约10 mg样品置于热重分析仪样品池内,以10℃·min-1的升温速率升至800℃,全程通入高纯N2,气体流量为30 mL·min-1。
2.4 CO2吸附容量测定采用热重法[9]测量复合氨基改性Mg-Al LDH的CO2吸附容量。取约10 mg样品放入样品池,在N2环境中加热到140℃,预处理30 min,降温至吸附温度(如30℃),恒温30 min,此时样品的质量为m1;将N2替换为纯CO2,恒温180 min,此时样品的质量为m2;前期研究发现150 min后,质量波动在±3%内,本研究将180 min内样品质量变化量与m1的比值(m2-m1)/m1定义为样品CO2吸附容量。
2.5 吸附脱附循环再生实验取约10 mg样品,在N2环境中加热到140℃预处理30 min,降温至预定吸附温度;将N2替换为纯CO2,恒温180 min;吸附完成后,样品温度以50℃×min-1的升温速率加热至预定脱附温度(如120℃),恒温30 min;脱附完成后,温度以25℃·min-1的降温速率降至预定吸附温度,恒温180 min;再重复吸附脱附过程若干次。
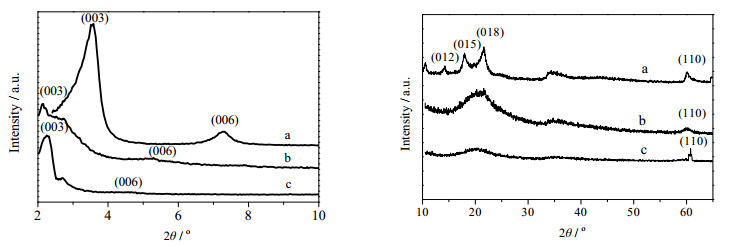
3 结果与讨论 3.1 二次氨基改性Mg-Al LDH的表征 3.1.1 XRD表征图 1为Mg-Al DS、Mg-Al N1和Mg-Al N2的X射线衍射图谱。由图可知,Mg-Al N1和Mg-Al N2都具有LDHs的特征峰(003)、(006)和(110),说明成功合成了LDHs[6, 7]。Mg-Al N1在2θ角为2.14°处有尖锐的(003)衍射峰,根据布拉格方程2d sinθ = nλ (θ为衍射半角,n衍射级数,λ = 0.15406 nm)可求得层板间距,减去层板平均厚度0.49 nm[6]可得Mg-Al N1的层间距为3.62 nm,与未改性的Mg-Al DS的层间距3.35 nm相比有所增加,可推测氨基硅烷插入LDHs层间。Mg-Al N1和Mg-Al N2的层间距分别为3.62 nm和3.72 nm,层间距都大于3 nm,层间阴离子在层间以双层交叉的形式排列,从层间距角度讲,氨基硅烷插入层间更为容易,有利于更多的氨基硅烷插入LDHs层间。相比于Mg-Al DS,Mg-Al N1、Mg-Al N2的(003)、(006)峰强度和锐度都明显降低,同时在15~30°出现峰的重叠,这是由于经过超声剥落改性,LDHs的结晶度下降[7]。
|
图 1 Mg-Al DS (a)、Mg-Al N2 (b)和Mg-Al N1(c)的X衍射图谱 Fig.1 XRD patterns of Mg-Al DS (a), Mg-Al N2 (b) and Mg-Al N1 (c) |
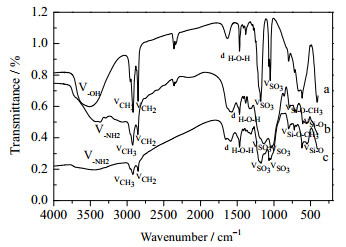
图 2为Mg-Al DS、Mg-Al N1和Mg-Al N2的傅里叶红外光谱图。由图可知,改性前后层状双氢氧化物表面吸收峰发生了明显的变化。改性后在3300、1180、817、798和466 cm-1处出现了新的吸收峰,其中,3300 cm-1是-NH2伸缩振动峰;817和1180 cm-1是Si-O-CH3的伸缩振动峰;466和798 cm-1是Si-O的伸缩振动峰;改性后在3500 cm-1处的-OH伸缩振动峰明显减弱,这是由于改性过程中氨基硅烷和层板上的羟基反应[6~8],使得层板表面的羟基数目减少,对应的峰强度减弱。这均表明氨基硅烷成功接枝在层状双氢氧化物表面。此外,2349 cm-1为CO2吸收峰,是样品吸附空气中的CO2所致,而复合改性样品在测试前经过充分的真空干燥处理,对应的峰很小或几乎没有。
|
图 2 Mg-Al DS (a)、Mg-Al N1 (b)和Mg-Al N2 (c)的傅里叶红外光谱图 Fig.2 FT-IR spectra of pure Mg-Al DS (a), Mg-Al N1 (b) and Mg-Al N2 (c) |
氨基负载量是影响固体材料CO2吸附性能的重要指标。复合氨基改性Mg-Al LDH的C、H、N、S元素的质量百分含量由元素分析仪测定,通过改性前后N元素质量百分含量的变化,可计算出LDHs的氨基负载量(氨基负载量= N元素的质量百分数×1000/14)。表 1为不同氨基硅烷加入量下制备的复合氨基改性Mg-Al LDH的元素分析结果,由表可知,未改性的Mg-Al LDH,其N元素质量百分含量约为0,氨基改性后,N元素含量显著增加,结合EA和FT-IR表征结果推测改性后LDHs中N元素是以氨基的形式存在;随着剥落再改性过程氨基硅烷加入量的增加,复合氨基改性Mg-Al LDH的氨基负载量增大,氨基硅烷按氨基硅烷和甲苯体积比4:100加入时制备的Mg-Al LDH氨基负载量达到饱和;对比第1、2、7组和第1、9、14组数据发现,每经过一次改性,LDHs的氨基负载量都有较大幅度的提高,且阴离子表面活性剂法和超声剥落法对氨基负载量的提高贡献相当;对于Mg-Al N1,氨基负载量最高可达4.80 mmol·g-1,与Wang等[6]采用阴离子表面活性剂法、以相同氨基硅烷为改性剂制备的氨基改性Mg-Al LDH最高氨基负载量3.60 mmol·g-1相比,氨基负载量提高了33.3%;对于Mg-Al N2,氨基负载量最高可达6.20 mmol·g-1,与姜哲等[8]采用相同氨基硅烷为改性剂制备的氨基改性Mg-Al LDH最高氨基负载量2.76 mmol·g-1相比,氨基负载量提高了125%。这均表明采用复合改性法可有效提高LDHs的氨基负载量,相较于剥落法和阴离子表面活性剂法等氨基改性方法优势显著。
|
|
表 1 氨基改性Mg-Al LDH的元素分析结果 Table 1 Elemental analysis of amine modified Mg-Al LDHs |
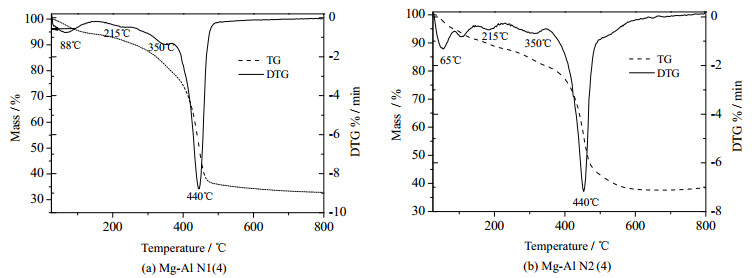
采用热重分析仪测量了复合氨基改性Mg-Al LDH的热稳定性,其结果如图 3所示。由图可知,TG曲线显示有两个主要的失重阶段。第一阶段20~105℃,共失重4.5%~6.5%,这个阶段的失重主要来自于样品上的水分和吸附的CO2[9],(a)和(b)中第一个失重峰的温度不同是由两种氨基硅烷性质不同引起的,而(b)中多一个峰可能是因为N2既含有伯胺也含有仲胺,存在两个CO2脱附温度。第二阶段105~800℃,共失重55%~62.5%,此阶段的失重来自于阴离子表面活性剂和氨基硅烷的碳链分解。DTG曲线上215℃的失重峰来自于LDHs的脱水反应[10],随后的350和440℃峰来自于样品中阴离子表面活性剂和氨基硅烷的碳链分解。215℃出现失水峰,说明此温度下Mg-Al N1(4)和Mg-Al N2(4)的层状结构很可能已经受到破坏。本研究过程中最高温度为180℃,复合氨基改性Mg-Al LDH在使用温度范围内具有良好的热稳定性。
|
图 3 复合氨基改性Mg-Al LDH的TG和DTG曲线 Fig.3 TG and DTG curves of amine modified Mg-Al LDHs |
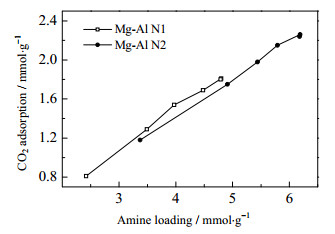
Mg-Al N1和Mg-Al N2在30℃、0.1 MPa纯CO2环境下,吸附容量随氨基负载量的变化曲线如图 4所示。由图可知,吸附剂Mg-Al N1和Mg-Al N2的吸附容量均随氨基负载量的增大而增大,对于Mg-Al N1,氨基负载量为4.80 mmol·g-1时,CO2吸附容量高达1.81 mmol·g-1,对于Mg-Al N2,氨基负载量为6.20 mmol·g-1时,CO2吸附容量高达2.26 mmol·g-1,说明复合氨基改性Mg-Al LDH具有良好的吸附性能。这是由于氨基是氨基改性固体吸附材料的吸附活性中心[11],LDHs的氨基负载量越大,吸附活性位点越多,能够吸附的CO2越多;复合改性法制备氨基改性Mg-Al LDH时,经过两次氨基改性过程,每经过一次改性,LDHs的氨基负载量都有较大幅度的提高,得到的Mg-Al LDH相较于一次改性产物具有更高的氨基负载量,因而具有更好的吸附性能。相同氨基负载量下,Mg-Al N1的CO2吸附容量比Mg-Al N2大,这是由于N-氨乙基-γ-氨丙基三甲氧基硅烷(N2)除了含有伯胺外,还含有仲胺和亚甲基,较长的碳链使其内部的氨基不容易接触到CO2分子,氨基利用率低,抑制了吸附。Wang等[7]也发现,N-氨乙基-γ-氨丙基三甲氧基硅烷的氨基利用率比3-氨丙基三甲氧基硅烷低。
|
图 4 Mg-Al N1和Mg-Al N2的CO2吸附容量随氨基负载量的变化曲线 Fig.4 CO2 adsorption capacities of Mg-Al N1 and Mg-Al N2 with different amine loadings |
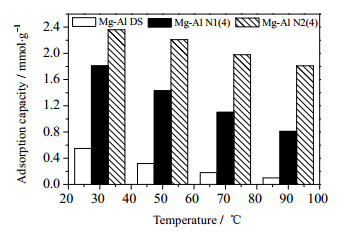
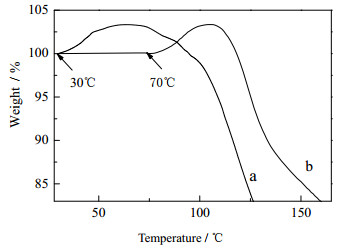
温度是影响LDHs CO2吸附性能的重要因素之一。在30、50、70和90℃、0.1 MPa、纯CO2环境下,Mg-Al DS、Mg-Al N1(4)和Mg-Al N2(4)的CO2吸附容量如图 5所示。由图可知,LDHs的CO2吸附容量随温度的升高而降低,这是由于该反应为放热反应,升高温度不利于吸附的进行;图 6为3-氨丙基三甲氧基硅烷(N1)和N-氨乙基-γ-氨丙基三甲氧基硅烷(N2)在纯CO2环境下的TG曲线,由图可知,N1在30℃下质量开始增加,N2在70℃以后质量才逐渐增加,这是由于伯胺位点和仲胺位点对CO2的吸附具有不同的初始反应温度,仲胺位点的更高[7],同时N2在30~70℃质量增加不明显,可能是因为N2的黏性较大,在低温下阻碍了CO2的传质。所以N1适合低温吸附,N2在高温下更具优势,这也解释了随着温度的升高Mg-Al N2的CO2吸附容量下降趋势比Mg-Al N1更为缓慢的现象。Mg-Al N2在90℃、0.1 MPa CO2环境下,其吸附容量高达1.79 mmol·g-1,因此,具有用于电厂烟道气吸附的潜能。
|
图 5 Mg-Al DS、Mg-Al N1(4)和Mg-Al N2(4)在不同温度下的CO2吸附容量 Fig.5 CO2 adsorption capacities of Mg-Al DS, Mg-Al N1(4) and Mg-Al N2(4) at different temperatures |
|
图 6 氨基硅烷N1(a)和N2(b)在纯CO2环境下的TG曲线 Fig.6 TG profiles of aminosilanes N1(a) and N2(b) under CO2 atmosphere |
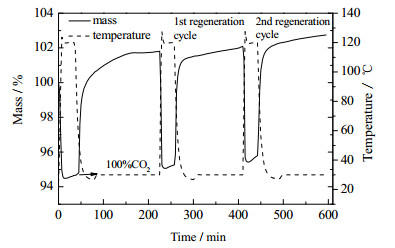
吸附剂的循环再生是工业过程的重点研究内容,吸附剂的循环使用性能是评价吸附剂好坏的重要指标。脱附温度对脱附效果及吸附剂的活性影响很大。因此,以前期实验中具有较佳吸附性能的吸附剂Mg-Al N2(4)为研究对象,选择了4个不同的吸附温度(30、50、70和90℃)和脱附温度(120、140、160和180℃)进行组合,对其脱附性能及高温下吸附剂的活性进行了研究。图 7为吸附剂再生的一个实例。Mg-Al N2(4)在氮气气氛中经过140℃脱水除杂处理,降温至30℃,同时气氛变为纯CO2,CO2气体引入后,吸附剂Mg-Al N2(4)的质量开始增加,150 min后,将Mg-Al N2(4)的温度迅速提高至脱附温度(120℃);经过30 min脱附过程,Mg-Al N2(4)的温度再次降到吸附温度进行吸附,完成一个完整的吸附/脱附过程。针对每组吸附脱附温度,共进行两次吸附脱附过程。Mg-Al N2(4)的CO2吸附容量由吸附脱附的质量差计算得到。
|
图 7 Mg-Al N2(4)的质量和温度随时间的变化 Fig.7 TG mass and temperature curves as a function of time for Mg-Al N2 |
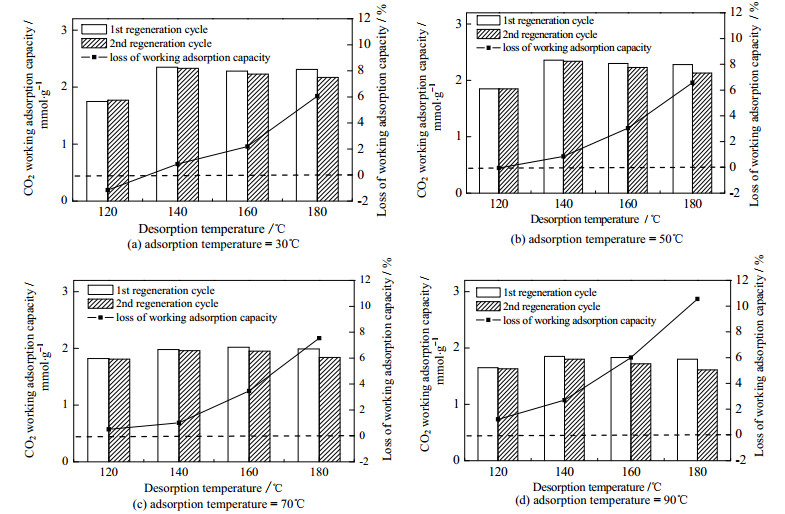
图 8为不同吸附和脱附温度下Mg-Al N2(4)的CO2吸附容量和吸附剂失活情况对比图。由图可知,在所选择的4个脱附温度中,120℃下进行脱附时,吸附剂的CO2吸附容量比其它温度的低,经分析这是由于120℃下Mg-Al N2(4)吸附的CO2未脱附完全,仍有部分CO2吸附在LDHs表面。脱附温度高于140℃,吸附剂开始失活,随着脱附温度的升高,吸附剂的失活率(吸附剂的失活率=吸附剂第一次和第二次循环使用后的吸附容量的差值/吸附剂第一次循环使用后的吸附容量)急剧增加,脱附温度为180℃时,失活率高达10.56%,这可能是氨基官能团在高温下部分分解造成的[6]。因此,从节约能源、脱附效果及吸附剂的活性等方面综合考虑,脱附温度应在140℃左右。
|
图 8 吸附脱附温度对Mg-Al N2(4)的CO2吸附容量和吸附剂失活的影响 Fig.8 Effects of adsorption/desorption temperature on CO2 adsorption capacity and deactivation of Mg-Al N2(4) |
在脱附温度140℃,吸附温度为30℃情况下,研究了吸附剂Mg-Al N2(4)的循环使用性能,结果如图 9所示。由图可知,循环使用5次后,吸附剂Mg-Al N2(4)的CO2吸附容量基本不变,显示了良好的吸附性能和重复使用性能。
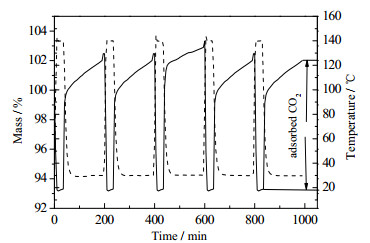
|
图 9 吸附剂的循环使用性能 Fig.9 Adsorption/desorption cycling results of Mg-Al N2(4) |
采用复合改性法成功将3-氨丙基三甲氧基硅烷(N1)和N-乙基-γ-氨丙基三甲氧基硅烷(N2)接枝到层状双氢氧化物表面,相较于剥落法和阴离子表面活性剂法等常用的氨基改性方法,制备的Mg-Al LDH具有更高的氨基负载量。Mg-Al LDH的CO2吸附容量随氨基负载量的增大而增大,当氨基负载量为4.80 mmol·g-1,30℃、CO2为0.1 MPa时,Mg-Al N1吸附容量高达1.81 mmol·g-1;当氨基负载量为6.20 mmol·g-1,30℃、CO2为0.1 MPa时,Mg-Al N2吸附容量高达2.26 mmol·g-1。随着吸附温度的升高,层状双氢氧化物的吸附容量下降,当氨基负载量为6.20 mmol·g-1,90℃、CO2为0.1 MPa时,Mg-Al N2的吸附容量仍达1.79 mmol·g-1,具有电厂烟道气吸附的潜能。吸附脱附循环再生实验显示,Mg-Al N2在140℃下脱附完全,重复使用5次后,吸附性能基本保持不变,显示了良好的重复使用性能。
| [1] | Li F, Duan X. Applications of layered double hydroxides[J]. Cheminform , 2006, 37(24): 193-223. |
| [2] | Wang Q, Hui H T, Guo Z, et al. Morphology and composition controllable synthesis of Mg-Al-CO3 hydrotalcites by tuning the synthesis pH and the CO2 capture capacity[J]. Applied Clay Science , 2012, 55(1): 18-26. |
| [3] | Iruretagoyena D, Shaffer M S P, Chadwick D. Adsorption of carbon dioxide on graphene oxide supported layered double oxides[J]. Adsorption Journal of the International Adsorption Society , 2014, 20(2-3): 321-330. DOI:10.1007/s10450-013-9595-3. |
| [4] | Garciagallastegui A, Iruretagoyena D, Gouvea V, et al. Graphene oxide as support for layered double hydroxides:enhancing the CO2 adsorption capacity[J]. Chemistry of Materials , 2012, 24(23): 4531-4539. DOI:10.1021/cm3018264. |
| [5] | Garciagallastegui A, Iruretagoyena D, Mokhtar M, et al. Layered double hydroxides supported on multi-walled carbon nanotubes:preparation and CO2 adsorption characteristics[J]. Journal of Materials Chemistry , 2012, 22(28): 13932-13940. DOI:10.1039/c2jm00059h. |
| [6] | Wang J W, Stevens L A, Drage T C, et al. Preparation and CO2 adsorption of amine modified layered double hydroxide via anionic surfactant-mediated route[J]. Chemical Engineering Journal , 2012, 181-182(2): 267-275. |
| [7] | Wang J W, Stevens L A, Drage T C, et al. Preparation and CO2 adsorption of amine modified Mg-Al LDH via exfoliation route[J]. Chemical Engineering Science , 2012, 68(1): 424-431. DOI:10.1016/j.ces.2011.09.052. |
| [8] | JIANG Zhe (姜哲). Study on CO2 capture using layered double hydroxides as adsorbents (层状双氢氧化物吸附捕集温室气体CO2)[D]. Hangzhou (杭州): Zhejiang University of Technology (浙江工业大学), 2014. http://www.wanfangdata.com.cn/details/detail.do?_type=degree&id=Y2622673 |
| [9] | Gray M L, Hoffman J S, Hreha D C, et al. Parametric study of solid amine sorbents for the capture of carbon dioxide[J]. Energy & Fuels , 2009, 23(10): 4840-4844. |
| [10] | Tao Q, He H, Frost R L, et al. Nanomaterials based upon silylated layered double hydroxides[J]. Applied Surface Science , 2009, 255(7): 4334-4340. DOI:10.1016/j.apsusc.2008.11.030. |
| [11] | Zhao H L, Hu J, Wang J J, et al. CO2 capture by the amine-modified mesoporous materials[J]. Acta Physico-Chimica Sinica , 2007, 23(6): 801-806. DOI:10.1016/S1872-1508(07)60046-1. |




