近年来新型冠状病毒感染成为危害人类健康的重要事件,疫苗起到了至关重要作用[1]。mRNA疫苗凭借高保护率和快速研发效率,得到了广泛关注[2]。对比灭活和减毒疫苗,mRNA疫苗能精确表达抗原、可产生更为强烈的免疫反应[3];相对DNA疫苗和病毒载体疫苗,mRNA疫苗具有蛋白表达可预测性[4]、低免疫原性[5]、避免宿主基因组整合风险等优势[6];此外,mRNA疫苗生产平台灵活性强、流程易标准化[7]。mRNA不仅可以作为预防疫苗,还可用于很多疾病治疗,例如流感病毒[8]、HIV病毒[9]等引发的传染性疾病,以及非小细胞肺癌、胶质母细胞瘤等癌症[10]。预计2035年mRNA市场将达到230亿美元[11]。
mRNA制备包括RNA聚合酶催化下的体外转录反应和下游生物分离纯化[12-13]。T7 RNA聚合酶是使用最为广泛的体外转录反应合成酶[14],但转录后包含较多副产物和残留物,如流产性转录起始物、双链RNA(dsRNA)、酶、转录模板DNA、未反应的核苷酸等[15]。下游生物分离纯化过程通常包含捕获和精制2个阶段[16]。对于复杂的mRNA体外转录混合物体系,由于具有3’末端多聚腺嘌呤核糖核苷酸(poly(A))这一尾部特征结构,高选择性的亲和层析是最适合的捕获方法[17-18]。目前mRNA亲和层析分离采用的配基主要有2种,寡脱氧胸腺苷酸(Oligo(dT))和多尿苷酸(poly(U))。研究表明,对于配基为poly(U)的亲和层析介质,poly(U)与含poly(A)的mRNA结合能力较强,但洗脱时需升温至65 ℃以上才能达到较高的回收率[19],且还需额外添加减少非特异性吸附的物质,如尿素、甲酰胺等[20];对于配基为Oligo(dT)的亲和层析介质,Oligo(dT)吸附mRNA后常温下用去离子水洗脱即可达到87% 的收率[21]。因此,绝大多数商业化mRNA亲和层析介质的配基采用Oligo(dT),表 1汇总了现有Oligo(dT)亲和层析介质的基本信息和动态结合载量情况,表中,dp为介质微球粒径,μm;dpore为介质微球平均孔径,nm;DBC为以层析柱体积为基准计的亲和层析介质动态结合载量,mg⋅mL−1。
|
|
表 1 常见的商业化Oligo(dT)亲和层析介质 Table 1 Typical commercial Oligo(dT) affinity resins |
由表 1可见,与文献[26]中蛋白A亲和层析介质50~80 mg⋅mL−1的DBC值相比,现有的Oligo(dT)亲和层析介质的DBC值普遍较低,难以满足规模化mRNA分离的需求[7]。因此,研发高载量的Oligo(dT)亲和层析介质非常重要,但目前缺乏对Oligo(dT) 亲和层析介质载量影响机制的探究。本研究将以poly(A)为模型分子,对比不同的Oligo(dT)亲和层析介质的静态吸附平衡、吸附动力学和DBC等性质,借助激光扫描共聚焦显微镜(CLSM)表征poly(A)在介质微球内的分布,结合理论计算分析介质载量的影响因素及相关机制,为高载量Oligo(dT)亲和层析介质的研发提供依据。
2 材料与方法 2.1 主要材料与仪器主要试剂:poly(A)(货号P9403,动态光散射测得的水力学直径约为6.8 nm),Sigma-Aldrich公司;Ribogreen荧光染料,上海闪晶分子生物科技有限公司;Poros Oligo (dT)25、Praesto Jetted(dT)25、NanoGel dT20和Monomix dT20等4种Oligo(dT)亲和层析介质的相关信息见表 1。这4种介质的基质种类不同,其中前3种介质的基质材料为聚苯乙烯,第4种介质的基质材料为聚甲基丙烯酸酯。
主要仪器:ÄKTApurifier 10 plus层析系统,GE Healthcare Life Sciences公司;Unano-1000微量分光光度计,杭州优米仪器有限公司;MultiScreenHTS真空抽滤系统(MSVMHTS00)和过滤板(MmtiScreen HTS BV),Millipore公司;恒温混匀仪,杭州奥盛仪器有限公司;Tricorn 5/50层析柱(5 mm×50 mm),Cytiva公司;激光扫描共聚焦显微镜(OLYMPUS IX83-FV3000),Olympus公司;纳米粒度电位分析仪(Malvern Zetasizer Nano-ZS ZEN3600),Malvern公司;压汞仪(AutoPore IV 9510),Micromeritics公司。
2.2 吸附条件筛选方法考察不同pH值、盐浓度对4种Oligo(dT) 亲和层析介质的吸附性能的影响:5种pH值分别为5.0、6.0、7.0、8.0、9.0;4种氯化钠浓度分别为0、200、400、600 mmol⋅L−1。不同pH值的缓冲液分别为20 mmol⋅L−1的柠檬酸盐缓冲液(pH值为5.0)、20 mmol⋅L−1的磷酸盐缓冲液(pH值分别为6.0和7.0)和20 mmol⋅L−1三羟甲基氨基甲烷(Tris)缓冲液(pH值分别为8.0和9.0)。不同盐浓度的缓冲液由1 mol⋅L−1的NaCl缓冲液与相应无盐缓冲液按不同比例配制而成。
采用96孔过滤板进行静态平衡吸附量Q*测定[27],具体步骤如下:第1步,将poly(A)溶解于缓冲液中,使之质量浓度为1.5 mg⋅mL−1,260 nm波长下精确测定poly(A) 初始质量浓度ρ0(mg⋅mL−1);第2步,用去离子水冲洗亲和层析介质,抽滤15 min,精确称重后转移至量筒内,静置过夜,加入适量的去离子水,配成介质体积比为10%的重悬浮介质匀浆液,将96孔过滤板的每孔加入100 μL (含10 μL介质)该介质匀浆液;第3步,用200 μL缓冲液平衡该介质3次,真空抽滤,去除缓冲液;第4步,将100 μL不同条件下的poly(A)溶液加入过滤板样品孔中,用封板膜密封过滤板的顶部和底部,在25 ℃、1 200 r⋅min−1转速下恒温震荡3 h;第5步,吸附平衡后,真空抽滤,收集滤液,260 nm波长下测定滤液中poly(A)平衡质量浓度ρ*(mg⋅mL−1),根据物料平衡计算亲和层析介质的Q*,Q*为以1g介质为基准计的poly(A)静态平衡吸附量,mg⋅g−1。
2.3 静态吸附等温线测定方法测定4种亲和层析介质的吸附等温线的方法如下:将poly(A)溶解于结合缓冲液,制备出质量浓度为4.0 mg⋅mL−1的母液,结合缓冲液含10 mmol⋅L−1 Tris、0.6 mol⋅L−1 NaCl、1 mmol⋅L−1乙二胺四乙酸(EDTA),pH=7.0。然后将母液依次稀释至质量浓度为3.2、2.4、1.6、0.8、0.4、0.2 mg⋅mL−1。用96孔过滤板的每列8个样品孔考察特定的介质,每个浓度使用3个平行孔,每孔加入100 μL重悬浮的介质匀浆液(含介质10 μL),用缓冲液冲洗3次,真空抽滤,去除缓冲液。将100 μL不同质量浓度的poly(A)溶液添加到相应的过滤板样品孔中,密封过滤板,在25 ℃、1 200 r⋅min−1转速下恒温震荡3 h,后续操作参照2.2节进行。用Langmuir-Freundlich方程拟合吸附等温线,具体表达式如下[28]:
| $ {Q^*} = \frac{{K{\rho ^{ * b}}}}{{1 + K{\rho ^{ * b}}}} \times {Q_{\text{m}}} $ | (1) |
式中:Qm为最大静态吸附容量,mg⋅g−1;K为亲和力常数,(mL⋅mg−1)b;b为经验常数。
由于较多的亲和层析介质在poly(A) 的测试质量浓度范围内Q*无法达到吸附等温线的平台区域,因此,本研究以ρ*为1 mg⋅mL−1时对应的静态平衡吸附量QC (mg⋅g−1)为参考,比较各介质对poly(A)的吸附能力[29]。
2.4 吸附动力学研究方法4种亲和层析介质对poly(A)的吸附动力学研究方法如下:96孔过滤板的每孔加入100 μL重悬浮的介质匀浆液(含介质10 μL),共使用6个样品孔。用结合缓冲液洗涤介质3次,将100 μL、ρ0为1.5 mg⋅mL−1的poly(A)溶液添加到1#孔内,用封板膜密封孔的上、下端,25 ℃、1 200 r⋅min−1转速下恒温振荡。以1#孔开始震荡为0时刻,分别在0、20、40、50、55、59 min将相同的poly(A)溶液添加到1~6#孔内,连续恒温振荡孵育共60 min。最后,真空抽滤,收集滤液,测定滤液中poly(A) 质量浓度ρ(mg⋅mL−1),得到ρ/ρ0随时间变化的吸附动力学曲线。
2.5 穿透曲线和动态结合载量测定方法使用10% 穿透的DBC (DBC10%)来表征4种亲和层析介质在层析柱内的动态吸附性能。Tricorn 5/50层析柱装填约0.5 mL介质,柱高约20 mm。用结合缓冲液充分平衡床层,直至UV260nm响应接近基线,分别在50、100、150 cm⋅h−1等流速下测定poly(A)穿透曲线,poly(A)料液质量浓度为1.0 mg⋅mL−1,按特定时间段分管收集出口样品,260 nm波长下测定收集液中poly(A)质量浓度,设定达到90% 穿透比例时终止上样,绘制穿透曲线,根据DBC10%值来确定亲和层析介质的动态结合载量。
2.6 介质吸附的微观观测采用CLSM观察poly(A)在4种亲和层析介质中的吸附过程。类似2.4节实验方法,吸附时间分别为1、5、10、20、40、60 min,以未吸附poly(A)的介质微球作为对照组,完成吸附后,真空抽滤。将介质用结合缓冲液冲洗3次,真空抽滤,配制成100 μL匀浆液(含10 μL介质)。取匀浆液10 μL,与100 μL稀释了133倍的Ribogreen染液[30]在25 ℃、1 200 r⋅min−1转速下避光振荡孵育1 h。
用CLSM观察亲和层析介质内poly(A)的分布。选择处于平均粒径附近的介质微球,选取介质微球的最大截面处,采集2维共聚焦图像。镜头选择60倍油镜、激光波长为488 nm、激光强度为饱和能量的0.1%~0.3%、光电倍增管值设为800 V、共聚焦图像的尺寸为1 024像素×1 024像素,图片经ImageJ软件处理。
2.7 静态吸附容量理论计算以典型的分子大小和平均分子量的mRNA(10 nm和100 kDa,30 nm和300 kDa,40 nm和600 kDa)为模型分子,忽略mRNA分子间的相互作用力和传质阻力,只考虑mRNA水力学直径的影响,并在单分子层吸附前提下,模拟计算亲和层析介质对mRNA的静态吸附容量Qcal(mg⋅g−1),分析dp和dpore对Qcal的影响,并比较多孔微球对mRNA的内表面静态吸附容量Qin和外表面静态吸附容量Qex。计算式如下[28]:
| $ {a_{{\text{ex}}}}{\text{ = }}\frac{{6 \times (1-\varepsilon )}}{{{d_{\text{p}}}}} $ | (2) |
| $a_{\text {in }}=\frac{4000 \times(1-\varepsilon) \times \varepsilon_{\mathrm{p}}}{d_{\text {pore }}}$ | (3) |
| $Q_{\text {cal }}=4 \times 10^{18} \times \frac{\left(a_{\mathrm{ex}}+a_{\text {in }}\right) \times M_{\mathrm{a}}}{\pi d^2 \times N_{\mathrm{A}} \times m \times \mathrm{CF}}$ | (4) |
式中:aex、ain分别为以1 mL柱体积为基准计的微球外、内比表面积,m2⋅mL−1;ε为柱空隙率;εp为微球孔隙率;Ma为mRNA的平均分子量,kDa;d为mRNA水力学直径,nm;NA为阿伏伽德罗常数,mol−1;m为1 μL介质对应的干重,mg⋅μL−1;CF为柱压缩因子。
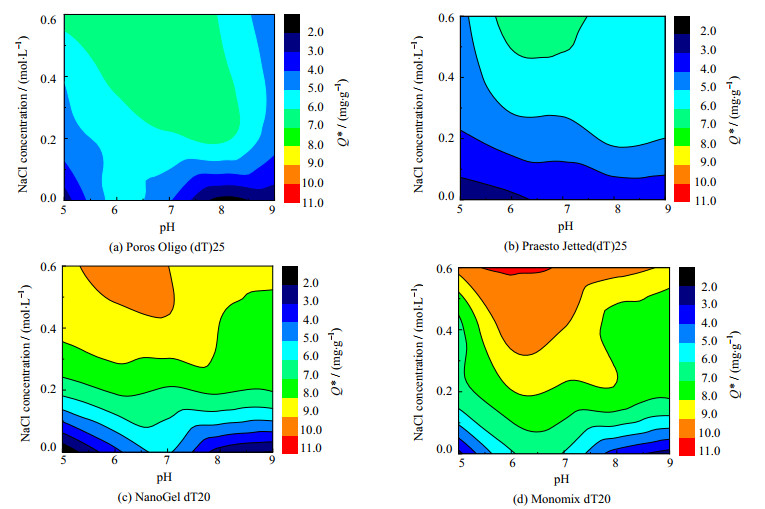
3 结果与讨论 3.1 吸附条件筛选不同pH和NaCl浓度条件下,Poros Oligo (dT)25、Praesto Jetted(dT)25、NanoGel dT20和Monomix dT20等4种亲和层析介质对poly(A)的Q*如图 1所示。由图 1可见,4种亲和层析介质对poly(A)的Q*值均随NaCl浓度增大而增大,这主要是因为,NaCl浓度增大对静电作用产生屏蔽效应,减弱了Oligo(dT)配基与poly(A)磷酸基团之间的电荷斥力,两者之间的碱基更容易形成氢键,从而促进了与poly(A)结合。研究中还发现,NaCl浓度过高时,poly(A)易形成沉淀,因此选用0.6 mol⋅L−1作为合适的NaCl上样浓度。由图 1还可见,高NaCl浓度下、pH=6.0~7.0时,4种亲和层析介质对poly(A)均有较高的Q*值。这是因为,弱酸性条件可能降低poly(A)磷酸基团的电离度、减小核酸带电荷量,促进Oligo(dT)配基与poly(A)之间的氢键形成。由图 1还可见,低NaCl浓度下、pH=5.0或pH=9.0时,Q*值急剧下降。可能由于在较强的酸性条件下(pH=5.0),碱基中的N原子被质子化,氢键形成更加困难;而在碱性条件下(pH=9.0),poly(A)的磷酸基团所带的负电荷量增大,Oligo(dT)配基与poly(A)之间的电荷排斥作用增强,导致与poly(A)难以结合。
|
图 1 不同pH和NaCl浓度条件下4种亲和层析介质对poly(A)的Q*比较 Fig.1 Poly(A) adsorption capacities of the four affinity resins under different pH and NaCl concentrations |
基于上述不同pH和NaCl浓度下的Q*值分析,可确定4种亲和层析介质合适的上样条件均为NaCl浓度为0.6 mol⋅L−1、pH值为6.0~7.0。
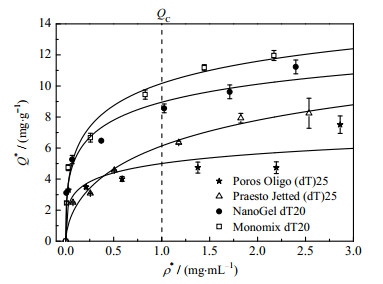
3.2 静态吸附等温线及模型拟合基于3.1节的实验结果,为了比较不同亲和层析介质的Qm,如图 2所示,测定了pH=7.0、0.6 mol⋅L−1 NaCl条件下4种亲和层析介质的吸附等温线,并采用Langmuir-Freundlich方程进行拟合,得到的拟合参数列于表 2。
|
图 2 4种亲和层析介质对poly(A)的吸附等温线及Langmuir- Freundlich模型拟合曲线(pH =7.0、0.6 mol⋅L−1 NaCl) Fig.2 Poly(A) adsorption isotherms of the four affinity resins at pH=7.0 and 0.6 mol⋅L−1 NaCl and the corresponding Langmuir-Freundlich model fitting profiles |
|
|
表 2 4种亲和层析介质的吸附等温线Langmuir- Freundlich模型拟合参数 Table 2 Fitting results of adsorption isotherms of the four affinity resins with Langmuir-Freundlich model |
由图 2可见,Q*随ρ*增大而变大,且增长幅度逐渐变小,但吸附等温线最终并没有达到平稳阶段,这可能是核酸特有的吸附现象。随着更多的poly(A)被吸附,介质微球表面所带负电荷量增加,对溶液中游离的poly(A)静电斥力增强,且在吸附接近饱和时,核酸分子之间的空间位阻对poly(A)的吸附行为影响较大。因此,吸附等温线并不符合Langmuir方程[31],但Langmuir-Freundlich方程拟合效果较好[21]。
由表 2可见,Poros Oligo (dT)25和Praesto Jetted(dT)25这2种亲和层析介质的静态吸附容量较低(QC分别为4.9和6.1 mg⋅g−1),这可能是由于其dpore相对较大,导致其可及吸附表面积减小。由表 2还可见,相比于其他3种亲和层析介质,Praesto Jetted(dT)25的K值(0.578) 最小,且QC/Qm值小于40%,需要更高的poly(A) 质量浓度来达到较大的Q*值,可能是介质的配基密度、间隔臂等因素导致其对poly(A)的亲和力较弱。由图 2可见,当ρ*较高时(ρ* > 2.86 mg⋅mL−1),Poros Oligo (dT)25介质的Q*有较大幅度增大,这说明高ρ*值可能导致吸附机理发生改变[21]。
由表 2可见,Monomix dT20和NanoGel dT20这2种亲和层析介质的静态吸附容量较大(QC分别为10.2和9.0 mg⋅g−1)。经分析,主要有以下2种解释:一是poly(A)可扩散进入这2种介质微球的孔道内,而且由于其dpore较小,可及吸附表面积大,导致静态吸附容量较高;二是poly(A)难以扩散至介质微球内部孔道,主要在微球表层吸附,由于Monomix dT20的dp(30 μm)比其他3种亲和层析介质(均为50 μm)小,故拥有较大的比表面积,从而静态吸附容量最大,而NanoGel dT20可能配基密度较高,表面可及吸附位点多,导致较大的静态吸附容量。这2种亲和层析介质的K值均接近1.00、QC/Qm值接近50%,对poly(A)的亲和性较强。原因可能是,这2种亲和层析介质的配基为dT20,链长小于Poros Oligo (dT)25和Praesto Jetted(dT)25介质的dT25,所带负电荷量较小,对poly(A)的排斥力较小,故亲和力较强。此外,间隔臂分子结构及其长度等因素也可能影响亲和层析介质的亲和力[21]。
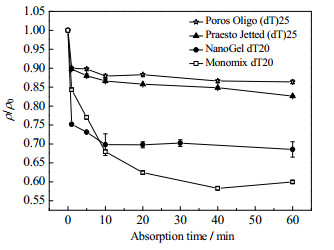
3.3 吸附动力学为了进一步探究poly(A)在4种亲和层析介质微球中吸附行为的差异,考察pH=7.0、0.6 mol⋅L−1 NaCl条件下4种亲和层析介质对poly(A)的吸附动力学,结果如图 3所示。
|
图 3 4种亲和层析介质对poly(A)吸附动力学曲线比较(pH=7.0、0.6 mol⋅L−1 NaCl) Fig.3 Poly(A) adsorption kinetics of the four affinity resins at pH 7.0 and 0.6 mol⋅L−1 NaCl |
由图 3可见,Poros Oligo (dT)25、Praesto Jetted(dT)25和NanoGel dT20这3种亲和层析介质吸附poly(A)过程中,ρ/ρ0变化主要集中在前1 min。经推测,介质与poly(A)结合主要为对流传质主导的微球表层吸附,而微球内部扩散传质主导的孔内吸附较少,因而传质阻力小,达到吸附平衡所需时间短。由图 3还可见,Monomix dT20吸附poly(A)过程中,ρ/ρ0的大幅度变化持续了约20 min,40 min后趋于稳定,达到吸附平衡。这表明,在Monomix dT20介质中可能同时存在poly(A)的表层吸附和深层孔扩散吸附,而微球内部传质阻力较大,达到吸附平衡时间较长。相比于其他3种介质,dpore最小的Monomix dT20介质中存在poly(A)的深层孔扩散吸附,可能与其聚甲基丙烯酸酯的基质材料有关。由图 3还可见,在前1 min内,NanoGel dT20介质溶液的ρ/ρ0变化最大,可能是由于该介质的配基链长、间隔臂长度等因素导致介质与poly(A)的亲和性更强;此外,配基密度高也可使该介质吸附poly(A)分子多。
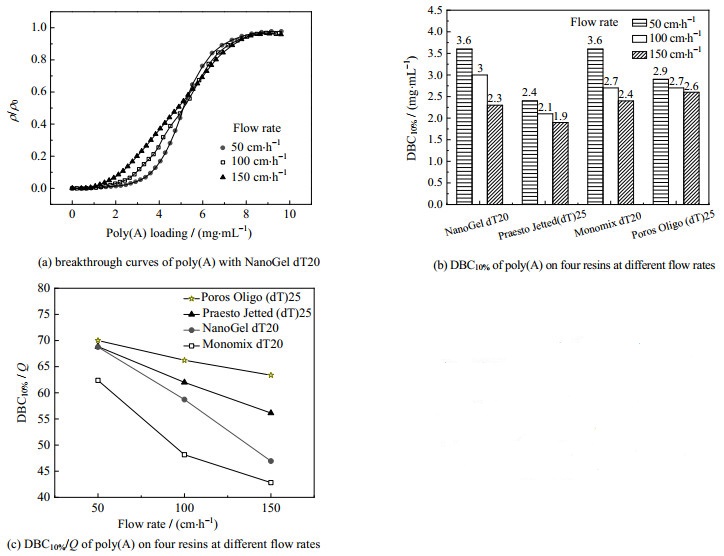
3.4 动态结合载量采用DBC10%表征4种亲和层析介质在层析柱内分离过程的动态吸附性能,考察流速对亲和层析介质动态吸附过程的影响,并用DBC10%/Q (Q为上样条件下的静态平衡吸附量,mg⋅mL−1)表征传质阻力。3种流速下NanoGel dT20的穿透曲线、4种亲和层析介质在pH=7.0和0.6 mol⋅L−1 NaCl条件下的DBC10%和DBC10%/Q实验结果见图 4。
|
图 4 NanoGel dT20穿透曲线及4种亲和层析介质吸附poly(A)的动态吸附性能比较(pH=7.0、0.6 mol⋅L−1 NaCl) Fig.4 Breakthrough curves of the NanoGel dT20 resin and dynamic poly(A) adsorption performance of the four affinity resins at different flow rates (pH=7.0, 0.6 mol⋅L−1 NaCl) |
由图 4(b)、(c)可见,NanoGel dT20和Monomix dT20这2种亲和层析介质对poly(A)的DBC10%值较高,且受流速影响较明显,DBC10%/Q随流速增加而大幅度下降。由前文可知,Monomix dT20的Q值比NanoGel dT20高,但图 4(b)显示DBC10%值却与NanoGel dT20接近,可能由于Monomix dT20介质的dpore相对较小,大部分poly(A)分子由于停留时间短、扩散传质阻力大等原因而未能扩散至介质微球内部孔中,仅在微球表层吸附,导致DBC10%没有明显高于NanoGel dT20;而且,随着流速增大,Monomix dT20介质中的poly(A)的扩散时间缩短,导致其DBC10%/Q大幅度下降。而NanoGel dT20仅依靠微球表层的poly(A)吸附就能达到较高的DBC10%值,这可能与其具有比Monomix dT20稍大的dpore、较小的扩散传质阻力、较大的可及吸附表面积有关,此外配基密度、配基长度和间隔臂等性质也会影响其DBC10%,该结果与3.3节的推论相符。至于NanoGel dT20的DBC10%/Q受流速影响较大,分析原因可能是由于介质配基密度较高,导致基球带电荷量较大,对poly(A)的静电排斥力更强,影响了配基对poly(A)的吸附动力学,故传质阻力更大,吸附所需时间更长。正如Vanjur等[31]报道,固定在表面的DNA探针密度会影响其与目标互补链的静电斥力,改变吸附平衡和吸附动力学。
由图 4(b)、(c)还可见,Praesto Jetted(dT)25和Poros Oligo (dT)25这2种亲和层析介质对poly(A)的DBC10%相对略低,这可能与其dpore较大导致的可及吸附表面积较小有关。由3.2节可知,Praesto Jetted(dT)25的Q值高于Poros Oligo (dT)25,但图 4(b)显示DBC10%值却较小,可能也是由于微球表面高配基密度影响了配基对poly(A)的吸附动力学。由图 4(c)可见,随着流速增加,这2种亲和层析介质的DBC10%/Q值变化幅度不大,表明传质阻力并没有随流速的增加而明显增加,推测是由于这2种亲和层析介质对poly(A)的吸附主要为表层吸附,扩散传质所占比例较小,总传质速率受流速影响较小。
由图 4(c)还可见,在低流速下(50 cm⋅h−1),Poros Oligo (dT)25、Praesto Jetted(dT)25和NanoGel dT20这3种亲和层析介质的DBC10%/Q值都接近70%,且均高于Monomix dT20,表明这3种亲和层析介质的传质阻力较小、总传质速率较高,进一步推测,这3种亲和层析介质对poly(A)的吸附主要为对流传质主导的表层吸附,而Monomix dT20介质则主要为表层吸附和微球深层孔扩散吸附,与3.3节的结论一致。
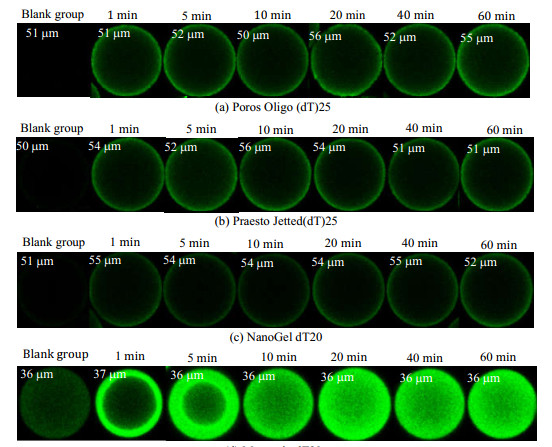
3.5 CLSM结果及分析借助CLSM分析,从微观视角考察4种亲和层析介质微球中poly(A)的分布状态及其随时间变化情况,结果如图 5所示。结合此宏观吸附实验结果分析不同亲和层析介质的吸附特性。
|
图 5 4种亲和层析介质吸附poly(A)随时间变化的CLSM结果 Fig.5 CLSM profiles of poly(A) adsorption as a function of time by the four affinity resins |
由图 5(a)~(c)可见,绿色荧光主要分布在介质微球表层,表明poly(A)主要吸附在Poros Oligo (dT)25、Praesto Jetted(dT)25和NanoGel dT20这3种亲和层析介质的外表层,且1 min之后荧光强度没有明显变化,与3.3节结果一致,可能原因是具有较大dpore的聚苯乙烯微球内部存在较多狭窄孔道,从而阻碍了poly(A)的微球内部孔扩散。对于Monomix dT20介质(见图 5(d)),随着吸附时间延长,荧光呈环状逐渐向内扩展,表明poly(A)逐渐扩散至微球内部;20 min后微球荧光强度分布基本稳定,达到吸附平衡,与3.3节的吸附动力学变化规律一致。
3.6 静态吸附容量理论计算及分析静态吸附容量是影响介质DBC的重要参数,为了更好地探究亲和层析介质载量的主要影响因素,对不同dp、dpore下亲和层析介质微球对mRNA的Qcal进行了理论计算及分析。
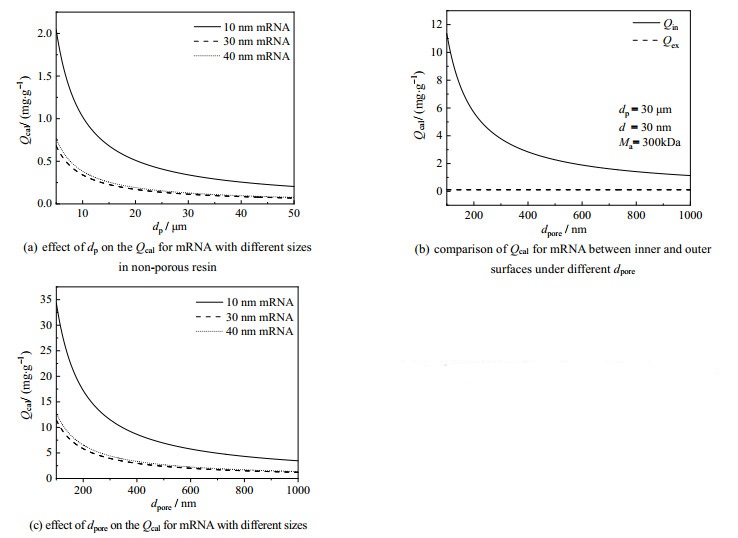
针对3种不同水力学直径的mRNA,在ε=0.4、m=0.6 mg⋅μL−1、CF=1.2条件下,且介质无孔,Qcal~dp的理论计算结果如图 6(a)所示。由图 6(a)可见,在dp=5~50 μm时,随着dp增大,Qcal下降,且Qcal值均小于3 mg⋅g−1,这是因为,对于无孔微球,mRNA仅存在表面吸附,dp越大,外表面积相对越小,从而导致较低的吸附容量。由图 6(a)还可见,mRNA的水力学直径很小时(10 nm),Qcal值较大,这是因为,较小的mRNA分子占据空间小,同样的外表面积可吸附数量更多的mRNA分子,从而Qcal值较大。由图 6(a)的Qcal值可知,仅靠介质微球的表面吸附无法达到较高的mRNA静态吸附容量。
|
图 6 介质微球的dp和dpore对mRNA的Qcal影响的理论计算结果 Fig.6 Theoretical Qcal calculation results for mRNA in resins with different dp and dpore |
对于多孔亲和层析介质,假设εp= 0.5、mRNA分子均能扩散进入孔内且占据所有孔内表面,以dp=30 μm的微球为例,微球内、外表面对mRNA的Qcal~dpore理论计算结果如图 6(b)所示;针对3种不同水力学直径的mRNA,Qcal~dpore理论计算结果如图 6(c)所示。由图 6(b)可见,dpore=100~1 000 nm时,多孔介质微球的Qin是Qex的10~100倍,因此,增加微球内孔的可及吸附表面积对提升介质微球对mRNA的静态吸附容量至关重要。由图 6(c)可见,随着dpore增大,Qcal下降显著,较大的mRNA分子(30 nm和40 nm)在介质中的Qcal=1~14 mg⋅g−1,而最小的mRNA分子(10 nm) Qcal=4~35 mg⋅g−1。这是因为,dpore对介质的可及吸附表面积影响较大,dpore增大时,会导致介质微球可及吸附表面积变小,从而导致Qcal值变小。在实际吸附过程中,mRNA分子并不能扩散进入介质微球孔内,孔内的可及吸附表面积还与mRNA分子大小有关,dpore过小时,因大分子的mRNA孔扩散传质受到阻碍,可及吸附表面积减小,从而导致Qcal值减小。因此,针对不同大小的mRNA分子应定制不同孔径的微球,以达到较大的静态吸附容量和动态结合载量。
4 结语(1) 以poly(A)为模型分子,考察了4种Oligo(dT)亲和层析介质对poly(A)的吸附特性,发现最佳吸附条件均为高盐浓度和pH=6~7;
(2) 4种介质中,Monomix dT20介质的静态吸附容量最大,且poly(A)能扩散至其深层孔内,而其他3种介质中poly(A)均主要为表层吸附,静态吸附容量稍低,与CLSM荧光分布结果一致,这可能与基质材料有关。然而,Monomix dT20介质的DBC10%相对并不显著的大,可能是由于其dpore相对较小导致扩散传质阻力较大;
(3) NanoGel dT20介质与Monomix dT20介质相比,dpore稍大,扩散传质阻力小,可及吸附表面积大,两者对poly(A)的DBC10%值接近,均较高;而Poros Oligo (dT)25和Praesto Jetted(dT)25这2种介质的dpore偏大,可及吸附表面积偏小,DBC10%相对略低;
(4) 比较不同亲和层析介质的吸附特性,影响载量的主要因素有基质种类和dpore,其他因素包括配基密度、间隔臂、配基长度等。对于基质种类,聚苯乙烯基质可能孔道结构较为特别,内部存在较多狭窄孔道,导致孔扩散吸附较少,降低了Qm,但其对DBC的影响有待进一步探究;对于dpore,需要针对不同大小的mRNA分子定制不同孔径的微球,以平衡扩散传质阻力与可及吸附表面积之间的矛盾,从而有效增大静态吸附容量和动态结合载量。此外,由于本研究使用的poly(A)分子直径较小,与长链mRNA的吸附行为可能存在一定差异,相关影响有待深入研究。
| [1] |
CHEN W, ZHU F C. Challenges in the development of a vaccine against COVID-19[J]. Engineering, 2020, 6(10): 1067-1069. DOI:10.1016/j.eng.2020.08.012 |
| [2] |
THOMPSON M G, BURGESS J L, NALEWAY A L, et al. Prevention and attenuation of COVID-19 with the BNT162b2 and mRNA-1273 vaccines[J]. New England Journal of Medicine, 2021, 385(4): 320-329. DOI:10.1056/NEJMoa2107058 |
| [3] |
FAN Y J, CHAN K H, HUNG I F N. Safety and efficacy of COVID-19 vaccines: A systematic review and meta-analysis of different vaccines at phase 3[J]. Vaccines, 2021, 9(9): 989. DOI:10.3390/vaccines9090989 |
| [4] |
ISLAM M A, REESOR E K G, XU Y J, et al. Biomaterials for mRNA delivery[J]. Biomaterials Science, 2015, 3(12): 1519-1533. DOI:10.1039/C5BM00198F |
| [5] |
ZHONG Z F, MC CAFFERTY S, COMBES F, et al. mRNA therapeutics deliver a hopeful message[J]. Nano Today, 2018, 23: 16-39. DOI:10.1016/j.nantod.2018.10.005 |
| [6] |
LIU M A. A comparison of plasmid DNA and mRNA as vaccine technologies[J]. Vaccines, 2019, 7(2): 37. DOI:10.3390/vaccines7020037 |
| [7] |
ROSA S S, PRAZERES D M F, AZEVEDO A M, et al. mRNA vaccines manufacturing: challenges and bottlenecks[J]. Vaccine, 2021, 39(16): 2190-2200. DOI:10.1016/j.vaccine.2021.03.038 |
| [8] |
FELDMAN R A, FUHR R, SMOLENOV I, et al. mRNA vaccines against H10N8 and H7N9 influenza viruses of pandemic potential are immunogenic and well tolerated in healthy adults in phase 1 randomized clinical trials[J]. Vaccine, 2019, 37(25): 3326-3334. DOI:10.1016/j.vaccine.2019.04.074 |
| [9] |
GUARDO A C, JOE P T, MIRALLES L, et al. Preclinical evaluation of an mRNA HIV vaccine combining rationally selected antigenic sequences and adjuvant signals (HTI-TriMix)[J]. AIDS, 2017, 31(3): 321-332. DOI:10.1097/QAD.0000000000001276 |
| [10] |
XU S Q, YANG K P, LI R, et al. mRNA vaccine era-mechanisms, drug platform and clinical prospection[J]. International Journal of Molecular Sciences, 2020, 21(18): 6582. DOI:10.3390/ijms21186582 |
| [11] |
XIE W, CHEN B P, WONG J. Evolution of the market for mRNA technology[J]. Nature Reviews Drug Discovery, 2021, 20(10): 735-736. DOI:10.1038/d41573-021-00147-y |
| [12] |
TABOR S. DNA-dependent RNA polymerases[J]. Current Protocols in Molecular Biology, 1991, 13(1): 3.8.1-3.8.4. |
| [13] |
孙程洁, 成殷, 王冲. mRNA疫苗的研究进展及监管概述[J]. 中国药事, 2022, 36(1): 3-9. SUN C J, CHENG Y, WANG C. Research progress and regulatory overview of mRNA vaccine[J]. Chinese Pharmaceutical Affairs, 2022, 36(1): 3-9. |
| [14] |
WANG W Y, LI Y W B, WANG Y Q, et al. Bacteriophage T7 transcription system: an enabling tool in synthetic biology[J]. Biotechnology Advances, 2018, 36(8): 2129-2137. DOI:10.1016/j.biotechadv.2018.10.001 |
| [15] |
MU X, GREENWALD E, AHMAD S, et al. An origin of the immunogenicity of in vitro transcribed RNA[J]. Nucleic Acids Research, 2018, 46(10): 5239-5249. DOI:10.1093/nar/gky177 |
| [16] |
荆淑莹, 史策, 姚善泾, 等. 连续流层析及用于抗体分离的新进展[J]. 高校化学工程学报, 2021, 35(1): 1-12. JING S Y, SHI C, YAO S J, et al. Progress on continuous chromatography and its application in antibody separation[J]. Journal of Chemical Engineering of Chinese Universities, 2021, 35(1): 1-12. |
| [17] |
ARORA S, SAXENA V, AYYAR B V. Affinity chromatography: A versatile technique for antibody purification[J]. Methods, 2017, 116: 84-94. DOI:10.1016/j.ymeth.2016.12.010 |
| [18] |
RIO D C, ARES JR M, HANNON G J, et al. Enrichment of poly(A)+ mRNA using immobilized oligo(dT)[J]. Cold Spring Harbor Protocols, 2010, 2010(7): 1-3. |
| [19] |
PHILLIPS L A, PANG R H L, PARK J J, et al. Poly(U)-agarose affinity chromatography: Specific, sensitivity selectivity, and affinity of binding[J]. Preparative Biochemistry, 1980, 10(1): 11-26. DOI:10.1080/00327488008061715 |
| [20] |
OCHOA J L, KEMPF J, EGLY J M. Interaction of poly(A) with different adsorbents for affinity chromatography of nucleic acids[J]. International Journal of Biological Macromolecules, 1980, 2(1): 33-38. DOI:10.1016/0141-8130(80)90007-0 |
| [21] |
MENCIN N, ŠTEPEC D, MARGON A, et al. Development and scale-up of oligo-dT monolithic chromatographic column for mRNA capture through understanding of base-pairing interactions[J]. Separation and Purification Technology, 2023, 304: 122320. DOI:10.1016/j.seppur.2022.122320 |
| [22] |
GRINSTED J, LIDDELL J, BOULEGHLIMAT E, et al. Purification of therapeutic & prophylactic mRNA by affinity chromatography[J]. Cell & Gene Therapy Insights, 2022, 8(2): 341-355. |
| [23] |
Purolite. Praesto jetted (dT)18-DVB [EB/OL]. [2023-03-24]. http://www.tinyblog.cn/?p=4107.
|
| [24] |
Nanomicro Technology. Instructions of NanoGel dT20 [EB/OL]. [2023-03-24]. http://www.nanomicro.com/companyfile/9/#c_portalResCompanyFile_list-1615975699206-3.
|
| [25] |
Sepax Technologies. Monomix dT20 mRNA affinity resin [EB/OL]. [2023-03-24]. http://www.sepax-tech.com.cn/products/progych/proqh/2021-08-09/62.html.
|
| [26] |
FREIHERR VON ROMAN M, BERENSMEIER S. Improving the binding capacities of protein a chromatographic materials by means of ligand polymerization[J]. Journal of Chromatography A, 2014, 1347: 80-86. DOI:10.1016/j.chroma.2014.04.063 |
| [27] |
褚文宁, 林东强, 姚善泾. 基于微孔过滤板的蛋白吸附高通量筛选方法[J]. 化工学报, 2017, 68(6): 2399-2406. CHU W N, LIN D Q, YAO S J. High-throughput screening methods for protein adsorption evaluation with microtiter filter plate[J]. CIESC Journal, 2017, 68(6): 2399-2406. |
| [28] |
CARTA G, JUNGBAUER A. Protein chromatography: Process development and scale-up[M]. Weinheim: Wiley-VCH, 2010.
|
| [29] |
褚文宁. 基于高通量筛选的混合模式层析分离人血白蛋白和抗体研究[D]. 杭州: 浙江大学, 2019. CHU W N. High-throughput screening for human serum albumin and antibody separation with mixed-mode chromatography [D]. Hangzhou: Zhejiang University, 2019. |
| [30] |
JONES L J, YUE S T, CHEUNG C Y, et al. RNA quantitation by fluorescence-based solution assay: Ribogreen reagent characterization[J]. Analytical Biochemistry, 1998, 265(2): 368-374. DOI:10.1006/abio.1998.2914 |
| [31] |
VANJUR L, CARZANIGA T, CASIRAGHI L, et al. Non-langmuir kinetics of DNA surface hybridization[J]. Biophysical Journal, 2020, 119(5): 989-1001. DOI:10.1016/j.bpj.2020.07.016 |




