2. 中石化节能环保工程科技有限公司,山东 东营 257026
2. Sinopec Energy and Environmental Engineering Co., Ltd., Dongying 257026, China
有机胺化学吸收法是当前烟气CO2捕集最经济的手段,已经成为商业应用最为成熟的技术之一。关于有机胺的研究已有50多年的历史,并已有多种有机胺用于商业捕集CO2[1~3]。在实际工业应用过程中发现,胺溶液降解会造成溶剂损耗不断增大、吸收CO2效率持续降低[4~7]。因为烟气会携带约5%的O2进入吸收塔,此外吸收塔、解吸塔、重沸器等设备不可能完全密闭不进空气,贫胺液的装卸等也会携带空气进入碳捕集装置内,则会使空气中的氧气与胺溶剂发生氧化反应,导致溶剂降解[8]。据统计,因有机胺及其降解产物的逸散会造成0.01~0.8 kg·(t CO2)-1的溶剂损失[9~12]。有机胺降解会引起溶液发泡、设备管道腐蚀、堵塞等问题[13, 14]。醇胺降解产物会使溶剂黏度增加,增大溶剂发泡倾向,进而增加胺液在吸收塔和解吸塔内夹带量,增大溶剂损失;另一方面,发泡还会堵塞吸收塔、再生塔及换热器等设备。降解产物中的有机酸会破坏管道设备内壁FeS(硫化铁)保护层,引起腐蚀。
Lepaumier等[15]研究结果表明,所有的胺氧化降解都产生了羧酸(<1%),主要为甲酸、乙酸、甲醇酸、草酸等,导致溶剂失效;另外还检测到硝酸盐和亚硝酸盐(<200 ppm)。Martell[3]研究认为Fe3+的存在会使有机胺氧化降解反应速率加快两倍。Bedell等[17]通过对比厌氧热降解和氧化降解产物,提出MDEA氧化降解过程中会生成季铵盐,此季铵盐可能会作为催化剂加快歧化反应,使MDEA降解加快。
中石化节能环保工程科技有限公司与中国石油大学(华东) CCUS联合实验室开发了以AEEA为主吸收剂、MDEA、DEA、PZ为活化剂的复合CO2吸收剂(三类吸收剂经过大量试验筛选得出),复合吸收剂循环吸收能力和吸收速率都大于MEA,胺液循环量小,可减小循环泵的动力消耗[16, 17];且复合吸收剂再生温度低,再生能耗低,符合工业中“高吸收能力、低能耗”高效CO2吸收剂的评价标准[18, 19]。该吸收剂在胜利电厂4万吨/年CO2捕集纯化工程中进行了应用,但出现了较严重的降解现象,进而导致了管道和设备的腐蚀。为探究降解原因,本文将对分别添加了MDEA、DEA、PZ三种活化剂的AEEA复合吸收剂的循环性能及降解情况进行研究,分析降解途径,为降解抑制研究打下基础。
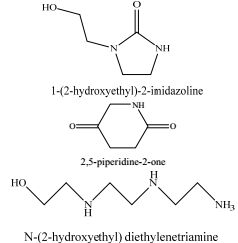
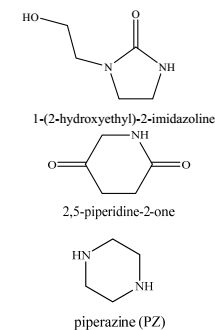
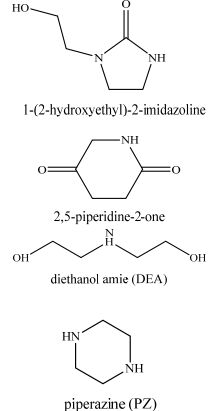
2 实验试剂和仪器 2.1 实验试剂本实验所用实验试剂主要有C4H12N2O (羟乙基乙二胺,分析纯),C4H11NO2 (二乙醇胺,分析纯),C5H13NO2 (N-甲基二乙醇胺,分析纯),C4H10N2 (哌嗪,分析纯)。本实验单胺与所有复配胺溶液总质量分数都为10%,用去离子水配制。采用85%(V/V) CO2(≥ 99%)、15%(V/V) N2 (≥ 99%)模拟电厂烟气。
2.2 实验仪器本实验所用仪器设备主要有玻璃反应釜(郑州南北仪器设备有限公司,S212-1L),精密增力电动搅拌器(江苏省金坛市宏华仪器,JJ-125W),转子流量计(苏州化工仪表有限公司,LZB-DK800-4F),数字皂膜流量计(北京捷思达仪分析仪器研发中心,GL-102B),恒温油浴锅(江苏省金坛市阳光仪器厂,HH-DR1),精密电子天平(上海精科天美贸易有限公司,JH502),雷磁pH/mv计(上海精密科学仪器有限公司,PHS-3C),智能实验室反应釜(上海延征实验仪器有限公司,YZSR-250),安捷伦气质联用仪(美国安捷伦科技有限公司,7890B-5977A GC/MSD)。
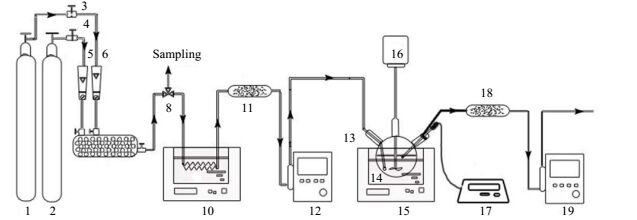
在搅拌反应釜内进行CO2循环吸收实验,该釜采用油浴加热的方式维持吸收液温度稳定。循环吸收实验装置示意图如图 1所示。
|
图 1 吸收过程试验流程图 Fig.1 Schematic diagram of the experimental setup for absorption 1. CO2 cylinder 2. N2 cylinder 3, 4. gas pressure reducing valve 5, 6. rotameter 7. gas mixing buffer tank 8. tee valve 9. spiral glass tube 10. water bath pot 11, 18. silica gel drying tube 12, 19. soap film flowmeter 13. inlet of reaction kettle 14. porous bubble tube 15. oil bath pan 16. motor agitator 17. intelligent electronic pH meter |
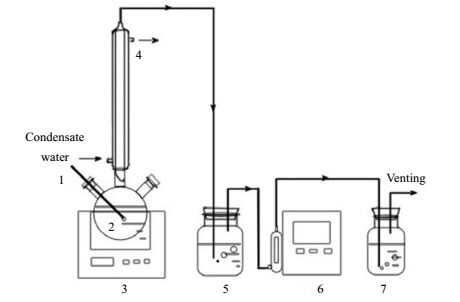
解吸实验通过直接加热法使富胺溶液脱去CO2重新生成贫胺溶液,再生过程采用恒温油浴锅加热,并利用电磁搅拌器进行搅拌,以保证溶液受热均匀及再生完全。循环解吸实验装置如图 2所示。
|
图 2 再生过程试验流程图 Fig.2 Schematic diagram of the experimental setup for desorption 1. thermometer 2. flask 3. electric oil bath 4. condenser tube 5. gas bottle 6. soap film flowmeter 7. saturated calcium hydroxide |
(1) 基于AEEA为主的二元复配溶液初次吸收性能对比
配制总质量分数为10%,以AEEA为主要吸收剂,分别添加MDEA、DEA、PZ三种辅助吸收剂的基于AEEA为主的二元复配胺溶液,结果见图 3~图 5。
|
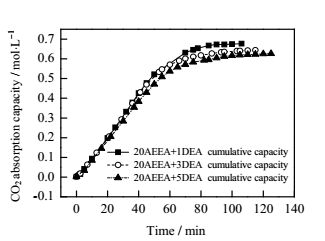
图 3 AEEA+DEA复配溶液初次吸收负荷随时间变化关系对比 Fig.3 Profiles of the first absorption capacity of AEEA and DEA mixture solutions as a function of time |
|
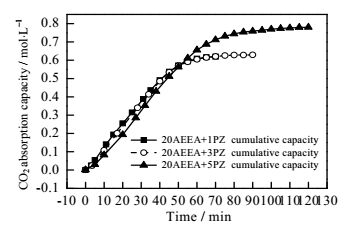
图 4 AEEA+PZ复配溶液初次吸收负荷随时间变化关系对比 Fig.4 Profiles of the first absorption capacity of AEEA and PZ mixture solutions as a function of time |
|
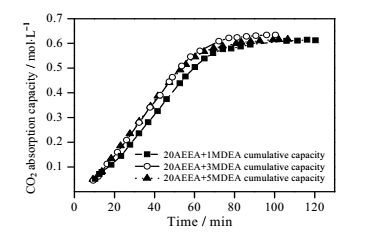
图 5 AEEA+MDEA复配溶液初次吸收负荷随时间变化关系对比 Fig.5 Profiles of the first absorption capacity of AEEA and MDEA mixture solutions as a function of time |
图 3为AEEA+DEA复配胺溶液在0.1 MPa、313 K条件下吸收负荷随时间变化关系对比。从图 3可知,反应一开始,AEEA与DEA复配溶液初次吸收负荷随时间增加而迅速增加,反应至80 min时,吸收反应变缓,最终缓慢吸收达饱和。20:1,20:3,20:5的AEEA与DEA复配溶液达吸收饱和后最终吸收负荷分别为:0.677,0.644和0.626 mol·L-1。3种复配比吸收溶液达吸收饱和用时最短的质量复配比为20:1,所以20:1复配比的AEEA与DEA溶液吸收效果最佳。
图 4为AEEA+PZ复配胺溶液在0.1 MPa、313 K条件下吸收负荷随时间变化关系对比。从图 4可知,20:1与20:3复配溶液吸收反应变化基本相同,吸收主要在前50 min内进行,反应至50 min时,吸收反应变缓,最终缓慢吸收达饱和,而此时20:5复配溶液吸收负荷继续增加,至90 min渐趋平缓。最终,20:1, 20:3, 20:5的AEEA与PZ复配溶液达吸收饱和后吸收负荷分别为:0.620,0.629和0.781 mol·L-1。AEEA与PZ复配溶液吸收负荷随PZ含量增加而增加,20:5的AEEA与PZ复配溶液吸收效果最佳。
图 5为AEEA + MDEA复配胺溶液在0.1 MPa、313 K条件下吸收负荷随时间变化关系对比。从图 5可知,AEEA与MDEA复配溶液吸收反应主要在前60 min内进行,反应至60 min时,吸收反应缓慢进行至吸收饱和。20:1,20:3,20:5的AEEA与PZ复配溶液达吸收饱和后吸收负荷分别为:0.606,0.630和0.611 mol·L-1。AEEA与MDEA复配溶液吸收效果最佳的复配比为20:3。
综上,基于AEEA二元复配胺溶液吸收负荷大小排序为:20:5 AEEA + PZ>20:1 AEEA + DEA>20:3 AEEA + MDEA,20:5 AEEA与PZ复配溶液吸收效果最佳。
(2) 基于AEEA为主的二元复配溶液初次解吸性能对比
针对筛选出的吸收效果最好的3种复配溶液20:5 AEEA + PZ,20:1 AEEA + DEA,20:3 AEEA+MDEA,按照2.2.2节中实验条件考察它们初次解吸过程中CO2再生率,结果列于图 6。
|
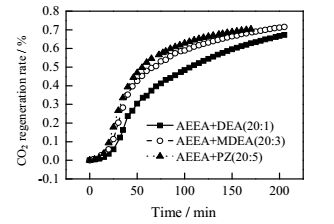
图 6 3种基于AEEA复配溶液初次解吸再生率随时间变化关系 Fig.6 Profiles of the first regeneration rates of 3 AEEA mixture solutions as a function of time |
图 6显示,20:5 AEEA + PZ复配溶液解吸完全用时170 min,用时最短;另外2种复配溶液解吸完全用时都为205 min。前170 min内,相同解吸时间下,20:5 AEEA + PZ再生率最大,20:3 AEEA+ MDEA次之,20:1 AEEA + DEA最小,但解吸完全后,20:3 AEEA + MDEA再生率最大,为75.2%,20:5 AEEA + PZ再生率略次之,为70.4%,20:1 AEEA + DEA再生率最小为67.3%。
对上述3种复配溶液解吸过程中温度变化进行记录,对比结果列于表 1。
| 表 1 3种AEEA复配溶液再生温度对比 Table 1 Comparision of the first regeneration temperatures of 3 AEEA mixture solutions |
表 1数据表明,20:3 AEEA + MDEA开始解吸温度最低,这是因为MDEA是叔胺,与CO2反应生成的碳酸氢盐相比氨基甲酸盐更不稳定易分解,但随着解吸反应进行,溶液中新生成的MDEA与CO2在高温下发生降解反应,生成的降解产物需更高的温度才能解吸再生为MDEA,从而使得溶液恒沸温度升高。PZ因属于环烷胺,比较稳定,在相同条件下不易降解,因此PZ与AEEA组成的复配溶液恒沸温度最低,则水蒸发量越小,再生能耗越小。
由此可见,质量分数比为20:5的AEEA与PZ复配溶液吸收效果和解吸效果较佳,具有潜在应用价值。
3.2 基于AEEA为主的二元复配溶液降解性能研究选取吸收效果最好的3种复配溶液20:5 AEEA + PZ,20:1 AEEA + DEA,20:3 AEEA + MDEA进行循环吸收-解吸实验,考察它们在循环吸收、解吸过程中的吸收负荷、解吸量变化,并试分析循环过程中胺的降解对吸收负荷和解吸量的关系。
(1) 20:5的AEEA与PZ复配溶液循环吸收、解吸性能与降解情况
配制质量分数比为20:5总质量分数为10%的AEEA + PZ混合胺溶液,考察循环吸收-解吸性能,并对解吸后贫液进行GC-MS分析。
复配比为20:5 AEEA + PZ复配胺溶液在0.1 MPa、313 K条件下6次循环吸收负荷随时间变化关系对比见图 7。
|
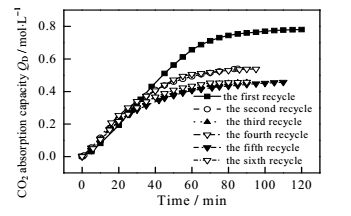
图 7 20:5 AEEA + PZ复配溶液6次循环吸收负荷与时间关系图 Fig.7 Profiles of absorption capacity of the 20:5 AEEA and PZ mixture solution during 6 cycling adsorption processes |
图 7显示,20:5 AEEA + PZ复配溶液在6次循环吸收过程中初次吸收负荷最大,为0.781 mol·L-1。6次吸收负荷大小顺序为:第1次>第4次≈第2次>第3次≈第5次≈第6次。为探究吸收负荷变化,对第2次吸收贫液、第5次吸收贫液进行GC-MS分析,并与第1次再生后贫液分析结果对比见表 2。
| 表 2 20:5 AEEA与PZ复配溶液第2次、第5次再生贫液与第1次再生贫液GC-MS分析 Table 2 Comparison of GC-MS results between the first and second/fifth lean solutions of the 20:5 AEEA and PZ mixture solution |
表 2中结果表明,该复配胺溶液首次解吸后出现一种降解产物2, 5-二哌啶酮,该物质不能参与CO2吸收反应,又因再生不完全,使得后续吸收负荷下降;第2次再生贫液中测得3种降解物质,新出现HEIA和N-(2-羟乙基)二乙烯三胺,AEEA单胺循环吸收实验证实后者是AEEA热降解产物,可促进后续吸收,提高溶液吸收能力,所以第2次吸收负荷增加。第5次再生中降解物经检测仅存在HEIA和2, 5-二哌啶酮,这两种物质不能与CO2反应,因而第5次吸收负荷再次下降。
对复配比为20:5 AEEA + PZ复配胺溶液在0.1 MPa、393 K条件进行6次循环解吸,所得实验结果见图 8。
|
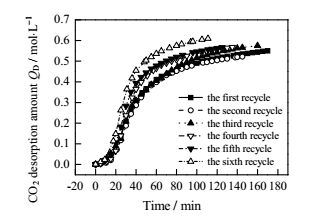
图 8 20:5 AEEA与PZ复配溶液6次CO2解吸量随时间变化对比 Fig.8 Profiles of CO2 desorption of the 20:5 AEEA and PZ mixture solution during 6 cycling desorption processes |
图 8表明,20:5 AEEA + PZ复配胺溶液解吸量一开始随时间增势较缓,是因为此时体系温度较低,再生反应慢,随时间增加,温度上升,反应加快,再生量迅速增加,当温度达到某一定值,溶液沸腾,此时再生反应缓慢,直至再生完全。图中显示,6次循环再生量基本随循环次数增加而增加,CO2再生量最高的是第6次解吸,为0.610 mol·L-1,CO2再生量最少的是第2次解吸,为0.522 mol·L-1。出现这一现象的原因可能是,随循环次数增加AEEA与CO2反应生成的氨基甲酸盐不断降解,该盐经高温加热,会降解生成乙酸盐等难再生分解的物质,那么可分解为CO2的氨基甲酸盐数量减少,因此前两次CO2再生量比较低;随着循环次数增加,溶液中热稳定性盐及其它降解物不断积累,达到饱和,起到抑制氨基甲酸盐降解的作用,溶液中有更多的氨基甲酸盐可分解为CO2;另一方面,AEEA经多次高温解吸,再生过程AEEA降解增加,则使得氨基甲酸盐再生为AEEA和CO2平衡右移,促进CO2再生,CO2解吸量又会增加。
(2) 20:1的AEEA与DEA复配溶液循环吸收、解吸性能与降解情况
配制质量分数比为20:1总质量分数为10%的AEEA + DEA混合胺溶液,考察循环吸收-解吸性能,并对解吸后贫液进行GC-MS分析。
复配比为20:1 AEEA + MDEA复配胺溶液在0.1 MPa、313 K条件下6次循环吸收负荷随时间变化关系对比见图 9。
|
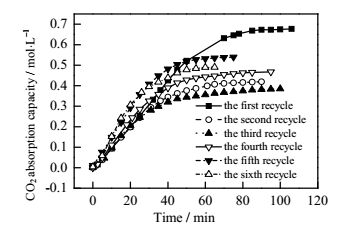
图 9 20:1 AEEA+DEA复配溶液6次循环吸收负荷与时间关系图 Fig.9 Profiles of absorption capacity of the 20:1 AEEA and DEA mixture solution during 6 cycling adsorption processes |
图 9显示,20:1 AEEA + DEA复配溶液在6次循环吸收过程中初次吸收负荷最大为0.677 mol·L-1。6次吸收负荷大小顺序为:第1次>第5次>第6次>第4次>第2次>第3次。为探究第4次吸收负荷和第5次吸收负荷增加原因,对该胺液第4次再生贫液、第5次再生贫液进行GC-MS分析,与第1次再生后贫液分析结果对比列于表 3。表中所列为贫液中检测到主要降解产物,其它物质因含量过低,检测手段有限在此不做探讨。
| 表 3 20:1 AEEA与DEA复配溶液第4次、第5次再生贫液与第1次再生后贫液GC-MS分析 Table 3 Comparison of GC-MS results between the first and fourth/fifth lean solutions of the 20:1 AEEA and DEA mixture solution |
表 3显示,复配胺溶液在第1次再生后只出现2种胺类降解产物物质,HEIA和2, 5-二哌啶酮都是AEEA与CO2反应生成的氨基甲酸盐的降解物,这两种降解物分子中存在羰基,使它们失去与CO2反应能力,从而使溶液循环吸收负荷下降。但第4次再生中出现新的胺降解物哌嗪,哌嗪吸收能力远远高于二乙醇胺,因此第4次贫液吸收负荷大大增加。随循环次数增加,第5次再生贫液中DEA降解生成的PZ量随之增加,因此第5次吸收负荷>第4次吸收负荷。
对复配比为20:1的AEEA + DEA复配胺溶液在0.1 MPa、393 K条件进行6次循环解吸,所得6次CO2解吸量随时间变化对比结果见图 10。
|
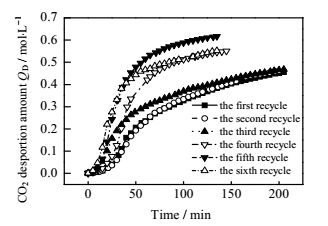
图 10 20:1AEEA与DEA复配溶液6次CO2解吸量随时间变化对比 Fig.10 Profiles of CO2 desorption of the 20:1 AEEA and DEA mixture solution during 6 cycling desorption processes |
图 10表明20:1的AEEA与DEA复配溶液CO2解吸量随时间增加而增加,增长率先小后大再小,反应一开始体系温度低反应较慢,随温度升高反应加快,继续解吸CO2在气液界面逐渐达到平衡,故反应又再次放缓。前3次CO2解吸量基本都为0.46 mol·L-1,第4次CO2解吸量增加至0.55 mol·L-1,原因可能是第4次吸收过程中出现降解物PZ,PZ与CO2反应生成的氨基甲酸盐相比DEA与CO2反应生成的氨基甲酸盐易解吸,另一方面,第4次解吸过程中PZ生成率增加,说明更多的DEA降解,促使DEA氨基甲酸盐分解生成DEA和CO2平衡右移,使更多的CO2得以解吸。第5次解吸量为0.616 mol·L-1,大于第4次解吸量,可能是因为溶液中氨基甲酸盐受热降解生成的热稳定性盐达到饱和,抑制氨基甲酸盐降解,则有更多的氨基甲酸盐可以分解释放CO2,又因为第5次吸收中有更多PZ参与CO2吸收反应,所以第5次解吸量增加。第6次循环吸收液中降解生成的PZ量较低,解吸过程PZ再生出的CO2气量相应减少,导致第6次解吸气量减小。
(3) 20:3的AEEA与MDEA复配溶液循环吸收性能与降解情况
配制质量分数比为20:3总质量分数为10%的AEEA + MDEA混合胺溶液,按照2.2节中实验条件考察循环吸收-解吸性能,并对解吸后贫液进行GC-MS分析。
复配比为20:3 AEEA + MDEA复配胺溶液在0.1 MPa、313 K条件下6次循环吸收负荷随时间变化关系对比见图 11。
|
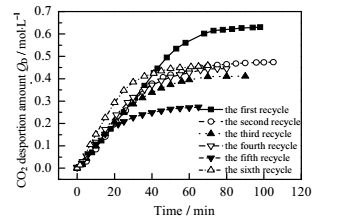
图 11 20:3AEEA与MDEA复配溶液6次循环吸收负荷与时间关系图 Fig.11 Profiles of absorption capacity of the 20:3 AEEA and MDEA mixture solution during 6 cycling adsorption processes |
图 11为20:3的AEEA与MDEA复配溶液6次循环吸收负荷与时间关系对比。该图显示,20:3的AEEA与MDEA复配溶液在6次循环吸收过程中初次吸收负荷最大为0.630 mol×L-1。6次吸收负荷大小顺序为:第1次>第2次>第6次>第4次>第3次>第5次。据此对第4次再生贫液、第6次再生贫液进行GC-MS分析,与第1次解吸后贫液分析结果对比列于表 4。
| 表 4 20:3AEEA与MDEA复配溶液第4次、第6次再生贫液与初次再生后贫液GC-MS分析对比 Table 4 Comparison of GC-MS results between the first and fourth/sixth lean solutions of the 20:3 AEEA and MDEA mixture solution |
表 4中结果表明,第1次再生后贫液中存在两种降解产物1-(2-羟乙基)-2-咪唑啉酮(HEIA)和2, 5-二哌啶酮,这两种降解产物因不能参与吸收CO2反应而使溶液吸收负荷下降,但在第3次再生后贫液中出现DEA。MDEA在CO2存在的高温条件下会发生去甲基化反应,生成DEA。经GC-MS分析可知DEA生成率为6.31%,DEA生成促进第4次吸收使吸收负荷增加。第6次再生贫液中检测到PZ,PZ是DEA热降解产物,而PZ的吸收能力大于DEA,因此第6次吸收负荷高于第4次和第5次吸收负荷。
对复配比为20:3 AEEA + MDEA复配胺溶液在0.1 MPa、393 K条件进行6次循环解吸,所得6次CO2解吸量随时间变化对比实验结果见图 12。
|
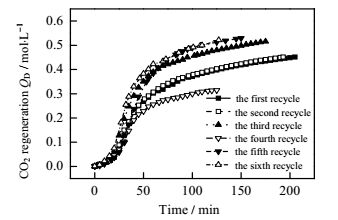
图 12 20:3AEEA与MDEA复配溶液6次再生量随时间变化 Fig.12 Profiles of regeneration of the 20:1 AEEA and MDEA mixture solution during 6 cycling regeneration processes |
图 12显示,AEEA与MDEA复配溶液CO2解吸气量随时间变化趋势说明该复配溶液再生反应也是先慢后快再慢。6次循环再生过程CO2解吸气量大小排序为:第5次≈第6次>第3次>第1次≈第2次>第4次。第5次和第6次解吸气量大致相同为0.52 mol·L-1,第4次解吸气量最小为0.315 mol·L-1,原因分析:MDEA相对比较稳定,与CO2反应生成的碳酸氢盐易分解重新生成MDEA和CO2,所以前2次解吸气量基本相同;第3次解吸过程中MDEA降解生成DEA,溶液中MDEA浓度降低,促进碳酸氢盐分解反再生MDEA和CO2,促进解吸气量增加;至第4次循环再生,溶液中存在DEA再生,DEA相比MDEA难再生,故解吸气量减少;第5次循环,溶液中热稳定性盐及其它降解物不断积累达到饱和,抑制氨基甲酸盐降解,溶液中有更多的氨基甲酸盐可分解为CO2,从而提高再生率,又有第5次再生过程中溶液中DEA降解生成PZ,DEA被消耗,促进DEA氨基甲酸盐分解平衡右移,提高CO2解吸气量。因此,在工业应用过程中为维持良好吸收效果必须在第4次吸收前补充同等浓度新鲜的AEEA与MDEA复配溶液。
(4) 6次循环吸收、解吸后胺降解程度对比
AEEA单胺溶液循环吸收、解吸过程中会发生降解,基于AEEA为主的二元复配溶液也会出现降解,为探究复配溶液降解情况,对同等体积、同等总质量分数的20:5 AEEEA + PZ、20:3 AEEA+MDEA、20:1 AEEA + DEA复配溶液以及AEEA单胺溶液经过6次循环吸收、解吸后贫液与新鲜混合溶液进行对比,因胺在解吸过程中不能完全再生,不适合以胺浓度变化对比胺降解程度,因此可用溶液中降解物的生成率表示胺的降解程度,降解物生成率越大胺降解越严重,结果见图 13。
|
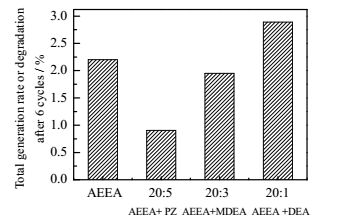
图 13 经过6次循环吸收、解吸后不同胺溶液中总降解物生成率对比 Fig.13 Comparison of total degradation ratios of AEEA mixture solutions after 6 regeneration cycles |
图 13显示,经过6次循环后,AEEA单胺溶液中降解物总生成率为2.2%,以AEEA为主吸收剂,向其中添加辅助吸收剂PZ、MDEA后,降解物总生成率降低,分别降至0.905%,1.95%,但添加DEA后,降解物总生成率增加0.69%。经过6次循环后,质量比20:5 AEEA与PZ混合胺溶液降解率最低,说明该混合胺溶液稳定性能最好,不易降解。
4 结论(1) 以AEEA为主吸收剂,以质量分数比20:1,20:3,20:5的复配比分别添加DEA、PZ、MDEA,得到的二元复配溶液进行初次吸收、解吸实验,得到:
① 初次吸收效果较好的三种混合胺溶液,吸收效果由高到低排列分别为:20:5 AEEA + PZ>20:1 AEEA + DEA>20:3 AEEA + MDEA。
② 吸收效果最佳的三种复配溶液初次解吸,20:3 AEEA+MDEA再生率75.2%,最大;20:5 AEEA + PZ再生率70.4%,次之;20:1 AEEA + DEA再生率67.3%,最小。其中,20:5 AEEA + PZ再生温度最低,说明再生能耗最低。
③ 综合吸收效果和解吸效果,20:5的AEEA与PZ复配溶液是最佳吸收剂。
(2) 以吸收效果最佳的三种复配溶液进行6次循环吸收、解吸实验,得到:
① 20:5 AEEA与PZ复合胺溶液6次吸收负荷大小顺序为:第1次>第4次≈第2次>第3次≈第5次≈第6次,第4次吸收负荷增加与AEEA降解物N-(2-羟乙基)二乙烯三胺有关;6次循环CO2解吸量基本随循环次数增加而增加,CO2再生量最高的是第6次解吸,为0.610 mol·L-1,CO2再生量最少的是第2次解吸,为0.522 mol·L-1。
② 20:1 AEEA与DEA复合胺溶液6次吸收负荷大小顺序为:第1次>第5次>第6次>第4次>第2次>第3次,第4次、第5次吸收负荷增加受DEA降解物哌嗪影响;6次循环CO2解吸量由大到小排序:第5次>第6次≈第4次>第3次≈第2次≈第1次。
③ 20:3 AEEA与MDEA复合胺溶液6次吸收负荷大小顺序为:第1次>第2次>第6次>第4次>第3次>第5次,第4次吸收负荷增加受MDEA降解物DEA影响,第6次吸收负荷增加受DEA降解物PZ影响;6次循环再生过程CO2解吸气量大小排序为:第5次≈第6次>第3次>第1次≈第2次>第4次。
(3) 对同等体积、同等总质量分数的20:5 AEEEA + PZ、20:3 AEEA + MDEA、20:1 AEEA + DEA复配溶液以及AEEA单胺溶液经过6次循环吸收、解吸后胺降解程度分析得到,降解程度由大到小排序为:20:1 AEEA+DEA>AEEA>20:3 AEEA + MDEA>20:5 AEEEA+PZ,说明AEEA与DEA复配会促进胺降解,而AEEA与PZ复配则能抑制胺降解。
| [1] | Rochelle G T. Amine scrubbing for CO2 capture[J]. Science , 2009, 325(5968): 1652-1654. |
| [2] | ZHOU Shan (周珊), WANG Shu-juan (王淑娟), Rochelle G T, et al. Experimental study on thermal degradation of organic amines in CO2 capture process (CO2 捕集过程中有机胺热降解的实验研究)[J]. Journal of Tsinghua University (Natural science)清华大学学报(自然科学版), 2012, 52(1):81-86. http://kns.cnki.net/KCMS/detail/detail.aspx?filename=qhxb201201017&dbname=CJFD&dbcode=CJFQ |
| [3] | Karl M, Wright R F, Berglen T F, et al. Worst case scenario study to assess the environmental impact of amine emissions from a CO2 capture plant[J]. International Journal of Greenhouse Gas Control , 2011, 5(3): 439-447. DOI:10.1016/j.ijggc.2010.11.001. |
| [4] | Metz B. IPCC special report on carbon dioxide capture and storage[R]. Geneva:Intergovernmental Panel on Climate Change, 2005. |
| [5] | ZHANG Wei-feng(张卫风), FANG Meng-xiang(方梦祥), WANG Shu-yuan(王树源), et al. Experimental study on separation of flue gas by hollow fiber membrane contactor(中空纤维膜接触器分离烟气中试验研究)[J]. High Tech Communication(高技术通讯) , 2004, 4(3): 40-43. |
| [6] | YAN Shui-ping(晏水平), FANG Meng-xiang(方梦祥), ZHANG Wei-feng(张卫风), et al. Analysis and progress of chemical absorption removal technology in flue gas(烟气中化学吸收法脱除技术分析与进展)[J]. Chemical Progress(化工进展) , 2006, 25(9): 1018-1024. |
| [7] | Holub P E, Critchfield J E, Su W Y. Amine degradation chemistry in CO2 service[C]. 48th Annual Laurance Reid Gas Conditioning Conference, Texas:Elsevier, 1998. |
| [8] | Freeman S A, Davis J, Rochelle G T. Degradation of aqueous piperazine in carbon dioxide capture[J]. International Journal of Greenhouse Gas Control , 2010, 4(5): 756-761. DOI:10.1016/j.ijggc.2010.03.009. |
| [9] | Lepaumier H, Picq D, Carrette P L. Degradation study of new solvents for CO2 capture in post-combustion[J]. Energy Procedia , 2009, 1(1): 893-900. DOI:10.1016/j.egypro.2009.01.119. |
| [10] | Lowe A, Beasley B, Berly T. Carbon capture and storage (CCS) in Australia, carbon capture:sequestration and storage[J]. The Royal Society of Chemistry , 2009, 6(5): 65-101. |
| [11] | Kohl A L, Nielsen R B. Gas purification(Fifth Edition)[M].Amsterdam: Gulf Publishing Company, 1997. |
| [12] | Douglas A, Costas T. Separation of CO2 from flue gas:a review[J]. Separation Science & Technology , 2005, 40(1-3): 321-348. |
| [13] | Lepaumier H, Picq D, Carrette P L. New amines for CO2 capture. Ⅱ. Oxidative degradation mechanisms[J]. Industrial & Engineering Chemistry Research , 2009, 48(20): 9068-9075. |
| [14] | Bedell S A. Oxidative degradation mechanisms for amines in flue gas capture[J]. Energy Procedia , 2009, 1(1): 771-778. DOI:10.1016/j.egypro.2009.01.102. |
| [15] | Bedell S A, Worley C M, Darst K, et al. Thermal and oxidative disproportionation in amine degradation-O2 stoichiometry and mechanistic implications[J]. International Journal of Greenhouse Gas Control , 2011, 5(3): 401-404. DOI:10.1016/j.ijggc.2010.03.005. |
| [16] | Sexton A J, Rochelle G T. Catalysts and inhibitors for oxidative degradation of monoethanolamine[J]. International Journal of Greenhouse Gas Control , 2009, 3(6): 704-711. DOI:10.1016/j.ijggc.2009.08.007. |
| [17] | Yazvikova N V, Zelenskaya L G, Balyasnikova L V. Mechanism of side reactions during removal of carbon dioxide from gases by treatment with monoethanolamine[J]. Zhurnal Prikladnoi Khimii , 1975, 48(3): 674-676. |
| [18] | Strazisar B R, Anderson R R, White C M. Degradation pathways for monoethanolamine in a CO2 capture facility[J]. Energy & Fuels , 2003, 17(4): 1034-1039. |
| [19] | Joel R, Arturo T. Degradation of aqueous solutions of alkanolamine blends at high temperature, under the presence of CO2 and H2S[J]. Chemical Engineering Communications , 2006, 193: 129-138. DOI:10.1080/009864490923592. |