我国是一个富煤、贫油、少气的国家,煤的主要元素C和H比例与乙炔接近,相关研究表明等离子体裂解煤制乙炔工艺的经济效益优于目前工业生产常用的甲烷部分氧化法[1]和电石法[2]。煤粉裂解生成乙炔后,在缓慢冷却时乙炔易分解为炭黑和氢气导致乙炔收率降低[3]。淬冷是等离子体裂解煤制乙炔过程中保证乙炔收率的重要工段之一,当淬冷带走热量速率远大于乙炔分解所需热量速率时,乙炔来不及分解为炭黑和氢气被固定下来,从而使淬冷后的体系组成与高温平衡体系组分组成较接近[4]。因而可以先在高温下进行煤炭向乙炔的转化,然后淬冷到常温下储存。但是由于等离子体体系温度高、反应速率快,其实际过程难以直接测量和监控[5],可靠的等离子温度诊断设备相当昂贵[6],故有必要对其进行模拟。
针对等离子裂解煤的反应阶段,复杂系统平衡组成的模拟方法中,热力学计算目前常用的方法有松弛法、化学计量法以及最小Gibbs自由能法,松弛法[7]和化学计量法[8]初值依赖性大,同时还需要知道反应的具体方程。最小Gibbs自由能法的优势在于与初始组分、反应的过程均无关,当初始输入组分的元素比一定,体系处于稳定状态时系统组分总Gibbs自由能最小[9]。目前热力学计算集中在等离子体反应器功率对目标产物收率的影响[10-11]、煤种元素最佳比例[12-13]、不同氢碳比、不同系统压力[14]对乙炔收率的影响等方面。在热力学平衡模拟的基础上,Price和Wenger [15]研究了煤粉中不同元素含量对乙炔收率的影响,认为较高的H/C和较低O/C摩尔比有利于乙炔的收率的提高,并得到了不同C-H-O比时的乙炔收率。
采用最小Gibbs自由能法对等离子体裂解煤制乙炔体系进行热力学计算时,是否考虑固相目前尚存在争议,陈宏刚等[16]认为裂解过程中存在焦炭故必须考虑固相碳,程易等[17]认为在等离子体的高温高活性环境中,化学反应非常迅速,来不及聚合成C(S),王鹏[18]认为,在反应器中,由于固相多存在于靠近冷壁的极薄区域中,因而在反应空间C-H平衡体系中并不存在固相。张铭[19]认为均相模型较好地体现了气态组分随温度的变化但不能反映结焦情况,非均相模型反映了结焦情况,但固态C所占比重不符合结焦程度。
热力学计算得到乙炔的量未考虑淬冷过程中乙炔的分解量,显然淬冷过程中乙炔的分解量必须加以考虑。李明东[20]总结了Tanzawa等[21]、Palmer和Domish[22]、John等[23]通过对稳态系统、流动系统、shock管等进行乙炔分解动力学的研究,表明乙炔分解在低温时为一个一级反应,高温时为二级反应。此外,清华大学程易课题组[24]通过实验室规模的实验,对等离子体裂解煤制乙炔的热力学平衡体系、淬冷时乙炔分解动力学等方面做了较多的研究,取得了有益的一些结果,但尚存在如下的二点不足:(1)在考察乙炔分解时,将淬冷过程温度视为线性变化,这与实际淬冷过程一般都有显著的非线性温度-时间变化规律[4]相比误差较大;(2)研究的乙炔浓度较低(约3 %),而实际等离子裂解煤制乙炔过程的乙炔浓度较高(可达10 %左右)。因此较高乙炔浓度下,淬冷过程中乙炔的分解尚需进一步深入研究。
本文拟通过等离子体裂解煤制乙炔的实验,结合等离子体裂解煤体系热力学平衡计算、动力学方程的筛选等建立淬冷过程的数学模型,并寻求淬冷前温度的确定方法,进而探索煤样含水量、淬冷前温度、时间常数等工艺参数对乙炔收率的影响,以期为等离子体裂解煤制乙炔技术的工业化开发提供一定的技术依据。
2 等离子体裂解煤制乙炔实验 2.1 实验原料实验时所用煤样分别来自新疆和江西,工业分析和元素分析如表 1、表 2所示。煤的工业分析是指水分(Mad)、灰分(Aad)、挥发分(Vad)以及固定碳(FCad)四种分析指标。元素分析主要包括碳含量(Cad)、氢含量(Had)、氧含量(Oad)、氮含量(Nad)、硫含量(St, ad)。
|
|
表 1 新疆煤样分析数据 Table 1 Sample analysis data of coal from Xinjiang |
|
|
表 2 江西煤样分析数据 Table 2 Sample analysis data of coal from Jiangxi |
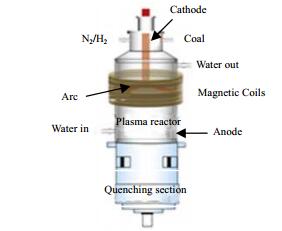
反应器为一个旋转弧等离子体炬[11],反应器内安装一个金属片作为电极阴极,反应器壁面为电极阳极,反应器外壁缠绕线圈,通过线圈的电流控制反应器内部磁场和电弧,反应器内部等离子体旋转弧高速扫射在反应器内壁形成等离子体面,反应器示意图如图 1所示:
|
图 1 实验装置示意图 Fig.1 Schematic diagram of the experimental setup |
煤粉和氢气混合进料,在反应器内的等离子体电弧面上反应裂解,裂解气进入淬冷器。淬冷器内径d = 180 mm,有效淬冷区长度h = 200 mm。
2.3 实验条件实验时煤粉混合氢气进料,淬冷剂为20℃的水,淬冷水冷却时间与裂解气停留时间相同,各组实验(江西煤1~3仅进料量不同)的输入量及经过计算得到的淬冷时间等实验操作参数如表 3所示:
|
|
表 3 实验操作参数 Table 3 Experimental parameters used in the study |
结合反应器结构尺寸及出口流量、组成求得新疆煤、江西煤1~3淬冷总时间t总分别为30.5、33.7、30.3、28.8 ms。淬冷器出口测量处温度T1约为373 K,实验时淬冷后出口产物经色谱分析的结果、出口气体总流量、根据出口组成及淬冷器结构参数计算得到的出口乙炔浓度如表 4所示:
|
|
表 4 出口流量及主要组分含量(不包含水蒸气,单位:摩尔分率) Table 4 Outlet flow rates and main component contents (mole fraction) |
等离子体裂解煤制乙炔淬冷时会伴随许多化学反应,其中乙炔的分解反应对乙炔收率的影响较大,在乙炔分解动力学的计算中,考虑涉及淬冷过程中乙炔反应的全面性和温度的适用范围等,本文选用Palmer和Domish[22]所提出的动力学方程:
| $ {{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{2}}}{\rm{-2C + }}{{\rm{H}}_{\rm{2}}}\;\;\;\;{\rm{d}}c{\rm{/d}}t{\rm{ = - }}{R_{\rm{1}}} $ | (1) |
同时由于体系中不含氧气组分,考虑了无氧气参与的碳直接气化反应、水煤气反应等,除乙炔分解外,淬冷过程中还存在如下反应,其相关的反应动力学方程为:
| $ {{\rm{C + 2}}{{\rm{H}}_{\rm{2}}}{\rm{-C}}{{\rm{H}}_{\rm{4}}}\;\;\;\;{\rm{d}}X{\rm{/d}}t{\rm{ = }}{R_{\rm{2}}}{{{\rm{(1 - }}X{\rm{)}}}^{{\rm{2/3}}}}} $ | (2) |
| $ {{\rm{C + }}{{\rm{H}}_{\rm{2}}}{\rm{O-CO + }}{{\rm{H}}_{\rm{2}}}\;\;\;\;{\rm{d}}X{\rm{/d}}t{\rm{ = }}{R_{\rm{3}}}{{{\rm{(1 - }}X{\rm{)}}}^{{\rm{2/3}}}}} $ | (3) |
| $ {{\rm{CO + }}{{\rm{H}}_{\rm{2}}}{\rm{O-C}}{{\rm{O}}_{\rm{2}}}{\rm{ + }}{{\rm{H}}_{\rm{2}}}\;\;\;\;{\rm{d}}c{\rm{/d}}t{\rm{ = - }}{R_{\rm{4}}}} $ | (4) |
| $ {{\rm{C}}{{\rm{H}}_{\rm{4}}}{\rm{ + 2 }}{{\rm{H}}_{\rm{2}}}{\rm{O-C}}{{\rm{O}}_{\rm{2}}}{\rm{ + 4 }}{{\rm{H}}_{\rm{2}}}\;\;\;\;{\rm{d}}c{\rm{/d}}t{\rm{ = - }}{R_{\rm{5}}}} $ | (5) |
| $ {\rm{C + C}}{{\rm{O}}_{\rm{2}}}{\rm{-2 CO}}\;\;\;\;{\rm{d}}X{\rm{/d}}t{\rm{ = }}{R_{\rm{6}}}{{\rm{(1 - }}X{\rm{)}}^{{\rm{2/3}}}} $ | (6) |
其中R1~R6都是与温度T有关的函数,详见文献[22, 25-27],程易等[24]提出的淬冷模型将淬冷过程温度视为线性变化,而实际淬冷过程一般都有显著的非线性关系,淬冷前期温度下降很快,淬冷后期温度变化较平缓,温度-时间关系较接近指数函数[4],如式(7):
| $T = ({T_0} - {T_{\rm{W}}})\exp ( - t/{\tau _{\rm{q}}}) + {T_{\rm{W}}}$ | (7) |
因此,本文采用式(7)来描述淬冷过程的温度分布,其中τq为模型的可调参数,τq的物理意义为体现淬冷速率的常数,即时间常数,与淬冷剂的种类、流量、温度及淬冷器的尺寸等相关。
显然,如果知道淬冷前的初始条件(包括T0、C0),根据式(1)~(7),结合实验条件(包括淬冷水温度TW、淬冷总时间t总等)及τq,借助ploymath软件就可确定淬冷后裂解气的组成及温度(对于同一次淬冷过程,不同反应所处的淬冷环境一样,故体现淬冷速率的τq相同)。
遗憾的是,由于等离子体的温度很高,目前尚难以可靠测定T0、C0,还只能通过某些方法进行估算,其中的关键是T0的确定(C0可采用T0所对应的热力学平衡的浓度)。王鹏[18]以热力学计算乙炔最大值时对应的温度作为T0,程易课题组[5]也进行了相关研究提出了估算方法,该方法以实验结果为基础,得到了出口RC/H(碳氢摩尔比)、C2H2/CH4的值与淬冷前温度间的对应关系图,从而可通过计算每次实验的RC/H及C2H2/CH4的值查图得淬冷前温度。但上述两估算方法的可靠性尚未定论。为此,本文将对T0的估算方法进行比较、研究,详见3.2.1节。
3.2 淬冷模型的验证根据热力学平衡原理,体系总自由能等于该体系各组分自由能之和,当体系达到化学平衡时,吉布斯自由能之和最小,温度和压力一定时的产物组成唯一确定。因此,可由体系吉布斯自由能方程(8)与质量守恒方程(9)进行热力学平衡计算:
| $G(N) = \sum\limits_{i = 1}^m {x_i^g} \left[ {(\frac{{G_i^\theta }}{{RT}})_i^g + \ln P + \ln \frac{{x_i^g}}{{\overline {{x^g}} }}} \right] + \sum\limits_{i = m + 1}^n {x_i^{cd}} \left( {\frac{{G_i^\theta }}{{RT}}} \right)_i^{cd}$ | (8) |
| $\sum\limits_{i = 1}^m {{a_{ij}}x_i^g} + \sum\limits_{i = m + 1}^n {{b_{ij}}x_i^{cd}} = {N_i}$ | (9) |
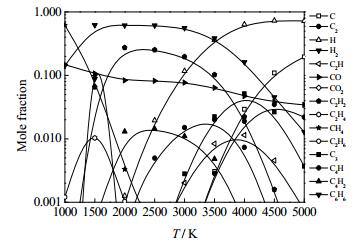
由3.1节可知,T0、C0还只能通过某些方法进行估算,目前的方法有王鹏[18]以及程易课题组[5]的估算方法,王鹏的估算方法与热力学计算关系紧密,程易的估算方法是根据实验结果及其所总结的规律确定。为此,本文进行了相关的热力学计算,模拟所用煤样元素比例如表 1、表 2所示,计算过程中热力学数据选自JANAF表[28],经过模拟计算,发现非均相模型的结果中,乙炔含量远低于实验出口乙炔含量,同时固相碳所占比重也与结焦量明显不符,故本文选取均相模型。将反应视为均相体系,模拟结果如图 2~5所示:
|
图 2 新疆煤组分平衡摩尔分数图 Fig.2 Diagram of equilibrium mole fraction of coal from Xinjiang |
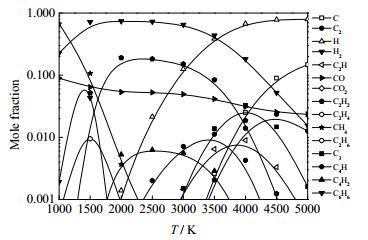
|
图 3 江西煤样1组分平衡摩尔分数图 Fig.3 Equilibrium mole fraction of coal sample 1 from Jiangxi |
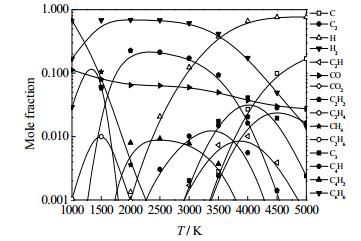
|
图 4 江西煤样2组分平衡摩尔分数图 Fig.4 Diagram of equilibrium mole fraction of coal sample 2 from Jiangxi |
|
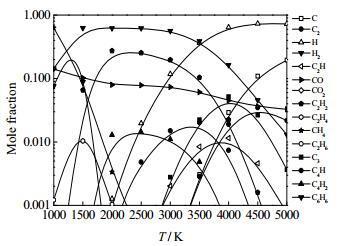
图 5 江西煤样3组分平衡摩尔分数图 Fig.5 Diagram of equilibrium mole fraction of coal sample 3 from Jiangxi |
由图 2~5可知,在1000~5000 K,热力学平衡时,乙炔的浓度先增加后减小,主要组分(H2、CO、C2H2)浓度在1400~1800 K与实验出口组成接近。
淬冷前温度T0 若根据程易课题组[5]的方法,则新疆煤、江西煤1~3分别为1630、1950、1840、1740 K;若根据王鹏[18]的方法,则分别为1900、2070、1960、2000 K。以上述两方法求得的T0,结合3.1节淬冷过程模型进行模拟,发现模拟结果与实验结果的误差较大,不太适合。为此,本文假设不同的T0,根据其对应的热力学平衡组成,进行了相关动力学计算,并与实验结果分析、比较。结果如表 5所示:
|
|
表 5 淬冷前温度的不同估算方法对淬冷模拟结果的影响 Table 5 Effects of pre-quenching temperature estimation methods on the simulation results of quenching processes |
由表 5可知,发现就本文的新疆煤、江西煤1~3而言,以热力学计算得到的乙炔浓度与出口组分中乙炔浓度等值时的温度再加30 K作为淬冷前温度T0,误差最小。因而提出新的淬冷前温度估算方法,即与淬冷过程裂解气出口乙炔摩尔组成相等的热力学计算结果所对应的温度加30 K作为淬冷前温度T0,根据图 2~5,得到的新疆煤和江西煤1~3热力学平衡得到的乙炔摩尔分率与裂解气出口乙炔摩尔分率相等时,对应的温度分别为1550、1450、1480、1500 K,相应估算淬冷前温度分别为1580、1480、1510、1530 K。
3.2.2 淬冷过程主要反应的动力学计算取新疆煤和江西煤1~3淬冷前温度T0分别为1580、1480、1510、1530 K,根据图 1~4,可求得相应的C0,以乙炔为例,分别为5.87×10-6、1.89×10-6、2.84×10-6、3.87×10-6 mol·mL-1。再根据3.1节所建立的模型,优化求得新疆煤和江西煤1~3的时间常数分别为11、12.7、11和10.6 ms(对比本文2.4节各组实验淬冷总时间可知,时间常数为总时间的0.2 ~ 0.5倍),相应的模拟结果如表 6所示:
|
|
表 6 淬冷模型的模拟结果(摩尔分率) Table 6 Simulation results from quenching models (mole fraction) |
从表 6可知,根据淬冷模型求得的淬冷后乙炔、氢气、一氧化碳、二氧化碳的含量与实验结果基本符合,对于甲烷,新疆煤模拟值与实验值比较接近,江西煤误差较大的原因暂不清楚,尚需继续研究,但甲烷含量不高且不是主要研究组分,从工程角度看,模型的误差处在合理的范围,故本文提出的淬冷过程模型可用于等离子体裂解煤制乙炔出口组成的估算。
根据表 6的模拟结果,经计算发现淬冷过程中乙炔的分解率不容忽略,新疆煤和江西煤1~3的乙炔分解率分别为16.2 %、3.17 %、4.58 %、6.98 %;而淬冷过程中甲烷、一氧化碳、二氧化碳基本变化不大,结果如表 7所示:
|
|
表 7 淬冷前后主要组分的浓度变化(单位:10-6 mol·mL-1) Table 7 Concentration variation of main components before and after quenching(unit: 10-6 mol·mL-1) |
此外,还发现每次淬冷过程实验的时间常数约为淬冷总时间的0.2 ~ 0.5倍的规律。
4 淬冷工段工艺参数的影响模拟为减少淬冷过程中乙炔的分解率,有必要对淬冷的工艺条件进行优化。鉴于新疆煤更有潜在的应用前景,本节选用新疆煤作为研究对象。
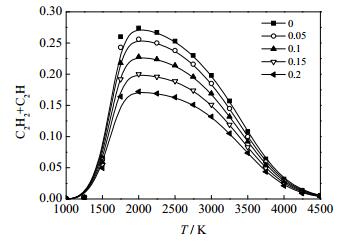
4.1 等离子体裂解煤煤样含水量与淬冷前乙炔含量关系的研究正常情况下不同煤样中元素比例相差较小,同一煤样差别更小,在实际生产中,样煤因为受潮可能会增加水含量,H和O的含量同时增大。此处在不加氢气的情况下,按照含水率分别为0 %、5 %、10 %、15 %、20 %分别进行模拟,得到的淬冷前乙炔含量(乙炔与极易转化为乙炔的C2H分子之和)与温度的关系,如图 6所示。
|
图 6 不同含水率对应的乙炔收率-温度关系热力学计算图 Fig.6 Thermodynamic simulation diagram of yield mole fraction- temperature relationship of acetylene under different water contents |
由图 6可知,含水量越高,乙炔最高含量越小,即当H:O按照2:1加入煤样时,氧元素对乙炔收率的阻碍作用大于氢元素的促进作用。表明在等离子体裂解煤制乙炔的工艺中,应当考虑先对煤样进行干燥。
4.2 时间常数的影响由淬冷过程的数学模型可知,改变时间常数即相当于改变淬冷速率,实际操作时可通过改变淬冷剂的种类、淬冷剂通入速率等实现时间常数的变化。就本文的新疆煤而言,当淬冷前温度为1580 K时,根据热力学计算得淬冷前乙炔浓度为5.87×10-6 mol·mL-1,不同时间常数对淬冷过程乙炔分解率的影响如表 8所示。
|
|
表 8 淬冷前温度1580 K时不同时间常数的影响 Table 8 Effects of different time-constants at pre-quenching temperature of 1580 K |
由表 8可知,相同淬冷前温度时,时间常数越大对应淬冷速率越小,淬冷效果越差,乙炔分解量越大;时间常数越小,乙炔分解量越小,但需要的淬冷速率越大,淬冷过程的运营成本相应增大,故需综合考虑选择合适的时间常数,建议取5 ~ 15 ms之间(淬冷总时间的0.2 ~ 0.5倍)。
4.3 淬冷前温度T0的影响不同的淬冷前温度对热力学平衡以及乙炔分解率均有影响,而淬冷前温度由反应器的输入功率调节。由前文计算可知新疆煤实验的时间常数为11 ms,此时不同淬冷前温度的影响如表 9所示。只考虑热力学平衡时,淬冷前乙炔浓度C0的变化规律由图 2可知先增大后减小,在1900 K附近取得最大值12.22×10-6 mol·mL-1;考虑淬冷时乙炔发生分解,则淬冷后乙炔浓度C1的变化规律由表 9可知仍为先增大后减小,但合适的温度范围已发生变化,较好的T0为1650 K。
|
|
表 9 时间常数11 ms时不同淬冷前温度的影响 Table 9 Effects of different pre-quenching temperatures at time-constant of 11 ms |
其原因在于淬冷时乙炔分解量与温度相关,由乙炔分解动力学方程知T增大时,乙炔分解的量增大。在考虑的温度范围内,乙炔热力学平衡的浓度随温度的增大而先增大后减小,乙炔分解量随温度增大逐渐增大,两者之差为出口乙炔浓度,从而使得合适淬冷前温度降低。
5 结论(1) 根据热力学计算及乙炔分解的动力学方程,建立了等离子体裂解煤制乙炔工艺中淬冷过程的数学模型,并提出了淬冷前温度的估算方法。模型的模拟结果与实验结果基本符合。
(2) 淬冷过程中乙炔的分解率不容忽略,而淬冷过程中甲烷、一氧化碳、二氧化碳的浓度基本变化不大。
(3) 乙炔收率随着煤中含水量增大而降低,等离子体裂解煤制乙炔的工艺中宜先对煤样进行干燥。
(4) 乙炔的收率由淬冷前热力学平衡得到的乙炔的量与乙炔在淬冷过程中分解的量共同决定,在一定的淬冷时间常数下,淬冷前温度越高,乙炔的分解量越大,结合热力学平衡中乙炔含量随温度先增后减的趋势,等离子裂解煤制乙炔工艺中有合适的淬冷前温度,该温度与热力学平衡时乙炔浓度最高点所对应的温度不一定相同。
符号说明:
|
|
| [1] | Su C, Wang D, Wang T. Simulation of partial oxidation of natural gas with detailed chemistry:Influence of addition of H2, C2H6, and C3H8[J]. Chemical Engineering Science, 2010, 65(8): 2608-2618. DOI:10.1016/j.ces.2009.12.035. |
| [2] | Yan B, Cheng Y, Jin Y. Cross-scale modeling and simulation of coal pyrolysis to acetylene in hydrogen plasma reactors[J]. AIChE Journal, 2013, 59(6): 2119-2133. DOI:10.1002/aic.13984. |
| [3] | Baumann H, Bittner D, Beiers H G, et al. Pyrolysis of coal in hydrogen and helium plasmas[J]. Fuel, 1988, 67(8): 1120-1123. DOI:10.1016/0016-2361(88)90380-8. |
| [4] | DAI Bo (戴波). Study on the production of acetylene by hydrogen plasma pyrolysis of coal (氢等离子体裂解煤制取乙炔的研究)[D]. Beijing (北京). Tsinghua university (清华大学), 2000. http://cdmd.cnki.com.cn/Article/CDMD-10003-2006106509.htm |
| [5] | Yan B, Xu P, Jin Y, . Understanding coal/hydrocarbons pyrolysis in thermal plasma reactors by thermodynamic analysis[J]. Chemical Engineering Science, 2012, 84(52): 31-39. |
| [6] | TAO Xiao-hang(陶潇杭), SU Bao-gen(苏宝根), ZHANG Zhi-guo(张治国), et al. Research progress of thermal plasma temperature diagnosis method(热等离子体温度诊断方法研究进展)[J]. Journal of Chemical Engineering of Chinese Universities(高校化学工程学报), 2017, 31(5): 1001-1008. DOI:10.3969/j.issn.1003-9015.2017.05.001. |
| [7] | Trochet M, Béland L K, Joly J F, et al. Diffusion of point defects in crystalline silicon using the kinetic activation-relaxation technique method[J]. Physical Review B, 2015, 91(22): 224106. DOI:10.1103/PhysRevB.91.224106. |
| [8] | Kulik D A. Dual-thermodynamic estimation of stoichiometry and stability of solid solution end members in aqueous-solid solution systems[J]. Chemical Geology, 2006, 225(3-4): 189-212. DOI:10.1016/j.chemgeo.2005.08.014. |
| [9] | Freitas A C D, Guirardello R. Thermodynamic analysis of methane reforming with CO2, CO2+ H2O, CO2+ O2 and CO2+ air for hydrogen and synthesis gas production[J]. Journal of CO2 utilization, 2014, 7(1): 30-38. |
| [10] | Yan C, Yan B, Li T, et al. Experimental study on coal tar pyrolysis in thermal plasma[J]. Plasma Chemistry and Plasma Processing, 2015, 35(2): 401-413. DOI:10.1007/s11090-014-9608-3. |
| [11] | Ma J, Su B, Wen G, , et al. Kinetic modeling and experimental validation of the pyrolysis of propane in hydrogen plasma[J]. International Journal of Hydrogen Energy, 2016, 48(1): 22689-22697. |
| [12] | CHEN Hong-gang(陈宏刚), ZHAO Hui(赵辉), SUN Ya-ling(孙亚玲), et al. Thermodynamic analysis of hydrogen-carbon-oxygen-argon system for coal pyrolysis in hydrogen-argon thermal plasma(氢/氩热等离子体裂解煤碳-氢-氧-氩多相多组分体系的热力学分析)[J]. The Chinese Journal of Process Engineering(过程工程学报), 2009, 9(1): 79-83. DOI:10.3321/j.issn:1009-606X.2009.01.016. |
| [13] | Wu C, Chen J, Cheng Y. Thermodynamic analysis of coal pyrolysis to acetylene in hydrogen plasma reactor[J]. Fuel Processing Technology, 2010, 91(8): 823-830. DOI:10.1016/j.fuproc.2009.09.013. |
| [14] | MA Jie (马杰). Study on the acetylene of magnetic rotary arc plasma pyrolysis of coal (磁旋转弧等离子体裂解煤制乙炔研究)[D]. Hangzhou (杭州): Zhejiang University (浙江大学), 2016. http://cdmd.cnki.com.cn/Article/CDMD-10335-1017035174.htm |
| [15] | Price L C, Wenger L M. Study on main factors influencing acetylene formation during coal pyrolysis in arc plasma[J]. Process Safety & Environmental Protection, 2006, 84(3): 222-226. |
| [16] | CHEN Hong-gang(陈宏刚), XIE Ke-chang(谢克昌). The thermodynamic equilibrium analysis of hydrogen system in plasma pyrolysis of coal(等离子体裂解煤制乙炔碳-氢体系的热力学平衡分析)[J]. Chinese Journal of Process Engineering(过程工程学报), 2002, 2(2): 112-117. DOI:10.3321/j.issn:1009-606X.2002.02.004. |
| [17] | Chang Y, Pfender E. Thermochemistry of thermal plasma chemical reactions. Part Ⅰ. General rules for the prediction of products[J]. Plasma Chemistry and Plasma Processing, 1987, 7(3): 275-297. DOI:10.1007/BF01016518. |
| [18] | WANG Peng (王鹏). Study on water quenching process in acetylene process of plasma pyrolysis of coal (等离子体裂解煤制乙炔工艺中的水淬冷过程研究)[D]. Hangzhou (杭州): Zhejiang University (浙江大学), 2011. http://cdmd.cnki.com.cn/Article/CDMD-10335-1011244790.htm |
| [19] | ZHANG Ming (张铭). Research on the treatment of polymer waste by magnetic rotation arc plasma technology (磁旋转弧等离子体技术处理高分子废弃物的研究)[D]. Hangzhou (杭州): Zhejiang University(浙江大学), 2017. http://cdmd.cnki.com.cn/Article/CDMD-10335-1017243880.htm |
| [20] | LI Ming-dong (李明东). Study on the acetylene scheme of plasma pyrolysis of coal with coal-bed methane as coolant (以煤层气为冷却剂的等离子体裂解煤制乙炔方案研究)[D]. Beijing (北京). Tsinghua university (清华大学), 2004. http://cdmd.cnki.com.cn/Article/CDMD-10003-2006106537.htm |
| [21] | Tanzawa T, Gardiner W C J. ChemInform abstract:reaction mechanism of the homogeneous thermal decomposition of acetylene[J]. Journal of Physical Chemistry, 1980, 11(19): 236-239. |
| [22] | Palmer H B, Dormish F L. The kinetics of decomposition of acetylene in the 1500°K. region1[J]. Journal of Physical Chemistry, 1964, 68(6): 1553-1560. DOI:10.1021/j100788a049. |
| [23] | Kiefer J H, Von Drasek W A, Von Drasek W A. Mechanism of the homogeneous pyrolysis of acetylene[J]. International Journal of Chemical Kinetics, 1990, 22(7): 747-786. |
| [24] | Yan B, Cheng Y, Li T, et al. Detailed kinetic modeling of acetylene decomposition/soot formation during quenching of coal pyrolysis in thermal plasma[J]. Energy, 2017, 121: 10-20. DOI:10.1016/j.energy.2016.12.130. |
| [25] | Mühlen H J, Heek K H V, Jüntgen H. Kinetic studies of steam gasification of char in the presence of H2, CO2, and CO[J]. Fuel, 1985, 64(7): 944-949. DOI:10.1016/0016-2361(85)90149-8. |
| [26] | WU Xue-cheng(吴学成), WANG Qin-hui(王勤辉), LUO Zhong-yang(骆仲泱), et al. The model research model is established and verified by gasification parameters affecting the coal gasification of the airflow bed(气化参数影响气流床煤气化的模型研究(Ⅰ)——模型建立及验证)[J]. Journal of Zhejiang University (Engineering)(浙江大学学报(工学版)), 2004, 38(10): 1361-1365. DOI:10.3785/j.issn.1008-973X.2004.10.024. |
| [27] | Watkinson A P, Lucas J P, Lim C J. A prediction of performance of commercial coal gasifiers[J]. Fuel, 1991, 70(4): 519-527. DOI:10.1016/0016-2361(91)90030-E. |
| [28] | Chase M W. JANAF thermochemical tables[M].Gaithersburg: Government Printing Office, 1986. |




