2. 江苏美淼环保科技有限公司, 江苏 常州 213164
2. Jiangsu Maymuse Environmental Protection Technology Co. Ltd., Changzhou 213164, China
近年来,H2作为一种清洁能源获得了大量关注[1-2],国内外成熟制氢的方法包含化石燃料裂解、水煤气变换、氨分解等[3-4]。然而,形成的产物为含H2的混合气体,需要对其进行高效的分离纯化。其中,溶胶-凝胶法制备的微孔SiO2膜由于其独特的多孔网络,在H2分离上表现出很大的潜力[5]。然而,对于工业中潮湿和高温下的H2/CO2或H2/N2分离,SiO2中的硅氧基团(即Si─O─Si基团)在水蒸气作用下容易解离,导致结构坍塌[6],降低了膜的H2选择性[7-8]。
为了提高硅膜抗水蒸气性能,将有机基团加入SiO2网络中,可降低硅氧基团与水蒸气的接触,提高膜的水热稳定性[9-10]。然而,有机基团的引入也增大了硅网络的孔径,降低了从小分子CO2、CO或N2中分离H2所需的筛分性能。Yu等[11]和Kanezashi等[12]制备了双(三乙氧基硅基)甲烷(BTESM)、1, 2-双(三乙氧基硅基)乙烷(BTESE)、1, 6-双(三甲氧基硅基)己烷(BTMSH)、1, 4-双(三乙氧基硅基)苯(BTESB)和1, 8-双(三乙氧基硅基)辛烷(BTESO)等含不同有机基团前驱体制备的有机硅膜,发现加入了有机基团后,膜获得了较高的H2渗透率,但选择性降低。
为了提高H2的选择性,研究者采用Ni、Co、Zr、Pd和Nb等金属掺杂到硅网络中对膜进行修饰,对提高H2分离起到了一定的作用,同时也防止了网络结构在蒸汽氛围中的致密化[13-15]。Hove等[16]在BTESE有机硅膜中掺杂Zr,对H2/CO2的气体选择性从4提高到16。Song等[17]将Pd加入BTESE膜中,对H2的渗透率为7.26×10−7 mol⋅m−2⋅s−1⋅Pa−1,H2/N2的气体选择性为14。在这些金属掺杂中,金属均是以离子状态进入有机硅网络,研究表明金属最终与有机硅形成了金属M-O-Si的网络结构或者金属氧化物[18]。Zhang等[19]发现将金属引入有机硅中形成的金属氧化物可以使得有机硅膜孔径变大、H2吸附增强,从而显著增加H2渗透通量,但选择性呈下降趋势。而金属单质尤其是Pd对H2有较高的溶解度和较低的活化能[20-23],Pd膜H2的分离性大于1 000。这说明H2在金属和金属氧化物上的吸附是具有差异的。目前,硅膜中的金属状态对H2分离性能的影响研究较少。
综上,本研究将Pd2+加入BTESH中制备Pd/BTESH杂化硅膜,分别采用乙醇和乙二醇类溶剂及H2氛围3种方法还原形成金属单质Pd,研究Pd颗粒对有机硅结构和H2分离的影响,提高有机硅膜的H2分离性能以及水热稳定性。
2 实验 2.1 实验原料BTESH(质量分数为96%)购自麦克林试剂有限公司;α-Al2O3(孔径为1.0 μm和0.2 μm,质量分数为99.9%)购自阿拉丁试剂有限公司;正硅酸四乙酯(分析纯)购自国药集团化学试剂有限公司;正丁醇锆(分析纯)购自阿拉丁试剂有限公司;氯化钯(PdCl2,质量分数为98%)购自阿拉丁试剂有限公司;乙二醇(质量分数为99.5%)购自国药集团化学试剂有限公司;无水乙醇(质量分数为99.7%)购自国药集团化学试剂有限公司;大孔α-Al2O3片微滤膜(孔径为1 μm,孔隙率为40%,直径为28 mm)。
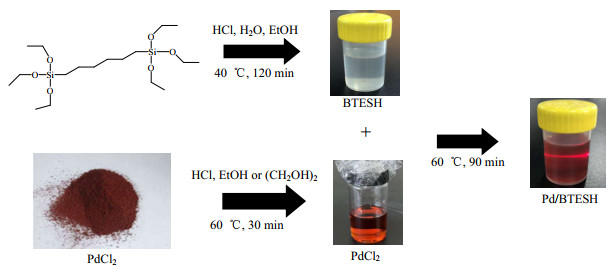
2.2 Pd/BTESH膜制备采用溶胶-凝胶技术制备膜。首先,制备BTESH溶胶:以BTESH: H2O: HCl: EtOH=1:60:0.2:94.71的物质的量配比,将BTESH硅源前驱体溶于无水乙醇中并进行搅拌,然后加入盐酸和水,在40 ℃的水浴下继续搅拌2 h后,将其用乙醇稀释为0.5% 的BTESH溶胶后放于冰箱中低温保存[24]。其次,制备含Pd溶液:在相关文献[18]基础上以PdCl2: HCl: EtOH=x: 0.15:9物质的量比制备(x=0.001 1、0.005 7、0.011),先将PdCl2溶解在浓HCl中,用乙醇或乙二醇作为溶剂,在60 ℃下搅拌30 min,制备出3种PdCl2浓度的溶液。最后,将上述BTESH溶胶中以相同的量分别加入3种PdCl2溶液中,60 ℃下继续搅拌90 min,形成物质的量比Pd: BTESH=0.2、1、2的混合溶胶,并采用乙醇溶剂调整BTESH在混合溶胶中的质量分数均为0.05%。另外,采用相同的制备方法,将上述中的乙醇全部换为乙二醇作为溶剂,制备Pd/BTESH溶胶。制备流程及实物如图 1所示。
|
图 1 Pd/BTESH溶胶的制备流程及实物图 Fig.1 Preparation process and physical images of Pd/BTESH sol |
膜的制备:采用大孔α-Al2O3片作为支撑体。首先,预先负载1.0 μm和0.2 μm的α-Al2O3颗粒,在550 ℃下焙烧20 min,重复3次,在支撑体表面形成颗粒层[25]。然后将正硅酸四乙酯与正丁醇锆水解共聚得到的SiO2-ZrO2溶胶[17]涂覆在上述支撑体上,在550 ℃下煅烧20 min,重复该过程10次以形成中间层。最后,在载体上涂覆Pd/BTESH溶胶,并在250 ℃下煅烧20 min,该过程重复3次,形成连续的分离层。溶剂为乙醇、乙二醇制备的膜,放于空气氛围下煅烧,而溶剂为乙醇的膜时,再次采用H2进行还原,N2作为保护气[26],通入流量比H2/N2=1:1的还原氛围在250 ℃下进行煅烧2 h。根据Pd/BTESH的物质的量比,将相应的有机硅溶胶、凝胶和膜命名为Pd/BTESH-0.2、Pd/BTESH-1和Pd/BTESH-2。
2.3 表征将BTESH和Pd/BTESH溶胶在60 ℃下真空干燥3 h后,在250 ℃煅烧20 min得到干凝胶,用研钵研磨成粉末并置于真空干燥皿中备用。采用X射线衍射仪(XRD,Rigaku,D/max 2500 PC)测定了干凝胶和膜中的晶体结构;采用傅里叶变换红外光谱仪(FTIR,Thermo Scientific,Nicolet iS50)测定了干凝胶的化学结构;采用场发射扫描电子显微镜(SEM,Zeiss,SUPRA 55)对膜进行形貌分析。
2.4 膜气体分离性能测试采用单组分的气体进行渗透试验。原料气从钢瓶导入膜组件上游,与下游大气压保持200 kPa的压差。将膜在N2氛围中于200 ℃加热10 h以去除吸附的水分,然后测试N2、H2的渗透性。水热稳定性测试:将气体通过水中湿润后,气体持续把水蒸气带入膜表面,进行气体渗透率测定。气体渗透率计算参照式(1),气体理想选择性计算参照式(2)。
| $ P = \frac{F}{{S\Delta p}} $ | (1) |
| $ {\alpha _{ij}} = \frac{{{P_i}}}{{{P_j}}} $ | (2) |
式中:P为气体渗透率;F为渗透气体流速,mol⋅s−1;S为膜的有效面积,m2;Δp为跨膜的压差,Pa;
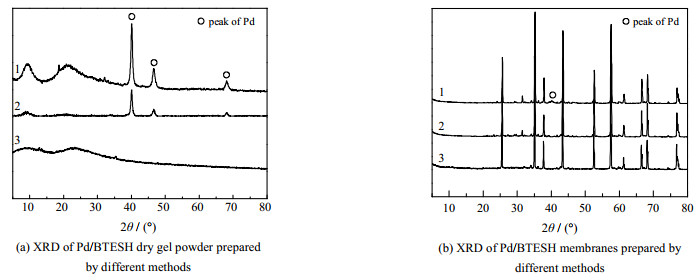
在形成的Pd-BTESH混合溶胶及制备的膜中,Pd往往以Pd2+的形式存在,而要形成Pd质点,需要进一步还原。本实验通过醇类化合物和H2还原,对制备的干凝胶及膜进行了研究。以醇为还原剂,其反应操作简单、条件温和,得到的Pd颗粒粒径小且分布均匀[27]。实验研究了乙醇和乙二醇两种醇类溶剂还原Pd。对还原后的Pd/BTESH-0.2干凝胶进行XRD测试,如图 2(a)所示。乙醇为溶剂的Pd-BTESH干凝胶的XRD图没有出现金属Pd的衍射峰,只有2θ=10°~25°的宽峰,表明乙醇没有还原能力,且不影响BTESH的无定形结构。而乙二醇为溶剂的Pd-BTESH干凝胶的XRD图在2θ=40.14°、46.70°和68.18°出现了金属Pd的衍射峰,说明Pd2+被成功还原成Pd。虽然乙醇和乙二醇都属于醇类弱还原剂,但乙二醇还原性大于乙醇,因此能将Pd2+成功还原成单质Pd。但BTESH的无定型结构变得不明显,说明Pd对BTESH的网络结构可能产生了一定影响。采用H2对金属还原也是一种常用的方法[26]。因此,将乙醇为溶剂的未被还原的干凝胶进一步采用H2还原,为了防止还原后的Pd颗粒再次发生氧化,用H2作为还原剂时加入N2氛围进行保护,设计在H2/N2=1:1的氛围中还原[28]。还原后的Pd-BTESH干凝胶出现了金属Pd的衍射峰[29-30]。H2/N2还原比乙二醇还原的衍射峰更强,无定型结构也较为明显。图 2(b)为Pd/BTESH-0.2膜表面的XRD图。乙醇和乙二醇还原的膜都只显示出载体Al2O3的衍射峰,并没有Pd的衍射峰,只有H2还原的膜在2θ=40.14°显示出微弱的Pd的衍射峰,这可能是因为乙二醇和乙醇作为弱还原剂,还原的金属Pd粒子较少,在膜表面难以检测,而H2作为强还原剂,还原Pd粒子程度较强[31]。
|
图 2 不同方法制备Pd/BTESH干凝胶和膜的XRD图 Fig.2 XRD patterns of Pd/BTESH dry gels and membranes prepared by different methods (1. reduction of H2/N2 2. reduction of ethylene glycol 3. reduction of ethanol) |
Pd/BTESH-0.2干凝胶和膜的实物图如图 3所示,可明显看出H2还原后的干凝胶颜色呈深黑色,更接近钯黑色,进一步验证了H2还原后在膜表面还原了较多的Pd颗粒,且颗粒较大、分散不均匀,而乙二醇还原的膜表面颜色变化不明显,可能还原的Pd颗粒较少。

|
图 3 不同方法制备Pd/BTESH-0.2干凝胶和膜图 Fig.3 Preparation of Pd/ BTESH-0.2 dry gels and membrane by different methods |
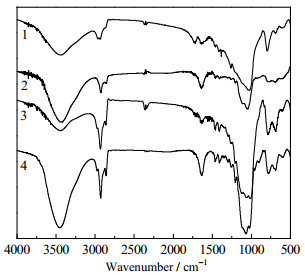
对不同还原方法制备的Pd/BTESH-0.2干凝胶进行红外光谱图测试表征其结构,如图 4所示,并与纯BTESH进行对比。可以发现所有干凝胶的红外特征峰大致相同,3 500 cm−1和2 900 cm−1左右分别是─OH和C─H的红外特征峰,在1 100 cm−1和790 cm−1附近均出现了归属于Si─O─Si结构的特征峰,说明均形成了硅网络结构,但图中乙醇还原后的Si─O─Si特征峰强度最高,乙二醇还原后峰强度逐渐降低,而H2还原后峰强度最低,可能由于Pd的还原度减弱了SiO2网络红外特征峰的强度[32]。乙醇还原的Pd/BTESH-0.2与乙二醇还原的Pd/BTESH-0.2的红外相比,Si─OH吸收峰强度不同,这可能是因为还原温度与乙醇和乙二醇本身的物理化学性质相关。如表 1所示,乙二醇比乙醇具有更大的沸点和黏度,在凝胶焙烧过程中不易被除去。
|
图 4 不同方法制备Pd/BTESH-0.2干凝胶的FT-IR图 Fig.4 FT-IR spectra of Pd/ BTESH-0.2 dry gels prepared by different methods (1. BTESH 2. H2/N2 reduction Pd/BTESH-0.2 3. ethanol reduction Pd/BTESH-0.2 4. ethylene glycol reduction Pd/BTESH-0.2) |
|
|
表 1 乙醇和乙二醇的物理性质 Table 1 Physical properties of ethanol and ethylene glycol |
图 5为BTESH膜和不同方法还原的Pd/BTESH-0.2膜表面与断面的SEM图。从图 5(a)~(d)可以看出,所有膜均呈现出连续、平整、无缺陷的表面。加入Pd后,膜表面能看到一些颗粒物凸起。采用H2/N2还原时膜表面的凸起物更大,这也从侧面说明其还原程度更大。从图 5(e)~(h)可以看出,分离层(与SiO2-ZrO2中间层难以区分)厚度约为700 nm。Pd的加入没有影响膜的厚度。这说明无论是氧化物或金属单质Pd,均能形成连续无缺陷的膜,对膜形貌的影响较小。

|
图 5 不同方法制备Pd/BTESH-0.2膜SEM图 Fig.5 SEM images of Pd/ BTESH-0.2 membranes prepared by different methods |
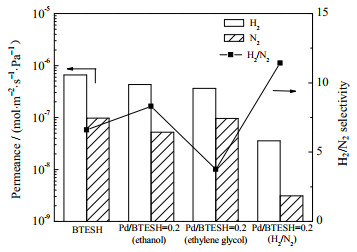
对不同还原方法制备的Pd/BTESH-0.2膜在200 ℃下进行H2、N2渗透率测试,并计算其H2/N2选择性,结果如图 6所示。BTESH膜表现了较高的H2渗透率,为6.54×10−7 mol⋅m−2⋅s−1⋅Pa−1,H2/N2选择性较小,仅为6.6。将Pd掺杂到BTESH中,在乙醇为溶剂的未还原态下,H2的渗透率为4.31×10−7 mol⋅m−2⋅s−1⋅Pa−1,选择性增大为8.3。对其进一步采用乙二醇还原,膜的H2渗透率和选择性均有所降低。而采用H2/N2氛围还原的Pd/BTESH-0.2膜表现出更好的H2/N2选择性,达到11.4。将2种还原法进行对比,乙二醇还原膜性能较差,可能是由于其还原的Pd粒子较少[27],以及残余乙二醇影响了BTESH的网络结构导致筛分性较弱。而采用H2/N2氛围还原,能较好地提升Pd/BTESH-0.2膜的H2/N2选择性。这说明Pd对H2具有选择性吸附作用。Lee等[33]和于洋等[34]分别报道了PdO对H2的传感特性和PdO的吸氢性能,PdO本身在室温下是不稳定的,由于体积中含有氧,PdO暴露在H2下会还原成Pd,从而使得H2吸附在Pd上,最大吸附效率为98.41%。
|
图 6 BTESH膜与不同还原方法制备的Pd/BTESH-0.2膜的性能图 Fig.6 Gas permeation performances of BTESH and Pd/BTESH-0.2 membranes prepared by different reduction methods |
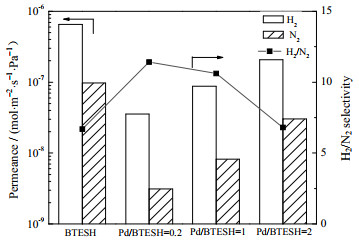
采用H2/N2还原法考察了不同Pd掺杂量对Pd/BTESH膜的H2、N2渗透率和H2/N2选择性的影响,如图 7所示。随着Pd掺杂量的增大,H2渗透率表现出先降低后升高的趋势,选择性的趋势相反。这可能是由于有机硅除了自身内部的孔外,还有颗粒间孔,而BTESH粒径较大,且具有柔性的长碳链,Pd粒子掺杂主要以填充的形式进入有机硅颗粒之间,形成更为致密的分离层,最终导致气体渗透率的降低,选择性增大。Kanezashi等[35]也发现了相似的结果,他们将Al加入BTESM膜中,发现随着Al掺杂量的增加,孔体积和比表面积都随之减小,导致膜的气体渗透率下降。而随着Pd掺杂量的继续增加,形成Pd粒子增大导致间隙孔也增大,因此,气体渗透率增大,选择性降低[29]。综上,Pd/BTESH-0.2膜表现出最佳的H2/N2选择性为11.4,相对于纯的BTESH膜,H2/N2选择性提高了72%。
|
图 7 BTESH膜与不同Pd掺杂量的Pd/BTESH膜的性能图 Fig.7 Gas permeation performances of BTESH and Pd/BTESH membranes with different Pd contents |
表 2给出了BTESH、Pd/BTESH和其他掺杂有机硅膜的H2、N2渗透率和H2/N2选择性的比较[6, 36]。本研究中具有柔性的长碳链的BTESH膜表现出较高的气体渗透率,与掺杂Nb、Ta的有机硅膜相比,Pd/BTESH膜具有更好的选择性,但渗透率较低。
|
|
表 2 金属掺杂有机硅膜的性能比较 Table 2 Comparison of metal-doped organosilica membranes of gas separation performeance |
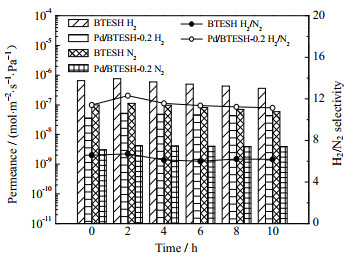
对最佳的Pd/BTESH-0.2膜进行水热稳定实验,并与无掺杂的BTESH膜进行对比。如图 8所示,在200 ℃的水蒸气下,测试膜的H2、N2渗透率随时间的变化。在持续通入2 h水蒸气后,Pd/BTESH-0.2膜H2的渗透率由3.55×10−8 mol⋅m−2⋅s−1⋅Pa−1增加到5.19×10−8 mol⋅m−2⋅s−1⋅Pa−1,表明允许H2通过的微孔略有增加,但仍不允许N2通过,从而提高了膜渗透选择性率。这种现象可能是蒸汽中极少量可移动SiO2基团丢失造成的[26]。逐渐稳定后,Pd/BTESH-0.2膜的H2和N2渗透率随着时间的延长保持不变,而选择性也基本保持在11.2~12.1,表现出较好的水热稳定性。这说明Pd的加入不影响BTESH有机硅膜的水热稳定性。
|
图 8 BTESH和Pd/BTESH-0.2膜的H2、N2渗透率及选择性在水蒸气下随着时间的变化 Fig.8 H2, N2 permeance and selectivity of BTESH and Pd/BTESH-0.2 membranes as a function of test time under water vapor |
将Pd2+掺杂到BTESH中成功制备了无缺陷的杂化膜,研究了Pd还原方法、Pd掺杂量对Pd/BTESH膜用于H2分离的影响。在还原中,乙醇对Pd没有还原能力,而采用乙二醇和H2/N2氛围均能还原Pd,并且H2/N2还原能力更好。随着Pd掺杂量的增加,H2的渗透率先降低后增加,H2/N2选择性相反。优化Pd掺杂量后,得到最优的添加比例。Pd颗粒还原前在具有较长柔性桥联基团的BTESH中分散良好,但通过H2还原成的金属Pd分散不均匀,导致膜表面出现较大的Pd颗粒沉积,而乙二醇还原后膜表面的Pd颗粒分散较为均匀。在200 ℃水蒸气中,Pd/BTESH有机硅膜表现出较好的水热稳定性,在多种H2工业中具有更为广泛的应用前景。
| [1] |
BUDHI Y W, RIONALDO H, PADAMA A A B, et al. Forced unsteady state operation for hydrogen separation through Pd–Ag membrane after start-up[J]. International Journal of Hydrogen Energy, 2015, 40(32): 10081-10089. DOI:10.1016/j.ijhydene.2015.05.182 |
| [2] |
GEORGIS D, LIMA F V, ALMANSOORI A, et al. Thermal management of a water–gas-shift membrane reactor for high-purity hydrogen production and carbon capture[J]. Industrial & Engineering Chemistry Research, 2014, 53(18): 7461-7469. |
| [3] |
LEI J J, SONG H T, WEI Y B, et al. A novel strategy to enhance hydrothermal stability of Pd-doped organosilica membrane for hydrogen separation[J]. Microporous and Mesoporous Materials, 2017, 253: 55-63. DOI:10.1016/j.micromeso.2017.06.041 |
| [4] |
ZHU Q, QU Y J, LIU D T, et al. Two-dimensional layered materials: High-efficient electrocatalysts for hydrogen evolution reaction[J]. ACS Applied Nano Materials, 2020, 3(7): 6270-6296. DOI:10.1021/acsanm.0c01331 |
| [5] |
OCKWIG N W, NENOFF T M. Membranes for hydrogen separation[J]. Chemical Reviews, 2007, 107(10): 4078-4110. DOI:10.1021/cr0501792 |
| [6] |
QURESHI H F, NIJMEIJER A, WINNUBST L. Influence of sol-gel process parameters on the micro-structure and performance of hybrid silica membranes[J]. Journal of Membrane Science, 2013, 446: 19-25. DOI:10.1016/j.memsci.2013.06.024 |
| [7] |
CASTRICUM H L, SAH A, KREITER R, et al. Hybrid ceramic nanosieves: Stabilizing nanopores with organic links[J]. Chemical Communications, 2008(9): 1103-1105. DOI:10.1039/b718082a |
| [8] |
KANEZASHI M, YADA K, YOSHIOKA T, et al. Organic–inorganic hybrid silica membranes with controlled silica network size: Preparation and gas permeation characteristics[J]. Journal of Membrane Science, 2010, 348(1/2): 310-318. |
| [9] |
SONG H T, ZHAO S F, CHEN J W, et al. Hydrothermally stable Zr-doped organosilica membranes for H2/CO2 separation[J]. Microporous and Mesoporous Materials, 2016, 224: 277-284. DOI:10.1016/j.micromeso.2016.01.001 |
| [10] |
DUKE M C, DA COSTA J C D, DO D D, et al. Hydrothermally robust molecular sieve silica for wet gas separation[J]. Advanced Functional Materials, 2006, 16(9): 1215-1220. DOI:10.1002/adfm.200500456 |
| [11] |
YU X, NAGASAWA H, KANEZASHI M, et al. Improved thermal and oxidation stability of bis(triethoxysilyl)ethane (BTESE)-derived membranes, and their gas-permeation properties[J]. Journal of Materials Chemistry A, 2018, 6(46): 23378-23387. DOI:10.1039/C8TA07572G |
| [12] |
KANEZASHI M, YONEDA Y, NAGASAWA H, et al. Gas permeation properties for organosilica membranes with different Si/C ratios and evaluation of microporous structures[J]. AIChE Journal, 2017, 63(10): 4491-4498. DOI:10.1002/aic.15778 |
| [13] |
IGI R, YOSHIOKA T, IKUHARA Y H, et al. Characterization of Co-doped silica for improved hydrothermal stability and application to hydrogen separation membranes at high temperatures[J]. Journal of the American Ceramic Society, 2008, 91(9): 2975-2981. DOI:10.1111/j.1551-2916.2008.02563.x |
| [14] |
KANEZASHI M, FUCHIGAMI D, YOSHIOKA T, et al. Control of Pd dispersion in sol-gel-derived amorphous silica membranes for hydrogen separation at high temperatures[J]. Journal of Membrane Science, 2013, 439: 78-86. DOI:10.1016/j.memsci.2013.03.037 |
| [15] |
KANEZASHI M, SANO M, YOSHIOKA T, et al. Extremely thin Pd-silica mixed-matrix membranes with nano-dispersion for improved hydrogen permeability[J]. Chemical Communications, 2010, 46(33): 6171-6173. DOI:10.1039/c0cc01461c |
| [16] |
TEN HOVE M, NIJMEIJER A, WINNUBST L. Facile synthesis of zirconia doped hybrid organic inorganic silica membranes[J]. Separation and Purification Technology, 2015, 147: 372-378. DOI:10.1016/j.seppur.2014.12.033 |
| [17] |
SONG H T, ZHAO S F, LEI J J, et al. Pd-doped organosilica membrane with enhanced gas permeability and hydrothermal stability for gas separation[J]. Journal of Materials Science, 2016, 51(13): 6275-6286. DOI:10.1007/s10853-016-9924-5 |
| [18] |
ZHANG H Y, WEN J L, SHAO Q, et al. Fabrication of La/Y-codoped microporous organosilica membranes for high-performance pervaporation desalination[J]. Journal of Membrane Science, 2019, 584: 353-363. DOI:10.1016/j.memsci.2019.05.023 |
| [19] |
ZHANG H F, WEI Y B, QI H. Palladium-niobium bimetallic doped organosilica membranes for H2/CO2 separation[J]. Microporous and Mesoporous Materials, 2020, 305: 110279. DOI:10.1016/j.micromeso.2020.110279 |
| [20] |
BOON J, PIETERSE J A Z, VAN BERKEL F P F, et al. Hydrogen permeation through palladium membranes and inhibition by carbon monoxide, carbon dioxide, and steam[J]. Journal of Membrane Science, 2015, 496: 344-358. DOI:10.1016/j.memsci.2015.08.061 |
| [21] |
LI X T, LI A W, LIM C J, et al. Hydrogen permeation through Pd-based composite membranes: Effects of porous substrate, diffusion barrier and sweep gas[J]. Journal of Membrane Science, 2016, 499: 143-155. DOI:10.1016/j.memsci.2015.10.037 |
| [22] |
NAGA MAHESH K, BALAJI R, DHATHATHREYAN K S. Palladium nanoparticles as hydrogen evolution reaction (HER) electrocatalyst in electrochemical methanol reformer[J]. International Journal of Hydrogen Energy, 2016, 41(1): 46-51. DOI:10.1016/j.ijhydene.2015.09.110 |
| [23] |
GUDARZI D, RATCHANANUSORN W, TURUNEN I, et al. Promotional effects of Au in Pd–Au bimetallic catalysts supported on activated carbon cloth (ACC) for direct synthesis of H2O2 from H2 and O2[J]. Catalysis Today, 2015, 248: 58-68. DOI:10.1016/j.cattod.2014.04.011 |
| [24] |
LIN D R, HU L J, YOU H, et al. Comparison of new periodic, mesoporous, hexylene-bridged polysilsesquioxanes with Pm3n symmetry versus sol–gel polymerized, hexylene-bridged gels[J]. Journal of Non-Crystalline Solids, 2014, 406: 139-143. DOI:10.1016/j.jnoncrysol.2014.09.045 |
| [25] |
ASAEDA M, YANG J H, SAKOU Y. Porous silica-zirconia (50%) membranes for pervaporation of iso-propyl alcohol (IPA)/water mixtures[J]. Journal of Chemical Engineering of Japan, 2002, 35(4): 365-371. DOI:10.1252/jcej.35.365 |
| [26] |
刘华华, 杨靖, 王亚琼. 制备钯金属纳米颗粒的还原方法及还原机理[J]. 过滤与分离, 2012, 22(3): 15-19. LIU H H, YANG J, WANG Y Q. Reducing methods and mechanism for preparation of palladium metal nano-particles[J]. Journal of Filtration & Separation, 2012, 22(3): 15-19. DOI:10.3969/j.issn.1005-8265.2012.03.004 |
| [27] |
何武强. 溶剂稳定的钯金属纳米颗粒的制备[J]. 化工技术与开发, 2009, 38(6): 20-21, 52. HE W Q. Preparation of solvent-stabilized palladium nanoparticles[J]. Technology & Development of Chemical Industry, 2009, 38(6): 20-21, 52. DOI:10.3969/j.issn.1671-9905.2009.06.007 |
| [28] |
JIANG J, ISLAM S, DONG Q B, et al. Deposition of an ultrathin palladium (Pd) coating on SAPO-34 membranes for enhanced H2/N2 separation[J]. International Journal of Hydrogen Energy, 2020, 45(58): 33648-33656. DOI:10.1016/j.ijhydene.2020.09.087 |
| [29] |
张恒飞, 刘为, 雷姣姣, 等. Pd掺杂量对有机无机杂化SiO2膜H2/CO2分离性能和水热稳定性能的影响[J]. 无机材料学报, 2018, 33(12): 1316-1322. ZHANG H F, LIU W, LEI J J, et al. Pd doping on H2/CO2 separation performance and hydrothermal stability of organic-inorganic hybrid SiO2 membranes[J]. Journal of Inorganic Materials, 2018, 33(12): 1316-1322. |
| [30] |
ZHANG H F, WEI Y B, NIU S F, et al. Fabrication of Pd-Nb bimetallic doped organosilica membranes by different metal doping routes for H2/CO2 separation[J]. Chinese Journal of Chemical Engineering, 2021, 36: 67-75. DOI:10.1016/j.cjche.2020.09.003 |
| [31] |
YANG J, FAN W Q, BELL C M. Effect of calcination atmosphere on microstructure and H2/CO2 separation of palladium-doped silica membranes[J]. Separation and Purification Technology, 2019, 210: 659-669. DOI:10.1016/j.seppur.2018.08.041 |
| [32] |
彭黎琼, 谢金花, 郭超, 等. 石墨烯的表征方法[J]. 功能材料, 2013, 44(21): 3055-3059. PENG L Q, XIE J H, GUO C, et al. Review of characterization methods of graphene[J]. Journal of Functional Materials, 2013, 44(21): 3055-3059. DOI:10.3969/j.issn.1001-9731.2013.21.001 |
| [33] |
LEE Y T, LEE J M, KIM Y J, et al. Hydrogen gas sensing properties of PdO thin films with nano-sized cracks[J]. Nanotechnology, 2010, 21(16): 165503. DOI:10.1088/0957-4484/21/16/165503 |
| [34] |
于洋, 朱鸣, 张波, 等. 新型氧化钯在高真空多层绝热设备中不同数量级真空度下吸氢特性实验研究[J]. 真空科学与技术学报, 2021, 41(7): 659-667. YU Y, ZHU M, ZHANG B, et al. Research on hydrogen absorption characteristics of novel palladium oxide at different vacuum degrees in high vacuum multilayer insulation equipment[J]. Chinese Journal of Vacuum Science and Technology, 2021, 41(7): 659-667. |
| [35] |
KANEZASHI M, MIYAUCHI S, NAGASAWA H, et al. Pore size control of Al-doping into bis (triethoxysilyl) methane (BTESM)-derived membranes for improved gas permeation properties[J]. RSC Advances, 2013, 3(30): 12080-12083. DOI:10.1039/c3ra41971a |
| [36] |
QURESHI H F, BESSELINK R, TEN ELSHOF J E, et al. Doped microporous hybrid silica membranes for gas separation[J]. Journal of Sol-Gel Science and Technology, 2015, 75(1): 180-188. DOI:10.1007/s10971-015-3687-3 |




